녹은 소금 복합 금속 산화물 나노 입자의 합성
Summary
여기, 균일 한 복잡 한 금속 산화물 란타넘 hafnate 나노 입자를 준비 하기 위한 독특한, 상대적으로 낮은 온도, 녹은 소금 합성 방법을 보여 줍니다.
Abstract
실현 가능한 합성 방법의 개발이 새로운 속성의 성공적인 탐사 및 나노 재료의 잠재적인 응용 프로그램에 대 한 중요 합니다. 여기, 우리는 금속 산화물 나노 소재를 만들기 위한 녹은 소금을 합성 (MSS) 방법 소개. 다른 방법에 비해 이점이 그것의 간명, 초록색, 신뢰성, 확장성, 및 가해질 포함 됩니다. 담당자 pyrochlore 란타넘 하프늄 산화물 (라2Hf2O7)를 사용 하 여, 복잡 한 금속 산화물 나노 입자 (NPs)의 성공적인 합성에 대 한 MSS 프로토콜을 설명 합니다. 또한,이 메서드는 pH, 온도, 시간, 포스트 어 닐 링 등 다양 한 합성 매개 변수를 변경 하 여 다른 소재 기능 NPs를 생산 하는 독특한 능력. 이러한 매개 변수를 조정 하 여 우리는 매우 균일, 비 응집 하 고 높은 결정 NPs를 합성 수 있습니다. 구체적인 예를 들어, 우리는 더에 다양 한 입자 크기의 효과 탐험 수 있는 MSS 프로세스에 사용 되는 수산화 암모늄 용액의 농도 변경 하 여 라2Hf2O7 NPs의 입자 크기를 다 속성입니다. 그것은 MSS 메서드 나노 재료 등 널리 nanoscience 나노기술 커뮤니티에서 곧 나오는 년에서 고용에 대 한 더 많은 인기 있는 합성 방법 될 것으로 예상 된다.
Introduction
용융 소금 합성 (MSS) 그들의 구성 선구자에서 나노 재료를 준비 하기 위한 반응 매체로 녹은 소금의 사용을 포함 한다. 녹은 소금 역할을 용 매 반응 및 그들의 이동성 사이의 접촉면이 증가 하 여 향상 된 반응 속도 촉진 한다. MSS 방법의 성공을 위해 최고 중요성의 녹은 소금의 선택이입니다. 소금은 낮은 녹는점, 호환성 반응 종, 그리고 최적의 수성 가용성을 몇 가지 중요 한 품질 요구 사항을 충족 해야 합니다. 녹은 소금 이전; 고체 반응의 속도 향상 시키기 위해 사용 되었습니다. 그러나, 플럭스 시스템 녹은 소금만 소량에 사용 됩니다 (달리 MSS, 대량 반응에 대 한 수용 성 매체를 형성 하 고 합성된 나노 입자 크기, 모양, 결정 등의 속성을 컨트롤에 추가 됩니다에 등). 이런이 의미에서 MSS와 유출 방법1,,23다른 분말 야 금 방법의 수정입니다. 합성 온도5, (2) 증가 반응 동질성6의 정도 감소 하는 동안 용융 염 수 (1) 증가 반응 운동 속도4 의 고용 (3) 제어 결정 크기와 형태7, (4) 덩어리의 수준을 줄일.
나노 소재 수요에 과학 연구와 새로운 산업 응용 프로그램에 때문에 되었습니다 그들의 우수한 전기, 화학, 자석, 광학, 전자, 및 열 속성. 그들의 속성은 입자 크기, 모양, 및 결정에 매우 의존 합니다. 나노 소재에 대 한 다른 합성 방법에 비해, MSS 몇 가지 장점이 분명 한; 비록, 그것은 아직 아니에요 nanoscience 나노기술 커뮤니티에서 다른 합성 방법으로 유명한. 아래 설명 된 대로 이러한 장점에는 그것의 단순, 신뢰성, 확장성, 가해질, 환경 친화성, 비용 효율성, 상대적 낮은 합성 온도, 및 깨끗 한 표면8NPs의 무료 덩어리 포함 됩니다.
단순: MSS 프로세스 수 있습니다 쉽게 실시 간단한 실험실에서 기본적인 기능을 가진. 아니 정교한 계측 필요 합니다. 선구자 및 녹은 소금은 장갑 상자 처리에 대 한 필요와 함께 안정.
신뢰성: 농도, pH, 처리 시간, 및 어 닐 링 온도 같은 모든 초기 합성 매개 변수 최적화, 일단 높은-품질 및 순수한 제품 보장 하는 MSS 메서드를 사용 하는 경우. 모든 합성 단계가 제대로 수행 됩니다, 만약 최종 제품 좋은 품질 NPs에 필요한 모든 기본적인 기준을 달성 수 있습니다. MSS 메서드에 초보자 모든 합성 매개 변수는 제대로 그리고 신중 하 게 다음으로 합성 결과 변경 되지 않습니다.
확장성: MSS 메서드의 크기 및 모양을 제어 입자의 대량 생산 능력은 중요 합니다. 이 중요 한 요인은 산업 유용성 및 효율성에 대 한 허용 하기 때문에 중요 하다. 다른 합성 기법에 비해, MSS 생성할 수 있습니다 쉽게 충분 한 양의 제품 과정에서 화학 량 론 금액을 조정 하 여. 이 확장성9,10인 더 원하는 접근을 만드는 산업 수준에서의 편의 위해 수 있기 때문에이 방법의 중요 한 기능입니다.
가해질: MSS 방법 또한 다양 한 구성으로 나노 입자를 생산 하기 위해 받아들이기는 기술입니다. 간단한 금속 산화물 및 일부 불 화물, MSS 메서드에서 성공적으로 합성 된 복잡 한 금속 산화물의 나노 재료 포함 perovskites (ABO3)10,,1112, 13,14, 스피넬 (AB2O4)15,16, pyrochlore (2B2O7)4,,1718, 19, 그리고 orthorhombic 구조 (2B4O9)2,,320. 좀 더 구체적으로, 이러한 나노 페라이트, 티, niobates, 멀 라이트, 알루미늄 borate, wollastonite, 및 탄산된 인회석7,,921포함 됩니다. MSS 메서드는 나노4, 세라믹 분말 시체22, nanoflakes23, nanoplates7, nanorods24, 코어-쉘 등 다양 한 형태학의 나노 소재를 생산 하기 위해 사용 되었습니다. 나노 (NPs)25, 합성 조건 및 제품의 결정 구조에 따라.
환경 친화: 다량의 유기 용 제와 환경 문제를 생성 하는 유독한 대리인의 사용을 포함 하는 나노 소재를 만들기 위한 몇 가지 전통적인 방법. 녹색 화학의 수요에 그들의 사용 및 지속 가능한 프로세스에 의해 폐기물의 생성의 부분 또는 전체 제거는 요즘8. MSS 방법은 독성 화학 및 재생 재료를 채용 하 고 폐기물, 부산물, 그리고 에너지를 최소화 하 여 나노 재료를 합성 하는 환경 친화적인 접근 방식입니다.
상대 낮은 합성 온도: MSS 메서드의 처리 온도 상대적으로 기존의 고체 반응26 또는27솔-젤 연소 반응 필요한에 비해 낮은. 이 낮은 온도 높은-품질 NPs를 생산 하는 동안 에너지를 저장 합니다.
비용 효율성: 어떤 가혹한 또는 비용이 많이 드는 반응 물 또는 용 제도 어떤 특수 계측은 MSS 메서드가 필요 하지 않습니다. 물은 저렴 한 있습니다 사용된 녹은 소금 멀리 세척에 사용 되는 주요 용 매 이다. 또한, 복잡 한 구성 및 내 화 자연 나노 소재를 생산할 수 동안 간단한 유리 및 특수 계측 없이 필요한 실험 설치 포함.
덩어리 깨끗 한 표면을 가진 무료: MSS 동안 과정, 형성된 된 나노 입자는 그것의 높은 이온 강도 및 점도1,6, 와 함께 사용 되는 대량으로 녹은 소금 매체에 잘 분산 8. 콜 로이드 합성과 열 수/solvothermal는 대부분의 프로세스와 달리 아무 표면 보호층은 지속적인 성장 및 형성된 NPs의 응집을 방지 하는 데 필요한.
MSS 방법으로 복잡 한 금속 산화물 NPs의 모범적인 종합: 이성적으로 MSS 메서드는 유니버설으로 하 고 비용 효율적인 접근 및 대규모 물자의 충분히 넓은 스펙트럼 높은 과학자에 의해 환영 될 수 있습니다에 대 한 나노 재료를 합성 nanoscience 및 나노기술에서 근무. 여기, 란타넘 hafnate (라2Hf2O7) x 선 영상, k의 분야에서 다기능 응용 프로그램 때문에 선정 되었다-코팅, 열 장벽, 열감지 형광체, 발광, 유 전체 및 핵 폐기물 호스트입니다. 라2Hf2O7 주문 장애 상전이 함께 설계 될 그것의 높은 밀도, 큰 효과적인 원자 번호, 및 그것의 크리스탈 구조 가능성도 핑된 scintillators에 대 한 좋은 호스트 이기도 합니다. 그것은 화합물, “A”는 + 3 산화 상태와 희귀-지구 요소 및 “B” + 4 산화 상태와 전이 금속 요소를 나타냅니다의 A2B2O7 가족에 속한다. 그러나, 내 화 특성 및 복잡 한 화학 성분, 라2Hf2O7 NPs에 대 한 대규모 합성 방법과 적절 한 저온의 부족이 되었습니다.
근본적인 과학적 조사 및 고급 기술 응용 프로그램, 그것은 단 분산, 높은-품질, 고2B2O7 NPs 통일에 전제 조건. 여기 우리가 MSS 방법의 장점을 설명 하기 위해 예를 들어 높은 결정 질 라2Hf2O7 NPs의 합성을 사용 합니다. 그림 1에 표시 된 개요로, 우리의 이전 보고서를 다음과 같은 두 단계 프로세스 라2Hf2O7 NPs MSS 메서드에 의해 준비 되었다. 첫째, 단일 소스 복잡 한 전조 La(OH)3· HfO(OH)2· n H2O coprecipitation 경로 통해 준비 되었다. 두 번째 단계에서 크기를 제어할 수 있는 라2Hf2O7 NPs는 단일 소스 복잡 한 전조와 질 산 혼합물을 사용 하 여 손쉬운 MSS 과정을 통해 종합 되었다 (나노3: 알3 = 1:1, 어 금 니 비율)에 650 ° C 6 h에 대 한입니다.
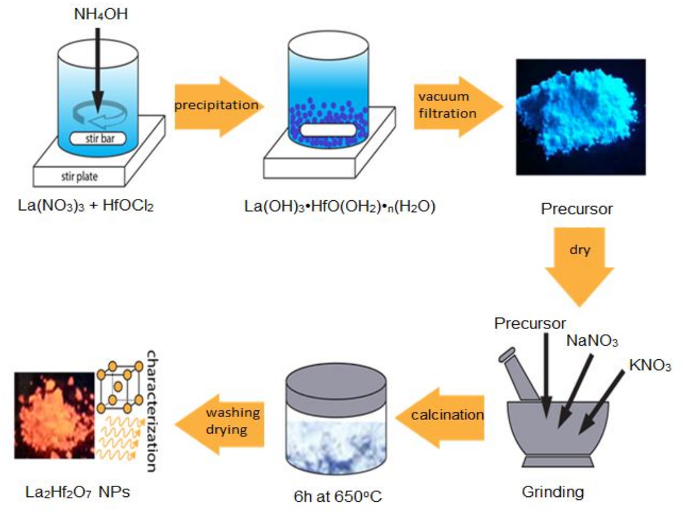
그림 1 : 회로도 합성의 단계 라 2 Hf 2 O 7 MSS 방법을 통해 NPs. 이 그림의 더 큰 버전을 보려면 여기를 클릭 하십시오.
Protocol
Representative Results
Discussion
그림 4에서 차트 MSS 메서드 및 합성된 나노 재료의 특징을 세밀 하 게 조정 대체 경로 대 한 계정을 여러 신뢰할 수 있는 제어 요소를 제공 합니다. 또한, 그것은 MSS 프로세스에서 중요 한 단계를 확인할 수 있습니다.
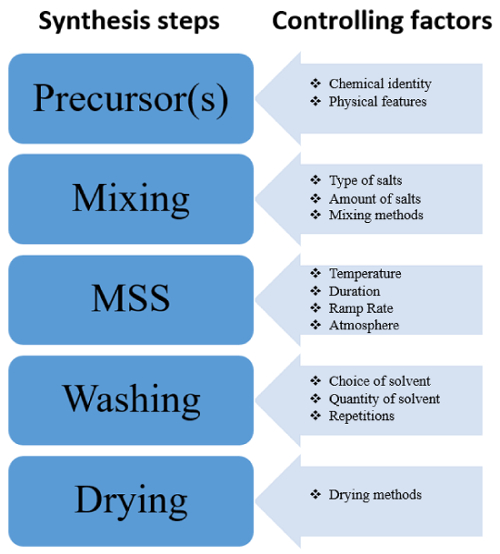
그림 4 : 순서도의 M…
Divulgazioni
The authors have nothing to disclose.
Acknowledgements
저자 체 (보너스 #1710160)와 미국 농 무부 식품 및 농업 (수상 #2015-38422-24059) 국립 과학 재단에서 제공 하는 금융 지원을 감사 합니다. 텍사스 대학 리오 그란데 계곡에 화학의 부는 로버트 A. 웰 치 재단 (부여 번호에서에서 부서 권한을 부여 하 여 제공 하는 관대 한 지원에 대 한 감사 BX-0048). S.K.G. 그의 풀브라이트 네루 박사 친목 (수상 #2268/FNPDR/2017)에 대 한 미국-인도 교육 재단 (USIEF)와 국제 교육 (IIE)의 연구소를 감사 하 고 싶습니다.
Materials
| Acetone, ACS, 99.5+% | Alfa Aesar | 67-64-1 | Dried over 4A sieves |
| Hafnium dichloride oxide octahydrate, 98+% (metals basis excluding Zr), Zr <1.5% | Alfa Aesar | 14456-34-9 | Hygroscopic |
| Lanthanum(III) nitrate hexahydrate | Aldrich | 10277-43-7 | Hygroscopic |
| Potassium nitrate, ReagentPlus R, ≥99.0% | Sigma-Aldrich | 7757-79-1 | Hygroscopic |
| Sodium nitrate, ReagentPlus R, ≥99.0% | Sigma-Aldrich | 7631-99-4 | |
| Ammonium hydroxide, 28% NH3, NH4OH | Alfa Aesar | 1336-21-6 | |
| Filter paper, P8 grade | Fisherbrand |
Riferimenti
- Kimura, T. Molten salt synthesis of ceramic powders. Advances in Ceramics. , 75-100 (2011).
- Mao, Y., Park, T. J., Wong, S. S. Synthesis of classes of ternary metal oxide nanostructures. Chemical Communications. (46), 5721-5735 (2005).
- Mao, Y., Zhou, H., Wong, S. S. Perovskite-phase metal oxide nanostructures: Synthesis, properties, and applications. Material Matters. 5, 50-53 (2010).
- Mao, Y., Guo, X., Huang, J. Y., Wang, K. L., Chang, J. P. Luminescent nanocrystals with A2B2O7 composition synthesized by a kinetically modified molten salt Method. The Journal of Physical Chemistry C. 113 (4), 1204-1208 (2009).
- Yu, Y., Wang, S., Li, W., Chen, Z. Low temperature synthesis of LaB6 nanoparticles by a molten salt route. Powder Technology. 323, 203-207 (2018).
- Liu, X., Fechler, N., Antonietti, M. Salt melt synthesis of ceramics, semiconductors and carbon nanostructures. Chemical Society Reviews. 42 (21), 8237-8265 (2013).
- Chang, Y., Wu, J., Zhang, M., Kupp, E., Messing, C. L. Molten salt synthesis of morphology controlled alpha-alumina platelets. Ceramics International. 43 (15), 12684-12688 (2017).
- Mao, Y., Park, T. J., Zhang, F., Zhou, H., Wong, S. S. Environmentally friendly methodologies for nanostructure synthesis. Small. 3 (7), 1122-1139 (2007).
- Liu, J. R., Hong, R. Y., Feng, W. G., Badami, D., Wang, Y. Q. Large scale production of strontium ferrite by molten salt assited coprecipitation. Powder Technology. 262, 142-149 (2014).
- Yuanbing, M., Banerjee, S., Wong, S. S. Large-scale synthesis of single-crystalline perovskite nanostructures. Journal of the American Chemical Society. 125 (51), 15718-15719 (2003).
- Mao, Y. Facile synthesis of ferromagnetic double perovskite oxide La2BMnO6 nanoparticles. RSC Advances. 2 (33), 12675-12678 (2012).
- Hailili, R., Wang, C., Lichtfouse, E. Perovskite nanostructures assembled in molten salt based on halogen anions KX (X = F, Cl and Br): Regulated morphology and defect-mediated photocatalytic activity. Applied Catalysis B: Enviromental. 232, 531-543 (2018).
- Yuanbing Mao, J. P., McCloy, J. S. Magnetic properties of double perovskite oxide La2BMnO6 nanocrystals. Nanoscale. 5 (11), 4720-4728 (2013).
- Mao, Y., Wong, S. S. Reproducible composition and shape control of crystalline Ca1-xSrxTiO3 perovskite nanoparticles. Advanced Materials. 17 (18), 2194-2199 (2005).
- Rojas-Hernandez, R. E., et al. Original synthetic route to obtain a SrAl2O4 phosphor by the molten salt method: insights into the reaction mechanism and enhancement of the persistent luminescence. Inorganic Chemistry. 54 (20), 9896-9907 (2015).
- Reddy, M. V., Xu, Y., Rajarajan, V., Ouyang, T., Chowdari, B. V. R. Template free facile molten synthesis and energy storage studies on MCo2O4 (M = Mg, Mn) as anode for Li-ion batteries. ACS Sustainable Chemistry and Engineering. 3 (12), 3035-3042 (2015).
- Zuniga, J. P., Gupta, S. K., Pokhrel, M., Mao, Y. Exploring optical properties of La2Hf2O7:Pr3+ nanoparticles under UV and X-ray excitations for potential lighting and scintillating applications. New Journal of Chemistry. 42 (12), 9381-9392 (2018).
- Pokhrel, M., Wahid, K., Mao, Y. Systematic studies on RE2Hf2O7:5%Eu3+ (RE = Y, La, Pr, Gd, Er, and Lu) nanoparticles: Effects of the A-Site RE3+ cation and calcination on structure and photoluminescence. The Journal of Physical Chemistry C. 120 (27), 14828-14839 (2016).
- Wahid, K., Pokhrel, M., Mao, Y. Structural, photoluminescence and radioluminescence properties of Eu3+ doped La2Hf2O7 nanoparticles. Journal of Solid State Chemistry. 245, 89-97 (2017).
- Park, T. J., Papaefthymiou, G. C., Moodenbaugh, A. R., Mao, Y., Wong, S. S. Synthesis and characterization of submicron single-crystalline Bi2Fe4O9 cubes. Journal of Materials Chemistry. 15 (21), 2099-2105 (2005).
- Gilbert, M. R. Molten salt synthesis of titanate pyrochlore waste-forms. Ceramics International. 42 (4), 5263-5270 (2016).
- Huang, Z., et al. Molten salt synthesis of La2Zr2O7 ultrafine powders. Ceramics International. 42 (5), 6221-6227 (2016).
- Huang, Z., Duan, H., Liu, J., Zhang, H. Preparation of lanthanum cerate powders via a simple molten salt route. Ceramics International. 42 (8), 10482-10486 (2016).
- Wang, G., et al. Fabrication of rod-like Ti4O7 with high conductivity by molten salt synthesis. Materials Letters. 186, 361-363 (2017).
- Pokhrel, M., Burger, A., Groza, M., Mao, Y. Enhance the photoluminescence and radioluminescence of La2Zr2O7:Eu3+ core nanoparticles by coating with a thin Y2O3 shell. Optical Materials. 68, 35-41 (2017).
- Ramesh, G., Subramanian, V., Sivasubramanian, V. Dielectric properties of lead indium niobate ceramics synthesized by conventional solid state reaction method. Materials Research Bulletin. 45 (12), 1871-1874 (2010).
- Gupta, S. K., et al. Role of various defects in the photoluminescence characteristics of nanocrystalline Nd2Zr2O7: An introspection through spectroscopic and DFT calculations. Journal of Materials Chemistry C. 4 (22), 4988-5000 (2016).
- Wang, X., Zhu, Y., Zhang, W. Preparation of lanthanum zirconate nano-powders by molten salt method. Journal of Non-Crystalline Solids. 356 (20-22), 1049-1051 (2010).
- Popov, V. V., et al. Fluorite-pyrochlore phase transition in nanostructured Ln2Hf2O7 (Ln = La-Lu). Journal of Alloys and Compounds. 689, 669-679 (2016).
- Rybarczyk, M. K., Gontarek, E., Lieder, M., Titirici, M. M. Salt melt synthesis of curved nitrogen-doped carbon nanostructures: ORR kinetics boost. Applied Surface Science. 435, 543-551 (2018).
- Ozen, M., Mertens, M., Snikers, F., D’Hondt, H., Cool, P. Molten-salt synthesis of tetragonal micron-sized barium titanate from a peroxo-hydroxide precursor. Advanced Powder Technology. 28 (1), 146-154 (2017).
- Fazli, R., Fazli, M., Safaei-Naeini, Y., Golestani-Fard, F. The effects of processing parameters on formation of nano-spinel (MgAl2O4) from LiCl molten salt. Ceramics International. 39 (6), 6265-6270 (2013).
- Bortolani, F., Dorey, R. A. Molten salt synthesis of PZT powder for direct write inks. Journal of the European Ceramic Society. 30 (10), 2073-2079 (2010).
- Zhou, H., Mao, Y., Wong, S. S. Probing structure-parameter correlations in the molten synthesis of BaZrO3 perovskite submicron-sized particles. Chemistry of Materials. 19 (22), 5238-5249 (2007).
- Kimura, T., Machida, M., Yamaguchi, T., Newnham, R. E. Products of reaction between PbO and Nb2O5 in molten KCl or NaCl. Journal of the American Ceramic Society. 66 (10), 195-197 (1983).
- Liu, S., et al. A novel rechargeable zinc-air battery with molten salt electrolyte. Journal of Power Sources. 342, 435-441 (2017).
- Huang, Z., Li, B., Liu, J. Molten-salt synthesis of oxyapatite La9.33Si6O26 powders as electrolytes for intermediate temperature solid oxide fuel cells. Physica status solidi A – Applicationand Materials Science. 207 (10), 2247-2251 (2010).
- Ahmed, J., Mao, Y. Synthesis, characterization and electrocatalytic properties of delafossite CuGaO2. Journal of Solid State Chemistry. 242 (1), 77-85 (2016).
- Ahmed, J., Mao, Y. Ultrafine iridium oxide nanorods synthesized by molten salt method toward electrocatalytic oxygen and hydrogen evolution reactions. Electrochimica Acta. 212, 686-693 (2016).

