Eine Fluoreszenz Fluktuation Spektroskopie Assay von Protein-Protein-Wechselwirkungen an den Zell-Zell-Kontakten
Summary
Dieses Protokoll beschreibt einen Fluoreszenz Fluktuation Spektroskopie basierende Ansatz zur Untersuchung von Interaktionen zwischen den Proteinen, die Vermittlung von Zell-Zell-Interaktionen, d.h. Proteine in der Zelle Verzweigungen direkt in lebenden Zellen lokalisiert. Wir bieten detaillierte Richtlinien auf Kalibrierung, Datenerfassung und -Analyse, einschließlich Korrekturen möglich Artefakt Quellen.
Abstract
Eine Vielzahl von biologischen Prozessen umfasst Zell-Zell-Interaktionen, in der Regel vermittelt durch Proteine, die an der Schnittstelle zwischen benachbarten Zellen interagieren. Von Interesse sind nur einige Proben in der Lage, speziell solche Interaktionen direkt in lebenden Zellen zu sondieren. Hier präsentieren wir Ihnen einen Test um die Bindung der Proteine an den Oberflächen von benachbarten Zellen, Zell-Zell Kontakte zu messen. Dieser Test besteht aus zwei Schritten: Mischen von Zellen mit dem Ausdruck der Proteine des Interesses mit verschiedenen fluoreszierenden Proteinen verschmolzen, gefolgt von Fluoreszenz Fluktuation Spektroskopie Messungen bei Zell-Zell-Kontakte mit einem konfokalen Laser-scanning-Mikroskop. Wir zeigen die Machbarkeit des Assays in einem biologisch relevanten Kontext durch die Messung der Wechselwirkungen von Amyloid Vorläufer-Like Protein 1 (APLP1) über Zell-Zell-Verbindungen. Wir bieten detaillierte Protokolle über die Datenerfassung mit Fluoreszenz-basierte Techniken (Scannen Kreuzkorrelation Fluoreszenzspektroskopie, Kreuzkorrelation Anzahl und Helligkeit Analyse) und den gewünschten Gerätes Kalibrierungen. Darüber hinaus diskutieren wir wichtige Schritte in der Datenanalyse und Gewusst wie: identifizieren und beheben Sie externe, falsche Signal Variationen, wie Sie durch Immunofluoreszenz oder Zelle Bewegung.
Im Allgemeinen der vorgestellte Test gilt für alle Homo- oder Zellkulturmodells Proteinprotein Interaktion auf Zell-Zell Kontakte zwischen den Zellen der gleichen oder unterschiedlichen Typen und kann auf eine kommerzielle konfokale Laser-scanning-Mikroskop implementiert werden. Eine wichtige Voraussetzung ist die Stabilität des Systems, das muss ausreichen, um die Sonde diffusiven Dynamik der interessierenden Proteine über mehrere Minuten.
Introduction
Viele biologische Prozesse auftreten, an den Standorten der Zell-Zell-Interaktionen, z.B. Zellezelle Adhäsion1,2,3, Zell-Zell-Fusion-4 und zelluläre Anerkennung5. Solche Ereignisse sind besonders wichtig bei der Entwicklung von mehrzelligen Lebewesen und für die Zell-Zell-Kommunikation, z. B. während Immunantworten. Diese Prozesse werden in der Regel durch Proteine vermittelt, die an der Oberfläche, d. h. an der Plasmamembran (PM) der benachbarten Zellen lokalisiert sind und spezifische Wechselwirkungen, die auf der Zell-Zell-Kontakt genau geregelten in Raum und Zeit sind zu unterziehen. In vielen Fällen diese Interaktionen sind direkte Homo- oder Zellkulturmodells Protein-Protein- Trans -Wechselwirkungen, aber können auch beinhalten, Ionen oder Liganden als extrazelluläre linker1. Obwohl von grundlegender Bedeutung, fehlt von Assays sondieren dieser spezifischen Protein-Protein-Interaktionen direkt in der natürlichen Umgebung von lebenden Zellen. Viele Methoden erfordern entweder Zellaufschluss (z. B. biochemische Tests wie z. B. co-Immunopräzipitation6), Fixierung (z. B. einige der Höchstauflösung optische Mikroskopie-Techniken und der Zell-Zell-Elektronen-Mikroskopie 7Kontakte), oder sind unspezifisch, z. B. Aggregation / Adhäsion assays8,9. Um dieses Problem zu überwinden, wurden Fluoreszenztechniken umgesetzt, basierend auf Fluoreszenz Resonanz Energie Transfer (FRET)10 oder Fluoreszenz Ergänzung11. Um ausreichend geringe Abstände zwischen Fluorophore zu erreichen, erfordern diese Methoden jedoch Fluoreszenzmarkierungen auf der extrazellulären Seite der Proteine10, potenziell Trans Interaktionen behinderen.
Hier präsentieren wir Ihnen eine alternative Fluoreszenz basierende Assays für Protein-Protein-Wechselwirkungen an den Zell-Zell-Kontakten. Dieser Ansatz verbindet Fluoreszenz Kreuzkorrelation Ansätze (Fluoreszenzspektroskopie Kreuzkorrelation Scan (sFCCS), Kreuzkorrelation Anzahl und Helligkeit (CcN & B)) und Mischen von Zellen mit dem Ausdruck einer Fusion-Konstrukt des Proteins Interesse, z. B. eine Adhäsion-Rezeptor. Die untersuchten Rezeptoren in den zwei interagierenden Zellen mit zwei spektral getrennte fluoreszierende Proteine (FPs), von der intrazellulären gekennzeichnet sind (siehe Abbildung 1A).
Die eingesetzten Methoden basieren auf der statistischen Auswertung der Fluoreszenz Schwankungen induziert durch die diffusive Bewegung von fluoreszierenden Fusionsproteinen durch die fokalen Volumen von einem konfokalen Laser-scanning-Mikroskop. Mehr im Detail Sonden der Assay die Co Diffusion der Proteine des Interesses an beiden benachbarten PMs an den Zell-Zell-Kontakten. Wenn die Proteine Trans Interaktionen durchmachen, tragen diese Trans -komplexe fluoreszierende Proteine in beiden spektralen Kanälen ausstrahlen, wodurch korrelierte Fluoreszenz Schwankungen der beiden Strahler. Auf der anderen Seite, wenn keine Bindung auftritt, werden die Nummer Schwankungen der Proteine in PMs vor, verursacht keine korrelierten Schwankungen unabhängig. Die Übernahme kann auf zwei Arten durchgeführt werden: 1) sFCCS basiert auf einer linienförmigen Scan über die Zell-Zell-Kontakt und effektiv Sonden die Interaktionen in einem Ort befindet sich im Kontaktbereich. Durch eine zeitliche Analyse der Fluoreszenz Schwankungen informiert sFCCS auch Dynamik, d. h. die Diffusionskoeffizienten von Proteinkomplexen; (2) CcN & B basiert auf eine pixelweise Analyse einer Sequenz von Bildern bei der Zell-Zell-Kontaktbereichen erworben. Es hat Fähigkeit, Sonde und Karte Interaktionen entlang der gesamten Region (in einer Bildebene) zu kontaktieren, aber liefert keine Informationen auf Dynamik. Beide Methoden sind kombinierbar mit einer Analyse der molekularen Helligkeit, d. h. die durchschnittliche Fluoreszenzsignal einzelne diffundierende Proteinkomplexe in der Zeiteinheit abgegebene und geben damit Schätzungen der Stöchiometrie von Proteinkomplexen im Zell-Zell-Kontakte.
In diesem Artikel bieten wir ausführliche Protokolle zur Probenvorbereitung, Kalibrierung, Datenerfassung und Analyse durchführen den vorgestellten Test auf eine kommerzielle konfokale Laser-scanning-Mikroskop. Die Experimente können auf jedem Instrument ausgestattet mit Photon counting oder analogen Detektoren und einem Objektiv mit hoher numerischer Apertur durchgeführt werden. Weiter wichtige Schritte des Protokolls zu diskutieren und mehrere Prozesse verursacht artifizielle Signalschwankungen, z. B. Detektor Lärm, Immunofluoreszenz oder Zelle Bewegung Korrektur Regelungen vorsehen. Entwickelt um die Wechselwirkungen zwischen adhärente Zellen Sonde, Assays für Aussetzung Zellen geändert werden kann, oder angepasst Modell Membran-Systeme, z. B. giant Unilamellar Vesikeln (GUVs) oder riesigen Plasma Membranvesikel (GPMVs), so dass die Quantifizierung von Interaktionen in verschiedenen Lipid-Umgebungen oder in Ermangelung einer organisierten Zytoskelett12,13.
Scannen Kreuzkorrelation Fluoreszenzspektroskopie ist eine modifizierte Version der Fluoreszenz-Spektroskopie Kreuzkorrelation14 und wurde speziell für die Sonde langsam diffusiven Dynamik in Lipid-Membranen-15. Es basiert auf einer Linie Scan Akquisition senkrecht zur PM mit fluoreszierenden Proteinen von Interesse. Um Wechselwirkungen zwischen zwei unterschiedlich beschriftete Protein Arten Sonde, erfolgt die Übernahme in zwei Spektralkanäle mit zwei Laser-Linien und zwei Erkennung Fenster für die spektral getrennte Fluorophore. Durch die langsame Diffusion Dynamik von Proteinen in der PM (D≤ ~ 1 µm2/s), eine Cross-Talk-freie Messung kann durch den Wechsel der Erregung System von Linie auf15Linie durchgeführt werden. Die Analyse beginnt mit: (1) eine Ausrichtung Algorithmus Korrektur der seitlichen Zellbewegung basierend auf abschnittsweise durchschnittlich ~ 1000 Zeilen, (2) die Bestimmung der Position mit maximale Fluoreszenz-Signald.h. die Uhr Position, in jedem Block und (3) verschieben alle Blöcke bis hin zum gemeinsamen Ursprung12,15, in jeden Kanal separat. Anschließend wird eine automatische Auswahl der Pixel entspricht der PM durchgeführt, indem der Zentralregion aus einem “glockenförmig” Anfall von der Summe aller ausgerichteten Linien (z. B. Zentrum ± 2.5σ). Integration des Signals in jeder Zeile ergibt die Membran Fluoreszenz Zeitreihen F(t) in jedem Kanal (g = Grün-Kanal, R = Rot-Kanal). Beachten Sie, dass die Pixelgröße klein genug, z. B. muss < 200 nm, die Form des Punktes zu rekonstruieren Funktion zu verbreiten und finden Sie ihre Mitte, entsprechend der Position des Premierministers. In Gegenwart von erheblichen Immunofluoreszenz Fluoreszenz Zeitreihen in jedem Kanal können mit einer Doppel-exponential-Funktion modelliert und dann mit der folgenden Formel korrigiert:16
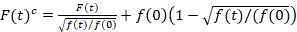 . (1)
. (1)
Es ist wichtig zu beachten, dass diese Formel effektiv korrigiert die Amplituden und Diffusionszeiten aus der Korrelationsanalyse von F(t)c, im Vergleich zu Parameterschätzungen, die sich aus der unkorrigierte F(t)würde. Dann das Auto und Kreuzkorrelation Funktionen (ACFs / CCFs) der Fluoreszenz Signale werden berechnet:
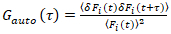 , (2).
, (2).
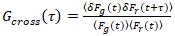 , (3).
, (3).
wo δFich = Fich(t) – 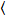 Fich(t)
Fich(t)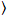 und ich = g, R.
und ich = g, R.
Eine zweidimensionale Diffusion Modell ist dann auf alle Korrelation Funktionen (CFs) ausgestattet:
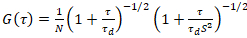 . (4)
. (4)
Dabei bezeichnet N die Anzahl der fluoreszierende Proteine in der Beobachtung Volumen und τd Diffusionszeit für jeden Kanal. Dieses Modell berücksichtigt, dass in der beschriebenen experimentellen Einstellung Diffusion von Proteinen in der Uhr tritt in der X-Z-Ebene, im Gegensatz zu der häufig verwendete Konfiguration der Fluoreszenz Korrelation Spektroskopie (FCS) auf Membranen sondieren Experimente Verbreitung in der X-y-Ebene die konfokale Volumen17. Die Taille w0 und der Struktur Faktor S, beschreibt die Dehnung von fokalen Volumen in Z, S wZ = wZ/w0, stammen aus einer Punkt-FCS Kalibrierung Messung mit spektral ähnliche Farbstoffe und gleichen optischen Einstellungen durchgeführt mit bereits vorhandenen Werten für den Diffusionskoeffizienten DFarbstoff:
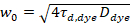 , (5).
, (5).
wo τd, Farbstoff die gemessene durchschnittliche Verbreitung der Farbstoffmoleküle anpassen eines Modells zur dreidimensionalen Diffusion an den Daten entnommen ist Berücksichtigung Konto Übergänge von einem Bruchteil T aller N Moleküle zu einem Triplett-Zustand mit einer Zeitkonstante ττ:
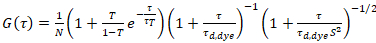 . (6)
. (6)
Schließlich sind die Diffusionskoeffizienten (D), molekulare Helligkeitswerte (ε) und die relative Kreuzkorrelation von sFCCS Daten (rel.cc.) wie folgt berechnet:
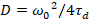 , (7).
, (7).
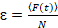 , (8).
, (8).
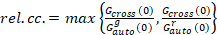 , (9).
, (9).
Wo befindet sich die Amplitude der Kreuzkorrelation Funktion Güberqueren(0) und 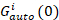 ist die Amplitude der Autokorrelationsfunktion in der ich-th Kanal.
ist die Amplitude der Autokorrelationsfunktion in der ich-th Kanal.
Diese Definition der relativen Kreuzkorrelation, d. h. mit max statt in der Gleichung 9 bedeuten berücksichtigt, die die maximale Anzahl von komplexen zwei Protein-Arten in unterschiedlichen Konzentrationen von begrenzt ist die in einer geringeren Anzahl vorkommenden Arten.
Kreuzkorrelation Anzahl und Helligkeit basiert auf einen Augenblick Analyse der Fluoreszenzintensität für jeden Bildpunkt ein Bildstapel erwarb im Laufe der Zeit an einer festen Position in der Probe in der Regel bestehend aus ca. 100-200 Bildern, mit zwei spektralen Kanäle () g = Grün-Kanal, R = Rot-Kanal). Aus dem zeitlichen Mittelwert 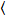 ich
ich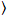 ich und Varianz
ich und Varianz 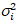 , die molekulare Helligkeit εi und Nummer nich werden in jedem Pixel und Spektralkanal berechnet (Ich = g, R)18:
, die molekulare Helligkeit εi und Nummer nich werden in jedem Pixel und Spektralkanal berechnet (Ich = g, R)18:
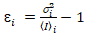 , (10).
, (10).
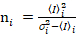 . (11)
. (11)
Es ist wichtig zu beachten, dass im Idealfall eine wahre Photon counting Detektor Formeln zuweisen. Für analoge Systeme gelten die folgenden Gleichungen19,20:
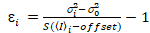 , (12).
, (12).
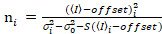 . (13)
. (13)
Hier, S ist der Umrechnungsfaktor zwischen erkannten Photonen und die aufgezeichneten digitalen Grafen 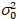 ist das Auslesen Rauschen und Offset bezieht sich auf den Detektor Intensität Offset. Im Allgemeinen sollten diese Mengen für jeden Melder, basierend auf der Messung der Detektor Varianz als eine Funktion der Intensität für stetigen Beleuchtung19, z. B. einer reflektierenden Metalloberfläche oder getrocknete Farbstofflösung kalibriert werden. Der Versatz kann durch Messung der Pulsrate für eine Probe ohne Anregungslicht bestimmt werden. Durch die Durchführung einer linearen Regression der Detektor-assoziierten Varianz
ist das Auslesen Rauschen und Offset bezieht sich auf den Detektor Intensität Offset. Im Allgemeinen sollten diese Mengen für jeden Melder, basierend auf der Messung der Detektor Varianz als eine Funktion der Intensität für stetigen Beleuchtung19, z. B. einer reflektierenden Metalloberfläche oder getrocknete Farbstofflösung kalibriert werden. Der Versatz kann durch Messung der Pulsrate für eine Probe ohne Anregungslicht bestimmt werden. Durch die Durchführung einer linearen Regression der Detektor-assoziierten Varianz 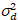 versus Intensität (ich) Grundstück, S und
versus Intensität (ich) Grundstück, S und 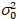 ermittelten19werden können:
ermittelten19werden können:
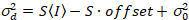 . (14)
. (14)
Zu guter Letzt die Kreuzkorrelation Helligkeit wird in jedem Pixel berechnet und versteht man im Allgemeinen als21
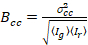 , (15).
, (15).
wo 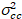 ist die Kreuz-Varianz
ist die Kreuz-Varianz 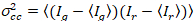 .
.
Zur langlebige Schwankungen zu filtern, werden alle CcN & B Berechnungen durchgeführt nach einem Güterwagen, Filterung, unabhängig für jedes Pixel-22. Kurz, ni, εich (Ich = g, f) und Bcc in Schiebe-Segmente von z. B. 8-15 Frames berechnet. Die so erhaltenen Werte können dann gemittelt werden, um das letzte Pixel Anzahl und Helligkeit Werte zu erhalten.
Stöchiometrie-Analyse
Um die Stöchiometrie der Proteinkomplexe an den Zell-Zell-Kontakten abschätzen zu können, kann die molekulare Helligkeit separat in jedem spektralen Kanal für die sFCCS oder CcN & B Daten analysiert werden. In sFCCS erhält man einen Helligkeitswert pro Messung in jedem Kanal. In CcN & B erhält man ein Histogramm Helligkeit alle Pixel, die die Zell-Zell-Kontakt und der durchschnittliche (oder mittlere) Wert kann als repräsentative Helligkeit für die Messung verwendet werden. Durch die Ausführung der gleichen Analyse auf eine Monomere Referenz können alle Helligkeitswerte normalisiert werden, um den durchschnittlichen Oligomere Zustand der erkannten Proteinkomplexe direkt zu erhalten. An dieser Stelle ist es wichtig, auf das Vorhandensein von nicht-fluoreszierende FPs zu korrigieren, die zu einer Unterschätzung der oligomere Zustand führen kann. Dies erfolgt in der Regel durch die Messung der Helligkeit von einem Homo-dimeres Referenz Protein23,24 mit einfarbigen sFCS oder Nummer und Helligkeit (N & B).
Protocol
Representative Results
Discussion
Die hier beschriebene experimentelle Vorgehensweise ermöglicht die Untersuchung von Protein-Protein Trans Interaktionen bei Zell-Zell-Kontakten, Fluoreszenz Fluktuation Spektroskopie Techniken, nämlich sFCCS und CcN & B. Diese Methoden beinhalten eine statistische Analyse der Fluoreszenz-Schwankungen, die durch zwei spektral getrennte FPs verschmolzen, benutzt von Interesse an einen Kontakt von zwei benachbarten Zellen, jeweils mit dem Ausdruck einer oder der andere Fusionsproteins emittiert. Das Vorhandensein…
Divulgazioni
The authors have nothing to disclose.
Acknowledgements
Diese Arbeit wurde teilweise unterstützt von der Deutschen Forschungsgemeinschaft (DFG) 254850309 zu gewähren. Die Autoren danken Madlen Luckner für kritische Lektüre des Manuskripts.
Materials
| DMEM growth medium | PAN-Biotech | P04-01548 | |
| DPBS w/o: Ca2+ and Mg2+ | PAN-Biotech | P04-36500 | |
| DPBS w: Ca2+ and Mg2+ | PAN-Biotech | P04-35500 | |
| Trypsin EDTA | PAN-Biotech | P10-023100 | |
| TurboFect Transfection Reagent | Thermo Fisher Scientific | R0531 | |
| HEK 293T cells | DSMZ | ACC 635 | |
| Alexa Fluor 488 NHS Ester | Thermo Fisher Scientific | A20000 | |
| Rhodamine B | Sigma-Alderich | 83689-1G | |
| Plasmid DNA | Addgene | NA | See reference 12 (Dunsing et. al., MBoC 2017),for a detailed description of all plasmids |
| 6-well plate | Starlab | CC7672-7506 | |
| 35-mm glass bottom dishes | CellVis | D35-14-1.5-N | |
| Zeiss LSM780 confocal | Carl Zeiss | NA | |
| MATLAB software package | MathWorks | 2015b | |
| Neubauer cell counting chamber | Marienfeld | 640110 |
Riferimenti
- Alberts, B., Johnson, A., Lewis, J., Raff, M., Roberts, K., Walter, P. . Molecular biology of the cell. , (2002).
- Tepass, U., Truong, K., Godt, D., Ikura, M., Peifer, M. Cadherins in embryonic and neural morphogenesis. Nature Reviews Molecular Cell Biology. 1 (2), 91-100 (2000).
- Harris, T. J. C., Tepass, U. Adherens junctions: from molecules to morphogenesis. Nature Reviews Molecular Cell Biology. 11 (7), 502-514 (2010).
- Hernández, J. M., Podbilewicz, B. The hallmarks of cell-cell fusion. Development. 144 (24), 4481-4495 (2017).
- Huppa, J. B., Davis, M. M. T-cell-antigen recognition and the immunological synapse. Nature Reviews Immunology. 3 (12), 973-983 (2003).
- Kaden, D., Voigt, P., Munter, L. -. M., Bobowski, K. D., Schaefer, M., Multhaup, G. Subcellular localization and dimerization of APLP1 are strikingly different from APP and APLP2. Journal of cell science. 122, 368-377 (2009).
- Yap, A. S., Michael, M., Parton, R. G. Seeing and believing: recent advances in imaging cell-cell interactions. F1000Research. 4, 273 (2015).
- Kashef, J., Franz, C. M. Quantitative methods for analyzing cell-cell adhesion in development. Biologia dello sviluppo. 401 (1), 165-174 (2015).
- Soba, P., et al. Homo- and heterodimerization of APP family members promotes intercellular adhesion. The EMBO Journal. 24 (20), 3624-3634 (2005).
- Kim, S. A., Tai, C. -. Y., Mok, L. -. P., Mosser, E. A., Schuman, E. M. Calcium-dependent dynamics of cadherin interactions at cell-cell junctions. Proceedings of the National Academy of Sciences of the United States of America. 108 (24), 9857-9862 (2011).
- Feinberg, E. H., et al. GFP Reconstitution Across Synaptic Partners (GRASP) Defines Cell Contacts and Synapses in Living Nervous Systems. Neuron. 57 (3), 353-363 (2008).
- Dunsing, V., Mayer, M., Liebsch, F., Multhaup, G., Chiantia, S. Direct evidence of amyloid precursor-like protein 1 trans interactions in cell-cell adhesion platforms investigated via fluorescence fluctuation spectroscopy. Molecular biology of the cell. 28 (25), 3609-3620 (2017).
- Schneider, F., et al. Diffusion of lipids and GPI-anchored proteins in actin-free plasma membrane vesicles measured by STED-FCS. Molecular Biology of the Cell. 28 (11), 1507-1518 (2017).
- Bacia, K., Kim, S. A., Schwille, P. Fluorescence cross-correlation spectroscopy in living cells. Nature methods. 3 (2), 83-89 (2006).
- Ries, J., Schwille, P. Studying Slow Membrane Dynamics with Continuous Wave Scanning Fluorescence Correlation Spectroscopy. Biophysical Journal. 91 (5), 1915-1924 (2006).
- Ries, J., Chiantia, S., Schwille, P. Accurate Determination of Membrane Dynamics with Line-Scan FCS. Biophysical Journal. 96 (5), 1999-2008 (2009).
- Chiantia, S., Ries, J., Schwille, P. Fluorescence correlation spectroscopy in membrane structure elucidation. Biochimica et Biophysica Acta (BBA) – Biomembranes. 1788 (1), 225-233 (2009).
- Digman, M. A., Dalal, R., Horwitz, A. F., Gratton, E. Mapping the number of molecules and brightness in the laser scanning microscope. Biophysical journal. 94 (6), 2320-2332 (2008).
- Dalal, R. B., Digman, M. A., Horwitz, A. F., Vetri, V., Gratton, E. Determination of particle number and brightness using a laser scanning confocal microscope operating in the analog mode. Microscopy research and technique. 71 (1), 69-81 (2008).
- Unruh, J. R., Gratton, E. Analysis of Molecular Concentration and Brightness from Fluorescence Fluctuation Data with an Electron Multiplied CCD Camera. Biophysical Journal. 95 (11), 5385-5398 (2008).
- Digman, M. A., Wiseman, P. W., Choi, C., Horwitz, A. R., Gratton, E. Stoichiometry of molecular complexes at adhesions in living cells. Proceedings of the National Academy of Sciences of the United States of America. 106 (7), 2170-2175 (2009).
- Hellriegel, C., Caiolfa, V. R., Corti, V., Sidenius, N., Zamai, M. Number and brightness image analysis reveals ATF-induced dimerization kinetics of uPAR in the cell membrane. The FASEB journal official publication of the Federation of American Societies for Experimental Biology. 25 (9), 2883-2897 (2011).
- Dunsing, V., Luckner, M., Zühlke, B., Petazzi, R. A., Herrmann, A., Chiantia, S. Optimal fluorescent protein tags for quantifying protein oligomerization in living cells. Scientific Reports. 8 (1), 10634 (2018).
- Chen, Y., Johnson, J., Macdonald, P., Wu, B., Mueller, J. D. Observing Protein Interactions and Their Stoichiometry in Living Cells by Brightness Analysis of Fluorescence Fluctuation Experiments. Methods in enzymology. 472, 345-363 (2010).
- . Absolute Diffusion Coefficients: Compilation of Reference Data for FCS Calibration Available from: https://www.picoquant.com/images/uploads/page/files/7353/appnote_diffusioncoeffients.pdf (2010)
- Foo, Y. H., Naredi-Rainer, N., Lamb, D. C., Ahmed, S., Wohland, T. Factors affecting the quantification of biomolecular interactions by fluorescence cross-correlation spectroscopy. Biophysical journal. 102 (5), 1174-1183 (2012).
- Baum, M., Erdel, F., Wachsmuth, M., Rippe, K. Retrieving the intracellular topology from multi-scale protein mobility mapping in living cells. Nature Communications. 5, 4494 (2014).
- Wohland, T., Rigler, R., Vogel, H. The standard deviation in fluorescence correlation spectroscopy. Biophysical journal. 80 (6), 2987-2999 (2001).
- Ries, J., et al. Automated suppression of sample-related artifacts in Fluorescence Correlation Spectroscopy. Optics Express. 18 (11), 11073 (2010).
- Ries, J., Schwille, P. New concepts for fluorescence correlation spectroscopy on membranes. Physical Chemistry Chemical Physics. 10 (24), 3487 (2008).
- Mayer, M. C., et al. Amyloid precursor-like protein 1 (APLP1) exhibits stronger zinc-dependent neuronal adhesion than amyloid precursor protein and APLP2. Journal of Neurochemistry. 137 (2), 266-276 (2016).
- Linkert, M., et al. Metadata matters: access to image data in the real world. The Journal of Cell Biology. 189 (5), 777-782 (2010).
- Trullo, A., Corti, V., Arza, E., Caiolfa, V. R., Zamai, M. Application limits and data correction in number of molecules and brightness analysis. Microscopy Research and Technique. 76 (11), 1135-1146 (2013).
- Nolan, R., et al. nandb-number and brightness in R with a novel automatic detrending algorithm. Bioinformatics. 33 (21), 3508-3510 (2017).
- Hammond, G. R. V., Sim, Y., Lagnado, L., Irvine, R. F. Reversible binding and rapid diffusion of proteins in complex with inositol lipids serves to coordinate free movement with spatial information. The Journal of cell biology. 184 (2), 297-308 (2009).
- Hendrix, J., Dekens, T., Schrimpf, W., Lamb, D. C. Arbitrary-Region Raster Image Correlation Spectroscopy. Biophysical journal. 111 (8), 1785-1796 (2016).
- Hendrix, J., et al. Live-cell observation of cytosolic HIV-1 assembly onset reveals RNA-interacting Gag oligomers. The Journal of cell biology. 210 (4), 629-646 (2015).
- Hendrix, J., Schrimpf, W., Höller, M., Lamb, D. C. Pulsed Interleaved Excitation Fluctuation Imaging. Biophysical Journal. 105 (4), 848-861 (2013).
- Honigmann, A., et al. Scanning STED-FCS reveals spatiotemporal heterogeneity of lipid interaction in the plasma membrane of living cells. Nature Communications. 5 (1), 5412 (2014).
- Chojnacki, J., et al. Envelope glycoprotein mobility on HIV-1 particles depends on the virus maturation state. Nature Communications. 8 (1), 545 (2017).
- Godin, A. G., et al. Revealing protein oligomerization and densities in situ using spatial intensity distribution analysis. Proceedings of the National Academy of Sciences of the United States of America. 108 (17), 7010-7015 (2011).
- Müller, J. D., Chen, Y., Gratton, E. Resolving Heterogeneity on the Single Molecular Level with the Photon-Counting Histogram. Biophysical Journal. 78 (1), 474-486 (2000).
- Kim, S. A., Heinze, K. G., Bacia, K., Waxham, M. N., Schwille, P. Two-Photon Cross-Correlation Analysis of Intracellular Reactions with Variable Stoichiometry. Biophysical Journal. 88 (6), 4319-4336 (2005).
- Jenkins, E., et al. Reconstitution of immune cell interactions in free-standing membranes. Journal of cell science. 132 (4), (2018).

