Hvordan å stabilisere Protein: stabilitet skjermene termisk skifte analyser og Nano differensial skanning Fluorimetry i Virus-X prosjektet
Summary
En protokoll er presentert for å raskt teste temperaturstabilitet proteiner i en rekke forhold gjennom termisk Skift analyser og nano differensial skanning fluorimetry. Buffer systemer, salter og tilsetningsstoffer, sammen er med tre unike stabilitet skjermer, assayed med proteiner å identifisere egnet bufferne for funksjonell og strukturelle studier.
Abstract
Horizon2020 Virus-X prosjektet ble etablert i 2015 for å utforske virosphere av valgte ekstreme naturtyper og oppdage romanen virale proteiner. For å vurdere den potensielle bioteknologiske verdien av disse proteinene, analyse av protein er strukturer og funksjoner en sentral utfordring i dette programmet. Stabiliteten av protein prøven er viktig å gi meningsfylt analyseresultatene og øke crystallizability av målene. Termisk Skift analysen (TSA), en fluorescens-basert teknikk, er etablert som en populær metode for å optimalisere betingelsene for protein stabilitet i høy gjennomstrømming. I TSAs er de ansatt fluorophores ytre, miljøvennlig fargestoffer. Et alternativ, tilsvarende teknikk er nano differensial skanning fluorimetry (nanoDSF), som er avhengig av protein innfødt fluorescens. Vi presenterer her en roman osmolyte skjerm, en 96-stand skjerm av organisk tilsetningsstoffer utformet for å veilede krystallisering studier gjennom foreløpige TSA eksperimenter. Sammen med tidligere utviklet pH og salt skjermer gir settet med tre skjermer en omfattende analyse av protein stabilitet i en rekke buffer systemer og tilsetningsstoffer. Nytten av skjermene er demonstrert i TSA og nanoDSF analyse av lysozyme og Protein X, et mål protein av viruset-X prosjektet.
Introduction
Mange bioteknologisk nyttig enzymer stammer fra viral kilder, slik som tobakk etch virus (TEV) protease1 og menneskelige rhinovirus type 3 C (HRV 3 C) protease2. Horizon2020 Virus-X prosjekt (figur 1)3. Målet med dette programmet er (a) for å utvide rekkevidden av egenskapene til kjente enzym familier og (b) for å karakterisere romanen enzymer i ennå ukjent funksjon (enzym X). Krystallografisk struktur besluttsomhet spiller en avgjørende rolle i målet protein karakterisering, spesielt i de tilfellene hvor protein sekvensene ha utviklet seg utover anerkjennelse4. Protein stabilitet er en nøkkelfaktor i krystallisering prosessen; prøver må være conformationally homogent og strukturelt lyd over en periode til skjemaet høy kvalitet, diffracting krystaller. Videre er det viktig for aktivitet analyser som proteiner finnes i deres aktive eksteriør, som kan være ledes av et gunstig molekylær miljø.
Til tross for utviklingen i teknologien tilgjengelig for crystallographers forblir protein krystallisering en tidkrevende og arbeidskrevende empirisk prosess5. Foreløpig Biofysiske eksperimenter for å forbedre protein stabiliteten i løsningen gir klart et bedre utgangspunkt for protein krystallisering og bruker vanligvis bare en relativt liten mengde protein eksempel6,7, 8,9. Det store antallet mål proteiner til studeres i dette prosjektet også nødvendiggjør skalerbare, høy gjennomstrømming stabilitet analyser. En av de mest populære metodene for pre krystallisering Biofysiske karakteristikk av proteiner er termisk Skift analysen (også kjent som TSA eller differensial skanning fluorimetry, DSF)10,11.
TSAs benytter en miljøsensitive fluorescerende farge til å spore den termiske denaturering av protein prøver. Mange brukte fargestoffer har variabel fluorescens aktivitet avhengig av polariteten til miljøet, ofte viser en høy fluorescens utgang i hydrofobe miljøer, men gjennomgår rask slukke i polar miljøer12. Proteiner føre generelt uttalt økning i dye fluorescens som sine hydrofobe kjerner bli eksponert under rødsprit, ofte etterfulgt av en nedgang i dye fluorescens ved svært høye temperaturer som proteiner begynner å samlet (figur 2).
Mens en hydrophobicity-sensitive fargestoff er et godt valg for en generell bruk TSA fargestoff, kan det være uegnet for proteiner med store, løsemiddel-eksponerte hydrofobe regioner, som ofte viser detrimentally høye fluorescens. Fluorophores med alternative former for handlingen eksisterer (se diskusjon), men i stedet kan det være ønskelig å spore rødsprit gjennom iboende protein fluorescens med nanoDSF.
Tryptofan rester som er begravet i upolart regioner i et protein fluoresce med et utslipp maksimalt 330 nm. Som et protein utvalg utfolder seg, og disse rester bli utsatt for en polar løsemiddel gjennomgår utslipp maksimal en bathochromic endring til 350 nm13. nanoDSF utnytter dette skiftet i utslipp maksimal å undersøke utfoldelsen av et protein utvalg uten behov for ytre fluorophores14.
Smelt kurver viser enkelt rødsprit trinn kan analyseres ved å tilpasse dataene til en Boltzmann sigmoidal modell. Temperaturen på vendepunkt unfolding overgangen (Tm) er brukt som et kvantitativt mål for protein termisk stabilitet og en målestokk for å sammenligne favorability av ulike forhold.
Smelt kurver av samme proteinet i ulike forhold har noen ganger en grad av heterogenitet som kan gjøre en Boltzmann sigmoidal passende unfeasible. For å skille Tm verdier fra data som avviker fra klassisk kurve topologi, kan numeriske metoder brukes som ansatt i NAMI, en åpen kildekode TSA data analyse program11. Alternative termodynamisk rammer kan også brukes til å analysere mer komplekse buer med flere rødsprit trinn, for eksempel ProteoPlex metodikk15.
Stabilitet skjermene ble laget for bruk i TSA og nanoDSF eksperimenter å raskt identifisere gunstige vilkår for et mål protein (Figur 3, skjermen komposisjoner er tilgjengelig i ytterligere opplysninger). Informasjonen samlet med skjermene kan brukes på mange stadier av krystallografisk rørledning inkludert: prøve lagringen; rensing, minimere utbytte forlis gjennom protein utspiller seg under en renselsesprosess; analysen design, forsterke protein funksjonalitet i aktivitet analyser med termisk stabilisere buffere og krystallisering, guiding rasjonelt utformet krystallisering prøvelser.
Velge en egnet buffer system basis for et protein utvalg er avgjørende; inkompatibel pH-verdier kan føre til deaktivering eller denaturering av et protein. Men kan tilstedeværelsen av co krystallisert buffer molekyler løst i en rekke X-ray krystall strukturer (tabell 1) også være indikativ av en stabiliserende effekt som separat for enkel pH regulering og i stedet stammer fra kjemiske vise egenskaper av buffer molekylet.
Formulert med flere gods buffere17,18,19 sammen med andre vanligvis biologisk-kompatible buffer systemer, er pH-skjermen utformet for å deconvolute kjemiske effekten av et buffer molekyl på protein stabilitet fra den faktiske pH av resulterende løsningen. Ved å gi tre pH-verdier for hvert buffer system og innlemme pH verdien redundans mellom ulike systemer, kan pH skjermen identifisere både gunstige pH-verdier og gunstige buffer systemer for et mål protein.
Salt skjermen inneholder vanlige laboratorium salter som chaotropes, komplekseringsmidler, tungmetaller og reduksjonsmidler. Skjermen kan gi en generell ytelsesindikator slektskap av et protein utvalg til miljøer med høy ioniske styrke, men hver undergruppe av forbindelser kan også gi informasjon om potensielle strukturen i et protein. For eksempel kunne en chelant betydelig destabilisere et protein være indikativ av viktige strukturelle metaller i utvalget. Hvis prøven også sterkt stabiliseres ved en metall kation i skjermbildet, kan dette gi lovende utgangspunkt for videre strukturelle eksperimenter.
Osmolytes er løselig forbindelser som påvirker osmotisk egenskapene for miljøet. I naturen, kan de brukes som “kjemiske chaperones”, håndheve folding av uordnede proteiner og stabilisere dem, spesielt i stress forhold20,21,22. Disse egenskapene gjør dem attraktive tilsetningsstoffer i protein krystallografi; brukes som cryoprotectants i crystal høsting, montering og lagring behandler23. Osmolytes’ potensielle bruk strekker seg også til rensing av proteiner. En betydelig andel av rekombinante proteinene i E. coli kan være uløselig og vanskelig å komme i opprinnelig tilstand ved hjelp av standard rensing metoder. Osmolytes kan brukes til å stabilisere og berge proteiner fra uløselig fraksjoner, økende rensing gir24.
Osmolyte skjermen ble utformet med etablerte forbindelser i Protein databank oppføringer25 og26 databasen Dragon Explorer of Osmoprotection-Associated veier (DEOP) og optimalisert iteratively bruke standard proteiner. Skjermen er bygget rundt åtte underklasser av osmolyte: glyserol, sukker og polyols, ikke-rengjøringsmiddel sulfobetaines (NDSBs), betaines og deres analoger, organophosphates, dipeptides, aminosyrer og deres derivater og en siste diverse gruppe. Hver osmolyte finnes i flere konsentrasjoner basert på løselighet og effektiv konsentrasjon områder for sammenligning.
Protocol
Representative Results
Discussion
Viktige sider i protokollen inkludere sentrifugering trinn og skikkelig tetting av 96-brønns plate for TSA eksperimenter (trinn 1.5). Sentrifugering sikrer at betingelsen protein prøven og skjermen komme i kontakt og bland. I tillegg hvis en utette plate brukes for en TSA eksperimentet, er det en betydelig risiko løsemiddel fordamper hele eksperimentet, forårsaker en økning i prøven konsentrasjon og øke sjansen for tidlig protein aggregering.
TSAs og nanoDSF er mottakelig for et bredt spekter av protein prøver; de aller fleste av prøver kan produsere interpretable smelte kurver med en hydrophobicity-baserte reporter fargestoff eller gjennom dye-ledig nanoDSF. Hvis standard fluorescens kilder ikke er egnet for protein, er den enkleste endringen protokollen som kan utforskes valg av fluorophore. Flere alternative fargestoffer kan være egnet for TSA eksperimenter. Eksempler inkluderer N-[4-(7-diethylamino-4-methyl-3-coumarinyl)phenyl]maleimide (CPM), en forbindelse som fluoresces etter reagere med en thiol27, og 4-(dicyanovinyl) julolidine (DCVJ), et stoff som varierer sin fluorescens basert på den stivhet av omgivelsene, øke sin fluorescens som et protein eksempel utfolder seg28,29 (sistnevnte fargestoff krever ofte høye konsentrasjoner av utvalg).
Alternative metoder for smelte curve analyse er tilgjengelige hvis Tm ikke automatisk beregnes av instrumentet. Hvis dataene er homogen og eneste rødsprit trinn er tydelig i smelte kurvene, kan avkortet dataset monteres i en Boltzmann sigmoid med følgende ligning:
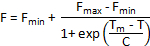
Der F er fluorescens intensiteten temperatur T, Fmin og Fmax fluorescens intensiteten før og etter rødsprit overgangen, Tm er henholdsvis midtpunktet temperaturen av rødsprit overgang og C er skråningen på Tm. Denne metoden fungerer bra for enkel totrinns rødsprit prosesser, er det uegnet for komplekse smelte kurver med flere overganger.
En av de store fordelene med TSA er dens tilgjengelighet; TSA eksperimenter kan utføres i ethvert RT PCR-system med filtre på egnet bølgelengder for fluorescens fargestoff ansatt. Dette kombinert med den lave kostnaden for forbruksvarer, betjening og relativt lav mengde protein trengs, gjør TSA en verdifull teknikk for et bredt spekter av prosjektet skalaer, både i industrien og akademia.
Og angir gunstige buffer forhold, inneholder skjermene noen brønner som kan gi hint til tilstedeværelsen av strukturelle metaller i et eksempel protein. Brønner som kan være av spesiell interesse i skjermbildet salt er G6 og G7, som inneholder 5 mM EDTA og 5 mM EGTA, henholdsvis. Betydelig termisk destabilisering i disse brønnene kan være tegn på viktig metall ioner i protein som er sequestered av komplekseringsmidler. Forbindelser i skjermbildet osmolyte kan også potensielt tilby ledetråder til funksjonen av et protein. Mange av forbindelsene i skjermen tilhører klasser av molekyl som er vanlige underlag av enzymer. For eksempel tilskrives generell stabilisering by av saccharides (finnes i brønner A11-B10) for lysozyme deres strukturelle likhet med etablerte underlag av enzym, N-acetylglucosamine oligomers30.
TSA og nanoDSF protokollene skissert ovenfor kan også tilpasses til å studere protein-ligand interaksjoner. Ligander som binder seg spesifikt til et protein kan øke sin termisk stabilitet ved å innføre nye samhandlinger i komplekset. En doseavhengig positiv endring i protein Tm er en lovende tegn på en vellykket protein-ligand interaksjon. Hastighet, gjennomstrømning og lav pris av screening sammensatte biblioteker med TSAs har gjort det en svært populær metode i tidlig stadium medisiner.
Optimaliserer buffer betingelsene målet proteiner og deres ligand komplekser kan være avgjørende for prosjektets suksess, som mange litteratur eksemplene viser31,32,33,34. Med en typisk analysen tar under 2t inkludert oppstillingstid, representerer TSAs og nanoDSF kombinert med stabilitet skjermer en rask, billig teknikk for bufferen optimaliseringer.
Divulgazioni
The authors have nothing to disclose.
Acknowledgements
Dette prosjektet har mottatt finansiering fra europeiske Research Council (ERC) under EUs horisonten 2020 forskning og innovasjon programmet (grant avtalen n ° 685778). Dette arbeidet ble støttet av bioteknologi og Biological Sciences Research Council (BBSRC, gi tall BB/M011186/1, BB/J014516/1). DB takk til BBSRC doktor trening partnerskap Newcastle-Liverpool-Durham for en studentship og Durham University avdeling av biovitenskap for å bidra mot finansiering dette arbeidet. Vi takker Ian Edwards for hans hjelp og Durham University avdeling av kjemi massespektrometri avdelingen for instrumental analyse av Protein X. Vi er takknemlige for Arnthor Ævarsson for sitt arbeid med Virus-X prosjekt og takk også til Claire Hatty og NanoTemper GmbH for utlån og bistå med Prometheus NT.48 system for dette prosjektet. Til slutt, takk til Frances Gawthrop og Tozer frø for deres støtte som en del av BBSRC iCASE award.
Materials
| Lysozyme | Melford Laboratories | L38100 | Crystallised and lyophilised chicken egg white lysozyme. |
| The Durham pH Screen | Molecular Dimensions | MD1-101 | 96-well protein stability screen. See above for contents. |
| The Durham Salt Screen | Molecular Dimensions | MD1-102 | 96-well protein stability screen. See above for contents. |
| The Durham Osmolyte Screen | Various | #N/A | 96-well protein stability screen, not commercially available at the time of publication. See above for contents. |
| SYPRO Orange | Invitrogen | S6651 | Widely used fluorescent dye for protein staining in gels and DSF. |
| 96-well PCR Plate | Starlab | 1403-7700 | Semi-skirted clear plastic for use with AB 7500 Fast RT-PCR System. |
| 7500 Fast Real-time PCR System | Applied Biosystems | 4362143 | 96-well format RT-PCR system. Alternative systems can be used. Analysis of data performed using free, open-access software NAMI. AB software tailored to DSF experiments using the 7500 Fast available at additional cost. |
| Prometheus NT.48 | NanoTemper Technologies | #N/A | Label-free DSF system with up to 48-sample capacity. Can calculate unfolding temperatures (Tm and Tonset), critical denaturant concentrations (Cm), free folding energy (ΔG and ΔΔG), and aggregation results (Tagg) using built-in software. |
| Prometheus NT.48 Series nanoDSF Grade Standard Capillaries | NanoTemper Technologies | PR-C002 | Prometheus NT.48 Series nanoDSF Grade Standard Capillaries. "High sensitivity" variants are available at a higher cost for use with low-concentration samples (<200 µg ml-1). |
Riferimenti
- Kapust, R. B., Waugh, D. S. Controlled intracellular processing of fusion proteins by TEV protease. Protein Expression and Purification. 19 (2), 312-318 (2000).
- Cordingley, M. G., Register, R. B., Callahan, P. L., Garsky, V. M., Colonno, R. J. Cleavage of small peptides in vitro by human rhinovirus 14 3C protease expressed in Escherichia coli. Journal of Virology. 63 (12), 5037-5045 (1989).
- Hjorleifsdottir, S., Aevarsson, A., Hreggvidsson, G. O., Fridjonsson, O. H., Kristjansson, J. K. Isolation, growth and genome of the Rhodothermus RM378 thermophilic bacteriophage. Extremophiles. 18 (2), 261-270 (2014).
- Alva, V., Nam, S. Z., Söding, J., Lupas, A. N. The MPI bioinformatics Toolkit as an integrative platform for advanced protein sequence and structure analysis. Nucleic Acids Research. 44, 410-415 (2016).
- McPherson, A. Protein Crystallization. Methods in molecular biology. 1607, 17-50 (2017).
- Ericsson, U. B., Hallberg, B. M., DeTitta, G. T., Dekker, N., Nordlund, P. Thermofluor-based high-throughput stability optimization of proteins for structural studies. Analytical Biochemistry. 357 (2), 289-298 (2006).
- Reinhard, L., Mayerhofer, H., Geerlof, A., Mueller-Dieckmann, J., Weiss, M. S. IUCr Optimization of protein buffer cocktails using Thermofluor. Acta Crystallographica Section F Structural Biology and Crystallization Communications. 69 (2), 209-214 (2013).
- Boivin, S., Kozak, S., Meijers, R. Optimization of protein purification and characterization using Thermofluor screens. Protein Expression and Purification. 91 (2), 192-206 (2013).
- Kozak, S., Lercher, L., Karanth, M. N., Meijers, R., Carlomagno, T., Boivin, S. Optimization of protein samples for NMR using thermal shift assays. Journal of Biomolecular NMR. 64 (4), 281-289 (2016).
- Semisotnov, G. V., Rodionova, N. A., Razgulyaev, O. I., Uversky, V. N., Gripas’, A. F., Gilmanshin, R. I. Study of the “molten globule” intermediate state in protein folding by a hydrophobic fluorescent probe. Biopolymers. 31 (1), 119-128 (1991).
- Grøftehauge, M. K., Hajizadeh, N. R., Swann, M. J., Pohl, E. Protein-ligand interactions investigated by thermal shift assays (TSA) and dual polarization interferometry (DPI). Acta Crystallographica Section D: Biological Crystallography. 71, 36-44 (2015).
- Steinberg, T. H., Jones, L. J., Haugland, R. P., Singer, V. L. SYPRO Orange and SYPRO Red Protein Gel Stains: One-Step Fluorescent Staining of Denaturing Gels for Detection of Nanogram Levels of Protein. Analytical biochemistry. 239, 223-237 (1996).
- Burstein, E. A., Vedenkina, N. S., Ivkova, M. N. Fluorescence and the location of tryptophan residues in protein molecules. Photochemistry and Photobiology. 18 (4), 263-279 (1973).
- Haffke, M., Rummel, G., Boivineau, J., Münch, A., Jaakola, V. -. P. nanoDSF: label-free thermal unfolding assay of G-protein-coupled receptors for compound screening and buffer composition optimization. Application Note NT-PR-008. , (2016).
- Chari, A., et al. ProteoPlex: stability optimization of macromolecular complexes by sparsematrix screening of chemical space. Nature Methods. 12 (9), 859-865 (2015).
- Laskowski, R. A. PDBsum: summaries and analyses of PDB structures. Nucleic Acids Research. 29 (1), 221-222 (2001).
- Good, N. E., Winget, G. D., Winter, W., Connolly, T. N., Izawa, S., Singh, R. M. Hydrogen ion buffers for biological research. Biochimica. 5 (2), 467-477 (1966).
- Good, N. E., Izawa, S. Hydrogen ion buffers. Methods in enzymology. 24, 53-68 (1972).
- Ferguson, W. J., et al. Hydrogen ion buffers for biological research. Analytical biochemistry. 104 (2), 300-310 (1980).
- Welch, W. J., Brown, C. R. Influence of molecular and chemical chaperones on protein folding. Cell stress & chaperones. 1 (2), 109-115 (1996).
- Diamant, S., Eliahu, N., Rosenthal, D., Goloubinoff, P. Chemical chaperones regulate molecular chaperones in vitro and in cells under combined salt and heat stresses. The Journal of biological chemistry. 276 (43), 39586-39591 (2001).
- Yancey, P. H. Organic osmolytes as compatible, metabolic and counteracting cytoprotectants in high osmolarity and other stresses. Journal of Experimental Biology. 208 (15), 2819-2830 (2005).
- Garman, E. F., Owen, R. L. Cryocooling and radiation damage in macromolecular crystallography. Acta Crystallographica Section D Biological Crystallography. 62 (1), 32-47 (2006).
- de Marco, A., Vigh, L., Diamant, S., Goloubinoff, P. Native folding of aggregation-prone recombinant proteins in Escherichia coli by osmolytes, plasmid- or benzyl alcohol- overexpressed molecular chaperones. Cell Stress & Chaperones. 10 (4), 329 (2005).
- Berman, H. M., et al. The protein data bank. Nucleic acids research. 28 (1), 235-242 (2000).
- Bougouffa, S., Radovanovic, A., Essack, M., Bajic, V. B. DEOP: A database on osmoprotectants and associated pathways. Database. 2014, 1-13 (2014).
- Alexandrov, A. I., Mileni, M., Chien, E. Y. T., Hanson, M. A., Stevens, R. C. Microscale Fluorescent Thermal Stability Assay for Membrane Proteins. Structure. 16 (3), 351-359 (2008).
- Kung, C. E., Reed, J. K. Fluorescent molecular rotors: a new class of probes for tubulin structure and assembly. Biochimica. 28 (16), 6678 (1989).
- Iio, T., Itakura, M., Takahashi, S., Sawada, S. 9-(Dicyanovinyl)julolidine binding to bovine brain calmodulin. Journal of biochemistry. 109 (4), 499-502 (1991).
- Veros, C. T., Oldham, N. J. Quantitative determination of lysozyme-ligand binding in the solution and gas phases by electrospray ionisation mass spectrometry. Rapid Communications in Mass Spectrometry. 21 (21), 3505-3510 (2007).
- Kean, J., Cleverley, R. M., O’Ryan, L., Ford, R. C., Prince, S. M., Derrick, J. P. Characterization of a CorA Mg2+ transport channel from Methanococcus jannaschii using a Thermofluor-based stability assay. Molecular membrane biology. 25 (8), 653-661 (2008).
- Geders, T. W., Gustafson, K., Finzel, B. C. Use of differential scanning fluorimetry to optimize the purification and crystallization of PLP-dependent enzymes. Acta Crystallographica Section F. 68 (5), 596-600 (2012).
- Morgan, H. P., Zhong, W., McNae, I. W., Michels, P. A., Fothergill-Gilmore, L. A., Walkinshaw, M. D. Structures of pyruvate kinases display evolutionarily divergent allosteric strategies. Royal Society open science. 1 (140120), (2014).
- Moretti, A., Li, J., Donini, S., Sobol, R. W., Rizzi, M., Garavaglia, S. Crystal structure of human aldehyde dehydrogenase 1A3 complexed with NAD+ and retinoic acid. Scientific reports. 6 (35710), (2016).

