制造淀粉样蛋白-β-分泌阿尔金酸微珠,用于模拟阿尔茨海默氏病
Summary
该协议说明了一种细胞封装方法,通过快速物理凝胶化藻酸盐来固定细胞。获得微珠允许随着时间的推移对淀粉样蛋白-α进行受控和持续分泌,并可用于研究在体外和体内的分泌淀粉样蛋白的影响。
Abstract
根据淀粉样级联假说,阿尔茨海默氏病(AD)发展的最早诱因是有毒淀粉样蛋白-β(A+)片段的积累,最终导致该疾病的经典特征:淀粉样斑块,神经纤维纠结和突触和神经元损失。缺乏反映疾病进展的相关非转基因前模型是阻碍发现有效药物治疗的主要因素之一。为此,我们开发了一种用于制造含有淀粉样分泌细胞的藻酸盐微珠的规程,用于研究慢性A+生产的影响。
在这项研究中,使用了以前用人类APP基因转染的中国仓鼠卵巢细胞,分泌A+(即7PA2细胞)。通过封装在藻酸盐中的7PA2细胞,建立了持续释放A+的三维(3D)体外模型。该工艺经过优化,以500-600μm的珠直径为目标,用于进一步进行体内研究。对7PA2细胞封装在藻酸盐中进行了优化,改变了制造参数,如藻酸盐浓度、凝胶流速、静电电位、头部振动频率、凝胶溶液。随着时间的推移,对分泌A+的水平进行了分析,并比较了藻酸盐珠和标准细胞培养方法(高达96小时)。
发现1.5 x 106 7PA2细胞/mL的浓度和2%(w/v)的藻酸盐浓度与HEPES缓冲,随后在0.5M氯化钙中凝胶化5分钟,可制造最稳定的微珠。制造微珠是1)的均匀大小,2)平均直径为550μm,3)包含约100-150个细胞每个微珠和4)能够分泌A+。
总之,我们针对含有淀粉样蛋白7PA2细胞的稳定藻酸盐微珠的生成优化方法,可以生成AD在体外和体内的重要方面。
Introduction
由于大脑的复杂性和复杂性,神经退行性疾病建模具有挑战性。在阿尔茨海默氏病 (AD) 中,突触功能的逐渐丧失和神经元的死亡被认为是淀粉样蛋白β (A+) 肽在淀粉样蛋白前体异常处理后持续过度生产和积累的下游效应蛋白质(APP)根据淀粉样级联假说1。
为了了解这种淀粉样蛋白引起的病理机制,并有助于确定新的治疗靶点,科学家开发了各种体内临床前模型。一类模型利用博鲁斯将合成A+肽注射到大鼠大脑中2,3,4。这种模型的主要局限性是,它们依赖于单点或重复处理,在高浓度的A+肽沉积在一次。这与疾病5中A+释放的慢性、持续性质不一致。另一类体内模型是转基因动物模型,表达一个或多个基因突变与疾病6、7、8、9的家族变异有关。 10.然而,由于家族性AD只占所有阿尔茨海默氏症病例的不到5%,这些模型在人类中转化为零星的AD的相关性是值得怀疑的12。转基因方法的另一个缺点是从出生开始加速A+形成,这转化为认知功能缺陷和病理变化过快和积极,类似于患者零星AD的疾病进展12.例如,5x FAD 模型在 1.5 个月内产生斑块13。
有趣的是,这两个类别导致与AD研究2,3,4,5,6相关的认知功能的变化,有时它们伴随着疾病的病理特征的出现,如淀粉样斑块6,8,tau磷酸化6,7和/或突触和神经元损失7,9, 14.但是,虽然这些类型的模型可能让我们深入了解大脑中高浓度淀粉样蛋白的影响,这些淀粉样蛋白通常与 AD 的后期阶段相关,但它们未能反映早期的变化,以响应长期和持续接触 A_ 肽12,如突触标记15和细胞外基质16中分量的改变表达。因此,仍然需要创建一个慢性模型,更准确地说明持续A+分泌对体内认知的影响,并说明病理学的变化。
为此,我们开发了一个系统,通过固定水凝胶微珠中的淀粉样分泌细胞,从而以受控的方式持续分泌A+,随后可以植入成年大鼠大脑中,以模拟方面零星的AD。
藻酸盐是选定的生物材料,因为它是生物相容性,不会诱导任何不良反应时植入体内17。藻酸盐水凝胶中的细胞封装在过去四十年中已经建立得很好。其翻译到诊所的第一个例子被报告用于治疗1型糖尿病17。最早成功封装兰格汉岛的报告可追溯到1980年。移植含有胰岛素分泌细胞的微珠,彻底改变了糖尿病患者恢复胰腺功能的治疗方案,无需胰岛素注射治疗18。这些工作报告细胞封装如何保护它们免受外部应力,无论是机械或化学。事实上,藻酸珠作为屏障,将细胞从周围环境中分离,保持其表型,同时允许充分访问周围的介质以获得营养和清除细胞副产品19。此外,使用藻酸盐允许匹配软组织的机械特性20。藻酸盐水凝胶可以调整到1-30 kPa的刚度,通过简单地改变藻酸盐浓度和交联密度20,21。这是一个重要方面,不仅保持体外封装细胞的体型表达,而且避免在体内移植后产生任何炎症效应。
在此协议中,使用7PA2细胞——一种用人类APP V717F突变基因23稳稳转染的中国仓鼠卵巢细胞系。这些细胞不断产生APP的催化产物,包括A+1-4224,25,并已用于生成A+作为合成生产的替代品,在临床前,急性体内研究26。我们描述了一种在”软”藻酸盐微珠中固定7PA2细胞的制造方法,旨在允许生物分子持续分泌。作为概念的证明,我们报告A+1-42肽随时间的释放。使用的藻酸盐是一种低粘度藻酸盐,分子量为120,000-190,000克/摩尔,锰与古音比为1.56(M/G)。
在进一步的研究中,这些微珠可以安全地移植到与AD相关的大鼠大脑区域(例如海马区),以研究慢性A+分泌对体内行为和病理前体的影响。此外,该系统还可用于研究体外和体外慢性A+释放的影响。例如,含有7PA2的藻酸盐微珠可以在体外与神经元或天体化培养物共同培养,以评估慢性A+暴露对与AD相关的细胞机制的影响。此外,该方法还可用于检查慢性A+生产与外体电生理学长期强效之间的关系。
该协议的亮点是制造方法的模块化和灵活性,通过微调制造参数,使具有目标尺寸的藻酸盐珠成为可能。根据不同的应用,可以调整协议,以获得关于微珠大小、封装细胞密度和微珠刚度的定制目标。该协议可用于各种细胞类型的封装,开发更相关的三维(3D)体外模型,研究不同的病理。我们最近报道了如何使用藻酸盐封装细胞来模拟癌症进展20的早期阶段。
封装过程的概念基于通过喷嘴悬浮在藻酸盐溶液中的细胞层状喷射。振动头以受控的频率干扰喷射,从而产生大小相等的藻酸盐液滴。外部电场允许分离形成的藻酸盐基液滴,当与富在二价离子(如钙离子)中的溶液接触时,可以快速交叉链接,保持其球形。凝胶溶液中的孵育允许形成球形微珠,其中含有细胞的均质物理水凝胶27。微珠和藻酸水凝胶的目标大小允许长期(数周)与细胞培养基交换营养和氧气。图 1A显示了所用封装装置的示意图(图 1B)。
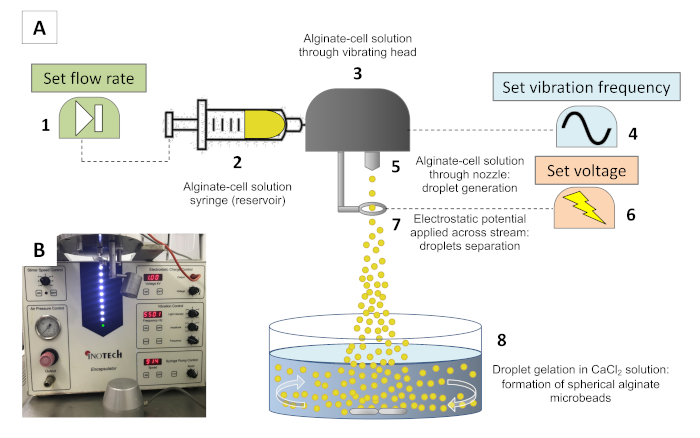
图 1:封装系统。(A) 封装系统的原理表示。藻酸细胞悬浮液被加载到注射器 (2) 中,然后以注射器泵 (1) 处设定的挤出速度通过储液罐进料。在储液罐中,振动帽 (3) 以波形发生器 (4) 设置的频率振动,以相等的时间间隔中断流,形成大小相等的液滴。当溶液通过喷嘴 (5) 馈入并形成液滴时,在电压发生器 (6) 设置的电极 (7) 上施加静电电位,该电极对液滴表面稍有电荷,使流因排斥而扩散静电。当液滴与凝胶浴(8)啮合时,Ca2+驱动的藻酸盐交联会导致球形微珠的形成。(B) 在制造藻酸盐微珠之前封装器的照片。请点击此处查看此图的较大版本。
根据预期用途,可以更改微珠大小。为了控制微珠的大小,对图1A和协议中概述的各种参数进行了相应的调整。使用的喷嘴的内径对液滴的大小有重大影响;进一步调整封装参数,即挤出速度、振动频率和电压,是实现一致尺寸分布的关键。表1概述了不同的参数如何改变通过该系统实现的微珠的大小。
| 参数 | 喷嘴尺寸 | 振动频率 | 流量 | 电极电压 |
 |
 |
 |
 |
|
| 珠子尺寸 |
 
|
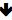 |
 |
– |
表 1:制造参数及其对微珠尺寸的影响。该表说明了每个参数如何影响所制造微珠的产生尺寸,而不管喷嘴和所用溶液的粘度如何。
Protocol
Representative Results
Discussion
本文概述的方法对于封装实现小尺寸的藻酸盐微珠分布的细胞非常有用。它还提供了在免疫隔离环境中生长细胞的优势,保护细胞免受外部压力。此外,在藻酸盐中封装细胞更密切地模拟生理条件,特别是细胞与细胞的相互作用和基质刚度20。这些因素对于后续在相关应用中的使用都特别重要,例如体内移植,排除了周围组织的潜在免疫反应17。此外,该协议的一个主要优点是根据感兴趣的应用易于调谐:可以修改协议并优化制造更大或更小、更软或更硬的珠子的参数。所述方法用于制造足够小的珠子,以便注射微创方法,足够大,足以承载大量细胞,并提供足够的 A+ 释放,从而产生可观察到的行为和病理效应在动物模型中注射。
该协议的成功取决于许多关键步骤。小心的细胞处理和最佳的细胞培养技术对于维持细胞活力和功能很重要20,28。使用标准培养条件确保保持7PA2细胞的正常功能,如观察。与 2D 培养相比,这允许封装的单元为 A+1-42提供类似的释放配置文件。此外,与高粘度藻酸盐溶液相比,低粘度藻酸盐溶液可确保更好的结果。这确保了均匀的层状射流通过喷嘴挤压,并在制造珠27的基质内均匀分布细胞。用于封装细胞的材料必须具有非常快速的凝胶机制,允许保留形状。
该协议的另一个关键步骤是在凝胶化后处理制造微珠。在这里,我们展示了使用大孔塑料移液器转移珠子的检索。或者,将含有微珠的氯化钙溶液倒入网状过滤器中,可用于珠子检索。大型(5、10 或 25 mL)血清学移液器可用于绘制微珠,然后通过网状过滤器进行清洗,而不是浇注。与浇注相比,这样做的好处是对程序无菌性更有信心。然而,其局限性是,如果一些珠子被移液器压缩,可能会失真,此外,如果大量微珠没有被拯救,它们可能会降低产量。
这种方法已经用于封装不同的细胞系,以建模和研究不同的疾病(例如,从封装的胰腺胰岛释放胰岛素)。我们方法的新颖性是利用该协议产生的微珠的移植,作为模拟体内阿尔茨海默氏病重要方面的有用方法。当比较A+从封装细胞的释放配置文件(图4)与由bolus注射产生的A+水平(如在其他研究3,26中报告),A+的更慢性和持续释放可以预期。图 6说明了可能实现的预测趋势。使用这个系统进行体内建模更与疾病的进展方式相关,在药物发现和开发中可能更有用。
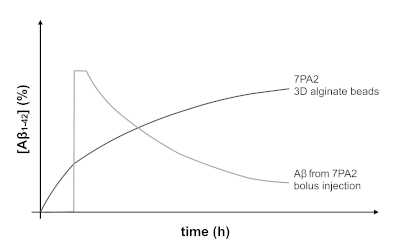
图 6:与博鲁斯注射相比,从封装的7PA2细胞中预测A+1-42的释放配置文件。含有7PA2的微珠的A+释放的轮廓允许测试与AD相关的动物模型中慢性和持续A+的影响。相反,Bolus注射会在短时间内产生A+水平的峰值,然后迅速清除A+的大脑。请点击此处查看此图的较大版本。
Divulgazioni
The authors have nothing to disclose.
Acknowledgements
作者要感谢卡延·苏雷斯帕兰先生、乔纳森·乌贝图博士、多米尼克·格鲁津斯基先生、陈昭小姐和蒂埃里博士试点,感谢他们在优化藻酸盐微珠制造、细胞培养和A+检测方面所做的帮助,以及有用的科学讨论。
Materials
| µManager software | Vale Lab, UCSF, USA | v.1.46 | |
| 0.22 um PES filter | Merck, UK | SLGP033RS | |
| 15mm Netwell insert 74 um mesh filter | Constar, usa | #3477 | |
| Alginic acid sodium salt from brown algae | Sigma-Aldrich,uk | A0682 | |
| Calcium chloride | Sigma-Aldrich,uk | C1016 | |
| CellTiter96 AQueous One Solution cell proliferation assay | Promega, USA | G3580 | |
| Encapsulator | Inotech | IE-50 | serial no. 05.002.01-2005 |
| HEPES | Sigma-Aldrich,uk | H4024 | |
| Hu Aβ 1-42 ELISA | ThermoFisher, UK | KHB3441 | |
| ImageJ software | ImageJ | v1.49p | |
| Inverted light microscope | Olympus | CKX41 | |
| Leica microscope | Leica microsystems, UK | DMI6000B | |
| Neo sCMOS Camera | Ander, UK | 5.5 | |
| Phosphate buffered saline | Sigma-Aldrich,uk | D1408 | |
| Sodium chloride | Sigma-Aldrich,uk | 433209 | |
| Trispdium citrate dihydrate | Sigma-Aldrich,uk | W302600-K | |
| Trypsin-EDTA solution | Sigma-Aldrich,uk | T4049 |
Riferimenti
- Hardy, J. A., Higgins, G. A. Alzheimer’s disease: the amyloid cascade hypothesis. Science. 256, 184-185 (1992).
- Karthick, C., et al. Time-dependent effect of oligomeric amyloid-β (1-42)-induced hippocampal neurodegeneration in rat model of Alzheimer’s disease. Neurological Research. 41 (2), 139-150 (2018).
- Watremez, W., et al. Stabilized Low-n Amyloid-β Oligomers Induce Robust Novel Object Recognition Deficits Associated with Inflammatory, Synaptic, and GABAergic Dysfunction in the Rat. Journal of Alzheimer’s Disease. 62 (1), 213-226 (2018).
- Brouillette, J., et al. Neurotoxicity and memory deficits induced by soluble low-molecular-weight amyloid-β1-42 oligomers are revealed in vivo by using a novel animal model. Journal of Neurosciences. 32 (23), 7852-7861 (2012).
- Solana, C., Tarazona, R., Solana, R. Immunosenescence of Natural Killer Cells, Inflammation, and Alzheimer’s Disease. International Journal of Alzheimer’s Disease. , 3128758 (2018).
- Sturchler-Pierrat, C., et al. Two amyloid precursor protein transgenic mouse models with Alzheimer disease-like pathology. Proceedings of the National Academy of Sciences of the United States of America. 94 (24), 13287-13292 (1997).
- Tomiyama, T., et al. A mouse model of amyloid beta oligomers: their contribution to synaptic alteration, abnormal tau phosphorylation, glial activation, and neuronal loss in vivo. Journal of Neurosciences. 30 (14), 4845-4856 (2010).
- Saito, T., et al. Single App knock-in mouse models of Alzheimer’s disease. Nature Neurosciences. 17 (5), 661-663 (2014).
- Oddo, S., et al. Triple-Transgenic Model of Alzheimer’s Disease with Plaques and Tangles: Intracellular A and Synaptic Dysfunction. Neuron. 39 (3), 409-421 (2003).
- Leon, W. C., et al. A Novel Transgenic Rat Model with a Full Alzheimer’s-Like Amyloid Pathology Displays Pre-Plaque Intracellular Amyloid-β-Associated Cognitive Impairment. Journal of Alzheimer’s Disease. 20 (1), 113-126 (2010).
- Prince, M., et al. Dementia UK: Second Edition – Overview. Alzheimer’s Society. , 61 (2007).
- Cavanaugh, S. E., Pippin, J. J., Barnard, N. D. Animal models of Alzheimer disease: historical pitfalls and a path forward. Alternatives to animal experimentation. 31 (3), 279-302 (2014).
- Oakley, H., et al. Intraneuronal β-Amyloid Aggregates, Neurodegeneration, and Neuron Loss in Transgenic Mice with Five Familial Alzheimer’s Disease Mutations: Potential Factors in Amyloid Plaque Formation. The Journal of Neuroscience. 26 (40), 10129-10140 (2006).
- Forny-Germano, L., et al. Alzheimer’s Disease-Like Pathology Induced by Amyloid-β Oligomers in Nonhuman Primates. Journal of Neuroscience. 34 (41), 13629-13643 (2014).
- Masliah, E., et al. Altered expression of synaptic proteins occurs early during progression of Alzheimer’s disease. Neurology. 56 (1), 127-129 (2001).
- Lepelletier, F. X., Mann, D. M. A., Robinson, A. C., Pinteaux, E., Boutin, H. Early changes in extracellular matrix in Alzheimer’s disease. Neuropathology and Applied Neurobiology. 43 (2), 167-182 (2017).
- Calafiore, R., Basta, G. Clinical application of microencapsulated islets: Actual prospectives on progress and challenges. Advanced Drug Delivery Reviews. 67-68, 84-92 (2014).
- Lim, F., Sun, A. M. Microencapsulated islets as bioartificial endocrine pancreas. Science. 210 (4472), 908-910 (1980).
- Tran, N. M., et al. Alginate hydrogel protects encapsulated hepatic HuH-7 cells against hepatitis C virus and other viral infections. PLoS One. 9 (10), 109969 (2014).
- Rios de la Rosa, J. M., Wubetu, J., Tirelli, N., Tirella, A. Colorectal tumor 3D in vitro models: advantages of biofabrication for the recapitulation of early stages of tumour development. Biomedical Physics & Engineering Express. 4 (4), 045010 (2018).
- Tirella, A., Orsini, A., Vozzi, G., Ahluwalia, A. A phase diagram for microfabrication of geometrically controlled hydrogel scaffolds. Biofabrication. 1 (4), 045002 (2009).
- Smalley, K. S. M., Lioni, M., Herlyn, M. Life ins’t flat: Taking cancer biology to the next dimension. In Vitro Cellular & Developmental Biology – Animal. 42 (8-9), 242-247 (2006).
- Podlisny, M. B., et al. Aggregation of secreted amyloid beta-protein into sodium dodecyl sulfate-stable oligomers in cell culture. Journal of Biological Chemistry. 270 (16), 9564-9570 (1995).
- Portelius, E., et al. Mass spectrometric characterization of amyloid-β species in the 7PA2 cell model of Alzheimer’s disease. Journal of Alzheimer’s Disease. 33 (1), 85-93 (2013).
- Welzel, A. T., et al. Secreted amyloid β-proteins in a cell culture model include N-terminally extended peptides that impair synaptic plasticity. Biochimica. 53 (24), 3908-3921 (2014).
- O’Hare, E., et al. Orally bioavailable small molecule drug protects memory in Alzheimer’s disease models. Neurobiology of Aging. 34 (4), 1116-1125 (2013).
- Nedović, V., Willaert, R. Fundamentals of Cell Immobilisation Biotechnology. Methods and Technologies for Cell Immobilisation/Encapsulation. , 185-204 (2004).
- Omer, A., et al. Long-term Normoglycemia in Rats Receiving Transplants with Encapsulated Islets. Transplantation. 79 (1), 52-58 (2005).

