Tillverkning av amyloid-β-utsöndring Alginate Microbeads för användning vid modellering av Alzheimers sjukdom
Summary
Detta protokoll illustrerar en cell inkapsling metod genom snabb fysisk gelation av alginat att immobilisera celler. Erhållna mikrokulor möjliggör kontrollerad och ihållande utsöndring av amyloid-β över tid och kan användas för att studera effekterna av utsöndringen av amyloid-β i in vitro-och in vivo-modeller.
Abstract
Enligt amyloid Cascade hypotesen, den tidigaste utlösa i utvecklingen av Alzheimers sjukdom (AD) är ansamling av giftiga amyloid-β (Aβ) fragment, så småningom leder till de klassiska inslagen i sjukdomen: amyloid plack, neurofibrillära trassel och synaptisk och neuronala förlust. Avsaknaden av relevanta icke-transgena prekliniska modeller reflekterande av sjukdomsprogression är en av de viktigaste faktorerna som hindrar upptäckten av effektiva läkemedelsbehandlingar. För detta ändamål har vi utvecklat ett protokoll för tillverkning av alginat mikropärlor innehållande amyloid-utsöndring celler användbara för studiet av effekterna av kronisk Aβ produktion.
Kinesisk hamster äggstocksceller tidigare transfekterade med en mänsklig app gen, utsöndring Aβ (dvs 7pa2 celler), användes i denna studie. En tredimensionell (3D) in vitro-modell för ihållande frisättning av Aβ var fabricerade genom inkapsling av 7PA2 celler i alginat. Processen optimerades för att rikta en pärldiameter på 500-600 μm för ytterligare in vivo studier. Optimering av 7pa2 cell inkapsling i alginat utfördes förändra tillverknings parametrar, e.g., natriumalginat koncentration, gel flöde hastighet, elektrostatisk potential, huvud vibrationsfrekvens, gelbildande lösning. Nivåerna av utsöndras Aβ analyserades över tiden och jämfördes mellan alginatpärlor och standard cell odlingsmetoder (upp till 96 h).
En koncentration av 1,5 x 106 7pa2 celler/ml och en alginatkoncentration på 2% (w/v) BUFFRAD med Heper och efterföljande gelation i 0,5 M kalciumklorid i 5 min hittades för att tillverka de mest stabila Mikropärlorna. Fabricerade mikrokulor var 1) av enhetlig storlek, 2) med en genomsnittlig diameter på 550 μm, 3) som innehåller cirka 100-150 celler per mikropärla och 4) kan utsöndra Aβ.
Sammanfattningsvis kan vår optimerade metod för produktion av stabila alginatmikrokulor som innehåller amyloid-producerande 7PA2-celler göra det möjligt att modellera viktiga aspekter av AD både in vitro och in vivo.
Introduction
Modellering neurodegenerativ sjukdom är utmanande på grund av den komplexa och intrikata karaktär av hjärnan. Vid Alzheimers sjukdom (AD), den progressiva förlusten av synaptisk funktion och död nervceller tros vara en nedströms effekt av ihållande överproduktion och ackumulering av amyloid beta (Aβ) peptider efter onormal bearbetning av amyloid föregångare protein (APP) enligt amyloid Cascade hypotes1.
För att förstå mekanismerna i denna amyloid-inducerad patologi och för att underlätta identifieringen av nya behandlingsmål har forskarna utvecklat olika prekliniska in vivo-modeller. En kategori av modeller använder en bolusinjektion av en syntetisk Aβ-peptid i rått hjärnan2,3,4. Den största begränsningen av sådana modeller är att de förlitar sig på en enda punkt eller upprepade behandlingar med Aβ peptider i höga koncentrationer deponeras allt på en gå. Detta är oförenligt med kronisk, ihållande karaktär frisläppandet av Aβ i sjukdom5. En annan kategori av in vivo-modeller är transgena djurmodeller som uttrycker en eller flera genetiska mutationer kopplade till sjukdomens familjella variationer6,7,8,9, 10. eftersom familjär AD endast svarar för mindre än 5% av alla fall av Alzheimers11, är relevansen av dessa modeller i översättning till sporadiska AD hos människor tvivelaktig12. En annan nackdel med den transgena metoden är accelererad Aβ bildas från födseln, vilket leder till underskott i kognitiv funktion och patologiska förändringar för snabbt och aggressivt för att likna sjukdomsprogression hos sporadiska AD hos patienter12 . Till exempel ger 5x FAD-modellen plack i så lite som 1,5 månader13.
Intressant, båda dessa kategorier resultera i förändringar i kognitiv funktion av relevans för AD forskning2,3,4,5,6, och ibland de åtföljs av förekomst av patologiska kännetecken för sjukdomen såsom amyloida plack6,8, Tau fosforylering6,7 och/eller synaptisk och neuronala förlust7,9, 14. Men medan dessa typer av modeller kan ge oss en inblick i effekterna av höga halter av amyloid i hjärnan, som ofta förknippas med senare stadier av AD, de misslyckas med att återspegla de tidigare förändringarna uppvisade som svar på kronisk och ihållande exponering för Aβ peptid12, såsom förändrat uttryck för synaptiska markörer15 och komponenter i den extracellulära matrisen16. Därför återstår fortfarande ett behov av att skapa en kronisk modell som mer exakt illustrerar effekterna av ihållande Aβ sekretion på in vivo kognition och illustrerar förändringar i patologi.
För detta ändamål har vi utvecklat ett system som tillåter konstant, ihållande utsöndring av Aβ på ett kontrollerat sätt genom att immobilisera amyloid-utsöndringen celler inom hydrogel mikropärlor, som kan därefter implanteras i den vuxna råtta hjärnan att modellera aspekter av sporadiska annonser.
Alginat var det utvalda biomaterial eftersom det är biokompatibelt och inte inducerar några oönskade reaktioner vid implantat in vivo17. Cell inkapsling i alginathydrogels har varit väl etablerad under de senaste fyra decennierna. Det första exemplet på dess översättning till kliniken rapporterades för behandling av typ 1 diabetes mellitus17. Den tidigaste rapporten om framgångsrik inkapsling av öar i Langerhans går tillbaka till 1980. Transplantation av mikropärlor som innehåller insulinutsöndringen celler revolutionerade behandlingsalternativ för diabetespatienter som det restaurerade bukspottskörteln funktion, vilket eliminerar behovet av insulin injektion terapi18. Dessa verk rapporterar om hur cell inkapsling kan skydda dem från yttre påfrestningar, oavsett om mekanisk eller kemisk. Natriumalginat pärlor fungerar i själva verket som en barriär och isolerar celler från omgivningen och bevarar deras fenotyp, samtidigt som de ger tillräcklig tillgång till de omgivande medierna för näringsämnen och clearance av cellulära biprodukter19. Dessutom tillåter användning av alginat matchning av mekaniska egenskaper av mjuk vävnad20. Natriumalginat hydrogeler kan trimmas för att ha en styvhet på 1-30 kPa, genom att helt enkelt varierande alginatkoncentration och tvärbindningstäthet20,21. Detta är en viktig aspekt, inte bara för att bibehålla fenotypiska uttrycket av inkapslade celler in vitro, men också för att undvika eventuella inflammatoriska effekter efter inympningen in vivo22.
I detta protokoll, 7pa2 celler-en kinesisk hamster äggstock cell linje som är stabilt transfekterade med en mänsklig app V717F muterad gen23 -används. Dessa celler producerar kontinuerligt katalytiska produkter av app, inklusive Aβ1-4224,25, och har använts för att generera Aβ som ett alternativ till syntetisk produktion i prekliniska, akuta in vivo-studier26. Vi beskriver en tillverkningsmetod för immobilisera 7pa2 celler inom “mjuka” natriumalginat mikropärlor, utformade för att möjliggöra varaktig utsöndring av biomolekyler. Som ett konceptbevis, rapporterar vi om frisläppandet av Aβ1-42 peptid över tiden. Alginat som används är en lågviskositet alginat med en molekylvikt på 120000-190000 g/mol och en mannuronic till guluronic förhållandet 1,56 (M/G).
I ytterligare studier, dessa mikropärlor kan säkert transplanteras inom regioner i råtta hjärnan relevans för AD (t. ex., Hippocampus) att studera effekterna av kronisk Aβ sekretion på beteende in vivo och patologi ex vivo. Dessutom kan detta system användas för att studera effekterna av kronisk Aβ frisättning i in vitro-och ex vivo applikationer. Till exempel kan 7PA2-innehållande alginatmikropärlor samodlas in vitro med neuronala eller astrocytiska kulturer för att bedöma effekterna av kronisk Aβ-exponering på cellulära mekanismer som är förknippade med AD. Vidare, denna metod kan användas för att undersöka sambandet mellan kronisk Aβ produktion och långsiktig potentiering i ex vivo elektrofysiologi.
Höjdpunkten i detta protokoll är modularitet och flexibilitet i tillverkningsmetoden, vilket möjliggör tillverkning av alginat pärlor med en måldimension genom finjustering tillverknings parametrar. Beroende på ansökan, protokollet kan justeras för att få skräddarsydda mål när det gäller resestorlek, täthet av de inkapslade cellerna, och rese stelhet. Detta protokoll kan användas för inkapsling av en mängd olika celltyper, utveckla mer relevanta tredimensionella (3D) in vitro-modeller för att studera olika patologier. Vi rapporterade nyligen om hur alginate-inkapslade celler kan användas för att modellera tidiga stadier av cancer progression20.
Konceptet med inkapslingsprocessen bygger på extrudering av en laminär stråle av celler suspenderade i alginatlösning genom ett munstycke. Ett vibrerande huvud stör strålen med en kontrollerad frekvens som resulterar i lika stora alginatbaserade droppar. En extern elektrisk fält tillåter separation av de bildade alginate-baserade droppar, som vid kontakt med en lösning berikad i divalenta joner, såsom kalciumjoner, kan snabbt Cross-Link, bevara deras sfäriska form. Inkubering i gelationslösningen möjliggör bildandet av sfäriska mikropärlor som innehåller celler inom en homogen fysikalisk hydrogel27. Målstorleken på mikropärlor och alginathydrogels gör det möjligt att utbyta näringsämnen och syre med cell odlingsmedier under långa tidsperioder (veckor). Figur 1 A Visa en schematisk representation av den inkapslat apparat som används (figur 1B).
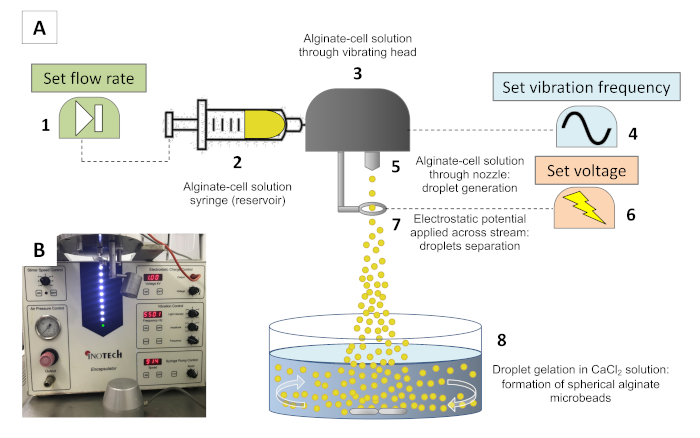
Figur 1 : Inkapslingssystemet. (A) schematisk representation av inkapslingssystemet. En alginatcell suspension lastas i en spruta (2) och matas genom en reservoar vid en extrudering hastighet inställd på sprutpumpen (1). I reservoaren vibrerar en vibrations hatt (3) med en frekvens som ställts in av en vågformsgenerator (4) för att störa strömmen med jämna mellanrum, vilket bildar lika stora droppar. Eftersom lösningen matas genom ett munstycke (5) och droppar bildas, en elektrostatisk potential appliceras över en elektrod (7) som fastställts av en spännings Generator (6), som något laddar ytan av dropparna, vilket gör att strömmen sprids till följd av repellerande elektrostatiska krafter. Som droppar engagera med gelation badet (8), ca2 +-driven tvärbindning av alginat resultat i bildandet av sfäriska mikropärlor. Bfotografi av inkapslaren före tillverkningen av alginatmikrokulor. Vänligen klicka här för att se en större version av denna siffra.
Microbead storlek kan ändras beroende på den avsedda användningen. För att kontrollera storleken på mikropärlan justeras de olika parametrarna som beskrivs i figur 1A och i protokollet i enlighet med detta. Den inre diametern av munstycket används har en betydande inverkan på storleken på dropparna; ytterligare justera inkapsling parametrar, nämligen extrudering hastighet, vibrationsfrekvens och spänning, är nyckeln till att uppnå en jämn storleksfördelning. Tabell 1 beskriver hur de olika parametrarna kan förändra storleken på mikropärlor uppnås med detta system.
| Parametern | Munstycke storlek | Vibrationsfrekvens | Flöde | Elektrod spänning |
 |
 |
 |
 |
|
| Pärlstorlek |
 
|
 |
 |
– |
Tabell 1: Tillverknings parametrar och deras påverkan på storleken på mikropärlor. Tabellen illustrerar hur varje parameter kan påverka den resulterande storleken på fabricerade mikrokulor, oberoende av munstycket och viskositeten hos den lösning som används.
Protocol
Representative Results
Discussion
Metoden som beskrivs i denna artikel är användbar för att kapsla in celler som uppnår en smal storleksfördelning av alginatmikropärlor27. Det ger också fördelen av växande celler i en immunisolerad miljö17,19, skydda dem från yttre stress. Dessutom, inkapsling av celler i alginat närmare härmar fysiologiska tillstånd, särskilt när det gäller cell-till-cell interaktioner och mat ris stelhet20. Dessa faktorer är alla särskilt viktiga för efterföljande användning i relevanta tillämpningar, såsom in vivo-inympningen, utesluter potentiella immunreaktioner i den omgivande vävnaden17. Dessutom är en stor fördel med detta protokoll lätt tunbarhet enligt tillämpning av intresse: det är möjligt att ändra protokollet och optimera parametrarna för tillverkning av större eller mindre, och mjukare eller styvare pärlor. Den beskrivna metoden används för att fabricera pärlor tillräckligt små för att injiceras med minimalt invasiva metoder, och tillräckligt stor för att vara värd för ett antal celler och ge en tillräcklig frisättning av Aβ att resultera i observerbara beteendemässiga och patologiska effekter vid injektion i djurmodeller.
Framgången för detta protokoll är beroende av ett antal kritiska steg. Noggrann cell hantering och optimala cell odlingstekniker är viktiga för att bibehålla cellernas lönsamhet och funktion20,28. Med hjälp av standard odlingsförhållanden säkerställer bevarandet av normal funktion av 7PA2-celler, som observerats. Detta möjliggör en liknande release profil för Aβ1-42 från inkapslade celler jämfört med 2D-kulturer. För att protokollet ska fungera optimalt garanterar dessutom en lösning med låg viskositet alginat bättre resultat jämfört med en alginatlösning med hög viskositet. Detta säkerställer att ett homogent laminärt stråle extruderas genom munstycket och en jämn fördelning av celler i matrisen av de fabricerade pärlorna27. Material som används för att kapsla in celler måste ha en mycket snabb gelation mekanism, vilket gör att behålla formen.
Ett annat kritiskt steg i detta protokoll är hanteringen av fabricerade mikrokulor efter gelation. Här visar vi hämtning av mikropärlor med hjälp av en stor bländare plastpipett för att överföra pärlorna. Alternativt kan hälla kalciumkloridlösning som innehåller mikropärlor i ett nätfilter användas för pärla hämtning. En stor (5, 10 eller 25 mL) serologisk pipett kan användas för att rita upp Mikropärlorna och sedan tvättas genom nätfiltret istället för att hälla. Fördelen med detta är ett högre förtroende för steriliteten i förfarandet jämfört med hälla. Men av begränsningarna är att vissa pärlor kan förvrängas om de komprimeras av pipetten, förutom att riskera en lägre avkastning om en stor del av mikrokulor inte räddas.
Detta tillvägagångssätt har använts för att kapsla in olika cellinjer för att modellera och studera olika sjukdomar (t. ex. frisättning av insulin från inkapslade bukspottskörteln Holmen). Nyheten i vårt förhållningssätt är en inympelse av mikropärlor som genereras med hjälp av detta protokoll som en användbar metod för modellering av viktiga aspekter av Alzheimers sjukdom in vivo. Vid jämförelse av release profilen för Aβ från inkapslade celler (figur 4) till nivåerna av Aβ som genereras av en bolusinjektion (såsom den som rapporterats i andra studier3,26), kan en mer kronisk och ihållande frisättning av Aβ Förväntade. Figur 6 illustrerar den förväntade tendens som kan uppnås. Använda detta system för in vivo modellering är mer relevant för hur sjukdomen fortskrider och kan vara mer användbar i Drug discovery och utveckling.
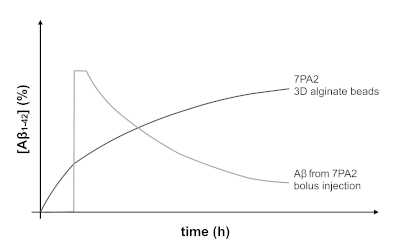
Figur 6 : Förväntad release profil för Aβ1-42 från inkapslade 7pa2-celler jämfört med en bolusinjektion. Profilen för Aβ release från inympade 7pa2-innehållande mikrokulor gör det möjligt att testa effekterna av kronisk och ihållande Aβ i en djurmodell av relevans för AD. Omvänt, en bolusinjektion skulle skapa en topp i Aβ nivåer under en kort tidsperiod, följt av en snabb clearance av Aβ från hjärnan. Vänligen klicka här för att se en större version av denna siffra.
Divulgazioni
The authors have nothing to disclose.
Acknowledgements
Författarna vill tacka herr kajen suresparan, Dr Jonathan wubetu, herr Dominik Grudzinski, Miss Chen Zhao, och Dr Thierry pilot för deras hjälp i optimering av natriumalginat rese Fabrication, cellkultur och Aβ upptäckt, och användbara vetenskapliga Diskussioner.
Materials
| µManager software | Vale Lab, UCSF, USA | v.1.46 | |
| 0.22 um PES filter | Merck, UK | SLGP033RS | |
| 15mm Netwell insert 74 um mesh filter | Constar, usa | #3477 | |
| Alginic acid sodium salt from brown algae | Sigma-Aldrich,uk | A0682 | |
| Calcium chloride | Sigma-Aldrich,uk | C1016 | |
| CellTiter96 AQueous One Solution cell proliferation assay | Promega, USA | G3580 | |
| Encapsulator | Inotech | IE-50 | serial no. 05.002.01-2005 |
| HEPES | Sigma-Aldrich,uk | H4024 | |
| Hu Aβ 1-42 ELISA | ThermoFisher, UK | KHB3441 | |
| ImageJ software | ImageJ | v1.49p | |
| Inverted light microscope | Olympus | CKX41 | |
| Leica microscope | Leica microsystems, UK | DMI6000B | |
| Neo sCMOS Camera | Ander, UK | 5.5 | |
| Phosphate buffered saline | Sigma-Aldrich,uk | D1408 | |
| Sodium chloride | Sigma-Aldrich,uk | 433209 | |
| Trispdium citrate dihydrate | Sigma-Aldrich,uk | W302600-K | |
| Trypsin-EDTA solution | Sigma-Aldrich,uk | T4049 |
Riferimenti
- Hardy, J. A., Higgins, G. A. Alzheimer’s disease: the amyloid cascade hypothesis. Science. 256, 184-185 (1992).
- Karthick, C., et al. Time-dependent effect of oligomeric amyloid-β (1-42)-induced hippocampal neurodegeneration in rat model of Alzheimer’s disease. Neurological Research. 41 (2), 139-150 (2018).
- Watremez, W., et al. Stabilized Low-n Amyloid-β Oligomers Induce Robust Novel Object Recognition Deficits Associated with Inflammatory, Synaptic, and GABAergic Dysfunction in the Rat. Journal of Alzheimer’s Disease. 62 (1), 213-226 (2018).
- Brouillette, J., et al. Neurotoxicity and memory deficits induced by soluble low-molecular-weight amyloid-β1-42 oligomers are revealed in vivo by using a novel animal model. Journal of Neurosciences. 32 (23), 7852-7861 (2012).
- Solana, C., Tarazona, R., Solana, R. Immunosenescence of Natural Killer Cells, Inflammation, and Alzheimer’s Disease. International Journal of Alzheimer’s Disease. , 3128758 (2018).
- Sturchler-Pierrat, C., et al. Two amyloid precursor protein transgenic mouse models with Alzheimer disease-like pathology. Proceedings of the National Academy of Sciences of the United States of America. 94 (24), 13287-13292 (1997).
- Tomiyama, T., et al. A mouse model of amyloid beta oligomers: their contribution to synaptic alteration, abnormal tau phosphorylation, glial activation, and neuronal loss in vivo. Journal of Neurosciences. 30 (14), 4845-4856 (2010).
- Saito, T., et al. Single App knock-in mouse models of Alzheimer’s disease. Nature Neurosciences. 17 (5), 661-663 (2014).
- Oddo, S., et al. Triple-Transgenic Model of Alzheimer’s Disease with Plaques and Tangles: Intracellular A and Synaptic Dysfunction. Neuron. 39 (3), 409-421 (2003).
- Leon, W. C., et al. A Novel Transgenic Rat Model with a Full Alzheimer’s-Like Amyloid Pathology Displays Pre-Plaque Intracellular Amyloid-β-Associated Cognitive Impairment. Journal of Alzheimer’s Disease. 20 (1), 113-126 (2010).
- Prince, M., et al. Dementia UK: Second Edition – Overview. Alzheimer’s Society. , 61 (2007).
- Cavanaugh, S. E., Pippin, J. J., Barnard, N. D. Animal models of Alzheimer disease: historical pitfalls and a path forward. Alternatives to animal experimentation. 31 (3), 279-302 (2014).
- Oakley, H., et al. Intraneuronal β-Amyloid Aggregates, Neurodegeneration, and Neuron Loss in Transgenic Mice with Five Familial Alzheimer’s Disease Mutations: Potential Factors in Amyloid Plaque Formation. The Journal of Neuroscience. 26 (40), 10129-10140 (2006).
- Forny-Germano, L., et al. Alzheimer’s Disease-Like Pathology Induced by Amyloid-β Oligomers in Nonhuman Primates. Journal of Neuroscience. 34 (41), 13629-13643 (2014).
- Masliah, E., et al. Altered expression of synaptic proteins occurs early during progression of Alzheimer’s disease. Neurology. 56 (1), 127-129 (2001).
- Lepelletier, F. X., Mann, D. M. A., Robinson, A. C., Pinteaux, E., Boutin, H. Early changes in extracellular matrix in Alzheimer’s disease. Neuropathology and Applied Neurobiology. 43 (2), 167-182 (2017).
- Calafiore, R., Basta, G. Clinical application of microencapsulated islets: Actual prospectives on progress and challenges. Advanced Drug Delivery Reviews. 67-68, 84-92 (2014).
- Lim, F., Sun, A. M. Microencapsulated islets as bioartificial endocrine pancreas. Science. 210 (4472), 908-910 (1980).
- Tran, N. M., et al. Alginate hydrogel protects encapsulated hepatic HuH-7 cells against hepatitis C virus and other viral infections. PLoS One. 9 (10), 109969 (2014).
- Rios de la Rosa, J. M., Wubetu, J., Tirelli, N., Tirella, A. Colorectal tumor 3D in vitro models: advantages of biofabrication for the recapitulation of early stages of tumour development. Biomedical Physics & Engineering Express. 4 (4), 045010 (2018).
- Tirella, A., Orsini, A., Vozzi, G., Ahluwalia, A. A phase diagram for microfabrication of geometrically controlled hydrogel scaffolds. Biofabrication. 1 (4), 045002 (2009).
- Smalley, K. S. M., Lioni, M., Herlyn, M. Life ins’t flat: Taking cancer biology to the next dimension. In Vitro Cellular & Developmental Biology – Animal. 42 (8-9), 242-247 (2006).
- Podlisny, M. B., et al. Aggregation of secreted amyloid beta-protein into sodium dodecyl sulfate-stable oligomers in cell culture. Journal of Biological Chemistry. 270 (16), 9564-9570 (1995).
- Portelius, E., et al. Mass spectrometric characterization of amyloid-β species in the 7PA2 cell model of Alzheimer’s disease. Journal of Alzheimer’s Disease. 33 (1), 85-93 (2013).
- Welzel, A. T., et al. Secreted amyloid β-proteins in a cell culture model include N-terminally extended peptides that impair synaptic plasticity. Biochimica. 53 (24), 3908-3921 (2014).
- O’Hare, E., et al. Orally bioavailable small molecule drug protects memory in Alzheimer’s disease models. Neurobiology of Aging. 34 (4), 1116-1125 (2013).
- Nedović, V., Willaert, R. Fundamentals of Cell Immobilisation Biotechnology. Methods and Technologies for Cell Immobilisation/Encapsulation. , 185-204 (2004).
- Omer, A., et al. Long-term Normoglycemia in Rats Receiving Transplants with Encapsulated Islets. Transplantation. 79 (1), 52-58 (2005).

