Aktiveret tvær kædet Agopstået for den hurtige udvikling af affinitets kromatografi harpiks-antistof opsamling som et casestudie
Summary
I denne procedure, en dsred-baserede epitop ligand er immobiliseret til at producere en meget selektiv affinitet harpiks til opsamling af monoklonale antistoffer fra rå planteekstrakter eller cellekultur supernatants, som et alternativ til protein a.
Abstract
Oprensning af monoklonale antistoffer (mAbs) opnås almindeligvis ved protein en affinitets kromatografi, som kan tegner sig for op til 25% af de samlede procesomkostninger. Alternative, omkostningseffektive fangst trin er derfor værdifulde for industriel produktion, hvor der produceres store mængder af en enkelt mAb. Her præsenterer vi en metode til immobilisering af en dsred-baserede epitop ligand til en cross-linked agopstået harpiks tillader selektiv opsamling af hiv-neutraliserende antistof 2f5 fra rå planteekstrakter uden at bruge protein a. Den lineære epitop eldkwa blev først genetisk smeltet til fluorescerende protein dsred og fusions proteinet blev udtrykt i transgene tobak (Nicotiana Nicotiana tabacum) planter før rensning ved immobiliseret metalionaffinitets kromatografi. Desuden blev en metode baseret på aktiveret tvær kædet agopstået optimeret til høj ligand tæthed, effektiv kobling og lave omkostninger. PH-og buffer sammensætningen og den opløselige ligand-koncentration var de vigtigste parametre under koblings proceduren, som blev forbedret ved hjælp af en metode til design af eksperimenter. Den resulterende affinitet harpiks blev testet for sin evne til selektivt binde Target mAb i en rå plante-ekstrakt og elueringsbuffer blev optimeret til høj mAb opsving, produkt aktivitet og affinitet harpiks stabilitet. Metoden kan let tilpasses andre antistoffer med lineære epitoper. De nye harpiks giver mulighed for blidere elueringsforhold end protein A og kan også reducere omkostningerne ved et indledende erobrings trin for Mab-produktion.
Introduction
Biofarmaceutiske produkter er vigtige for behandlingen af et bredt spektrum af sygdomme i næsten alle grene af medicin1. Monoklonale antistoffer (mAbs) dominerer det biofarmaceutiske marked, med verdensomspændende salg forventes at nå næsten €110.000.000.000 i 20202. Den favoriserede udtryks platform for MABS er ovarie cellelinjer fra kinesisk hamster, som typisk producerer høje Mab-titre på op til 10 g ∙ L-1 i kultur supernatanten3,4. Men, produktionen af mAbs i pattedyr cellekulturer er dyrt på grund af de høje omkostninger ved mediet og behovet for steril gæring5. Alternative udtryks platforme såsom planter kan tilbyde en hurtigere, enklere, billigere og mere skalerbar tilgang til industriel produktion6,7.
Ud over de omkostninger, der er forbundet med pattedyrscelle kulturer, er den udbredte brug af protein en affinitets kromatografi til produkt opsamling en stor omkostningsfaktor for industriel produktion af mAbs. Protein A findes naturligt på overfladen af Staphylococcus aureus celler, og det binder sig til fragment crystallizable (FC) regionen af visse murine og humane antistoffer, og dermed fungere som en forsvarsmekanisme til at omgå det humorale immunsystem8. Protein A er blevet branchens guld standard for opsamling af MABS fra cellekultur supernatanter og er også meget udbredt af forskersamfundet, fordi det er meget selektivt, typisk opnå Mab renheds på ~ 95% i et enkelt trin8. Ikke overraskende har salget af protein A i løbet af de sidste to årtier nøje afspejlet salget af mAbs8. Afhængigt af produktions skalaen kan omkostningerne til protein A svare til mere end 25% af de samlede procesomkostninger og dermed påvirke markedsprisen for terapeutiske MABS, som kan være op til €2.000 g-15,9. Derfor har alternative kromatografi harpiks med en lignende rensnings evne potentiale til at reducere produktionsomkostningerne betydeligt, hvilket gør antistof baserede terapier tilgængelige for et større antal patienter10,11 ,12. Sådanne alternativer kan også omgå ulemperne ved protein en kromatografi, herunder de barske elueringsforhold ved lav pH-værdi (typisk < 3.5), der potentielt kan forårsage, at mAbs undergår konformationsmæssige ændringer, der fremmer sammenlægning13 . Det er vigtigt, at protein A kun er selektivt for FC-regionen i visse IgG-underklasser, så ikke-funktionelle molekyler med trunkerede bindings domæner kan være co-rense med det intakte produkt5, hvorimod Mab-derivater såsom enkelt kædede variable fragmenter må ikke binde til protein A overhovedet.
Her beskriver vi en alternativ affinitets kromatografi harpiks til opsamling af hiv-neutraliserende Mab 2f5 ved hjælp af sin lineære epitop eldkwa (et bogstav aminosyre kode)5,14. Vi genetisk smeltet 2f5 epitop til C-endestation af det fluorescerende protein dsred, som fungerede som en bærer og reporter molekyle, og producerede den resulterende protein Dsred-2F5-Epitope (DFE) i transgene tobak ( Nicotiana Nicotiana tabacum) planter. DFE blev renset ved en enkelt trins immobiliseret metalionaffinitets kromatografi (IMAC). Immobilisering af den rensede DFE affinitets ligand på en tværbundet agopat harpiks blev opnået ved kemisk kobling ved hjælp af N-hydroxysuccinimide (NHS)-aktiverede Cross-linked aghas kolonner. Statistiske eksperimentelle design blev derefter brugt til at optimere immobilisering procedure og kobling effektivitet15. Rensnings strategien for mAb 2F5 blev evalueret med hensyn til antistof renhed, udbytte og ligand-stabilitet. I modsætning til protein A, som binder FC-regionen, er DFE bundet til den komplementaritets bestemmende region 2F5, der sikrer rensning af molekyler med en intakt paratope. Vores koncept kan nemt tilpasses til enhver Mab med en lineær epitop eller til andre peptidbaserede affinitets-ligander, som let kan identificeres ved mikroarray undersøgelser16.
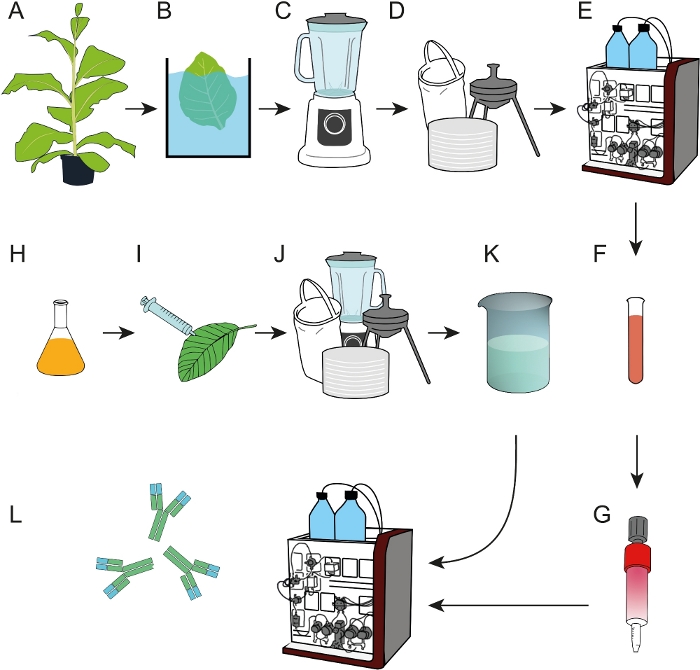
Figur 1: proces flow skema til fremstilling af epitop affinitet harpiks, der kan anvendes til opsamling af MABS fra rå planteekstrakter eller cellekultur supernatants. A) tilhørsforholdet LIGAND DFE blev udtrykt i transgene tobaksplanter. Et varme udfældnings trin (B) blev inkluderet, før de høstede blade blev homogeniseret (C). (D) den rå planteekstrakt blev præciseret ved posefiltre ring, dybde filtrering og 0,2 μm steril filtrering. (E) DFE blev derefter RENSET af iMac. (F, G) Den rensede DFE Affinity ligand blev immobiliseret på EDC/NHS-aktiverede Cross-linked aghas kolonner. (H) bakteriekulturer, der transporterer T-DNA-kodnings antistof 2F5, blev anvendt til forbigående ekspression i N. benthamiana -planter (i) dyrket i en phytotron. J) blade af N. benthamiana blev høstet og forarbejdet som beskrevet i D. (K) Mab 2f5 blev renset fra det afklarede uddrag ved hjælp af DFE-tilknytnings kolonnerne (L). Venligst klik her for at se en større version af dette tal.
Protocol
Representative Results
Discussion
Anvendelser af den nye affinitets harpiks
Vi har vist, at brugerdefinerede affinitets kromatografi harpiks til opsamling af MABS kan fremstilles ved at immobilisere en ligand indeholdende en Mab-specifik epitop til NHS-aktiveret Cross-linked agopstod. At designe en sådan harpiks, var det nødvendigt at kende epitop sekvens og til at bruge en lineær epitop. De resulterende harpiks er fordelagtige for erobring af mAbs, fordi de potentielt kunne erstatte dyre protein en affinitets kromatografi trin. Interaktionen mellem 2F5 og DFE i vores casestudie blev medieret af epitope – paratope binding, så vores ligand bør være mere selektiv end protein A, som binder til FC-regionen af de fleste murine og humane IgGs. Fordi individuelle ligander er nødvendige for hver Mab, kan vores metode i første omgang synes egnet primært til antistoffer, der produceres på en meget stor skala. Men ved at kombinere vores tilgang med hurtige plante-baserede forbigående protein udtryk, kan nye affinitets ligander forberedes på mindre end 2 uger27 med minimal indsats28. Derfor er metoden også velegnet til små mAb rensning.
Produktion og potentielle forbedringer af affinitets ligand
Planter tilbyder en hurtig og sikker produktionsplatform for Affinity ligander5,29,30, såsom DFE fusion protein featured i vores casestudie. Blanching plantematerialet reducerede i høj grad mængden af værtscelle proteiner i et enkelt trin og blev let integreret i en standard afklarings rutine. Men, inddrivelse af ligand var lav i den nuværende opsætning, sandsynligvis på grund af sin moderat termisk stabilitet og nogle ikke-specifik binding til filter lagene, som rapporteret for andre produkter31,32,33. Ingeniør luftfartsselskabet til at øge sin termiske stabilitet kan derfor bidrage til at forbedre ligand udbytte i fremtiden, som beskrevet for malariavaccine kandidat CCT, antitumor enzym PpADI eller en mesofile β-glucosidase34, 35af36. Det samme gælder for dybde filtrerings trinnet, hvor protein teknik kan medvirke til at reducere den ikke-specifikke binding til Filtermaterialet37. Produktionsomkostningerne for DFE og lignende ligander kunne også reduceres ved at forbedre den generelle effektivitet af præciseringen ved hjælp af flokkulanter eller filter additiver38,39.
Når DsRed bruges som transportør, danner det et tetramerisk kompleks. Dette er fordelagtigt, fordi det øger antallet af epitoper per ligand, men det kan også gøre ligand mere modtagelig for demontering eller denaturering under affinitets kromatografi. Et monomere bære protein som mcherry kan derfor være at foretrække, fordi det er stabilt ved lav pH-værdi40, og inkluderingen af tandem gentagelser af epitop vil øge lydens aviditet og dermed øge harpiks kapaciteten5, 26 , 41. for simple bære-epitope proteiner (dvs. dem uden disulfid obligationer eller post-translationelle modifikationer) mikrobielle produktionssystemer kan reducere fremstillingsomkostningerne og gøre ligander mere konkurrencedygtige med protein A. For eksempel er grøn fluorescerende protein blevet udtrykt i bakterieceller med et afkast på ~ 1 g · kg-1 biomasse, hvilket i væsentlig grad ville reducere ligand produktionsomkostninger42.
Uanset udtryks værten, en renset affinitet ligand var påkrævet under koblingen for at minimere immobilisering af Host celle proteiner eller mediekomponenter, der ellers kan reducere harpiks selektivitet og kapacitet. Optagelsen af en poly-histidine tag til iMac rensning øget renhed til ~ 90% i et enkelt trin, lette hurtig og billig ligand produktion5,43,44. Fusions tagens position er imidlertid vigtig, fordi den har potentialet til at hæmme epitop binding eller til at inducere spalningen af enten tagget eller epitop fra bæreren45,46.
Immobilisering af Affinity ligand på NHS-aktiverede kromatografikolonner
Immobilisering blev udført manuelt eller ved hjælp af et kromatografi system. De små buffer mængder pr. kolonne syntes at favorisere manuel håndtering (f. eks. på grund af den minimale affaldsmængde). Hvis der er behov for flere/større kolonner, gør kromatografisystemet imidlertid det lettere at styre koblings forholdene (f. eks. regulerede strømningshastigheder) og er derfor mere tilbøjelige til at opnå reproducerbare resultater med hensyn til DBC. Vores data tyder på, at koblings bufferen og pH har en vigtig effekt på koblings effektiviteten og de samlede kolonne omkostninger. Screenings faktorer, der påvirker koblings reaktionen og justerer dem for hvert bære protein (eller endda for hvert luftfartsselskab – ligand fusion), kan derfor forbedre koblings effektiviteten og harpiks ydeevnen, og vi anbefaler denne fremgangsmåde.
Test 2F5 isolation ved hjælp af DFE affinitet harpiks
Produkt udbytte og renhed er vigtige aspekter af harpiks ydeevne, og i tilfælde af DFE opnåede vi et afkast på 105 ± 11% (± SD, n = 3) og en renhed på 97 ± 3% (± SD, n = 3), som er sammenlignelig med ydeevnen af benchmark protein A harpiks25 ,26. En anden vigtig Præstationsindikator for harpiks i almindelighed (og især for dem, der er baseret på Affinity ligands) er DBC ved 10% produkt gennembrud, fordi denne parameter påvirker mængden af harpiks, der kræves for en bestemt proces og dermed omkostningerne. For DFE ligand, den oprindelige DBC var ~ 4 g · L-1 harpiks, som er ~ 13% af den tilsvarende værdi for protein A under lignende betingelser (kun 2 min kontakttid)25,47 men ca. 15 gange højere sammenlignet med andre brugerdefinerede affinitet harpiks såsom anti-FSH-immun affinitet ligand bruger den samme opholdsperiode på 2 min48. Dfe’en af DFE faldt til 15% af startværdien efter 25 binde-og elute cyklusser, hvorimod der kræves mere end 50 cyklusser for samme tab af DBC i kommercielt protein A harpiks49. Det er dog vigtigt at bemærke, at vores luftfartsselskab endnu ikke er blevet optimeret i samme omfang som protein A, som er blevet grundigt undersøgt og forbedret i løbet af de sidste fire årtier8.
Hidtil har vi forbedret harpiks stabilitet og produkt genvinding ved at skifte fra en lav-pH elueringsbuffer til en høj koncentration af magnesiumchlorid (figur 3), som anbefalet i tidligere undersøgelser13. Den karakteristiske røde farve af affiniteten ligand ikke falmer væsentligt under de 25 binde-og-elute cyklusser, så vi spekulerer på, at endogene plante proteaser i de afklarede planteekstrakter31 kan have afkortet og dermed inaktiveret epitop af ligand. Derfor, designe proteaseresistente linkers til at forbinde bæreren og epitop kan bidrage til at opretholde den oprindelige DBC over et udvidet antal cyklusser. I betragtning af den hurtige og enkle ekspression og oprensning af DFE ligand, dens ligetil kobling til kommerciel kromatografi harpiks, og dens fremragende produkt udbytte og renhed, mener vi, at vores metode tilbyder et passende alternativ til protein A for rensning af mAbs og antistof derivater, som ikke binder sig til protein A, især hvis forbedringer af bæreren og linker kan forbedre DBC og ligand stabilitet. Denne antagelse blev understøttet af den lille forskel i dissociationskonstant af DFE-renset og protein A-renset 2F5 antistof5, hvilket indikerer, at vores nye affinitet ligand tillader genopretning af høj kvalitet MABS.
Fordele og nuværende begrænsninger af metoden
Produktion af affinitet ligand som en genetisk fusion med et bære protein øger Opløselighed i vandige buffere og dermed kompatibilitet med typiske ligand kobling betingelser. I modsætning hertil kan blind peptider afledt af fast fase peptidsyntese have begrænset opløselighed under disse forhold på grund af deres sekvens50, som ikke kan ændres, fordi det er dikteret af aminosyren sekvens af epitop anerkendt af Mab til renses. Andre har derfor brugt en on-harpiks syntese af peptidligands51. Den statiske bindings kapacitet for den resulterende harpiks var høj (~ 80 g · L-1), men processen med harpiks forberedelse er langvarig, en dynamisk bindende kapacitet blev ikke rapporteret, og den opnåede renhed og nyttiggørelse var lavere end i vores tilgang. En yderligere fordel ved en fusion protein ligand i laboratorieskala er, at ligand og varianter deraf kan hurtigt produceres, renses og testes med minimal indsats i en nem at bruge High-through Expression system52.
De to nuværende begrænsninger af den metode, der præsenteres her, er den lave dynamiske bindingsevne på 3 g · L-1 og dens 90% reduktion i løbet af 25 binde-og-elute cyklusser5. Disse begrænsninger kan håndteres i fremtiden ved at anvende mindre strenge laste betingelser og erstatte den nuværende DsRed carrier med en konstrueret, mere stabil variant hhv. For eksempel har en fordobling af den aktuelle kontakttid fra 2 til 4 minutter potentialet til at fordoble den dynamiske bindings kapacitet, som det blev vist for nogle proteiner A-harpiks26.
Fejlfinding
Følgende tabel fremhæver potentielle problemer, der kan opstå i løbet af denne protokol, og giver tips til, hvordan du løser dem (tabel 1).
| Tabel 1: potentielle problemer, der kan opstå, og mulige rettelser. | |||
| Protokol trin | Problem | Retters | Lave |
| 1 | Planter vokser ikke | Kompromitterede vækstbetingelser | Kontroller pH og ledningsevne af gødning |
| Kontroller temperatur og lysforhold | |||
| 2 og 3 | Store mængder af Host celle proteiner er til stede efter ekstraktion | Ufuldstændig nedbør | Kontroller temperaturen under blanchering |
| Kontroller omrøringen i blanchbadet | |||
| 2 og 3 | Intet produkt fundet i plante ekstrakten | Blanching temperatur for høj | Kontroller temperatur og pH under blanchering |
| pH i blanchering buffer for lav | |||
| 3 | Store stængel-eller bladdele forbliver efter ekstraktion | Ufuldstændig blanding i Blender | Sørg for, at plantematerialet ikke danner en prop i blenderen |
| 3 | Hurtig trykstigning under dybde filtrering | Forkert valg af filter og/eller retning | Kontroller filtertype og-retning |
| 4 | Lille fusionsprotein under eluering/en masse fusionsprotein i gennemstrømnings | IMAC-harpiks blev ikke ladet med metalioner | Kontroller, om IMAC-harpiksen er korrekt opladet med ioner |
| Fusion protein mistede Affinity-tagget | Undgå intens sollys og høje temperaturer under plantedyrkning | ||
| 4 | Fusionsprotein tabt under koncentrationen | Fusionsprotein bundet til membranen | Kontroller membran typen |
| Sørg for, at koncentrationsfaktoren ikke var for høj | |||
| 5 | Lav koblings ydelse | Forkert sekvens af tilkoblings reagens tilsætning | Kontroller reagenserne etiketter og sekvens af tilsætning |
| Ukorrekt klargøring af kolonnerne før kobling | Kontroller betingelserne for kolonne klargøringen | ||
| 5 og 6 | Lav mAb-ydelse | Lavt mAb-udtryk i plante biomassen | Test mAb-udtryk i biomasse |
| Lav ligand tæthed | Kontrollere renheden af fusionsprotein præparatet | ||
| 7 | Meget lave/høje proteinkoncentrationer i Bradford assay | Bobledannelse under pipettering | Check for bobler i 96-brønd palte |
| 7 | Lav mAb-koncentration under SPR-måling | Kompromitteret protein en chip | Sammenlign med resultaterne af standard mAb med kendt koncentration |
| Ukorrekt prøve fortynding | Kontrollér fortyndings hastigheden og buffer- | ||
Tabel 1: fejlfinding.
Divulgazioni
The authors have nothing to disclose.
Acknowledgements
Vi vil gerne anerkende Ibrahim Al Amedi for at dyrke de transgene tobaksplanter og Dr. Thomas Rademacher for at levere tobaks ekspressions vektoren. Forfatterne ønsker at takke Dr. Richard M. Twyman for redaktionel assistance og Markus Sack for frugtbare diskussioner om DFE Affinity ligand struktur. Dette arbejde blev delvis finansieret af de interne programmer Fraunhofer-Gesellschaft under Grant No. Tiltrække 125-600164 og staten Nordrhein-Westfalen under Leistungszentrum Grant No. 423 “netværksbaseret, adaptiv produktion”. Dette arbejde blev støttet af Deutsche Forschungsgemeinschaft (DFG) inden for rammerne af forsknings uddannelsesgruppen “tumor målrettet lægemiddel levering” Grant 331065168. GE Healthcare støttede offentliggørelsen af denne artikel i åben adgang.
Materials
| 10L/20L Bucket | n/a | n/a | Blanching equipment |
| 2100P Portable Turbidimeter | Hach | 4650000 | Turbidimeter |
| ÄKTApure | GE Helthcare | 29018226 | Chromatography system |
| Allegra 25R | Beckman Coulter | 369434 | Centrifuge |
| Amine Coupling Kit | GE Healthcare | BR100050 | SPR chip coupling kit |
| Amine Coupling Kit | GE Healthcare | BR100050 | SPR chip coupling kit |
| Antibody 2G12 | Fraunhofer IME | n/a | Standard for SPR quantification |
| Blender | Waring | 800EG | Blender |
| BP-410 | Fuhr | 2632410001 | Bag filter |
| CanoScan 5600F | Canon | 2925B009 | Scanner |
| Centrifuge tube 50 mL self-standing | Labomedic | 1110504 | Reaction tube |
| Chelating Sepharose FF | GE Helthcare | 17-0575-01 | Chromatography resin |
| Cond 3320 | WTW | EKA 3338 | Conductometer |
| Design-Expert(R) 8 | Stat-Ease, Inc. | n/a | DoE software |
| Discovery Compfort | Gilson | F81029 | Multichannel pipette |
| Disodium phosphate | Carl Roth GmbH | 4984.3 | Media component |
| Diverse bottles | Schott Duran | n/a | Glas bottles |
| Dri Block DB8 | Techne | Z381373 | Heat block |
| DsRed | Fraunhofe IME | n/a | Standart |
| EDTA | Carl Roth GmbH | 8043.2 | Buffer component |
| EnSpire | Perkin Elmer | 2390-0000 | Plate reader |
| ETHG-912 | Oregon Scientific | 086L001499-230 | Thermometer |
| F9-C | GE Helthcare | 29027743 | Fraction collector |
| Ferty 2 Mega | Kammlott | 5.220072 | Fertilizer |
| Forma -86C ULT freezer | ThermoFisher | 88400 | Freezer |
| HEPES | Carl Roth GmbH | 9105.3 | Buffer component |
| Hettich Centrifuge Mikro 200 | Hettich | 2400 | Centrifuge |
| HiPrep 26/10 | GE Helthcare | GE17-5087-01 | Chromtography column |
| HiTrap NHS-activated Sepharose HP, 1 mL | GE Helthcare | 17-0716-01 | Chromatography columns |
| Hydrochloric acid | Carl Roth GmbH | 4625.1 | Buffer component |
| Imidazole | Carl Roth GmbH | 3899.2 | Buffer component |
| K700 | Pall | 5302305 | Depth filter layer |
| KM02 basic | IKA | n/a | Magnetic stirrer |
| KS50P 60D | Pall | B12486 | Depth filter layer |
| L/S 24 | Masterflex | SN-06508-24 | Tubing |
| Lauda E300 | Lauda Dr Wobser GmbH | Z90010 | Immersion circulator |
| Magnesium chloride | Carl Roth GmbH | KK36.2 | Buffer component |
| Masterflex L/S | Masterflex | HV-77921-75 | Peristaltic pump |
| Minisart 0.2 µm | Sartorius | 16534K | Filter unit |
| Nalgene Rapid-Flow PES bottle top filter | Thermo Fischer Scientific | 595-4520 | Vacuum filtration of SPR buffers |
| Nickel sulphate | Carl Roth GmbH | T111.1 | Buffer component |
| Novex NuPAGE 4-12% BisTris LDS gels | Invitrogen | NP0336BOX | LDS-PAA gels |
| Novex X-cell Mini Cell | Invitrogen | EI0001 | PAGE chamber |
| NuPAGE 20x running buffer | Invitrogen | NP0002 | Buffer concentrate |
| NuPAGE antioxidant | Invitrogen | NP0005 | Antioxidant |
| PageRuler protein ladder (10-180 kDa) | Invitrogen | 26616 | Protein standart |
| Perforated bucked | n/a | n/a | Blanching |
| PH 3110 | WTW | 2AA110 | PH meter |
| PowerPac HC | Biorad | 1645052 | Electrophoresis module |
| Protein A from Staphylococcus aureus | Sigma-Aldrich | P7837-5MG | Coating of SPR chips |
| Sephadex G-25 fine, cross linked dextran | GE Helthcare | 17003301 | Chromatography resin |
| Silicone spoon | n/a | n/a | Spoon |
| Simply Blue SafeStain | Invitrogen | LC6060 | Gel staining solution |
| Sodium acetate | Carl Roth GmbH | 6773.1 | Buffer component |
| Sodium acetate | Carl Roth GmbH | X891.1 | Media component |
| Sodium azide | Sigma Aldrich | S2002-100G | Media component |
| Sodium chloride | Carl Roth GmbH | P029.2 | Buffer component |
| Sodium citrate | Carl Roth GmbH | HN13.2 | Buffer component |
| Sodium bisulfite | Carl Roth GmbH | 243973-100G | Media component |
| Sodium phosophate | Carl Roth GmbH | T877.2 | Media component |
| SPR Affinity Sensor – High Capacity Amine | Sierra Sensors GmbH/Bruker Daltonics | SPR-AS-HCA | SPR chip |
| SPR-2/4 Surface Plasmon Resonance Analyzer | Sierra Sensors GmbH/Bruker Daltonics | n/a | SPR device |
| SSM3 | Stuart | 10034264 | Mini Gyro-rocker |
| Heated vessel, 20 L | Clatronic | n/a | Blanching chamber |
| Sterile syringes, 2 mL | B. Braun | 4606027V | Syringes |
| Syringe adpter (Union Luer F) | GE Helthcare | 181112-51 | Syringe adapter |
| TE6101 | Sartorius | TE6101 | Precision scale |
| Tween-20 (Polysorbate) | Merck | 8170721000 | Buffer component |
| Unicorn 6.4 | GE Helthcare | 29056102 | Chromatography software |
| Vacuum bags | Ikea | 203.392.84 | Plant storge |
| VelaPad 60 | Pall | VP60G03KNH4 | Filter housing |
| Vortex-Genie 2 | Scientific industries | SI-0236 | Vortex |
| XK-26/20 column housing | GE Helthcare | 28-9889-48 | Chromtography column |
Riferimenti
- Kesik-Brodacka, M. Progress in biopharmaceutical development. Biotechnology and Applied Biochemistry. 65 (3), 306-322 (2018).
- Ecker, D. M., Jones, S. D., Levine, H. L. The therapeutic monoclonal antibody market. MAbs. 7 (1), 9-14 (2015).
- Jayapal, K., Wlaschin, K. F., Hu, W. S., Yap, M. G. S. Recombinant Protein Therapeutics from CHO Cells – 20 Years and Counting. Chemical Engineering Progress. 103, 40-47 (2007).
- Kunert, R., Reinhart, D. Advances in recombinant antibody manufacturing. Applied Microbiology and Biotechnology. 100 (8), 3451-3461 (2016).
- Rühl, C., Knödler, M., Opdensteinen, P., Buyel, J. F. A linear epitope coupled to DsRed provides an affinity ligand for the capture of monoclonal antibodies. Journal of Chromatography A. 1571, 55-64 (2018).
- Edgue, G., Twyman, R. M., Beiss, V., Fischer, R., Sack, M. Antibodies from plants for bionanomaterials. Nanomedicine and Nanobiotechnology. 9 (6), e1462 (2017).
- Buyel, J. F., Fischer, R. Very-large-scale production of antibodies in plants: The biologization of manufacturing. Biotechnology Advances. 35 (4), 458-465 (2017).
- Bolton, G. R., Mehta, K. K. The role of more than 40 years of improvement in protein A chromatography in the growth of the therapeutic antibody industry. Biotechnology Progress. 32 (5), 1193-1202 (2016).
- Kelley, B. Industrialization of mAb production technology: the bioprocessing industry at a crossroads. MAbs. 1 (5), 443-452 (2009).
- Brochier, V., Ravault, V. High throughput development of a non protein A monoclonal antibody purification process using mini-columns and bio-layer interferometry. Engineering in Life Sciences. 16 (2), 152-159 (2016).
- Arakawa, T., Futatsumori-Sugai, M., Tsumoto, K., Kita, Y., Sato, H., Ejima, D. MEP HyperCel chromatography II: binding, washing and elution. Protein Expression and Purification. 71 (2), 168-173 (2010).
- Barroso, T. B., Aguiar-Ricardo, R. J., Roque, A. C. Structural evaluation of an alternative Protein A biomimetic ligand for antibody purification. Journal of Computer-aided Molecular Design. 28 (1), 25-34 (2014).
- Mazzer, A. R., Perraud, X., Halley, J., O’Hara, J., Bracewell, D. G. Protein A chromatography increases monoclonal antibody aggregation rate during subsequent low pH virus inactivation hold. Journal of Chromatography A. 1415, 83-90 (2015).
- Sack, M., et al. Functional analysis of the broadly neutralizing human anti-HIV-1 antibody 2F5 produced in transgenic BY-2 suspension cultures. FASEB Journal. 21 (8), 1655-1664 (2007).
- Buyel, J. F., Fischer, R. Characterization of Complex Systems Using the Design of Experiments Approach: Transient Protein Expression in Tobacco as a Case Study. Journal of Visualized Experiments. (83), 51216 (2014).
- Trasatti, J. P., Woo, J., Ladiwala, A., Cramer, S., Karande, P. Rational design of peptide affinity ligands for the purification of therapeutic enzymes. Biotechnology Progress. 34 (4), 987-998 (2018).
- Buyel, J. F., Gruchow, H. M., Boes, A., Fischer, R. Rational design of a host cell protein heat precipitation step simplifies the subsequent purification of recombinant proteins from tobacco. Biochemical Engineering Journal. 88, 162-170 (2014).
- Simonian, M. H., Smith, J. A. Spectrophotometric and colorimetric determination of protein concentration. Current Protocols in Molecular Biology. 76 (Chapter 10), (2006).
- Buyel, F. J., Kaever, T., Buyel, J., Fischer, R. Predictive models for the accumulation of a fluorescent marker protein in tobacco leaves according to the promoter/5’UTR combination. Biotchnology and Bioengeneering. 110 (2), 471-483 (2013).
- Piliarik, M., Vaisocherova, H., Homola, J. Surface plasmon resonance biosensing. Methods in Molecular Biology. 503, 65-88 (2009).
- Buyel, J. F., Fischer, R. Scale-down models to optimize a filter train for the downstream purification of recombinant pharmaceutical proteins produced in tobacco leaves. Biotechnology Journal. 9 (3), 415-425 (2014).
- Baird, G. S., Zacharias, D. A., Tsien, R. Y. Biochemistry, mutagenesis, and oligomerization of DsRed, a red fluorescent protein from coral. Proceedings of the National Academy of Sciences, USA. 97 (22), 11984-11989 (2000).
- Vrzheshch, P. V., Akovbian, N. A., Varfolomeyev, S. D., Verkhusha, V. V. Denaturation and partial renaturation of a tightly tetramerized DsRed protein under mildly acidic conditions. FEBS Letters. 487 (2), 203-208 (2000).
- Firer, M. A. Efficient elution of functional proteins in affinity chromatography. Journal of Biochemical and Biophysical Methods. 49 (1-3), 433-442 (2001).
- Pabst, T. M., et al. Engineering of novel Staphylococcal Protein A ligands to enable milder elution pH and high dynamic binding capacity. Journal of Chromatography A. 1362, 180-185 (2014).
- Müller, E., Vajda, J. Routes to improve binding capacities of affinity resins demonstrated for Protein A chromatography. Journal of Chromatography B. 1021, 159-168 (2016).
- Shamloul, M., Trusa, J., Vadim, M., Vidadi, Y. Optimization and Utilization of Agrobacterium-mediated Transient Protein Production in Nicotiana. Journal of Visualized Experiments. (86), 51204 (2014).
- Rademacher, T., et al. Plant cell packs: a scalable platform for recombinant protein production and metabolic engineering. Plant Biotechnology Journal. , (2018).
- Saxena, L., Iyer, B. K., Ananthanarayan, L. Purification of a bifunctional amylase/protease inhibitor from ragi (Eleusine coracana) by chromatography and its use as an affinity ligand. Journal of Chromatography. B. 878 (19), 1549-1554 (2010).
- Kurppa, K., Reuter, L. J., Ritala, A., Linder, M. B., Joensuu, J. J. In-solution antibody harvesting with a plant-produced hydrophobin-Protein A fusion. Plant Biotechnology Journal. 16 (2), 404-414 (2018).
- Menzel, S., et al. Optimized Blanching Reduces the Host Cell Protein Content and Substantially Enhances the Recovery and Stability of Two Plant-Derived Malaria Vaccine Candidates. Frontiers in Plant Science. 7 (159), 1-7 (2016).
- Yigzaw, Y., Piper, R., Tran, M., Shukla, A. A. Exploitation of the adsorptive properties of depth filters for host cell protein removal during monoclonal antibody purification. Biotechnology Progress. 22 (1), 288-296 (2006).
- Menzel, S., et al. Downstream processing of a plant-derived malaria transmission-blocking vaccine candidate. Protein Expression and Purification. 152, 122-130 (2018).
- Vöpel, N., Boes, A., Edgü, G., Beiss, V. Malaria vaccine candidate antigen targeting the pre-erythrocytic stage of Plasmodium falciparum produced at high level in plants. Biotechnology Journal. 9 (11), 1435-1445 (2014).
- Lee, C. W., Wang, H. J., Hwang, J. K., Tseng, C. P. Protein thermal stability enhancement by designing salt bridges: a combined computational and experimental study. PLoS ONE. 9 (11), e112751 (2014).
- Zhu, L., Cheng, F., Piatkowski, V., Schwaneberg, U. Protein engineering of the antitumor enzyme PpADI for improved thermal resistance. Chembiochem. 15 (2), 276-283 (2014).
- Khanal, O., et al. Contributions of depth filter components to protein adsorption in bioprocessing. Biotechnology and Bioengineering. 115 (8), 1938-1948 (2018).
- Buyel, J. F., Fischer, R. Downstream processing of biopharmaceutical proteins produced in plants: the pros and cons of flocculants. Bioengineered. 5 (2), 138-142 (2014).
- Buyel, J. F. Procedure to Evaluate the Efficiency of Flocculants for the Removal of Dispersed Particles from Plant Extracts. Journal of Visualized Experiments. (110), e53940 (2016).
- Fink, D., et al. Ubiquitous expression of the monomeric red fluorescent protein mCherry in transgenic mice. Genesis. 48 (12), 723-729 (2010).
- Gagnon, P. Technology trends in antibody purification. Journal of Chromatography A. 1221, 57-70 (2012).
- Figueira, M., Laramée, L., Murrell, J. C., Groleau, D., Míguez, C. Production of green fluorescent protein by the methylotrophic bacterium Methylobacterium extorquens. FEMS Microbiology Letters. 193 (2), 195-200 (2001).
- Bornhorst, J. A., Falke, J. J. Purification of proteins using polyhistidine affinity tags. Methods in enzymology. 326, 245-254 (2000).
- Sainsbury, F., Jutras, P. V., Vorster, J., Goulet, M., Michaud, D. A. Chimeric Affinity Tag for Efficient Expression and Chromatographic Purification of Heterologous Proteins from Plants. Frontiers in Plant Science. 7, 141-141 (2016).
- Krupka, M., et al. The Position of His-Tag in Recombinant OspC and Application of Various Adjuvants Affects the Intensity and Quality of Specific Antibody Response after Immunization of Experimental Mice. PLoS ONE. 11 (2), e0148497 (2016).
- Goel, A., et al. Relative position of the hexahistidine tag effects binding properties of a tumor-associated single-chain Fv construct. Biochimica et Biophysica Acta. 1523 (1), 13-20 (2000).
- Tustian, A. D., et al. Development of a novel affinity chromatography resin for platform purification of bispecific antibodies with modified protein a binding avidity. Biotechnology Progress. , (2018).
- Zandian, M., Jungbauer, A. An immunoaffinity column with a monoclonal antibody as ligand for human follicle stimulating hormone. Journal of Separation Science. 32 (10), 1585-1591 (2009).
- Kelley, B. Very large scale monoclonal antibody purification: the case for conventional unit operations. Biotechnology Progress. 23 (5), 995-1008 (2007).
- Petrou, C., Sarigiannis, Y., S, K. o. u. t. s. o. p. o. u. l. o. s. Ch. 1. Peptide Applications in Biomedicine, Biotechnology and Bioengineering. , 1-21 (2018).
- Menegatti, S., et al. Design of protease-resistant peptide ligands for the purification of antibodies from human plasma. Journal of Chromatography A. 1445, 93-104 (2016).
- Rademacher, T., et al. Plant cell packs: a scalable platform for recombinant protein production and metabolic engineering. Plant Biotechnology Journal. , 1-7 (2019).

