Correzione ad alta precisione dei cambiamenti cromatici 3D nell'era dell'imaging biologico a super-risoluzione utilizzando Chromagnon
Summary
La correzione dei cambiamenti cromatici nelle immagini di microscopia a fluorescenza multicolore tridimensionale (3D) è fondamentale per l’analisi quantitativa dei dati. Questo protocollo è stato sviluppato per misurare e correggere i cambiamenti cromatici nei campioni biologici attraverso l’acquisizione di immagini di riferimento adatte e l’elaborazione con il software open source, Chromagnon.
Abstract
La microscopia quantitativa a fluorescenza multicolore si basa sull’attenta corrispondenza spaziale dei canali di colore acquisiti a diverse lunghezze d’onda. A causa dell’aberrazione cromatica e dell’allineamento imperfetto delle telecamere, le immagini acquisite in ogni canale possono essere spostate e ingrandite, così come ruotate l’una rispetto all’altra in una qualsiasi delle tre dimensioni. Con il metodo di calibrazione classico, gli spostamenti cromatici sono misurati da perline multicolore attaccate alla superficie di un coverslip, e un certo numero di software sono disponibili per misurare gli spostamenti cromatici da tali campioni di calibrazione. Tuttavia, l’aberrazione cromatica può variare con profondità, cambiamento con condizioni di osservazione ed essere indotta dal campione biologico stesso, ostacolando così la determinazione della vera quantità di cambiamento cromatico nel campione di interesse e attraverso il volume. Correggere i cambiamenti cromatici a una maggiore precisione è particolarmente rilevante per la microscopia a super-risoluzione in cui solo lievi spostamenti cromatici possono influenzare le analisi quantitative e alterare l’interpretazione delle immagini multicolore. Abbiamo sviluppato un software open-source Chromagnon e metodi di accompagnamento per misurare e correggere i cambiamenti cromatici 3D nei campioni biologici. Qui forniamo un protocollo applicativo dettagliato che include requisiti speciali per la preparazione dei campioni, l’acquisizione dei dati e l’elaborazione del software per misurare i cambiamenti cromatici nei campioni biologici di interesse.
Introduction
L’imaging multicolore è uno degli aspetti fondamentali della microscopia biologica a fluorescenza, nei casi in cui la relazione spaziale di diverse molecole o strutture è di grande interesse. L’aberrazione cromatica, un’aberrazione ottica della luce policromatica causata dalla dispersione, cambia la posizione apparente degli oggetti colorati di interesse. Allo stesso modo, i microscopi dotati di più telecamere dedicate all’acquisizione di ogni colore hanno cambiamenti cromatici più complessi a causa delle differenze negli elementi ottici e dell’allineamento imperfetto tra i canali. Così, tali cambiamenti cromatici possono portare a una falsa conclusione a meno che non esplicitamente corretto dall’utente. Anche se i cambiamenti cromatici non sono stati un problema importante finché la risoluzione della microscopia è limitata dal limite di risoluzione classico, il recente sviluppo della microscopia a super-risoluzione1 ha spinto la necessità di una correzione più accurata dei cambiamenti cromatici.
È stata una pratica comune misurare gli spostamenti cromatici dei sistemi al microscopio utilizzando una diapositiva di calibrazione del tallone multicolore2. Il metodo di calibrazione basato sul tallone è appropriato per misurare gli spostamenti cromatici dall’intera ottica del microscopio alla superficie del coperchio2. Questo metodo, tuttavia, non è in grado di misurare i cambiamenti cromatici nei campioni biologici di interesse. È importante notare che molti campioni biologici sono tridimensionali (3D), e gli spostamenti cromatici di tali campioni sono diversi da quelli sulla superficie del coverslip. Inoltre, i cambiamenti cromatici cambiano con le condizioni di imaging2,3. Abbiamo misurato i cambiamenti cromatici nei campioni biologici 3D e abbiamo scoperto che l’incertezza dei cambiamenti cromatici era spesso pari a 350 nm con il classico metodo di calibrazione multicolore-perline3. Pertanto, i cambiamenti cromatici devono essere misurati in campioni biologici alla profondità di interesse e nelle condizioni di imaging utilizzate.
Qui, descriviamo le procedure per misurare i cambiamenti cromatici nei campioni biologici e correggere questi turni utilizzando il nostro software, Chromagnon3. Per misurare gli spostamenti cromatici nei campioni biologici, il nostro metodo utilizza due tipi di set di dati, un’immagine di “bersaglio” e un’immagine di “riferimento”. L’immagine “bersaglio” è un’immagine multicolore di interesse, ad esempio, immagini macchiate per DNA, involucro nucleare e microtubuli. Spesso è impossibile misurare i cambiamenti cromatici in tale immagine. Pertanto, abbiamo bisogno di un’immagine di “riferimento” dedicata per misurare i cambiamenti cromatici nel campione. L’unica definizione di immagine di “riferimento” è un’immagine multicolore dello stesso oggetto. In questo senso, un’immagine di perline multicolore è anche un tipo di immagine di riferimento. Qui descriviamo tre diversi tipi di immagine di riferimento che vengono utilizzati per misurare i cambiamenti cromatici nei campioni biologici: “immagini di riferimento trasversali”, “immagini di riferimento a campo luminoso” e “immagini di riferimento di calibrazione biologica”. Il tipo di immagine di riferimento dipende dal tipo di microscopio utilizzato o dalla precisione di correzione richiesta nella tabella 1.
| Diafonia | Campo luminoso | Calibrazione biologica (su un’altra diapositiva) | Calibrazione biologica (sullo stesso vetrino) | |
| Precisionea | +++ | + | B(B) b (B) | +++ |
| Semplicità | ++ | +++ | ++ | ++ |
| Microscopia applicabile | Campo largo | Campo largo | Tutti | Tutti |
| Disponibilità dell’allineamento locale | + | + | –c | –c |
|
a: Il numero di “” indica un aumento della valutazione. Single plus è di circa 50 nm e 3plus è di circa 15 nm in 3D. b: La precisione dipende da quanto le condizioni di imaging variabili sono mantenute costanti. c: La calibrazione locale misurata da campioni di perline multicolore può essere combinata come descritto nella sezione protocollo 4. |
||||
Tabella 1: Parametri quando si sceglie il tipo di immagini di riferimento.
Le “immagini di riferimento trasversali” hanno la massima precisione di correzione e sono relativamente semplici da realizzare3,4 ( Tabella1). Lo svantaggio è la loro limitazione nelle applicazioni di microscopia a causa della loro incapacità di misurare i cambiamenti cromatici nei percorsi di eccitazione. Inoltre, per ottenere tali immagini, il microscopio deve essere dotato di specchi dicrotice multibanda e di filtri di emissione controllati in modo indipendente dai filtri di eccitazione o dalle sorgenti luminose. La microscopia adatta include microscopia convenzionale a campo largo, microscopia di localizzazione a singola molecola (SMLM) come la microscopia di localizzazione foto-attivata/microscopia di ricostruzione ottica stocastica (PALM/STORM)5,6 e microscopia di espansione7 osservata con microscopia a campo largo. Un’immagine di riferimento cross-talk viene acquisita dal campione di destinazione stesso. È un’immagine di fluorescenza crosstalk (bleed-through) di un colorante ottenuto in tutti i canali richiesti. L’emissione di fluorescenza si espande sempre verso le lunghezze d’onda più lunghe, quindi i coloranti con la lunghezza d’onda di emissione più breve sono entusiasti di ottenere la fluorescenza a gambo incrociato in canali di lunghezze d’onda più lunghe. Ad esempio, quando il campione è macchiato di blu, verde e rosso, solo il colorante blu è eccitato e la luce di emissione viene ottenuta nei canali blu, verde e rosso. In questo protocollo, il DNA macchiato con 4,6-diamidino-2-fenilindole (DAPI) è stato utilizzato per ottenere la fluorescenza trasversale.
Le “immagini di riferimento a campo luminoso” sono un’alternativa più semplice e meno fototopede alle “immagini di riferimento incrociate”, ma sono le meno accurate3 (Tabella 1). Queste sono immagini di campo luminose del campione di destinazione, acquisite in tutti i canali di colore utilizzati nell’immagine di destinazione.
Le “immagini di riferimento di calibrazione biologica” hanno il vantaggio di essere applicabili a qualsiasi tipo di microscopia a causa della loro capacità di misurare i cambiamenti cromatici sia nei percorsi di eccitazione che di emissione3,8 (Tabella 1). La microscopia adatta comprende microscopia a campo largo, microscopia confocale, microscopia a foglio chiaro, esaurimento delle emissioni stimolate (STED)9,microscopia di illuminazione strutturata (SIM)10, Airyscan/SORA11,12, SMLM osservata con la modalità di fluorescenza totale della riflessione interna (TIRF), Olympus super risoluzione (OSR)13e così via. Un’immagine di riferimento di calibrazione biologica viene acquisita da un campione di calibrazione preparato in modo simile come il campione di destinazione, ma con colorazione di una singola struttura con più colori. La precisione di correzione eccelle la risoluzione della maggior parte della microscopia a super-risoluzione e la preparazione di un campione di calibrazione biologica può essere relativamente semplice. Un altro vantaggio è la disponibilità di immagini di riferimento multiple “media”. Pertanto, anche se le singole immagini contengono informazioni scadenti per la misurazione dei cambiamenti cromatici, il contenuto delle informazioni può essere aumentato calcolando la media di più immagini. La precisione dipende da quanto le condizioni di imaging sono mantenute costanti. A questo proposito, le migliori prestazioni si ottengono quando sia i campioni di riferimento di destinazione che quelli di riferimento si trovano sullo stesso vetrino, utilizzando, ad esempio, 8 vetrine a camere(tabella 1, più a destra). In questo protocollo, l’actin macchiato con tre colori di phalloidin è stato utilizzato come calibrazione biologica.
Una volta ottenuta un’immagine di riferimento, lo spostamento cromatico viene misurato e corretto dal nostro software Chromagnon. Non vi è alcuna limitazione sul numero di canali, sezioni e intervalli di tempo che Chromagnon può misurare e correggere i cambiamenti cromatici. Chromagnon misura i cambiamenti cromatici in due fasi. Il primo passo acquisisce i parametri di allineamento “globali” o “affini” della traslazione negli assi X, Y, z, l’ingrandimento lungo gli assi X, Y, z e la rotazione intorno all’asse . L’accuratezza di calcolo dell’allineamento globale è di 16 nm in 3D e di 8 nm in 2D. Il secondo passaggio è un “allineamento locale” iterativo 2D opzionale sulle immagini proiettate per ottenere una maggiore precisione. Nel processo di allineamento locale, le immagini sono suddivise in più regioni e vengono misurati i cambiamenti cromatici in queste regioni locali. Successivamente, le regioni vengono ulteriormente divise e gli spostamenti cromatici nelle sottoregioni vengono misurati iterativamente fino a quando il numero di pixel nell’area non raggiunge il numero minimo di pixel (in genere 60 x 60 pixel). La mappa di allineamento locale risultante viene combinata con il parametro di allineamento globale e viene applicata all’immagine di destinazione da una trasformazione elastica. Seguendo questo passaggio, la precisione del calcolo è stata migliorata a 14 nm in 3D e a 6 nm in 2D. L’allineamento locale non è adatto per le immagini di riferimento di calibrazione biologica perché la struttura biologica nel riferimento è diversa da quella nell’obiettivo (Tabella 1). Pertanto, solo l’allineamento globale viene utilizzato per le immagini di riferimento di calibrazione biologica.
I cambiamenti cromatici locali provengono da due fonti; distorsione locale strumentale al microscopio e inomogeneità strutturale biologica. Poiché la distorsione locale strumentale al microscopio è costante, questo può essere misurato dal campione di riferimento perline multicolore e corretto come parametro fisso. Chromagnon può combinare la mappa di distorsione locale strumentale al microscopio e i parametri di allineamento globali dalle calibrazioni biologiche (Tabella 1). Utilizzando questo metodo, si prevede che l’accuratezza media della calibrazione biologica sarà migliorata di un ulteriore 1-2 nm.
Qui, descriviamo un protocollo per correggere gli spostamenti cromatici delle immagini a fluorescenza 3D utilizzando il nostro software Chromagnon, dalla fascia bassa più facile alla massima precisione. Usiamo l’immunostaining delle cellule HeLa come esempio e le abbiamo osservate usando la microscopia 3D a campo largo e la 3D-SIM. Nella prima sezione viene descritto come preparare campioni target e campioni di calibrazione biologica. Questa parte del protocollo dovrebbe essere ottimizzata per gli obiettivi specifici della ricerca. Nella seconda sezione vengono descritti i metodi di acquisizione per tre tipi di immagini di riferimento al microscopio. L’ipotesi era quella di ottenere canali blu, verdi e rossi, ma la composizione dei canali dovrebbe essere modificata dagli obiettivi specifici della ricerca e dalle configurazioni del microscopio. Non importa se il microscopio è dotato di una singola telecamera o di più telecamere. Nella terza sezione, descriviamo come si può utilizzare il nostro software per misurare e correggere gli spostamenti cromatici dell’immagine di destinazione utilizzando immagini di riferimento. Infine, nella quarta sezione, descriviamo un metodo per integrare le immagini di riferimento della taratura biologica utilizzando la calibrazione locale strumentale di un microscopio.
Protocol
Representative Results
Discussion
La procedura per la correzione cromatica è un compromesso tra precisione e sforzo. Per risparmiare sforzi inutili, è meglio sapere quanta precisione è necessaria per il vostro studio. La massima precisione potrebbe non essere richiesta per l’imaging tradizionale a campo largo (dal vivo) e, pertanto, le immagini di riferimento luminose sono spesso sufficienti per correggere lo spostamento cromatico. Allo stesso modo, quando la condizione di imaging e l’ambiente sono costanti, l’uso ripetuto di una calibrazione biologica farà risparmiare tempo. D’altra parte, se si desidera una registrazione altamente accurata, sono necessarie immagini di riferimento trasversali o di calibrazione biologica di alta qualità. Per ottenere prestazioni ottimali, le immagini di riferimento devono essere ottenute con condizioni e tempi simili il più possibile le immagini di destinazione. Finché sia le immagini di riferimento che le immagini di destinazione sono ottenute dalla stessa microscopia, una maggiore risoluzione spaziale migliorerà la precisione di correzione. Se la deconvoluzione è disponibile sia per le immagini di riferimento che per le immagini di destinazione, l’implementazione di questa correzione prima della correzione può migliorare la precisione della correzione. Inoltre, per ottenere le migliori prestazioni, il teorema di campionamento per l’asse ottico (sezione) deve essere soddisfatto sia nel file di riferimento che in quello di destinazione per un’interpolazione precisa dei subpixel (passaggio del protocollo 2.1.3).
La mancata correzione del cambiamento cromatico porta a conclusioni errate. Inoltre, l’uso della calibrazione sbagliata può persino peggiorare i cambiamenti cromatici piuttosto che correggerli, e questo deve quindi essere evitato. Abbiamo riassunto le possibili cause degli errori e le loro soluzioni comuni nella tabella 2. Per esaminare la causa di un guasto, in primo luogo, è necessario controllare visivamente se lo spostamento cromatico nell’immagine di riferimento è corretto con precisione (passaggio del protocollo 3.12). La maggior parte degli errori sono dovuti alla qualità delle immagini di riferimento e sono facilmente risolvibili secondo le descrizioni nella tabella 2. Per quanto riguarda la qualità delle immagini di riferimento, è importante notare che la precisione dell’allineamento globale diminuisce se l’intero campo visivo non viene riempito con il campione (Figura 7, Tabella 2). Rispetto al buon esempio illustrato nella figura 7A, l’esempio non valido illustrato nella figura 7B contiene solo tre inviluppi nucleari nell’area superiore sinistra e Chromagnon non è riuscito ad allineare una parte di questa immagine. Questo perché il metodo di allineamento globale di Chromagnon divide il campo visivo in quattro regioni (Figura 7C) al fine di misurare le differenze di rotazione e ingrandimento con alta precisione3. Questo metodo, se correttamente utilizzato, è un ordine più preciso rispetto ad altri metodi lineari come la trasformazione polare del log e i metodi simplex3. Se una delle quattro regioni non è disponibile, Chromagnon passerà a metodi lineari meno efficaci. Pertanto, per ottenere prestazioni ottimali, gli esempi illustrati nella figura 7B e nella figura 7C sono indesiderati e le quattro aree devono essere riempite con oggetti. Gli utenti possono verificare se qualsiasi area quadratica del campo visivo non è disponibile per la misurazione esaminando il file di registro (“Chromagnon.log”; vedere il passaggio 3.10 del protocollo). Fortunatamente, questo problema può essere facilmente risolto calcolando la media di più immagini di calibrazione biologica o utilizzando l’allineamento locale per le immagini di riferimento crosstalk o bright-field (Tabella 2). Contrariamente al caso di mancata corretta delle immagini di riferimento, è più difficile identificare le immagini di destinazione. Poiché tali errori sorgono a causa di differenze nei formati di file, nelle condizioni di imaging, nei tempi di imaging, nei metodi di imaging/allineamento tra le immagini di riferimento e di destinazione (Tabella 2), gli utenti devono sempre prestare attenzione quando utilizzano immagini di riferimento ottenute in condizioni/intervalli diversi dalle immagini di destinazione. Alcune immagini di esempio sono disponibili per il test (https://github.com/macronucleus/Chromagnon) per ottenere un’idea concreta delle immagini di esempio buone e cattive.
| Problema | Causa | Soluzione |
| Impossibile correggere l’immagine di riferimento | Basso contrasto | Se possibile, acquisire un’immagine a contrasto più elevato. Se viene utilizzata un’immagine di riferimento di campo luminoso, riacquisire l’immagine in una soluzione basata sull’acqua per ottenere un contrasto maggiore della cella. In alternativa, provare ad applicare la riduzione del rumore computazionale (ad esempio il filtraggio gaussiano). Disattivare l’allineamento locale, che è più sensibile al disturbo. |
| Contaminazione di immagini non correlate | Se possibile, rimuovere l’origine delle immagini non correlate nell’esempio. Per le immagini di riferimento tra gambo, controllare gli spettri di eccitazione dei coloranti utilizzati per le immagini di destinazione. Se i coloranti sono eccitati durante l’acquisizione di un’immagine crosstalk (ad esempio Alexa Fluor 568 o 594), prendere in considerazione altri coloranti (ad esempio Alexa Fluor 555). Se le polveri sul chip della fotocamera creano un’ovvia differenza di canale, pulire il chip della fotocamera o utilizzare un metodo di applicazione a campo piatto computazionale. | |
| Un punto estremamente luminoso fatto da un raggio cosmico | Se possibile, acquisire nuovamente l’immagine. In alternativa, provate ad applicare la riduzione del rumore computazionale (ad es. filtro mediano o gaussiano). | |
| Artefatti di deconvoluzione (segnali artificiali ai bordi assiale e laterale) | Tagliare i pixel del bordo o le sezioni , dopo la deconvoluzione. Se un lato è tagliato, anche l’altro lato deve essere tagliato per mantenere il centro dell’immagine. | |
| La dimensione del passo di z troppo scarsa | Per soddisfare il criterio nyquist, come indicato nel protocollo 2.1.3, è necessario acquisire uno stack di tipo z. | |
| Aberrazione ottica | L’aberrazione sferica è la principale aberrazione causata dagli utenti. Scegliere l’obiettivo giusto per il campione e utilizzare uno spessore coverslip di 170 m. Se l’obiettivo è dotato di un anello di correzione, regolarlo per trovare la posizione in cui si ottiene il numero di fluorescenza più alto dalla messa a fuoco. Nel caso di un obiettivo di immersione dell’olio senza un anello di correzione, regolare l’indice di rifrazione dell’olio di immersione che aumenta il conteggio della fluorescenza al fuoco. | |
| Il campo visivo non è riempito (Fig. 7) | Nel caso delle immagini di riferimento della calibrazione biologica, mediamente molte immagini. Nel caso di immagini a gambo incrociato o a campo luminoso, utilizzare l’allineamento locale. | |
| Un bug software non identificato | Segnalare il problema tramite GitHub(https://github.com/macronucleus/Chromagnon/issues) | |
| Impossibile correggere l’immagine di destinazione | I metadati del file di immagine vengono persi | Utilizzare il formato di file dell’ambito originale che contiene metadati completi ed evitare la conversione in un file tiff a più pagine prima dell’elaborazione. Utilizzare lo stesso ordine dei canali come scritto nel protocollo 3.3. |
| Metodi di allineamento errati per la microscopia data | Non applicare il metodo di allineamento locale durante la misurazione da immagini di riferimento di calibrazione biologica alle immagini di destinazione. Non utilizzare immagini di riferimento a gambo incrociato diverse dalla microscopia a campo largo. | |
| Differenze nelle condizioni di imaging | Mantenere costanti le condizioni di imaging tra le immagini di riferimento e di destinazione come scritte nel protocollo 2.3.3. | |
| Differenze nel campione (compreso coverslip) | Utilizzare sempre lo stesso supporto di montaggio, coverslip (ad es. n. 1.5H) e una profondità di messa a fuoco simile. | |
| Deriva del microscopio dall’ultima | Effettuare una calibrazione tutte le volte ogni due settimane. Mantenere la temperatura costante e utilizzare una tabella mobile per evitare la deriva hardware del microscopio. |
Tabella 2: Risoluzione dei problemi relativi alla correzione cromatica.
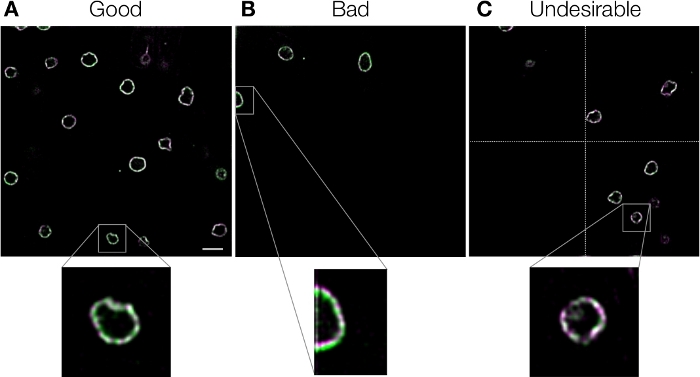
Figura 7: Esempi di immagini di riferimento. Busta nucleare in celle di lievito di fissione etichettate con GFP e mCherry. Le immagini sono state acquisite con la microscopia a campo largo convenzionale. I cambiamenti cromatici sono stati corretti utilizzando Chromagnon senza allineamento locale utilizzando le immagini stesse come immagini di riferimento. Le immagini sono state poi deconvolved per mostrare i dettagli. (A) Un buon esempio con molti oggetti nel campo visivo. (B) Un cattivo esempio con gli oggetti solo nell’angolo in alto a sinistra. Il disallineamento è evidente in una determinata regione dell’immagine. (C) Un esempio indesiderato in cui una delle quadrisezioni (separate da linee trasversali tratteggiate) è vuota. La barra della scala nel pannello A indica 5 m per la vista a campo intero e 1,25 m per la vista ingrandita ed è applicabile a tutti i pannelli. Fare clic qui per visualizzare una versione più grande di questa figura.
In questo protocollo sono stati descritti tre diversi tipi di riferimento(Tabella 1). Tra questi, le immagini di riferimento tra le gambo incrociate e le immagini di riferimento di calibrazione biologica necessitano di un’ulteriore attenta discussione. Per le immagini di riferimento ai concrologi, i campioni macchiati con DAPI o Hoechst 33342 e montati in glicerolo o supporti di montaggio commerciali possono essere utilizzati in modo efficiente per allineare i canali blu, verde e rosso. Allo stesso modo, Alexa Fluor 488 può essere utilizzato per allineare i canali verde e rosso. Tuttavia, ottenere la fluorescenza trasversale è spesso difficile dal momento che molti coloranti blu tranne DAPI e Hoechst sono dimmer e decadimento più velocemente rispetto alla maggior parte coloranti verdi e rossi. Inoltre, gli spettri di emissione dei coloranti moderni sono più stretti, il che rende difficile l’allineamento di più di tre canali con questo metodo. Attenzione dovrebbe essere prestata anche ad alcuni coloranti rossi comuni (ad esempio, Alexa Flour 568 e 594, ma non Alexa Fluor 555) che possono essere eccitati dalla luce viola, che impediscono di ottenere immagini di crosstalk ad alto contrasto da coloranti blu. Un altro inconveniente è che questo metodo non può misurare l’aberrazione cromatica dei percorsi di luce di eccitazione in eccitazione multicolore, perché solo una singola lunghezza d’onda di eccitazione viene utilizzata per l’eccitazione (Tabella 1). Poiché la microscopia più avanzata utilizza un’ottica di illuminazione alterata, l’applicazione di questo metodo è limitata. Tuttavia, la maggiore precisione di correzione è sufficientemente vantaggiosa per essere descritta in questo protocollo. In generale, un’immagine crosstalk deve essere scattata dopo un’immagine di destinazione per evitare effetti sbiancanti o fototossici. Per SMLM osservato con la modalità wide-field, un’immagine di riferimento deve essere acquisita prima di acquisire un’immagine di destinazione come coloranti a fluorescenza può essere sbiancata durante l’imaging.
Le immagini di riferimento della taratura biologica consentono agli utenti di allineare facilmente qualsiasi numero desiderato di canali a costo di una preparazione aggiuntiva del campione. Un altro vantaggio delle immagini di riferimento della taratura biologica è la disponibilità di “media” più riferimenti che aiuta a riempire tutti i campi visivi. Questo metodo può soffrire di differenze nelle condizioni di imaging se il campione di calibrazione viene preparato su un vetrino diverso. La maggior parte di questo problema può essere risolta se sia le destinazioni che i riferimenti vengono preparati sulla stessa diapositiva utilizzando le coperture a camere commerciali (Tabella 1) e altre condizioni di imaging sono mantenute costanti come nel passaggio di protocollo 2.3.3. In questo caso, ci si può aspettare una precisione di correzione simile a quella delle immagini di riferimento del gambo incrociato3. Il protocollo per l’utilizzo della falloidina come mostrato qui è uno dei modi più semplici per macchiare una singola struttura cellulare con più colori. Ci sono numerosi scenari possibili per preparare campioni di calibrazione biologica. Per l’immunostaining, un campione può essere etichettato con un singolo anticorpo primario seguito da colorazione con anticorpi secondari di più colori. In questo modo, una singola struttura di destinazione può essere etichettata con più colori. In alternativa, 5-ethynyl-2′-deoxyuridina, rilevata da etichette chimiche “click” appena sintetizzate DNA in più colori ad alta densità, come descritto nel dettaglio precedentemente8. Per le cellule vive, è utile preparare un ceppo transgenico che ospita due copie di un gene che vengono fuse in GFP o mCherry per etichettare la stessa struttura con due colori. Se il numero di copie del gene è critico come spesso osservato per le proteine della membrana, una singola copia del gene può essere tandemly fusa a GFP e mCherry (Figura 7). Le proteine fluorescenti fotoconvertibili, come mEOS218, possono essere utilizzate anche illuminando un livello moderato di luce viola per ottenere entrambe le specie proteiche con o senza fotoconversione. In basse condizioni di ossigeno, GFP può anche essere utilizzato come proteina fotoconvertibile dal verde al rosso19,20. La scelta del campione di calibrazione corretto renderà quindi l’esperimento più robusto.
Divulgazioni
The authors have nothing to disclose.
Acknowledgements
Questo studio è stato supportato da JSPS KAKENHI Grant Numbers JP19H03202 a A.M., JP18H05528 e JP17H03636 a T.H. e JP17H01444 e JP18H05533 a H.Y. L.S. riconoscono il supporto dei Welcome Trust Strategic Awards 091911 e 107457 / 15 / 15 / s risparmio avanzato presso Micron Oxford.
Materials
| 16% formaldehyde solution | Polyscience | 18814-10 | |
| 35 mm glass-bottom dish | MatTek | P35G-1.5-10-C | |
| Alexa Fluor 405 phalloidin | Thermo Fisher Scientific | A30104 | |
| Alexa Fluor 488 phalloidin | Thermo Fisher Scientific | A12379 | |
| Alexa Fluor 594 phalloidin | Thermo Fisher Scientific | A12381 | |
| Bovine Serum | Thermo Fisher Scientific | 16170078 | |
| Coverslip | Matsunami | No. 1S HT | |
| DAPI (4',6-Diamidino-2-Phenylindole, Dihydrochloride) | Thermo Fisher Scientific | D1306 | |
| Dulbecco’s Modified Eagle Medium with L-Gln and sodium pyruvate | Nacalai Tesque | 08458-16 | |
| Mounting medium (VECTASHIELD) | Vector Laboratories | H-1000 | |
| Mouse anti-tubulin monoclonal antibody (TAT1) | Described in Ref 15. | ||
| Nunc Lab-Tek II chambered coverglass (8 well) | Thermo Fisher Scientific | 155409 | |
| Rabbit anti-emerin polyclonal antibody (ED1) | A gift from Hiroshi Yorifuji, Gunma University, Gunma, Japan and Kiichi Arahata, National Center of Neurology and Psychiatry, Tokyo, Japan; deceased. | ||
| Secondary antibody with Alexa Fluor 488 | Thermo Fisher Scientific | A-11034 | |
| Secondary antibody with Alexa Fluor 555 | Thermo Fisher Scientific | A-21424 | |
| Secondary antibody with Alexa Fluor 594 | Thermo Fisher Scientific | A-11032 | |
| TetraSpeck Microspheres, 0.2 µm | Thermo Fisher Scientific | T7280 |
Riferimenti
- Schermelleh, L., et al. Super-resolution microscopy demystified. Nature Cell Biology. 21 (1), 72-84 (2019).
- Manders, E. M. M. Chromatic shift in multicolour confocal microscopy. Journal of Microscopy. 185 (3), 321-328 (1997).
- Matsuda, A., Schermelleh, L., Hirano, Y., Haraguchi, T., Hiraoka, Y. Accurate and fiducial-marker-free correction for three-dimensional chromatic shift in biological fluorescence microscopy. Scientific Reports. 8 (1), 7583 (2018).
- Grünwald, D., Singer, R. H. In vivo imaging of labelled endogenous β-actin mRNA during nucleocytoplasmic transport. Nature. 467 (7315), 604-607 (2010).
- Betzig, E., et al. Imaging intracellular fluorescent proteins at nanometer resolution. Science. 313 (5793), 1642-1645 (2006).
- Rust, M. J., Bates, M., Zhuang, X. Sub-diffraction-limit imaging by stochastic optical reconstruction microscopy (STORM). Nature Methods. 3 (10), 793-795 (2006).
- Chen, F., Tillberg, P. W., Boyden, E. S. Expansion microscopy. Science. 347 (6221), 543-548 (2015).
- Kraus, F., et al. Quantitative 3D structured illumination microscopy of nuclear structures. Nature Protocols. 2, 1011-1028 (2017).
- Hell, S. W. Far-Field Optical Nanoscopy. Science. 316 (5828), 1153-1158 (2007).
- Gustafsson, M. G. L. Surpassing the lateral resolution limit by a factor of two using structured illumination microscopy. Journal of Microscopy. 198 (2), 82-87 (2000).
- Schulz, O., et al. Resolution doubling in fluorescence microscopy with confocal spinning-disk image scanning microscopy. Proceedings of the National Academy of Sciences of United States of America. 110 (52), 21000-21005 (2013).
- Müller, C. B., Enderlein, J. Image Scanning Microscopy. Physical Review Letters. 104 (19), 198101 (1981).
- Hayashi, S., Okada, Y. Ultrafast superresolution fluorescence imaging with spinning disk confocal microscope optics. Molecular Biology of the Cell. 26 (9), 1743-1751 (2015).
- Yorifuji, H., et al. Emerin, deficiency of which causes Emery-Dreifuss muscular dystrophy, is localized at the inner nuclear membrane. Neurogenetics. 1 (2), 135-140 (1997).
- Woods, A., Sherwin, T., Sasse, R., MacRae, T. H., Baines, A. J., Gull, K. Definition of individual components within the cytoskeleton of Trypanosoma brucei by a library of monoclonal antibodies. Journal of Cell Science. 93 (3), 491-500 (1989).
- Tokunaga, M., Imamoto, N., Sakata-Sogawa, K. Highly inclined thin illumination enables clear single-molecule imaging in cells. Nature Methods. 5 (2), 159-161 (2008).
- Rueden, C. T., et al. ImageJ2: ImageJ for the next generation of scientific image data. BMC Bioinformatics. 18 (1), 529 (2017).
- McKinney, S. A., Murphy, C. S., Hazelwood, K. L., Davidson, M. W., Looger, L. L. A bright and photostable photoconvertible fluorescent protein for fusion tags. Nature Methods. 6 (2), 131-133 (2009).
- Sawin, K. E., Nurse, P. Photoactivation of green fluorescent protein. Current Biology. 7 (10), 606-607 (1997).
- Elowitz, M. B., Surette, M. G., Wolf, P. E., Stock, J., Leibler, S. Photoactivation turns green fluorescent protein red. Current Biology. 7 (10), 809-812 (1997).

