优化用于连续晶体学实验的内硫肽晶体的生长
Summary
本文的目的是让观众深入了解如何将用于生长大单蛋白晶体的小体积气扩散方案转化为用于连续晶体学的大体积批量微结晶方法。
Abstract
本文提出了一种协议,以促进创建适用于同步加速器和XFEL连续晶体学实验的大体积(>100μL)微晶浆料。该方法基于对蛋白质晶体相图的理解,以及如何利用这些知识。该方法分为三个阶段:(1)优化晶体形态,(2)过渡到批次,(3)缩放。第 1 阶段涉及发现衍射良好的单晶,希望但不一定以立方体状形态呈现。在第 2 阶段,阶段 1 条件通过晶体生长时间进行优化。这种策略可以将通过气相扩散生长的晶体转化为批量。一旦晶体生长可以在大约24小时内发生,就可以绘制蛋白质和沉淀剂混合物的形态图并用作缩放策略的基础(阶段3)。当晶体可以批量生长时,可以尝试缩放,并且随着体积的增加而优化晶体尺寸和浓度。内硫肽已被用作该方案的示范蛋白。提出的一些决定是针对内硫肽的。但是,希望它们的应用方式将激发一种思考该程序的方式,其他人可以适应自己的项目。
Introduction
室温(RT)大分子晶体学在结构生物学界再次流行。X射线自由电子激光(XFEL)光源的发展刺激了RT样品输送方法1,2,3,4的发展,这些方法现已应用于同步加速器5,6,7,8。RT方法不仅开辟了泵浦探针实验策略9,10,11,12的可能性,而且越来越多的证据表明它们促进了蛋白质13,14,15,16,17中的替代构象状态。
然而,低温方法在 1990 年代后期获得 RT 方法的牵引力的主要原因是零下晶体温度减缓了辐射损伤18。冷冻方法19开始允许从单个蛋白质晶体收集完整的数据集。XFEL和同步加速器的现代RT方法通过开发快速(> 100 Hz)晶体输送策略解决了单晶辐射损伤的问题1,2,3,4。这些方法允许从数千个单独暴露的晶体中收集完整的数据集。因此,这些RT给药方法需要生产大量含有均匀微晶体(>100 μL<50 μm晶体)的溶液。然而,由于冷冻方法往往只需要单晶,因此制造这种微晶浆料的方法目前在蛋白质晶体学实验室中并不普遍。
文献中有一些关于如何对连续晶体学样品进行部分微结晶优化程序的示例。在这里,应该区分膜蛋白和可溶性蛋白。优化在单油酸(或一些其他脂质)中生长的微膜蛋白晶体生长的用于脂质立方相(LCP)的方案已经很好地描述了20,21,22。然而,通常缺乏可溶性蛋白质(包括在非LCP条件下生长的膜蛋白)微结晶的方法。以前的研究集中在该过程的特定部分,例如微晶筛选23,24,增强成核24以及使用自由界面扩散25进行缩放,但不是完整的方法。
然而,最近描述了一种方法26 ,它试图提供完整的协议。像蛋白质晶体学的许多方面一样,它并不新鲜。Rayment (2002)27已经描述了提出的许多想法。该方法旨在向晶体学家展示如何从使用蒸汽扩散生长的单个晶体转换为生长数千个微晶体的批量方法。该方法侧重于蒸汽扩散作为共同起点,因为95%的蛋白质数据库(PDB)沉积来自在气相扩散板26中生长的晶体。然而,气相扩散不是微结晶的理想方法26,因此描述了一种将气相扩散转换为批量结晶的方法。一旦晶体可以批量生长,将途径扩展到更大的体积变得更加可行。鉴于蛋白质结晶的变幻莫测,作者会强调这种方法不是万无一失的。然而,该方案至少应该提供对蛋白质“结晶空间”的洞察。
该方法依赖于蛋白质结晶相图,以及对该图的理解如何在微结晶优化过程中起到指导作用。蛋白质相图通常描述为x/y图,沉淀剂和蛋白质浓度分别位于x轴和y轴上(图1A)。从纯水点(左下角 – 图1A),蛋白质和沉淀剂的浓度增加,直到达到溶解度线。溶解度线标记过饱和点(紫色线 – 图1A)。当蛋白质过饱和时,溶液在热力学上变得不稳定,并开始分离成两相:“富含蛋白质”和稳定的饱和溶液。这种分离可能发生在溶解度线以外的任何地方,其动力学取决于蛋白质的性质和溶液的成分。
当蛋白质和沉淀剂浓度太大时,蛋白质会不稳定地分解出溶液并导致无定形沉淀(粉红色区域 – 图1A)。然而,有序相分离可能发生在成核区域[详见Garcia-Ruiz(2003)28 ],并且晶体核具有形成倾向(绿色区域 – 图1A)。成核和生长从溶液中去除蛋白质并将液滴移动到亚稳区域,在那里生长可以继续,直到达到溶解度线[参见McPherson和Kuznetsov (2014)29 的详细讨论]。对于绝大多数结晶条件,该图是严重过度简化30。然而,无论如何,该图对于微晶体学家来说仍然非常有用,因为该图的映射允许确定溶解度线和成核动力学。
在制造微晶方面,结晶过程中需要优化的两个因素是晶体数量(Xn)及其平均最长尺寸(Xs)。X n 将与成核事件的数量 (n ) 成正比(公式 1)。
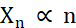 公式 1
公式 1
X s 与溶解度线 (Ps) 上方的游离蛋白浓度除以 Xn(方程 2)成正比。
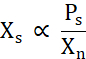 等式 2
等式 2
在理想情况下,每次成核事件都会产生一个可能的晶体,并且这些晶体中的每一个都可以平等地获得溶液中的可用蛋白质。 图 2 是 Xn 和 Xs 之间关系的理想场景的图形表示。实际上,晶体学家对Xn 和Xs 的主要控制是通过影响成核量或添加种子晶体。微晶体学家必须判断如何增加Xn ,以便可以产生合适的晶体浓度和晶体尺寸。
大多数结晶技术都需要一个“过渡期”(图1B)。例如,在蒸汽扩散实验中,在混合蛋白质和沉淀剂溶液时,每种溶液的浓度会随着液滴与孔溶液的平衡而变化。人们希望这些变化将逐渐将液滴过渡到结晶倾向增加的成核区。随着晶体开始成核和生长,溶液中的蛋白质量将开始下降,从而降低进一步成核的可能性。最终的成核量将取决于蛋白质和条件特异性,并且还取决于进入成核区的深度。鉴于需要过渡步骤的方法的成核区渗透有限,成核水平最终将限制在亚稳-成核区边界处的成核速率。
由于能够提高微晶体学家的成核水平非常重要,因此转向批量结晶方法非常重要。批量可以更好地利用整个成核区域(图1C)。在批量方法中,这个想法是将蛋白质和沉淀剂混合在一起,这样就可以产生过饱和溶液,而无需改变成分浓度。混合后应可立即成核。因此,批量方法允许理论上达到整个成核区。然后可以利用超过亚稳-成核边界的任何成核动力学增加。
如果晶体成核的基础水平不足以产生大的Xn,则可以使用微晶种方法。在微晶种中,预先生长的晶体被分解以产生结晶碎片浆液,该浆液可以作为新鲜晶体生长的支架31,32。微晶种已广泛用于连续晶体学样品制备,作为一种无需增加晶体成核即可增加 Xn 的方法(图 1C)。
从气相扩散到间歇的转变可以在相图上可视化为将实验起点从非过饱和或亚稳区域移动到成核区。这可以通过增加蛋白质和/或沉淀剂浓度和/或液滴内两者的比例来完成(图1D),并观察哪些条件产生快速出现的晶体(<24小时)26。完全的蒸气扩散滴平衡可能需要数天或数周33。因此,通过寻找显示快速出现的晶体的条件,可以找到批次条件,而不必转向替代结晶筛选形式,例如微批次34,35,36,37。
一旦找到成核区,就发现了批次条件,并且可以创建一个形态图 – 这里是一个粗略的相图 – 可以创建。在考虑是使用种子批次还是直接批次协议时,形态图非常有用。通过将Xn绘制为蛋白质和沉淀剂浓度的函数,可以对成核动力学进行评估26。如果 X n 在整个成核区域中保持较低水平,则可能需要晶种批次以使 Xn 足够大以限制晶体生长。该评估是扩展到更大体积(> 100 μL)过程的第一步。
该方法的设计使得它可以通过使用标准的气相扩散结晶设备在大多数结晶实验室中进行。还进行了许多研究,这些研究描述了在设备可用的情况下促进该过程许多部分的技术。这些包括但不限于动态光散射 (DLS)25,27、非线性成像 20、24、25、粉末衍射 20、24、27 和电子显微镜 26 [参见 Cheng 等人 (2020)40 以获得很好的评论]。
这项工作的目的是提供从小体积( 100 μL)批量结晶的方法的直观演示。来自 Cryphonectria parasitica 的Endothiapepsin已被用作证明这种翻译的示例系统。需要微晶体的实验类型和样品输送方法将影响理想的Xs 输出26。对于需要毫秒时间分辨率41 或气体动力虚拟喷嘴42的混合实验,最终Xs <5μm可能是可取的。在这种情况下,目标是产生衍射到约1.5 Å的蛋白质晶体,用于光子激活的泵浦探针实验,并使用固定目标传递方法。
为了说明使用内硫肽进行这种系列晶体学实验的样品要求, 表1 显示了假设实验的实验参数。示例信息基于下面描述的协议。鉴于对命中率和数据收集要求的一些保守估计,50毫克是整个实验的总样本消耗估计值。
图3显示了从最初的小体积蒸汽扩散结晶到大规模批次的完整优化过程的流程图。对于大多数系列晶体学项目,该协议将从步骤2开始:“过渡到批次”,因为目标蛋白质已经结晶。但是,为了完整起见,已包括步骤1,并提醒读者其重要性。找到产生衍射良好、单个大晶体的条件是微晶体优化的最佳起点。在步骤2中,可以将该条件从气相扩散优化为批量,并且可以绘制成核和亚稳区域的形态图。完成此操作后,可以在步骤 3 中将批处理条件缩放到更大的卷。在流程图结束时,晶体学家将创建一个可重复的大体积(> 100 μL)、微结晶、内硫肽的批量方案。然后可以将该方法应用于它们感兴趣的特定蛋白质。
Protocol
Representative Results
Discussion
所介绍的方法显示了如何优化内噻肽的结晶,从在稀疏基质96孔筛网中生长的大晶体(≥100μm最长尺寸)到在离心管(300μL 体积)中 通过批量生长的微晶体。该协议背后的想法是,优化内硫肽的步骤也可用于其他蛋白质。最终,回答了在XFEL和同步加速器上进行连续晶体学实验的产生大量(>100μL)微晶体(10-20μm)的问题。
该协议将大体积微结晶的任务分为三个步骤:(1)优化晶体形态,(2)过渡到批量,以及(3)缩放。在步骤1中,应在蒸汽扩散板中探索蛋白质可以产生的晶体形式范围。产生衍射到所需分辨率的单个盒状晶体的条件应该是目标。在步骤2中,可以将选定的条件从蒸汽扩散转换为批量。在这里,优化标准是晶体生长时间,并找到在24小时内产生蛋白质晶体的条件。还可以绘制形态图,使实验者了解溶解度线和成核区边界的位置。此形态图在步骤 3“缩放”中非常有用。形态图将指示单独成核是否可以增加Xn 并降低Xs。随着实验量的增加,Xn 和Xs 可以作为扩展成功的关键标准进行持续评估。
在Endothiapepsin的情况下,步骤1发现了内硫肽的潜在以前未知的晶体形态。这种形态具有与先前报道的相同的空间群,但对于连续晶体学来说,重要的是,它更像盒子的形状。单晶似乎也从单核点生长,不像其他条件产生的风扇(图4)。对于所选条件,步骤2已经部分满足,因为晶体生长发生在<24小时内。形态图表明,在步骤3中缩放时,直接或种子批处理方案都可能成功。初始按比例分批,产生了Xn 和Xs 范围分别为3.6±1.2 x 106 晶体·mL-1 和42 ± 4.1 μm的晶体的条件。这些晶体虽然对于一些系列晶体学实验来说是可以接受的,但被认为太大了。因此进行了额外的优化。最终方案制备的晶体浓度和尺寸范围分别为3.1 x 106 晶体·mL-1 和15 ± 3.9 μm。这对于计划的实验来说非常理想。
该方法侧重于将气相扩散板中生长的“可溶性”蛋白质晶体转化为批次。这种关注的原因是绝大多数可溶性蛋白质晶体是通过蒸汽扩散生长的26。然而,所提出的概念也可以应用于使用其他方法(例如微批次)生长的可溶性蛋白质晶体。这些概念也可能适用于在LCP中生长的膜蛋白晶体;因为这也是一个批量结晶过程。
该方案的一个关键方面是改变在蒸汽扩散板中生长的晶体条件的过程,以便它们可以批量生长。对于这种转换,该方法使用Beale等人(2019)提出的标准26。通过批量过程生长的晶体,即使在蒸汽扩散板中,也会迅速形成(<24小时)。该准则是基于蒸汽扩散液滴平衡速度的近似值,对于基于PEG的沉淀剂条件最为正确。然而,结晶条件将包含多种化合物,这些化合物会影响平衡时间。盐基结晶条件(例如高浓度氯化铵)的平衡可以在 1-2 天内完成。因此,24小时标准可能不适用于盐基条件。基于盐的条件也可以具有更复杂的相图26,30,这些相图可能不符合本协议中提出的原型。如果证明不可能扩展到更大的体积,则可能需要将盐基条件的时间标准减少到 12 或 6 小时。
这种方法的另一个限制是其明显的复杂性。优化内噻菌素微结晶的方案实际上从稀疏基质筛选中改变了原始条件。在PACT筛选中观察到的第一个命中是0.1 HEPES pH 7.0,0.2 M MgCl2和20%(w / v)PEG 6,000。最终的缩放结晶缓冲液为0.1 Tris-HCl pH 7.0,0.15 M MgCl2和40% (w / v)PEG 6,000。缓冲液从HEPES到Tris-HCl的变化以及MgCl 2 浓度也很有可能对该过程的成功贡献不大。将PEG 6,000浓度的增加作为唯一的优化,并且可以非常简单地实现。
然而,这种评估也过于简单化。它不仅忽略了结垢过程中遇到的问题(即 使用种子和淬灭),而且还忽略了这样一个事实,即仅仅因为这种蛋白质被证明是直截了当的,不能保证下一个也会被证明是。方案中建议的步骤之所以设计,是因为优化蛋白质结晶体积的缩放可能非常昂贵的蛋白质。在显示的七项内硫肽缩放试验中,消耗了100毫克蛋白质。诚然,其中一些步骤是为了根据该协议显示其后果而执行的。即便如此,100毫克的蛋白质,加上实验期间可能消耗的另外50毫克蛋白质(表1),可能是对时间或金钱的重大投资。
幸运的是,目前尚不清楚这种所需样品的质量是否在所有蛋白质中无处不在。内硫肽是高度可溶的,因此需要大浓度的蛋白质才能达到过饱和度。在其他情况下(目前正在优化中),过饱和度可以达到10甚至5 mg/mL。这些变量是蛋白质特异性的,当它们出现时需要接受。
该方法的其他局限性包括它依赖于复杂的设备,例如用于屏幕和孔板创建的液体处理机器人,以及在需要时自动对印版进行成像的成像仪。已经提供了替代例程来限制其中一些设备的需求,但是如果没有它们,协议将更加耗时。该协议还建议测试优化晶体的衍射。对于无法定期使用同步加速器的晶体学家来说,这些测试可能具有挑战性。可能不需要在每个步骤中进行控制,但强烈建议在确定匹配后进行这些测试,并在缩放前后进行。不幸的是,XFEL上的非衍射晶体并不少见。鉴于此,最好谨慎对待晶体衍射的假设。
最终,此处介绍的该协议和结果将为那些努力为连续晶体学实验生产样品的人提供指南,想法和示例。希望随着连续晶体学的进一步发展,该技术的样品需求将减少,从而减少对此类协议的需求。然而,即使在这种情况下,这里提出的策略对于那些希望探索其蛋白质结晶空间的人来说仍然有用。
Divulgazioni
The authors have nothing to disclose.
Acknowledgements
该项目已根据玛丽·斯克洛多夫斯卡-居里赠款协议第 701647 号获得了欧盟地平线 2020 研究和创新计划的资助。非常感谢瑞士光源光束线X10SA-PXII光束线科学家的帮助和支持。
Materials
| Swissci 96-well 2-Drop plates | Molecular Dimensions | MD11-002 | 96-well 2-drop crystallisation plate |
| Swissci 96-well 3-Drop plates | Molecular Dimensions | MD11-003 | 96-well 3-drop crystallisation plate |
| mosquito LCP liquid handling robot | sptlabtech | mosquito LCP | Crystallisation robot |
| ClearVue Sheets | Molecular Dimensions | MD6-015 | 96-well crystallization plate seals |
| Safe-Tube 1.5 mL | Eppendorf | 30120086 | 1.5 mL centrifuge tubes |
| Scaple | Swan and Morton | No. 3 scalple and No. 3 handle | Scalple for cutting open plate seals |
| MS 3 Vortex | IKA | 3319000 | Vortex for mixing solution and making seed stocks |
| 24-well XRL Plate | Molecular Dimensions | MD3-11 | 24-well hanging-drop plates |
| Tube revolver/rotator | Thermo Fischer Scientific | 88881001 | Tube revolver for mixing solution during scaling |
| Eppendorf Research plus pipettes | Eppendorf | Range of manual pipettes, 0.5-10, 1-20, 10-100, 100-1000 µL | |
| Eppendorf pipette tips | Eppendorf | Range of tip sizes for manual pipettes | |
| Suparen 600 | Prochem AG | Suparen 600 | Endothiapepsin solution |
| Sodium Acetate | Sigma-Aldrich | 241245-1KG | Sodium Acetate |
| Tris | Merck | 8382T014 | Tris |
| Magnesium Chloride | Sigma-Aldrich | M2670-1kg | Magnesium Chloride |
| PEG 6,000 | Sigma-Aldrich | 81255-1kg | PEG 6,000 |
| Ethelyene glycol | Sigma-Aldrich | 324558-1L | Ethelyene glycol for cyro-protecting the crystals |
| PACT Premier HT screen | Molecular Dimensions | MD1-36 | PACT Premier 96-well crystal screen |
| DOW CORNING high vacuum grease | Molecular Dimensions | MD6-02 | Grease for sealing 24-well plates |
| Hirschmann 22 x 22 mm glaser cover slides | Hirschmann | 8000104 | Cover slides for sealing 24-well sitting drop plates |
| Crystal pins | PSI | Manufactured inhouse | Thin-film supports for micro-crystals. |
| 1-1.3 mm SiLibeads Type S | Faust | 6239547 | Glass beads for making mico-seed stocks |
| Macbook Pro | Apple | Macbook Pro | Computer for performing data analysis |
| CCP4 software suite | CCP4 | Diffraction pattern data processing software | |
| Excel | Microsoft | Microsoft Office | Plotting tool for phase diagram |
| Hausser Scientific Bright-Line counting chamber | Thermo Fischer Scientific | 02-671-51B | Tool to calculate crystal concentration |
| PACT Premier | Molecular Dimensions | MD1-29-ECO | Sparse-matrix crystallization screen |
| Rock Imager | Formulatrix | Rock Imager | Temperature controlled crystal plate storage and imager |
| Rock MakerWeb | Formulatrix | Rock MakerWeb | Crystal plate creation and image storage stoftware |
| Formulator | Formulatrix | Formulator | 96-well crystal screen creation liquid handling robot |
| Leica MZ16 Microscope | Leica | Leica MZ16 | Light microscope |
| LAS V4.6 | Leica | LAS V4.6 | Software for Leica microscopes |
| Spectra/Por 3.5 kDa dialysis tubing | Spectrumlabs | Spectra/Por 3 Dialysis Membrane | 3.5 kDa dialysis membrane |
| Dialysis tubing closures | Spectrumlabs | Spectra/Por 3 Duniversal Closures | Clips to seal the dialysis tubing ends |
| Amicon 10 kDa centrifugal concentrator | Merck-Millipore | Amicon Ultra-15 10 kDa centrifugal concentrator | 10 kDa centrifugal filter |
| 5810 R swing bucket centrifuge | Eppendorf | 5810 R Centrifuge | Swing bucket centrifuge |
Riferimenti
- DePonte, D. P., et al. Gas dynamic virtual nozzle for generation of microscopic droplet streams. Journal of Physics D: Applied Physics. 41 (19), 195505 (2008).
- Hunter, M. S., et al. Fixed-target protein serial microcrystallography with an x-ray free electron laser. Scientific Reports. 4 (1), 6026 (2014).
- Weierstall, U., et al. Lipidic cubic phase injector facilitates membrane protein serial femtosecond crystallography. Nature Communications. 5 (1), 1-6 (2014).
- Roessler, C. G. G., et al. Acoustic Injectors for Drop-On-Demand Serial Femtosecond Crystallography. Structure. 24 (4), 631-640 (2016).
- Sherrell, D. A., et al. A modular and compact portable mini-endstation for high-precision, high-speed fixed target serial crystallography at FEL and synchrotron sources. Journal of Synchrotron Radiation. 22 (6), 1372-1378 (2015).
- Roedig, P., et al. A micro-patterned silicon chip as sample holder for macromolecular crystallography experiments with minimal background scattering. Scientific Reports. 5 (1), 1-11 (2015).
- Botha, S., et al. Room-temperature serial crystallography at synchrotron X-ray sources using slowly flowing free-standing high-viscosity microstreams. Acta Crystallographica Section D Biological Crystallography. 71 (2), 387-397 (2015).
- Weinert, T., et al. Serial millisecond crystallography for routine room-temperature structure determination at synchrotrons. Nature Communications. 8 (1), 542 (2017).
- Tenboer, J., et al. Time-resolved serial crystallography captures high-resolution intermediates of photoactive yellow protein. Science. 346 (6214), 1242-1246 (2014).
- Nango, E., et al. A three-dimensionalmovie of structural changes in bacteriorhodopsin. Science. 354 (6319), 1552-1557 (2016).
- Suga, M., et al. Light-induced structural changes and the site of O=O bond formation in PSII caught by XFEL. Nature. 543 (7643), 131-135 (2017).
- Mehrabi, P., et al. Liquid application method for time-resolved analyses by serial synchrotron crystallography. Nature Methods. 16 (10), 979-982 (2019).
- Halle, B. Biomolecular cryocrystallography: structural changes during flash-cooling. Proceedings of the National Academy of Sciences of the United States of America. 101 (14), 4793-4798 (2004).
- Fraser, J. S., et al. Hidden alternative structures of proline isomerase essential for catalysis. Nature. 462 (7273), 669-673 (2009).
- Fenwick, R. B., van den Bedem, H., Fraser, J. S., Wright, P. E. Integrated description of protein dynamics from room-temperature X-ray crystallography and NMR. Proceedings of the National Academy of Sciences of the United States of America. 111 (4), 445-454 (2014).
- Keedy, D. A., et al. Mapping the conformational landscape of a dynamic enzyme by multitemperature and XFEL crystallography. Elife. 4, (2015).
- Thomaston, J. L., et al. XFEL structures of the influenza M2 proton channel: Room temperature water networks and insights into proton conduction. Proceedings of the National Academy of Sciences of the United States of America. 114 (51), 13357-13362 (2017).
- Haas, D. J., Rossmann, M. G. Crystallographic studies on lactate dehydrogenase at -75 °C. Acta Crystallographica Section B Structural Crystallography and Crystal Chemistry. 26 (7), 998-1004 (1970).
- Hope, H. Cryocrystallography of biological macromolecules: a generally applicable method. Acta Crystallographica Section B Structural Science. 44 (1), 22-26 (1988).
- Wu, W., et al. Batch crystallization of rhodopsin for structural dynamics using an X-ray free-electron laser. Acta Crystallographica Section:F Structural Biology Communications. 71 (7), 856-860 (2015).
- Ishchenko, A., Cherezov, V., Liu, W. Preparation and delivery of protein microcrystals in lipidic cubic phase for serial femtosecond crystallography. Journal of Visualized Experiments. (115), e54463 (2016).
- Andersson, R., et al. Well-based crystallization of lipidic cubic phase microcrystals for serial X-ray crystallography experiments. Acta Crystallographica Section D: Structural Biology. 75 (10), 937-946 (2019).
- Luft, J. R., et al. The detection and subsequent volume optimization of biological nanocrystals. Structural Dynamics. 2 (4), 041710 (2015).
- Lee, D. B., et al. Supersaturation-controlled microcrystallization and visualization analysis for serial femtosecond crystallography. Scientific Reports. 8 (1), 1-10 (2018).
- Kupitz, C., et al. Microcrystallization techniques for serial femtosecond crystallography using photosystem II from Thermosynechococcus elongatus as a model system. Philosophical transactions of the Royal Society of London. Series B, Biological Sciences. 369 (1647), 20130316 (2014).
- Beale, J. H., et al. Successful sample preparation for serial crystallography experiments. Journal of Applied Crystallography. 52, 1385-1396 (2019).
- Rayment, I. Small-scale batch crystallization of proteins revisited: An underutilized way to grow large protein crystals. Structure. 10 (2), 147-151 (2002).
- García-Ruiz, J. M. Nucleation of protein crystals. Journal of Structural Biology. 142 (1), 22-31 (2003).
- McPherson, A., Kuznetsov, Y. G. Mechanisms, kinetics, impurities and defects: Consequences in macromolecular crystallization. Acta Crystallographica Section F:Structural Biology Communications. 70 (4), 384-403 (2014).
- Rupp, B. Origin and use of crystallization phase diagrams. Acta crystallographica. Section F, Structural biology communications. 71, 247-260 (2015).
- Luft, J. R., DeTitta, G. T. A method to produce microseed stock for use in the crystallization of biological macromolecules. Acta Crystallographica Section D Biological Crystallography. 55 (5), 988-993 (1999).
- Ireton, G. C., Stoddard, B. L. Microseed matrix screening to improve crystals of yeast cytosine deaminase. Acta crystallographica. Section D, Biological crystallography. 60 (3), 601-605 (2004).
- Forsythe, E. L., Maxwell, D. L., Pusey, M. Vapor diffusion, nucleation rates and the reservoir to crystallization volume ratio. Acta Crystallographica Section D Biological Crystallography. 58 (10), 1601-1605 (2002).
- Chayen, N. E., Shaw Stewart, P. D., Maeder, D. L., Blow, D. M. IUCr An automated system for micro-batch protein crystallization and screening. Journal of Applied Crystallography. 23 (4), 297-302 (1990).
- Chayen, N. E., Shaw Stewart, P. D., Blow, D. M. Microbatch crystallization under oil – a new technique allowing many small-volume crystallization trials. Journal of Crystal Growth. 122 (1-4), 176-180 (1992).
- Chayen, N. E. Comparative studies of protein crystallization by vapour-diffusion and microbatch techniques. Acta Crystallographica Section D: Biological Crystallography. 54 (1), 8-15 (1998).
- D’Arcy, A., Mac Sweeney, A., Stihle, M., Haber, A. The advantages of using a modified microbatch method for rapid screening of protein crystallization conditions. Acta Crystallographica – Section D Biological Crystallography. 59 (2), 396-399 (2003).
- Darmanin, C., et al. Protein crystal screening and characterization for serial femtosecond nanocrystallography. Scientific Reports. 6, 25345 (2016).
- Gati, C., et al. Atomic structure of granulin determined from native nanocrystalline granulovirus using an X-ray free-electron laser. Proceedings of the National Academy of Sciences of the United States of America. 114 (9), 2247-2252 (2017).
- Cheng, R. K. Y. Towards an optimal sample delivery method for serial crystallography at XFEL. Crystals. 10 (3), 215 (2020).
- Schmidt, M. Mix and Inject: Reaction Initiation by Diffusion for Time-Resolved Macromolecular Crystallography. Advances in Condensed Matter Physics. 2013, 1-10 (2013).
- Oberthuer, D., et al. Double-flow focused liquid injector for efficient serial femtosecond crystallography. Scientific Reports. 7 (1), 44628 (2017).
- McPherson, A., Gavira, J. A. Introduction to protein crystallization. Acta crystallographica. Section F, Structural biology communications. 70, 2-20 (2014).
- Yaoi, M., et al. Effect of stirring method on protein crystallization. Japanese Journal of Applied Physics, Part 2: Letters. 43 (10), 1318 (2004).
- Castro, F., Ferreira, A., Teixeira, J. J., Rocha, F. Influence of Mixing Intensity on Lysozyme Crystallization in a Meso Oscillatory Flow Reactor. Crystal Growth & Design. 18 (10), 5940-5946 (2018).
- Moews, P. C., Bunn, C. W. An X-ray crystallographic study of the rennin-like enzyme of Endothia parasitica. Journal of Molecular Biology. 54 (2), 395-397 (1970).
- Newman, J., et al. Towards rationalization of crystallization screening for small- to medium-sized academic laboratories: the PACT/JCSG+ strategy. Acta crystallographica. Section D, Biological. 61, 1426-1431 (2005).
- Ebrahim, A., et al. Resolving polymorphs and radiation-driven effects in microcrystals using fixed-target serial synchrotron crystallography. Acta Crystallographica Section D Structural Biology. 75, 151-159 (2019).
- Davy, B., et al. Reducing sample consumption for serial crystallography using acoustic drop ejection. Journal of Synchrotron Radiation. 26 (5), (2019).

