Optimalisering av veksten av endothiapepsinkrystaller for serielle krystallografieksperimenter
Summary
Målet med denne artikkelen er å gi betrakteren en solid forståelse av hvordan man transformerer deres små volum, dampdiffusjonsprotokoll, for dyrking av store, enkeltproteinkrystaller, til en storvolumbatchmikrokrystallisasjonsmetode for seriell krystallografi.
Abstract
Her presenteres en protokoll for å lette dannelsen av store volumer (> 100 μL) mikrokrystallinske oppslemminger egnet for serielle krystallografieksperimenter ved både synkrotroner og XFELer. Metoden er basert på en forståelse av proteinkrystallfasediagrammet, og hvordan denne kunnskapen kan utnyttes. Metoden er delt inn i tre faser: (1) optimalisering av krystallmorfologi, (2) overgang til batch og (3) skalering. Fase 1 innebærer å finne godt diffracting, enkeltkrystaller, forhåpentligvis, men ikke nødvendigvis, presentere i en kubelignende morfologi. I trinn 2 optimaliseres trinn 1-tilstanden med krystallveksttid. Denne strategien kan forvandle krystaller dyrket ved dampdiffusjon til batch. Når krystallvekst kan skje innen ca. 24 timer, kan et morfogram av proteinet og utfellingsblandingen plottes og brukes som grunnlag for en skaleringsstrategi (trinn 3). Når krystaller kan dyrkes i batch, kan skalering forsøkes, og krystallstørrelsen og konsentrasjonen optimaliseres når volumet økes. Endothiapepsin har blitt brukt som demonstrasjonsprotein for denne protokollen. Noen av beslutningene som presenteres er spesifikke for endothiapepsin. Det er imidlertid håpet at måten de har blitt brukt på, vil inspirere til en måte å tenke på denne prosedyren som andre kan tilpasse til sine egne prosjekter.
Introduction
Romtemperatur (RT) makromolekylær krystallografi er populært igjen innen strukturbiologi samfunnet. Utviklingen av X-ray Free Electron Laser (XFEL) lyskilder har ansporet utviklingen av RT-prøveleveringsmetoder 1,2,3,4, og disse metodene har nå blitt brukt på synkrotroner 5,6,7,8. Ikke bare åpner RT-metoder muligheten for pumpesondeeksperimentelle strageties 9,10,11,12, men det er også økende bevis på at de fremmer alternative konformasjonstilstander innen proteiner 13,14,15,16,17.
Imidlertid var hovedårsaken til at kryo-metoder fikk trekkraft over RT-tilnærminger på slutten av 1990-tallet bremset strålingsskader ved krystalltemperaturer undernull 18. Kryo-metoder19 begynte å tillate innsamling av et komplett datasett fra en enkelt proteinkrystall. Moderne RT-metoder ved XFEL og synkrotroner løste problemet med enkeltkrystallstrålingsskader ved utvikling av raske (> 100 Hz) krystallleveringsstrategier 1,2,3,4. Disse metodene tillater innsamling av et komplett datasett fra tusenvis av individuelt eksponerte krystaller. Disse RT-leveringsmetodene krever derfor produksjon av store mengder løsninger som inneholder homogene mikrokrystaller (> 100 μL < 50 μm krystaller). Men siden kryo-metoder har en tendens til å bare kreve enkeltkrystaller, er metoder for å lage slike mikrokrystallinske oppslemminger for tiden ikke allestedsnærværende på tvers av proteinkrystallografilaboratorier.
Det finnes eksempler i litteraturen på hvordan man utfører deler av mikrokrystallisasjonsoptimaliseringsprosedyren for seriekrystallografiprøver. Her bør det skilles mellom membran og løselige proteiner. Protokoller for å optimalisere veksten av mikromembranproteinkrystaller dyrket i monoolein (eller et annet lipid), for lipidisk kubisk fase (LCP), har blitt godt beskrevet20,21,22. Imidlertid mangler metoder for mikrokrystallisering av løselige proteiner, inkludert membranproteiner dyrket under ikke-LCP-forhold, generelt. Tidligere studier har fokusert på spesifikke deler av prosessen, for eksempel mikrokrystallscreening 23,24, forbedring av nukleering24 og skalering ved bruk av fri grensesnittdiffusjon 25, men ikke en komplett metode.
Imidlertid ble det nylig beskrevet en metode26 som forsøker å tilby en komplett protokoll. Som mange aspekter av proteinkrystallografi er det ikke nytt. Mange av de foreslåtte ideene ble allerede beskrevet av Rayment (2002) 27. Metoden tar sikte på å vise krystallografer hvordan man utfører konverteringen fra en enkelt krystall dyrket ved hjelp av dampdiffusjon, til en batchmetodikk for å dyrke tusenvis av mikrokrystaller. Metoden fokuserer på dampdiffusjon som et vanlig utgangspunkt, da 95% av alle Protein Data Bank (PDB) avsetninger kommer fra krystaller dyrket i dampdiffusjonsplater26. Dampdiffusjon er imidlertid ikke den ideelle metoden for mikrokrystallisering26, så en metodikk er beskrevet for å konvertere dampdiffusjon til batchkrystallisering. Når krystaller kan dyrkes i batch, blir skaleringsruter til større volumer mer praktisk. Gitt vagaries av proteinkrystallisering, vil forfatterne understreke at denne metoden ikke er feilsikker. Imidlertid bør protokollen i det minste gi et innblikk i “krystallisasjonsrommet” til et protein.
Denne metoden er avhengig av proteinkrystallisasjonsfasediagrammet og hvordan en forståelse av diagrammet kan fungere som en veiledning under mikrokrystallisasjonsoptimalisering. Et proteinfasediagram er ofte avbildet som et x/y-plott med utfellings- og proteinkonsentrasjoner på henholdsvis x– og y-aksen (figur 1A). Fra rentvannspunktet (nederst i venstre hjørne – figur 1A) øker konsentrasjonen av både protein og utfelling til løselighetslinjen er nådd. Løselighetslinjen markerer overmetningspunktet (lilla linje – figur 1A). Når et protein er overmettet, blir løsningen termodynamisk ustabil og vil begynne å separere seg i to faser: “proteinrik” og en stabil mettet løsning. Denne separasjonen kan forekomme hvor som helst utover løselighetslinjen, og dens kinetikk er avhengig av egenskapene til proteinet og komponentene i løsningen.
Når protein- og utfellingskonsentrasjonene er for store, vil proteinet brytes ustabilt ut av løsningen og resultere i amorft bunnfall (rosa region – figur 1A). Imidlertid kan bestilt faseseparasjon forekomme i kjerneområdet [se Garcia-Ruiz (2003) 28 for detaljert beskrivelse] og krystallkjerner har tilbøyelighet til å danne (grønn region – figur 1A). Nukleering og vekst fjerner protein fra løsningen og beveger dråpen inn i den metastabile regionen hvor veksten kan fortsette til løselighetslinjen er nådd [se McPherson and Kuznetsov (2014) 29 for detaljert diskusjon . Diagrammet er for de aller fleste krystallisasjonsforhold en grov overforenkling30. Uavhengig av dette er diagrammet fortsatt til stor nytte for mikrokrystallografer, da kartleggingen av diagrammet gjør det mulig å bestemme løselighetslinjen og kinetikken for kjernedannelse.
Når det gjelder å lage mikrokrystaller, er de to faktorene under krystallisering som må optimaliseres, antall krystaller (Xn) og deres gjennomsnittlige, lengste dimensjon (Xs). X n vil være proporsjonal med antall nukleasjonshendelser (n ) (Eq. 1).
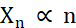 Ekv. 1
Ekv. 1
X s er proporsjonal med konsentrasjonen av fritt protein overløselighetslinjen (Ps) delt på Xn (Eq. 2).
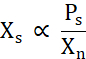 Tilsvarende 2
Tilsvarende 2
I en perfekt situasjon ville hver nukleasjonshendelse gi en mulig krystall, og hver og en av disse krystallene ville ha lik tilgang til det tilgjengelige proteinet i oppløsning. Figur 2 er en grafisk fremstilling fra et ideelt scenario av forholdet mellom Xn og Xs. I praksis er hovedkontrollen en krystallograf har over X,n og Xs ved å påvirke mengden kjernedannelse eller ved tilsetning av frøkrystaller. Mikrokrystallografen må bedømme hvordan man kan øke Xn slik at en passende krystallkonsentrasjon og krystallstørrelse begge kan opprettes.
De fleste krystallisasjonsteknikker krever en “overgangsperiode” (figur 1B). For eksempel, i et dampdiffusjonseksperiment, ved blanding av protein- og utfellingsløsninger, vil konsentrasjonene av hver endre seg når dråpen likevekter med brønnløsningen. Man håper at disse endringene gradvis vil overføre dråpen til nukleasjonssonen hvor tilbøyeligheten til krystallisering vil øke. Når krystaller begynner å kjerne og vokse, vil mengden protein i oppløsning begynne å falle, noe som reduserer sannsynligheten for ytterligere nukleering. Den endelige mengden kjernedannelse vil være protein- og tilstandsspesifikk, og også avhengig av dybden av penetrasjon av inn i nukleasjonssonen. Gitt den begrensede nukleasjonssonepenetrasjonen av metoder som krever et overgangstrinn, vil nukleasjonsnivået til slutt være begrenset til nukleasjonshastigheten ved grensen for metastabil-nukleasjonsområdet.
På grunn av viktigheten av å kunne øke nivået av nukleering for en mikrokrystallograf, er det viktig å flytte til en batchkrystallisasjonsmetodikk. Batch kan dra større nytte av hele nukleasjonsområdet (figur 1C). I batchmetoder er ideen å blande protein og utfelling sammen slik at en overmettet løsning opprettes uten behov for endringer i komponentkonsentrasjoner. Nukleering bør være mulig umiddelbart etter blanding. Batchmetoder tillater derfor at hele nukleeringssonen teoretisk nås. Enhver økning i nukleasjonskinetikken utover den metastabile nukleasjonsgrensen kan deretter utnyttes.
Hvis basalnivået av krystallkjernedannelse ikke er nok til å generere en stor Xn, kan mikrosåingsmetoder brukes. I mikrosåing brytes forvokste krystaller opp for å lage en oppslemming av krystallinske fragmenter som kan fungere som et stillas for frisk krystallvekst31,32. Mikrosåing har blitt mye brukt i seriell krystallografisk prøvepreparering som en måte å øke Xn uten behov for økende krystallkjernedannelse (figur 1C).
Overgangen fra dampdiffusjon til batch kan visualiseres på et fasediagram som å flytte det eksperimentelle utgangspunktet fra enten de ikke-overmettede eller metastabile områdene til nukleeringssonen. Dette kan gjøres ved å øke protein- og/eller utfellingskonsentrasjonene, og/eller forholdet mellom de to i dråpen (figur 1D), og observere hvilke forhold som gir krystaller som opptrer raskt (< 24 timer)26. Fullstendig dampdiffusjonsdråpebalanse kan ta dager eller uker33. Derfor, ved å lete etter forhold som viser raskt forekommende krystaller, kan batchforhold bli funnet uten å måtte flytte til alternative krystallisasjonsscreeningsformater som mikrobatch34,35,36,37.
Når nukleasjonssonen er funnet, er det funnet en batchtilstand og et morfogram – her et grovfasediagram – kan opprettes. Morfogrammet er til stor nytte når du vurderer om du skal bruke en sådd batch eller rett batchprotokoll. Ved å plotte Xn som funksjon av protein- og utfellingskonsentrasjonen, kan det gjøres en vurdering av nukleasjonskinetikken26. Hvis X n forblir lav over hele kjerneområdet, kan det være nødvendig med frøbatch for å gjøre Xn stor nok til å begrense krystallveksten. Denne vurderingen er det første trinnet i prosessen med å skalere til større volumer (> 100 μL).
Denne metoden ble utformet slik at den kunne utføres i de fleste krystallisasjonslaboratorier ved bruk av standard dampdiffusjonskrystallisasjonsutstyr. Det er også gjennomført mange studier som beskriver teknikker for å legge til rette for mange deler av denne prosessen, dersom utstyret skulle være tilgjengelig. Disse inkluderer, men er ikke begrenset til, dynamisk lysspredning (DLS) 25,27, ikke-lineær avbildning 20,24,25, pulverdiffraksjon 20,24,27 og elektronmikroskopi 26 [se Cheng et al. (2020) 40 for en fin gjennomgang].
Målet med dette arbeidet er å gi en visuell demonstrasjon av metoden for overgang fra lite volum ( 100 μL) batchkrystallisering. Endothiapepsin fra Cryphonectria parasitica har blitt brukt som et eksempelsystem for å demonstrere denne oversettelsen. Typen eksperiment og prøveleveringsmetode som mikrokrystallene er nødvendige for, vil påvirke den ideelleXs utgang26. For blandingsforsøk som krever en millisekunds tidsoppløsning41 eller gassdynamiske virtuelle dyser42, kan en endelig Xs på < 5 μm være ønskelig. I dette tilfellet var målet å produsere proteinkrystaller som diffrakterer til ca. 1, 5 Å, for et fotonaktivert pumpesondeeksperiment, og ved hjelp av en fast målleveringsmetode.
For å gi en illustrasjon av prøvekravene til et slikt seriekrystallografieksperiment ved bruk av endothiapepsin, viser tabell 1 de eksperimentelle parametrene til et hypotetisk eksperiment. Eksempelinformasjonen var basert på protokollen beskrevet nedenfor. Gitt noen konservative estimater på trefffrekvenser og datainnsamlingskrav, er 50 mg det totale prøveforbruksestimatet for hele eksperimentet.
Figur 3 viser et flytskjema over hele optimaliseringsprosessen fra første lille volum dampdiffusjonskrystallisering til storskala batch. For de fleste seriekrystallografiprosjekter vil denne protokollen begynne på trinn 2: “overgang til batch”, siden målproteinet allerede vil ha blitt krystallisert. Trinn 1 er imidlertid inkludert for fullstendighet og for å minne leserne om dens betydning. Å finne en tilstand som gir opphav til en brønndiffracting, enkelt, stor krystall er det beste utgangspunktet for mikrokrystalloptimalisering. I trinn 2 kan denne tilstanden deretter optimaliseres fra dampdiffusjon til batch, og et morfogram av nukleerings- og metastabile regioner kan plottes. Når dette er gjort, kan skalering av batchbetingelsen til større volumer utføres i trinn 3. Ved slutten av flytskjemaet vil en krystallograf ha opprettet en repeterbar, storvolum (> 100 μL), mikrokrystallisering, batchprotokoll for endothiapepsin. Denne metoden kan deretter brukes på deres spesielle protein av interesse.
Protocol
Representative Results
Discussion
Metoden som presenteres viser hvordan man optimaliserer krystalliseringen av endothiapepsin fra store krystaller (≥ 100 μm lengste dimensjon), dyrket i sparsomme matriser 96-brønns skjermer, til mikrokrystaller, dyrket i sentrifugerør (300 μL volum) via batch. Tanken bak protokollen er at trinnene som er tatt for å optimalisere endothiapepsin, også kan brukes til andre proteiner. Til slutt svarer du på problemet med å skape store volumer (>100 μL) mikrokrystaller (10-20 μm) for serielle krystallografieksperimenter ved XFEL og synkrotroner.
Protokollen deler oppgaven med mikrokrystallisering med stort volum i tre trinn: (1) Optimalisering av krystallmorfologi, (2) Overgang til batch og (3) Skalering. I trinn 1 bør rekkevidden av krystallformer som et protein kan opprette, utforskes i dampdiffusjonsplater. Forhold som gir opphav til enkle, bokslignende krystaller som diffrakterer til ønsket oppløsning bør være målet. I trinn 2 kan valgte betingelser deretter transformeres fra dampdiffusjon til batch. Her er optimaliseringskriteriet krystallveksttid og å finne forhold som gir opphav til proteinkrystaller innen 24 timer. Et morfogram kan også plottes, noe som gir eksperimentøren en ide om plasseringen av løselighetslinjen og nukleasjonssonegrensene. Dette morfogrammet er til stor nytte i trinn 3, skalering. Morfogrammet vil gi en indikasjon på om kjernedannelse alene kan øke Xn og drive ned Xs. Etter hvert som volumet av eksperimentet økes, kan X,n og Xs kontinuerlig vurderes som nøkkelkriteriene for skaleringssuksess.
Når det gjelder Endothiapepsin, avdekket trinn 1 det som potensielt var en tidligere ukjent krystallmorfologi for endothiapepsin. Denne morfologien hadde samme romgruppe som de tidligere rapporterte, men viktigst for seriekrystallografi, en mer bokslignende form. Enkeltkrystaller syntes også å vokse fra enkle nukleasjonspunkter, i motsetning til viftene opprettet fra andre forhold (figur 4). For den valgte tilstanden var trinn 2 allerede delvis tilfredsstilt da krystallveksten skjedde i < 24 timer. Morfogrammet indikerte at både en rett eller sådd batchprotokoll kan være vellykket ved skalering i trinn 3. Innledende skalering i rett batch, skapte en tilstand som produserte krystaller med et Xn og Xs område på henholdsvis 3,6 ± 1,2 x 106 krystaller · ml-1 og 42 ± 4,1 μm. Disse krystallene, selv om de var akseptable for noen serielle krystallografieksperimenter, ble ansett for store. Så ytterligere optimaliseringer ble utført. Den endelige protokollen produserte krystaller med en konsentrasjon og størrelsesområde på henholdsvis 3,1 x 106 krystaller·mL-1 og 15 ± 3,9 μm. Dette var mer enn ideelt for de planlagte eksperimentene.
Metoden fokuserer på transformasjon av “løselige” proteinkrystaller dyrket i dampdiffusjonsplater til batch. Årsaken til dette fokuset er at de aller fleste løselige proteinkrystaller dyrkes via dampdiffusjon26. Imidlertid kan konseptene som presenteres også brukes på løselige proteinkrystaller dyrket ved hjelp av andre metoder, for eksempel mikrobatch. Konseptene kan også gjelde membranproteinkrystaller dyrket i LCP; da dette også er en batchkrystallisasjonsprosess.
Et sentralt aspekt ved protokollen er prosessen med å transformere forholdene til krystaller dyrket i dampdiffusjonsplater slik at de kan dyrkes i batch. For denne transformasjonen bruker metoden kriteriet foreslått av Beale et al. (2019) 26. Krystaller dyrket via en batchprosess, selv i dampdiffusjonsplater, vil dannes raskt (< 24 timer). Dette kriteriet er en tilnærming basert på hastigheten på dampdiffusjonsdråpelikevekten, og er mest sant for PEG-baserte utfellingsforhold. Imidlertid vil krystallisasjonsbetingelsene inneholde et bredt utvalg av forbindelser som vil påvirke likevektstiden. Likevekten av saltbaserte krystallisasjonsbetingelser, f.eks. høykonsentrert ammoniumklorid, kan skje i løpet av 1-2 dager. Derfor kan 24-timerskriteriet ikke være sant for saltbaserte forhold. Saltbaserte forhold kan også ha mer komplekse fasediagrammer26,30 som kanskje ikke samsvarer med arketypen presentert i denne protokollen. En reduksjon av tidskriteriet for saltbaserte forhold til 12 eller 6 timer kan være nødvendig dersom skalering til større volumer viser seg umulig.
En annen begrensning ved denne metoden er dens tilsynelatende kompleksitet. Protokollen som ble fulgt for å optimalisere mikrokrystalliseringen av endothiapepsin, endret faktisk den opprinnelige tilstanden fra den sparsomme matriseskjermen relativt lite. Det første treffet observert i PACT-skjermen var 0,1 HEPES pH 7,0, 0,2 M MgCl2 og 20 % (w/v) PEG 6000. Den endelige skalerte krystallisasjonsbufferen var 0,1 Tris-HCl pH 7,0, 0,15 M MgCl2 og 40 % (w/v) PEG 6000. Det er også meget mulig at endringen i buffer fra HEPES til Tris-HCl, og MgCl2-konsentrasjon , bidro lite til prosessens suksess. Å forlate økningen i PEG 6,000-konsentrasjonen er den eneste optimaliseringen, og en som kunne vært oppnådd ganske enkelt.
Denne vurderingen er imidlertid også for forenklet. Det diskonterer ikke bare problemene som oppstår under skalering (dvs . bruk av frø og slukking), men også det faktum at bare fordi dette proteinet viste seg å være greit, er det ingen garanti for at det neste også vil vise seg å være. Trinnene som anbefales i protokollen, ble utarbeidet fordi optimalisering av skalering av proteinkrystallisasjonsvolumer kan være veldig proteindyrt. I løpet av de syv endothiapepsin-skaleringsforsøkene som er vist, ble 100 mg protein konsumert. Riktignok ble noen av disse trinnene utført for å vise konsekvensene i lys av denne protokollen. Likevel kan 100 mg av et protein, pluss potensielt ytterligere 50 mg for protein konsumert under et eksperiment (tabell 1), være en betydelig investering i enten tid eller penger.
Heldigvis er det ikke klart at denne massen av nødvendig prøve er allestedsnærværende på tvers av alle proteiner. Endothiapepsin var høyløselig og krevde derfor stor proteinkonsentrasjon for å nå overmetning. I andre (for tiden under optimalisering) kan overmetning nås ved 10 eller til og med 5 mg / ml. Slike variabler er proteinspesifikke og må omfavnes når de vises.
Andre begrensninger av metoden inkluderer dens avhengighet av komplekst utstyr som væskehåndteringsroboter for skjerm- og plateoppretting, og bildeapparater for automatisk bildeplater når det er nødvendig. Alternative rutiner har blitt tilbudt for å begrense behovet for noen av disse utstyrene, men protokollen vil være mer tidkrevende å følge uten dem. Protokollen foreslår også å teste diffraksjonen av optimaliserte krystaller. For krystallografer uten regelmessig tilgang til en synkrotron, kan disse testene vise seg å være utfordrende. Kontroller på hvert trinn er kanskje ikke nødvendig, men disse testene anbefales på det sterkeste når et treff er identifisert, og før og etter skalering. Ikke-diffraksjonerende krystaller ved en XFEL er dessverre ikke en uvanlig forekomst. Gitt dette er det bedre å feile på siden av forsiktighet angående antagelser om krystalldiffraksjon.
Til syvende og sist vil denne protokollen og resultatene som presenteres her, gi en veiledning, ideer og et eksempel til de som sliter med å produsere prøver for serielle krystallografieksperimenter. Forhåpentligvis, etter hvert som seriell krystallografi videreutvikles, vil prøvekravene til teknikken reduseres slik at behovet for protokoller som dette vil bli redusert. Men selv i dette tilfellet vil strategiene som presenteres her fortsatt være nyttige for de som ønsker å utforske krystallisasjonsrommet til proteinet deres.
Divulgazioni
The authors have nothing to disclose.
Acknowledgements
Dette prosjektet har mottatt finansiering fra EUs Horizon 2020 forsknings- og innovasjonsprogram under Marie Skłodowska-Curie grant agreement No 701647. Mange takk for hjelp og støtte fra strålelinjeforskere ved den sveitsiske lyskildestrålelinjen X10SA-PXII.
Materials
| Swissci 96-well 2-Drop plates | Molecular Dimensions | MD11-002 | 96-well 2-drop crystallisation plate |
| Swissci 96-well 3-Drop plates | Molecular Dimensions | MD11-003 | 96-well 3-drop crystallisation plate |
| mosquito LCP liquid handling robot | sptlabtech | mosquito LCP | Crystallisation robot |
| ClearVue Sheets | Molecular Dimensions | MD6-015 | 96-well crystallization plate seals |
| Safe-Tube 1.5 mL | Eppendorf | 30120086 | 1.5 mL centrifuge tubes |
| Scaple | Swan and Morton | No. 3 scalple and No. 3 handle | Scalple for cutting open plate seals |
| MS 3 Vortex | IKA | 3319000 | Vortex for mixing solution and making seed stocks |
| 24-well XRL Plate | Molecular Dimensions | MD3-11 | 24-well hanging-drop plates |
| Tube revolver/rotator | Thermo Fischer Scientific | 88881001 | Tube revolver for mixing solution during scaling |
| Eppendorf Research plus pipettes | Eppendorf | Range of manual pipettes, 0.5-10, 1-20, 10-100, 100-1000 µL | |
| Eppendorf pipette tips | Eppendorf | Range of tip sizes for manual pipettes | |
| Suparen 600 | Prochem AG | Suparen 600 | Endothiapepsin solution |
| Sodium Acetate | Sigma-Aldrich | 241245-1KG | Sodium Acetate |
| Tris | Merck | 8382T014 | Tris |
| Magnesium Chloride | Sigma-Aldrich | M2670-1kg | Magnesium Chloride |
| PEG 6,000 | Sigma-Aldrich | 81255-1kg | PEG 6,000 |
| Ethelyene glycol | Sigma-Aldrich | 324558-1L | Ethelyene glycol for cyro-protecting the crystals |
| PACT Premier HT screen | Molecular Dimensions | MD1-36 | PACT Premier 96-well crystal screen |
| DOW CORNING high vacuum grease | Molecular Dimensions | MD6-02 | Grease for sealing 24-well plates |
| Hirschmann 22 x 22 mm glaser cover slides | Hirschmann | 8000104 | Cover slides for sealing 24-well sitting drop plates |
| Crystal pins | PSI | Manufactured inhouse | Thin-film supports for micro-crystals. |
| 1-1.3 mm SiLibeads Type S | Faust | 6239547 | Glass beads for making mico-seed stocks |
| Macbook Pro | Apple | Macbook Pro | Computer for performing data analysis |
| CCP4 software suite | CCP4 | Diffraction pattern data processing software | |
| Excel | Microsoft | Microsoft Office | Plotting tool for phase diagram |
| Hausser Scientific Bright-Line counting chamber | Thermo Fischer Scientific | 02-671-51B | Tool to calculate crystal concentration |
| PACT Premier | Molecular Dimensions | MD1-29-ECO | Sparse-matrix crystallization screen |
| Rock Imager | Formulatrix | Rock Imager | Temperature controlled crystal plate storage and imager |
| Rock MakerWeb | Formulatrix | Rock MakerWeb | Crystal plate creation and image storage stoftware |
| Formulator | Formulatrix | Formulator | 96-well crystal screen creation liquid handling robot |
| Leica MZ16 Microscope | Leica | Leica MZ16 | Light microscope |
| LAS V4.6 | Leica | LAS V4.6 | Software for Leica microscopes |
| Spectra/Por 3.5 kDa dialysis tubing | Spectrumlabs | Spectra/Por 3 Dialysis Membrane | 3.5 kDa dialysis membrane |
| Dialysis tubing closures | Spectrumlabs | Spectra/Por 3 Duniversal Closures | Clips to seal the dialysis tubing ends |
| Amicon 10 kDa centrifugal concentrator | Merck-Millipore | Amicon Ultra-15 10 kDa centrifugal concentrator | 10 kDa centrifugal filter |
| 5810 R swing bucket centrifuge | Eppendorf | 5810 R Centrifuge | Swing bucket centrifuge |
Riferimenti
- DePonte, D. P., et al. Gas dynamic virtual nozzle for generation of microscopic droplet streams. Journal of Physics D: Applied Physics. 41 (19), 195505 (2008).
- Hunter, M. S., et al. Fixed-target protein serial microcrystallography with an x-ray free electron laser. Scientific Reports. 4 (1), 6026 (2014).
- Weierstall, U., et al. Lipidic cubic phase injector facilitates membrane protein serial femtosecond crystallography. Nature Communications. 5 (1), 1-6 (2014).
- Roessler, C. G. G., et al. Acoustic Injectors for Drop-On-Demand Serial Femtosecond Crystallography. Structure. 24 (4), 631-640 (2016).
- Sherrell, D. A., et al. A modular and compact portable mini-endstation for high-precision, high-speed fixed target serial crystallography at FEL and synchrotron sources. Journal of Synchrotron Radiation. 22 (6), 1372-1378 (2015).
- Roedig, P., et al. A micro-patterned silicon chip as sample holder for macromolecular crystallography experiments with minimal background scattering. Scientific Reports. 5 (1), 1-11 (2015).
- Botha, S., et al. Room-temperature serial crystallography at synchrotron X-ray sources using slowly flowing free-standing high-viscosity microstreams. Acta Crystallographica Section D Biological Crystallography. 71 (2), 387-397 (2015).
- Weinert, T., et al. Serial millisecond crystallography for routine room-temperature structure determination at synchrotrons. Nature Communications. 8 (1), 542 (2017).
- Tenboer, J., et al. Time-resolved serial crystallography captures high-resolution intermediates of photoactive yellow protein. Science. 346 (6214), 1242-1246 (2014).
- Nango, E., et al. A three-dimensionalmovie of structural changes in bacteriorhodopsin. Science. 354 (6319), 1552-1557 (2016).
- Suga, M., et al. Light-induced structural changes and the site of O=O bond formation in PSII caught by XFEL. Nature. 543 (7643), 131-135 (2017).
- Mehrabi, P., et al. Liquid application method for time-resolved analyses by serial synchrotron crystallography. Nature Methods. 16 (10), 979-982 (2019).
- Halle, B. Biomolecular cryocrystallography: structural changes during flash-cooling. Proceedings of the National Academy of Sciences of the United States of America. 101 (14), 4793-4798 (2004).
- Fraser, J. S., et al. Hidden alternative structures of proline isomerase essential for catalysis. Nature. 462 (7273), 669-673 (2009).
- Fenwick, R. B., van den Bedem, H., Fraser, J. S., Wright, P. E. Integrated description of protein dynamics from room-temperature X-ray crystallography and NMR. Proceedings of the National Academy of Sciences of the United States of America. 111 (4), 445-454 (2014).
- Keedy, D. A., et al. Mapping the conformational landscape of a dynamic enzyme by multitemperature and XFEL crystallography. Elife. 4, (2015).
- Thomaston, J. L., et al. XFEL structures of the influenza M2 proton channel: Room temperature water networks and insights into proton conduction. Proceedings of the National Academy of Sciences of the United States of America. 114 (51), 13357-13362 (2017).
- Haas, D. J., Rossmann, M. G. Crystallographic studies on lactate dehydrogenase at -75 °C. Acta Crystallographica Section B Structural Crystallography and Crystal Chemistry. 26 (7), 998-1004 (1970).
- Hope, H. Cryocrystallography of biological macromolecules: a generally applicable method. Acta Crystallographica Section B Structural Science. 44 (1), 22-26 (1988).
- Wu, W., et al. Batch crystallization of rhodopsin for structural dynamics using an X-ray free-electron laser. Acta Crystallographica Section:F Structural Biology Communications. 71 (7), 856-860 (2015).
- Ishchenko, A., Cherezov, V., Liu, W. Preparation and delivery of protein microcrystals in lipidic cubic phase for serial femtosecond crystallography. Journal of Visualized Experiments. (115), e54463 (2016).
- Andersson, R., et al. Well-based crystallization of lipidic cubic phase microcrystals for serial X-ray crystallography experiments. Acta Crystallographica Section D: Structural Biology. 75 (10), 937-946 (2019).
- Luft, J. R., et al. The detection and subsequent volume optimization of biological nanocrystals. Structural Dynamics. 2 (4), 041710 (2015).
- Lee, D. B., et al. Supersaturation-controlled microcrystallization and visualization analysis for serial femtosecond crystallography. Scientific Reports. 8 (1), 1-10 (2018).
- Kupitz, C., et al. Microcrystallization techniques for serial femtosecond crystallography using photosystem II from Thermosynechococcus elongatus as a model system. Philosophical transactions of the Royal Society of London. Series B, Biological Sciences. 369 (1647), 20130316 (2014).
- Beale, J. H., et al. Successful sample preparation for serial crystallography experiments. Journal of Applied Crystallography. 52, 1385-1396 (2019).
- Rayment, I. Small-scale batch crystallization of proteins revisited: An underutilized way to grow large protein crystals. Structure. 10 (2), 147-151 (2002).
- García-Ruiz, J. M. Nucleation of protein crystals. Journal of Structural Biology. 142 (1), 22-31 (2003).
- McPherson, A., Kuznetsov, Y. G. Mechanisms, kinetics, impurities and defects: Consequences in macromolecular crystallization. Acta Crystallographica Section F:Structural Biology Communications. 70 (4), 384-403 (2014).
- Rupp, B. Origin and use of crystallization phase diagrams. Acta crystallographica. Section F, Structural biology communications. 71, 247-260 (2015).
- Luft, J. R., DeTitta, G. T. A method to produce microseed stock for use in the crystallization of biological macromolecules. Acta Crystallographica Section D Biological Crystallography. 55 (5), 988-993 (1999).
- Ireton, G. C., Stoddard, B. L. Microseed matrix screening to improve crystals of yeast cytosine deaminase. Acta crystallographica. Section D, Biological crystallography. 60 (3), 601-605 (2004).
- Forsythe, E. L., Maxwell, D. L., Pusey, M. Vapor diffusion, nucleation rates and the reservoir to crystallization volume ratio. Acta Crystallographica Section D Biological Crystallography. 58 (10), 1601-1605 (2002).
- Chayen, N. E., Shaw Stewart, P. D., Maeder, D. L., Blow, D. M. IUCr An automated system for micro-batch protein crystallization and screening. Journal of Applied Crystallography. 23 (4), 297-302 (1990).
- Chayen, N. E., Shaw Stewart, P. D., Blow, D. M. Microbatch crystallization under oil – a new technique allowing many small-volume crystallization trials. Journal of Crystal Growth. 122 (1-4), 176-180 (1992).
- Chayen, N. E. Comparative studies of protein crystallization by vapour-diffusion and microbatch techniques. Acta Crystallographica Section D: Biological Crystallography. 54 (1), 8-15 (1998).
- D’Arcy, A., Mac Sweeney, A., Stihle, M., Haber, A. The advantages of using a modified microbatch method for rapid screening of protein crystallization conditions. Acta Crystallographica – Section D Biological Crystallography. 59 (2), 396-399 (2003).
- Darmanin, C., et al. Protein crystal screening and characterization for serial femtosecond nanocrystallography. Scientific Reports. 6, 25345 (2016).
- Gati, C., et al. Atomic structure of granulin determined from native nanocrystalline granulovirus using an X-ray free-electron laser. Proceedings of the National Academy of Sciences of the United States of America. 114 (9), 2247-2252 (2017).
- Cheng, R. K. Y. Towards an optimal sample delivery method for serial crystallography at XFEL. Crystals. 10 (3), 215 (2020).
- Schmidt, M. Mix and Inject: Reaction Initiation by Diffusion for Time-Resolved Macromolecular Crystallography. Advances in Condensed Matter Physics. 2013, 1-10 (2013).
- Oberthuer, D., et al. Double-flow focused liquid injector for efficient serial femtosecond crystallography. Scientific Reports. 7 (1), 44628 (2017).
- McPherson, A., Gavira, J. A. Introduction to protein crystallization. Acta crystallographica. Section F, Structural biology communications. 70, 2-20 (2014).
- Yaoi, M., et al. Effect of stirring method on protein crystallization. Japanese Journal of Applied Physics, Part 2: Letters. 43 (10), 1318 (2004).
- Castro, F., Ferreira, A., Teixeira, J. J., Rocha, F. Influence of Mixing Intensity on Lysozyme Crystallization in a Meso Oscillatory Flow Reactor. Crystal Growth & Design. 18 (10), 5940-5946 (2018).
- Moews, P. C., Bunn, C. W. An X-ray crystallographic study of the rennin-like enzyme of Endothia parasitica. Journal of Molecular Biology. 54 (2), 395-397 (1970).
- Newman, J., et al. Towards rationalization of crystallization screening for small- to medium-sized academic laboratories: the PACT/JCSG+ strategy. Acta crystallographica. Section D, Biological. 61, 1426-1431 (2005).
- Ebrahim, A., et al. Resolving polymorphs and radiation-driven effects in microcrystals using fixed-target serial synchrotron crystallography. Acta Crystallographica Section D Structural Biology. 75, 151-159 (2019).
- Davy, B., et al. Reducing sample consumption for serial crystallography using acoustic drop ejection. Journal of Synchrotron Radiation. 26 (5), (2019).

