경피 심실 보조 장치 /심장 유발 쇼크를위한 대퇴 동맥 우회 시스템에 왼쪽 아트리움의 사용
Summary
다음 기사에서는 경피좌 심실 보조 장치(pLVAD)와 CS의 좌심실 바이패스(LAFAB) 시스템을 우회하고 지원하는 대퇴동맥 우회(LAFAB) 시스템에 대한 좌심방인 심근 쇼크(CS)에 장치(예를 들어 탠덤하트)의 배치를 위한 단계별 절차를 설명합니다.
Abstract
대퇴동맥 우회(LAFAB) 계통에 대한 좌심방은 좌심방(LA)에서 혈액을 배출하여 좌심실을 우회하는 심장발생 쇼크(CS)에 사용되는 기계적 순환유지(MCS) 장치이며, 대퇴동맥을 통해 전신 동맥 순환으로 반납한다. 캐뉼라의 크기에 따라 2.5-5 L/min에 이르는 흐름을 제공할 수 있습니다. 여기에서는 LAFAB의 작용 메커니즘, 사용 가능한 임상 데이터, 심장 유발 쇼크에 대한 사용 표시, 이식 단계, 절차 후 치료 및 이 장치 사용 및 관리와 관련된 합병증에 대해 논의합니다.
또한 전배치 준비, 심초음파 지침 에 따른 경막 포심을 통한 장치의 경피 배치 및 장치 파라미터의 수술 후 관리를 포함한 장치 치료의 절차 적 구성 요소에 대한 간략한 비디오를 제공합니다.
Introduction
심장 유발 충격 (CS)은 심장이 신체의 요구를 충족시키기에 충분한 혈액과 산소를 전달할 수없는 수반되는 저혈압의 유무에 관계없이 조직 저구주입 상태이며 장기 부전의 결과로 발생합니다. 그것은 심혈관 혈관 조영술 및 내정간섭의 사회에 의해 단계 A로 E로 분류됩니다 (SCAI): 단계 A – CS를 위한 위험한 상태에 환자; 단계 B – 저혈압이나 빈맥이있는 CS의 시작 단계에서 환자는 저혈압이없는; 단계 C – 관류를 유지하기 위해 이노트로프 / 혈관 제기 또는 기계적 지원을 필요로하는 차갑고 습식 표현형의 고전적인 CS; 단계 D – 현재 의료 또는 기계적 지원에서 악화되어 고급 장치에 에스컬레이션이 필요합니다. 및 단계 E – 순환 붕괴와 진행 중인 심폐 소생술로 심장 마비를 적극적으로 경험하는 불응성 부정맥 환자를 포함한다1. CS의 가장 흔한 원인은 급성 MI (AMI)가 최근 보고된 분석2에서 케이스의 81%를 나타내고, 급성 보상심부전 (ADHF)입니다. CS는 고전적으로 혼잡과 관류 장애를 특징으로하며, 높은 충진 압력(폐 모세관 쐐기 압력[PCWP], 좌심실 단측 이연수 압력 [LVEDP], 중앙 정맥 압력 [CVP], 오른쪽 심실 단측 측압 [RVEDP]), 심장 출력 감소(CO), 심장 지수(CI-구성), 심장 지수(CI3) 감소 . 과거에, CS에 의해 복잡 AMI에 대 한 유일한 사용 가능한 치료는 초기 revascularization 및 의료 관리 이노트로프 및/또는 vasopresss4. 최근에는 기계순환지원(MCS) 장치의 출현과 혈관제의 에스컬레이션이 사망률 증가와 관련이 있다는 인식과 함께 AMI 및 ADHF 관련 CS5,6의 치료에 패러다임 변화가 있었습니다.
경피 심실 보조 장치(pVAD)의 현재 시대에는 산소 공급 기능 의 유무에 관계없이 원심또는 쌍실 순환 및 심실 지원을 제공하는 MCS 장치 플랫폼/구성이 많이 있습니다. AMI와 ADHF CS를 모두 치료하기 위해 pVAD를 꾸준히 증가했음에도 불구하고 사망률은 크게 변하지 않았습니다5. AMI8에서 좌심실(LV)의 조기 하역과 AMI CS9에서 MCS의 조기 사용에 대한 임상 적 이점에 대한 새로운 증거로 MCS의 사용이 계속 증가하고 있습니다.
대퇴동맥 바이패스(LAFAB) MCS 디바이스에 대한 좌심방은 왼쪽 아트리움(LA)에서 혈액을 배출하고 대퇴동맥을 통해 전신 동맥 순환으로 되돌리기 함으로써 LV를 우회한다(도 1). 그것은 캐뉼러의 크기에 따라 분당 2.5-5.0 리터 (L / m) 흐름 (LifeSPARC로 지정된 생명SPARC로 지정된 차세대 펌프)를 제공하는 외부 원심 펌프에 의해 지원됩니다. 혈액이 경부 정맥 캐뉼라를 통해 LA에서 추출되면, 대퇴 동맥에 배치 된 동맥 캐뉼라를 통해 환자의 몸으로 혈액을 다시 순환외부 원심 펌프를 통과합니다.
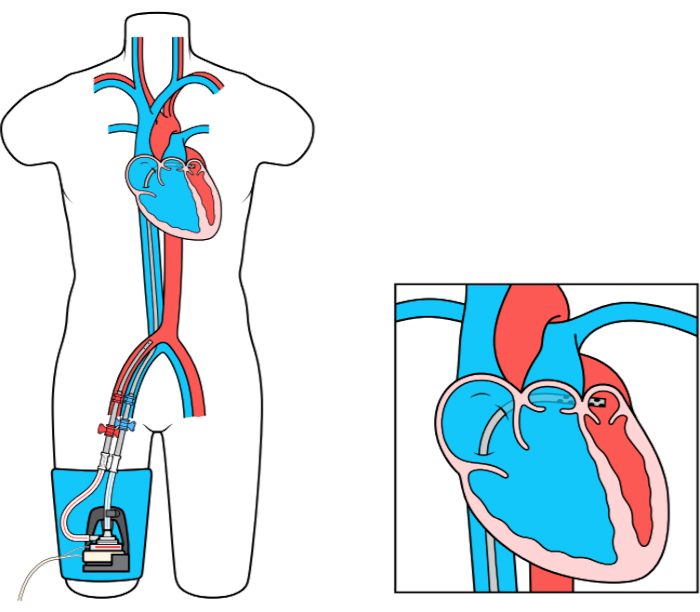
그림 1: LAFAB 설정. 이미지 제공 TandemLife, LivaNova US Inc.의 전액 출자 자회사 이 이 그림의 더 큰 버전을 보려면 여기를 클릭하십시오.
Protocol
Representative Results
Discussion
LAFAB 장치의 혈역학:
LAFAB 장치의 혈역학 프로파일은 다른 pVAD와 구별됩니다. LA에서 직접 혈액을 배출하고 대퇴 동맥에 반환함으로써 장치는 LV를 완전히 우회합니다. 이 과정에서 LV 엔드 확장기 부피와 압력을 감소시켜 LV 형상개선에 기여하여 LV 스트로크 작업의 감소를 이에 이수합니다. 그러나 혈액을 다시 일악 동맥/내림차순 대동맥으로 돌려보내면 후하량이 증가합…
Divulgazioni
The authors have nothing to disclose.
Acknowledgements
LifeSparc의 탠덤하트 팀에게.
Materials
| For LAFAB (TandemHeart) | |||
| Factory Supplied Equipment for circuit connections. | TandemLife | ||
| ProtekSolo 15 Fr or 17 Fr Arterial Cannula | TandemLife | ||
| ProtekSolo 62 cm or 72 cm Transseptal Cannula | TandemLife | ||
| TandemHeart Controller | TandemLife | For adjusting flows/RPM | |
| TandemHeart Pump | LifeSPARC | Centrifugal pump | |
| For RAPAB (ProtekDuo) | |||
| Factory Supplied Equipment to complete the circuit. | TandemLife | ||
| ProtekDuo 29 Fr or 31 Fr Dual Lumen Cannula | TandemLife | ||
| TandemHeart Controller | TandemLife | For adjusting flows/RPM | |
| TandemHeart Pump | LifeSPARC | Centrifugal pump |
Riferimenti
- Baran, D. A., et al. SCAI clinical expert consensus statement on the classification of cardiogenic shock. Catheterization and Cardiovascular Interventions. 94 (1), 29-37 (2019).
- Harjola, V. -. P., et al. Clinical picture and risk prediction of short-term mortality in cardiogenic shock. European Journal of Heart Failure. 17 (5), 501-509 (2015).
- Furer, A., Wessler, J., Burkhoff, D. Hemodynamics of Cardiogenic Shock. Interventional Cardiology Clinics. 6 (3), 359-371 (2017).
- Hochman, J. S., et al. Cardiogenic shock complicating acute myocardial infarction–etiologies, management and outcome: a report from the SHOCK Trial Registry. SHould we emergently revascularize Occluded Coronaries for cardiogenic shocK. Journal of the American College of Cardiology. 36 (3), 1063-1070 (2000).
- Shah, M., et al. Trends in mechanical circulatory support use and hospital mortality among patients with acute myocardial infarction and non-infarction related cardiogenic shock in the United States. Clinical Research in Cardiology. 107 (4), 287-303 (2018).
- van Diepen, S., et al. Contemporary Management of Cardiogenic Shock: A Scientific Statement From the American Heart Association. Circulation. 136 (16), 232-268 (2017).
- Alkhouli, M., et al. Mechanical Circulatory Support in Patients with Cardiogenic Shock. Current Treatment Options in Cardiovascular Medicine. 22 (2), 4 (2020).
- Basir, M. B., et al. Feasibility of early mechanical circulatory support in acute myocardial infarction complicated by cardiogenic shock: The Detroit cardiogenic shock initiative. Catheterization and Cardiovascular Interventions. 91 (3), 454-461 (2018).
- Basir, M. B., et al. Improved Outcomes Associated with the use of Shock Protocols: Updates from the National Cardiogenic Shock Initiative. Catheterization and Cardiovascular Interventions. 93 (7), 1173-1183 (2019).
- Alkhouli, M., Rihal, C. S., Holmes, D. R. Transseptal Techniques for Emerging Structural Heart Interventions. JACC: Cardiovascular Interventions. 9 (24), 2465-2480 (2016).
- Dennis, C., et al. Clinical use of a cannula for left heart bypass without thoracotomy: experimental protection against fibrillation by left heart bypass. Annals of Surgery. 156 (4), 623-637 (1962).
- Dennis, C., et al. Left atrial cannulation without thoracotomy for total left heart bypass. Acta Chirurgica Scandinavica. 123, 267-279 (1962).
- Fonger, J. D., et al. Enhanced preservation of acutely ischemic myocardium with transseptal left ventricular assist. Annals of Thoracic Surgery. 57 (3), 570-575 (1994).
- Thiele, H., et al. Reversal of cardiogenic shock by percutaneous left atrial-to-femoral arterial bypass assistance. Circulation. 104 (24), 2917-2922 (2001).
- Burkhoff, D., et al. A randomized multicenter clinical study to evaluate the safety and efficacy of the TandemHeart percutaneous ventricular assist device versus conventional therapy with intraaortic balloon pumping for treatment of cardiogenic shock. American Heart Journal. 152 (3), 469 (2006).
- Thiele, H., et al. Randomized comparison of intra-aortic balloon support with a percutaneous left ventricular assist device in patients with revascularized acute myocardial infarction complicated by cardiogenic shock. European Heart Journal. 26 (13), 1276-1283 (2005).
- Gregoric, I. D., et al. TandemHeart as a rescue therapy for patients with critical aortic valve stenosis. Annals of Thoracic Surgery. 88 (6), 1822-1826 (2009).
- Kar, B., et al. The percutaneous ventricular assist device in severe refractory cardiogenic shock. Journal of the American College of Cardiology. 57 (6), 688-696 (2011).
- Patel, C. B., Alexander, K. M., Rogers, J. G. Mechanical Circulatory Support for Advanced Heart Failure. Current Treatment Options in Cardiovascular Medicine. 12 (6), 549-565 (2010).
- Tempelhof, M. W., et al. Clinical experience and patient outcomes associated with the TandemHeart percutaneous transseptal assist device among a heterogeneous patient population. Asaio Journal. 57 (4), 254-261 (2011).
- Gregoric, I. D., et al. The TandemHeart as a bridge to a long-term axial-flow left ventricular assist device (bridge to bridge). Texas Heart Institute Journal. 35 (2), 125-129 (2008).
- Bruckner, B. A., et al. Clinical experience with the TandemHeart percutaneous ventricular assist device as a bridge to cardiac transplantation. Texas Heart Institute Journal. 35 (4), 447-450 (2008).
- Agarwal, R., et al. Successful treatment of acute left ventricular assist device thrombosis and cardiogenic shock with intraventricular thrombolysis and a tandem heart. Asaio Journal. 61 (1), 98-101 (2015).
- Vetrovec, G. W. Hemodynamic Support Devices for Shock and High-Risk PCI: When and Which One. Current Cardiology Reports. 19 (10), 100 (2017).
- Al-Husami, W., et al. Single-center experience with the TandemHeart percutaneous ventricular assist device to support patients undergoing high-risk percutaneous coronary intervention. Journal of Invasive Cardiology. 20 (6), 319-322 (2008).
- Vranckx, P., et al. Clinical introduction of the Tandemheart, a percutaneous left ventricular assist device, for circulatory support during high-risk percutaneous coronary intervention. International Journal of Cardiovascular Interventions. 5 (1), 35-39 (2003).
- Vranckx, P., et al. The TandemHeart, percutaneous transseptal left ventricular assist device: a safeguard in high-risk percutaneous coronary interventions. The six-year Rotterdam experience. Euro Intervention. 4 (3), 331-337 (2008).
- Vranckx, P., et al. Assisted circulation using the TandemHeart during very high-risk PCI of the unprotected left main coronary artery in patients declined for CABG. Catheterization and Cardiovascular Interventions. 74 (2), 302-310 (2009).
- Thomas, J. L., et al. Use of a percutaneous left ventricular assist device for high-risk cardiac interventions and cardiogenic shock. Journal of Invasive Cardiology. 22 (8), 360 (2010).
- Vranckx, P., et al. Assisted circulation using the Tandemhear , percutaneous transseptal left ventricular assist device, during percutaneous aortic valve implantation: the Rotterdam experience. Euro Intervention. 5 (4), 465-469 (2009).
- Pitsis, A. A., et al. Temporary assist device for postcardiotomy cardiac failure. The Annals of Thoracic Surgery. 77 (4), 1431-1433 (2004).
- Singh, G. D., Smith, T. W., Rogers, J. H. Targeted Transseptal Access for MitraClip Percutaneous Mitral Valve Repair. Interventional Cardiology Clinics. 5 (1), 55-69 (2016).
- Subramaniam, A. V., et al. Complications of Temporary Percutaneous Mechanical Circulatory Support for Cardiogenic Shock: An Appraisal of Contemporary Literature. Cardiology and Therapy. 8 (2), 211-228 (2019).
- Morley, D., et al. Hemodynamic effects of partial ventricular support in chronic heart failure: Results of simulation validated with in vivo data. The Journal of Thoracic and Cardiovascular Surgery. 133 (1), 21-28 (2007).
- Naidu, S. S. Novel Percutaneous Cardiac Assist Devices. Circulation. 123 (5), 533-543 (2011).
- Kapur, N. K., et al. Hemodynamic Effects of Left Atrial or Left Ventricular Cannulation for Acute Circulatory Support in a Bovine Model of Left Heart Injury. ASAIO Journal. 61 (3), 301-306 (2015).
- Smith, L., et al. Outcomes of patients with cardiogenic shock treated with TandemHeart percutaneous ventricular assist device: Importance of support indication and definitive therapies as determinants of prognosis. Catheterization and Cardiovascular Interventions. 92 (6), 1173-1181 (2018).
- Ergle, K., Parto, P., Krim, S. R. Percutaneous Ventricular Assist Devices: A Novel Approach in the Management of Patients With Acute Cardiogenic Shock. The Ochsner Journal. 16 (3), 243-249 (2016).
- Sultan, I., Kilic, A., Kilic, A.Short-Term Circulatory and Right Ventricle Support in Cardiogenic Shock: Extracorporeal Membrane Oxygenation, Tandem Heart, CentriMag, and Impella. Heart Failure Clinics. 14 (4), 579-583 (2018).
- Bermudez, C., et al. . Percutaneous right ventricular support: Initial experience from the tandemheart experiences and methods (THEME) registry. , (2018).
- Aggarwal, V., Einhorn, B. N., Cohen, H. A. Current status of percutaneous right ventricular assist devices: First-in-man use of a novel dual lumen cannula. Catheterization and Cardiovascular Interventions. 88 (3), 390-396 (2016).
- Kapur, N. K., et al. Mechanical circulatory support devices for acute right ventricular failure. Circulation. 136 (3), 314-326 (2017).
- Kapur, N. K., et al. Mechanical Circulatory Support for Right Ventricular Failure. JACC: Heart Failure. 1 (2), 127-134 (2013).
- Geller, B. J., Morrow, D. A., Sobieszczyk, P. Percutaneous Right Ventricular Assist Device for Massive Pulmonary Embolism. Circulation: Cardiovascular Interventions. 5 (6), 74-75 (2013).
- Bhama, J., et al. Initial Experience with a Percutaneous Dual Lumen Single Cannula Strategy for Temporary Right Ventricular Assist Device Support Following Durable LVAD Therapy. The Journal of Heart and Lung Transplantation. 35 (4), 323 (2013).
- O’Neill, B., et al. Right ventricular hemodynamic support with the PROTEKDuo Cannula. Initial experience from the tandemheart experiences and methods (THEME) registry category. Miscellaneous. , (2018).
- O’Brien, B., et al. Fluoroscopy-free AF ablation using transesophageal echocardiography and electroanatomical mapping technology. Journal of Interventional Cardiac Electrophysiology. 50 (3), 235-244 (2017).
- O’Brien, B., et al. Transseptal puncture — Review of anatomy, techniques, complications and challenges. International Journal of Cardiology. 233, 12-22 (2017).

