Single Particle Cryo-Electron Microscopy: Fra prøve til struktur
Summary
Strukturbestemmelse av makromolekylære komplekser ved hjelp av kryoEM har blitt rutine for visse klasser av proteiner og komplekser. Her oppsummeres denne rørledningen (prøvepreparering, screening, datainnsamling og prosessering), og leserne er rettet mot ytterligere detaljerte ressurser og variabler som kan endres ved mer utfordrende prøver.
Abstract
Kryo-elektronmikroskopi (cryoEM) er en kraftig teknikk for strukturbestemmelse av makromolekylære komplekser, via enkeltpartikkelanalyse (SPA). Den generelle prosessen innebærer i) vitrifisere prøven i en tynn film støttet på et cryoEM rutenett; ii) screening av prøven for å vurdere partikkelfordeling og iskvalitet; iii) hvis rutenettet er egnet, samle et enkelt partikkeldatasett for analyse; og iv) bildebehandling for å gi et EM tetthetskart. I denne protokollen gis en oversikt over hvert av disse trinnene, med fokus på variablene som en bruker kan endre under arbeidsflyten og feilsøking av vanlige problemer. Når ekstern mikroskopdrift blir standard i mange anlegg, vil variasjoner på bildeprotokoller for å hjelpe brukere med effektiv drift og avbildning når fysisk tilgang til mikroskopet er begrenset, bli beskrevet.
Introduction
Enkel partikkel CryoEM
For å undersøke livet på et molekylært nivå må vi forstå struktur. Mange teknikker for å sondere proteinstruktur er tilgjengelige, for eksempel NMR, røntgenkrystallografi, massespektrometri og elektronmikroskopi (EM). Til dags dato har de fleste strukturer deponert til Protein Databank (PDB) blitt løst ved hjelp av røntgenkrystallografi. Men fra ~ 2012 og fremover ble kryo-elektronmikroskopi (cryoEM) en mainstream-teknikk for proteinstrukturbestemmelse og bruken økte dramatisk. Totalt antall EM-kart deponert til Electron Microscopy Databank (EMDB) (per desember 2020) var 13 421 sammenlignet med 1 566 i 2012 (figur 1, www.ebi.co.uk). I 2012 var antall atomkoordinater modellert i kryoEM tetthetskart, avsatt til PDB bare 67, men per desember 2020 har 2309 strukturer blitt deponert så langt, en 35 ganger økning. Denne underliggende veksten i kvaliteten og mengden av kryoEM tetthetskart produsert, noen ganger referert til som “oppløsningsrevolusjonen”1, var forårsaket av en koalescens av fremskritt på flere områder: utvikling av nye kameraer for avbildning kjent som direkte elektrondetektorer; ny programvare; og mer stabile mikroskoper2,3,4.
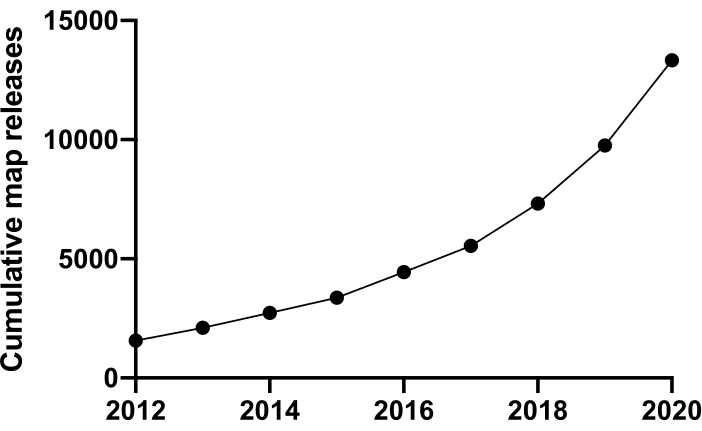
Figur 1: Kumulative innleveringer til EMDB fra 2012 til desember 2020. Klikk her for å se en større versjon av denne figuren.
Single particle analysis (SPA) er et kraftig verktøy for å generere biologisk innsikt i et bredt utvalg av prøvetyper ved å belyse høyoppløselige strukturer av isolerte komplekser5,6 inkludert virus7,8, membranproteiner9,10, spiralformede forsamlinger11 og andre dynamiske og heterogene makromolekylære komplekser12,13, hvis størrelser varierer etter størrelsesorden (fra 39 kDa 14,15 til titalls megadaltonn). Her beskrives en protokoll for en standard rørledning for cryoEM SPA fra prøve til struktur.
Før du tar fatt på denne rørledningen, bør en renset prøve bli utsatt for biokjemisk analyse for å vurdere sjansene for nedstrøms suksess. Forberedelse av en passende prøve er uten tvil den største barrieren mot SPA, spesielt for forbigående og heterogene (både komposisjons- og konformasjonskomplekser). Det makromolekylære komplekse preparatet bør inneholde så få forurensninger som mulig, med tilstrekkelig konsentrasjon til å gi mange partikler i hver kryoEM-mikrograf, og i en buffersammensetning som er godt egnet til kryoEM-analyse. Visse bufferbestanddeler, inkludert sukrose, glyserol og høy (~> 350 mM konsentrasjoner av salter, avhengig av prøvestørrelse, egenskaper og andre bufferbestanddeler) kan forstyrre prosessen med vitrifisering eller redusere signal-til-støy-forholdet i bilder, noe som hindrer strukturbestemmelse16.
Vanligvis bør størrelseseksklusjonskromatografi (SEC) og SDS- PAGE gelanalyse brukes til å vurdere prøverenhet17,18, men sirkulær dikromatisme, funksjonelle analyser, SEC kombinert med multi-vinkel lysspredning, og termiske stabilitetsanalyser er alle nyttige verktøy for kvalitativ analyse av makromolekylære komplekse preparater før kryoemanalyse. Resultatene fra disse biokjemiske analysene kan imidlertid gi liten innsikt i utvalgets strukturelle heterogenitet og dens oppførsel på et kryoEM-nett. Av denne grunn brukes negativ flekk EM rutinemessig som et raskt, billig og kraftig verktøy for å vurdere komposisjons- og konformasjons heterogenitet, og derfor en god måte å fastslå hvilken elutionfraksjon fra en rensing som er mest lovende, eller screening av forskjellige buffersammensetninger19,20. Når en lovende prøve er identifisert, kan vi fortsette til SPA cryoEM-rørledningen. Negativ flekk stemmer ikke alltid overens med de etterfølgende resultatene sett i cryoEM; Noen ganger ser en prøve dårlig ut av negativ flekk, men forbedres når den ses i glassaktig is i cryoEM. Noen ganger ser prøver utmerket ut under negative flekktrinn, men krever betydelig ytterligere optimalisering når du går videre til cryoEM. Men i de fleste tilfeller gir negativ flekk et nyttig kvalitetskontrolltrinn.
Vitrifisering
Det harde miljøet i vakuumsystemet til elektronmikroskopet forårsaker både dehydrering og strålingsskader på uløste biologiske prøver21. Derfor, for å avbilde prøven i en innfødt-lignende tilstand, må den biologiske prøven bevares før avbildning. For rensede preparater av makromolekylære komplekser er vitrifisering den valgte metoden for å muliggjøre visualisering ved kryoEM samtidig som atomdetaljene til komplekset bevares. Oppdagelsen av vitrifisering som en metode for prøvepreparering var et grunnleggende fremskritt innen elektronmikroskopi av biologiske prøver, som Dubochet ble anerkjent for i Nobelprisen i kjemi i 2017. Prøvevistrifisering innebærer å skape et tynt lag med løsning som inneholder prøven av interesse, vanligvis titalls nm tykk, suspendert på en cryoEM rutenettstøtte. Den tynne filmen fryses deretter ekstremt raskt i et kryoogen som flytende etan ved ~ -175 ° C. Frysehastigheten er ~ 106 ° C / s, rask nok til at amorf, eller glassaktig is dannes, suspenderer prøven i en tynn, solid film22.
Den første variabelen du må vurdere er cryoEM-rutenettstøtten som er valgt23. Et EM-rutenett består vanligvis av en amorf karbonfilm med perforeringer (enten vanlig eller uregelmessig), over en støttestruktur. Støttestrukturen er vanligvis et sirkulært metallgitter 3,05 mm i diameter, vanligvis laget av kobber, men andre metaller som gull eller molybden (som har foretrukne termiske ekspansjonsegenskaper24) kan brukes. Noen ganger påføres en ekstra tynn, kontinuerlig støtte over rutenettet, for eksempel grafen, grafenoksid eller et tynt (~ 1-2 nm) amorf karbonlag. Mens standard cryoEM-rutenett (vanligvis 400-200 mesh kobber med perforert (1,2 μm runde hull separert med 1,3 μm (r1.2/1.3), eller 2 μm separert med 2 μm karbon (r2/2)) karbonstøtte – selv om mange forskjellige mønstre er tilgjengelige) har blitt brukt i de aller fleste strukturer rapportert til de aller fleste strukturer rapportert å være tilgjengelige) nye nettteknologier med forbedret konduktivitet og redusert prøvebevegelse er rapportert25 . Utvalgte gitter blir utsatt for en glødeutladning / plasmarengjøringsbehandling for å gjøre dem hydrofile og mottagelige for prøveapplikasjon26.
Etter glødutladning er neste trinn tynn filmdannelse. Denne tynne filmen dannes oftest ved hjelp av filterpapir for å fjerne overflødig væske fra rutenettet. Selv om dette kan utføres manuelt, er en rekke dypfrysingsenheter kommersielt tilgjengelige, inkludert Vitrobot Mk IV (Thermo Fisher Scientific), EM GP II (Leica) og CP3 (Gatan). Med disse enhetene påføres ~ 3-5 μL prøve i oppløsning på EM-rutenettet, etterfulgt av oppblåsthet bort overflødig løsning ved hjelp av filterpapir. Gitteret, med en tynn film suspendert over det, blir deretter kastet i flytende etan avkjølt av flytende nitrogen (LN2) til ~ -175 °C. Når det er frosset, opprettholdes rutenettet ved en temperatur under devitrifiseringspunktet (-137 °C) før og under avbildning.
Prøvescreening og datainnsamling
Etter vitrifisering av et cryoEM-rutenett, er neste trinn å screene rutenettet for å vurdere kvaliteten og avgjøre om rutenettet er egnet til å gå videre til datainnsamling med høy oppløsning. Et ideelt kryoEM-rutenett har glassaktig is (i motsetning til krystallinsk is) med istykkelsen akkurat tilstrekkelig til å imøtekomme den lengste dimensjonen av prøven, noe som sikrer at den omkringliggende isen bidrar med så lite støy til det resulterende bildet som mulig. Partiklene i isen skal ha en størrelse og (hvis kjent) form i samsvar med biokjemi, og ideelt sett være monodisperse med en tilfeldig fordeling av partikkelretninger. Til slutt bør rutenettet ha nok områder av tilstrekkelig kvalitet til å tilfredsstille ønsket datainnsamlingslengde. Avhengig av prøven kan dette ta mange gjentakelser av vitrifisering og screening til optimale rutenett produseres. Både heldigvis og dessverre er det et stort utvalg av variabler som empirisk kan testes for å endre partikkelfordeling på cryoEM-rutenett (gjennomgått i 16,27). I dette manuskriptet vises representative resultater for et membranproteinprosjekt10.
Når et passende rutenett er identifisert, kan datainnsamlingen fortsette. Flere modeller av kryooverføringselektronmikroskoper for biologiske prøver er optimalisert for å samle inn høyoppløselige data på en automatisert måte. Vanligvis samles data på 300 kV- eller 200 kV-systemer. Automatisert datainnsamling kan oppnås ved hjelp av programvare som EPU (Thermo Fisher Scientific)28, Leginon29, JADAS30 og SerialEM31,32. En automatisert datainnsamling med moderne detektorer resulterer vanligvis i terabyte (TB) av rådata i en 24 timers periode (gjennomsnittlige datasett er ~ 4 TB i størrelse).
På grunn av COVID-19-restriksjonene som er på plass på store deler av verden (skrivetidspunkt desember 2020), har mange mikroskopifasiliteter gått over til å tilby ekstern tilgang. Når rutenettene er lastet inn i autoloaderen til et mikroskop, kan datainnsamling utføres eksternt.
Bildebehandling og modellbygging
Der en datainnsamlingsøkt vanligvis kan være 0,5-4 dager, kan påfølgende bildebehandling ta mange uker og måneder, avhengig av tilgjengeligheten av databehandlingsressurser. Det er standard for innledende bildebehandlingstrinn, nemlig bevegelseskorrigering og kontrastoverføringsfunksjon (CTF) estimering for å finne sted ‘på farten’ 33,34. For nedstrøms behandling er det en mengde programvarepakker tilgjengelig. Partikler “plukkes” og ekstraheres fra mikrografer35,36. Når partikler er ekstrahert, vil en standardprotokoll være å behandle partiklene gjennom flere runder med klassifisering (i både to dimensjoner (2D) og tre dimensjoner (3D) og / eller fokusert på bestemte interesseområder) for å nå en homogen undergruppe av partikler. Denne homogene undergruppen av partikler blir deretter gjennomsnittet sammen for å produsere en 3D-rekonstruksjon. På dette tidspunktet korrigeres data ofte ytterligere for å produsere et kart av høyeste kvalitet som er mulig, for eksempel gjennom CTF-presisering, forvrengningskorrigeringer37 og bayesiansk polering38 . Utfallet av denne bildebehandlingen er et 3D cryoEM-kart over det biologiske eksemplaret av interesse. Oppløsningsområdet nådd i et “standard” automatisert enkeltpartikkeleksperiment fra et rutenett av tilstrekkelig kvalitet, med data samlet inn på et 300 kV mikroskopsystem er vanligvis mellom 10 Å og 2 Å avhengig av størrelsen og fleksibiliteten til proteinkomplekset. Med et ideelt eksemplar er oppløsninger på ~1.2 Å nå nådd ved hjelp av SPA-arbeidsflyter5. Mens denne protokollen detaljer skritt mot å skaffe en EM tetthet kart, når dette er i hånden det kan tolkes videre gjennom montering og raffinering av en protein modell (hvis oppløsning er < 3.5 Å) eller bygge de novo39. Data knyttet til strukturbestemmelseseksperimenter kan deponeres i offentlige depoter på nettet, inkludert EM-tetthetskart (Electron Microscopy Data Bank)40, resulterende atomkoordinater (Protein Data Bank)41 og rådatasett (Electron Microscopy Public Image Archive)42.
I denne protokollen brukes det ytre membranproteinkomplekset RagAB (~ 340 kDa) fra Porphyromonas gingivalis som et eksempel makromolekylært kompleks10 (EMPIAR-10543). For de som er nye i cryoEM, er støtte for prøver gjennom dette datasamlebåndet fra utvalg til struktur tilgjengelig, underlagt fagfellevurdering, gjennom finansierte tilgangsordninger som iNEXT Discovery og Instruct.
Protocol
Representative Results
Discussion
I denne protokollen har vi beskrevet en grunnleggende rørledning som gjelder for prøver som kan brukes til rutinemessig SPA. Selv om denne filterpapir blottingsmetoden for tynn filmdannelse og vitrifisering utvilsomt er vellykket gitt bruken i de aller fleste SPA-prosjekter til dags dato, kommer den med en rekke ulemper. Disse inkluderer prøvesvekke, de langsomme tidsskalaene (sekunder) som kreves for å danne den tynne filmen og fryse prøven, rapporterte irreproducibility27 og rapporterte negative effekter av å bruke filterpapir for å utslette overflødig væske50. Nylig har nye teknologier blitt utviklet for å forbedre reproduserbarheten av tynn filmproduksjon51,52. Andre teknologier er utviklet som reduserer tiden mellom prøveapplikasjon og vitrifisering53,54,55. Mens filterpapirbaserte metoder for tynn filmdannelse forblir den mest allestedsnærværende metoden for SPA cryoEM prøvepreparering i skrivende stund, kan disse nye teknologiene gi en rekke fordeler når det gjelder effektivitet og reproduserbarhet av rutenett vitrifisering, samt skape nye muligheter til å bringe inn ytterligere eksperimentelle dimensjoner, for eksempel tidsoppløsning og rask blanding før vitrifisering.
Prosessen med nettscreening for de fleste brukere er for tiden en kvalitativ prosess som innebærer oppkjøp av lave forstørrelsesatlaser etterfulgt av å ta bilder med høy forstørrelse over hele rutenettet for å vurdere partikkelfordeling. Selv om dette er en tilstrekkelig robust tilnærming for noen typer prøver, kan det være vanskelig å vurdere for øyet om prøven faktisk er det forskeren håper å bilde eller har en foretrukket orientering, for eksempel med små (<200 kDa) prøver eller hvor lavoppløsningsmorfologien gjør det vanskelig å identifisere for øyet hvis en rekke partikkelfordelinger er til stede. For noen prosjekter er det umulig å avgjøre om prøven er som ønsket, for eksempel hvor en ligand er bundet eller hvor prøven blir screenet for å vurdere om en liten (f.eks. 10 kDa) underenhet fortsatt er til stede i forbindelse med et kompleks. For disse prosjektene vil helautomatiske rørledninger for dataanalyse kombinert med en "kort" 0,5- 1-timers samlinger, som kan gå gjennom bildebehandlingstrinn til 2D-klassifisering eller til og med 3D-klassifisering og raffinement, bidra til å effektivt avgjøre om en lengre samling er berettiget. Disse rørledningene er fortsatt under utvikling og er ikke mye implementert for tiden, men de har potensial til å forbedre effektiviteten av kryoEM rutenettscreening, spesielt for utfordrende prøver.
Forbedringer i direkte elektrondetektorer, samt modifikasjoner i mikroskopi kombinert med fremskritt innen bildebehandling som innsamling av bildeskiftdata, har økt gjennomstrømningen og kvaliteten på bilder som produseres under datainnsamlingen. Denne økningen i datahastigheten som samles inn fremhever behovet for grundig screening av cryoEM-rutenett før mange TB data blir samlet inn.
CryoEM SPA har blitt en virkelig mainstream strukturell biologi teknikk, og i mange tilfeller “gå til” tilnærming for noen klasser av prøver, for eksempel heterogene og labile makromolekylære komplekser. Mens protokollen her beskriver en grunnleggende oversikt over SPA-rørledningen, er hver seksjon som dekkes her (rutenett vitrifisering og screening, kryoEM og bildebehandling) et tema i seg selv og verdig leting under utviklingen av et SPA-prosjekt. Etter hvert som prøveforberedelses- og mikroskopiteknologier utvikler seg, og nye bildebehandlingsalgoritmer og tilnærminger kommer på nettet, vil SPA fortsette å utvikle seg som en rørledning, og hjelpe forskere med å få innsikt i komplekse biologiske systemer.
Divulgazioni
The authors have nothing to disclose.
Acknowledgements
Dette arbeidet ble støttet av iNEXT-Discovery (Grant 871037) finansiert av Horisont 2020-programmet til Europakommisjonen. J B. R. White er finansiert av Wellcome Trust (215064/Z/18/Z). FEI Titan Krios mikroskoper ble finansiert av University of Leeds (UoL ABSL award) og Wellcome Trust (108466/Z/15/Z). Vi takker M Iadanza for bruken av hans mikrografanalysemanus. Vi anerkjenner Diamond Light Source for tilgang og støtte av cryo-EM-anleggene på Storbritannias nasjonale Electron Bio-imaging Centre (eBIC) finansiert av Wellcome Trust, MRC og BBRSC.
Materials
| Blunt tweezers | Agar Scientific | AGT5022 | |
| Cryo EM round storage box | Agar Scientific | AGG3736 | |
| CryoEM autogrid boxes | ThermoFisher Scientific | 1084591 | |
| CryoEM grids | Quantifoil | N1-C14nCu30-01 | |
| Ethane gas | Boc | 270595-F | |
| LN2 foam dewar | Agar Scientific | AG81760-500 | |
| LN2 storage dewar | Worthington industries | HC 34 | |
| Pipette | Gilson | 10082012 | |
| Pipette tips | Star labs | s1111-1706 | |
| Syringe | BD | BD 300869 | |
| Type II lab water | Suez | select fusion | |
| Vitrobot | ThermoFisher Scientific | 1086439 | |
| Vitrobot filter paper | Whatman | 1001-055 | |
| Vitrobot styrophome container assembly | ThermoFisher Scientific | 1086439 | |
| Vitrobot tweesers | ThermoFisher Scientific | 72882-D | |
| Software | |||
| EPU | ThermoFisher Scientific | 2.8.1.10REL | |
| TEM server | ThermoFisher Scientific | 6.15.3.22415REL | |
| Tia | ThermoFisher Scientific | 5.0.0.2896REL | |
| Titan krios microscope | ThermoFisher Scientific | Titan Krios G2 |
Riferimenti
- Kuehlbrandt, W. The Resolution Revolution. Science. 343 (6178), 1443-1444 (2014).
- McMullan, G., Faruqi, A. R., Henderson, R. Direct Electron Detectors. Methods in Enzymology. , (2016).
- Elmlund, D., Le, S. N., Elmlund, H. High-resolution cryo-EM: the nuts and bolts. Current Opinion in Structural Biology. , (2017).
- Lyumkis, D. Challenges and opportunities in cryo-EM single-particle analysis. Journal of Biological Chemistry. , (2019).
- Nakane, T., et al. Single-particle cryo-EM at atomic resolution. Nature. , (2020).
- Yip, K. M., Fischer, N., Paknia, E., Chari, A., Stark, H. Atomic-resolution protein structure determination by cryo-EM. Nature. , (2020).
- Conley, M. J., et al. Calicivirus VP2 forms a portal-like assembly following receptor engagement. Nature. 565 (7739), 377-381 (2019).
- Hesketh, E. L., et al. The 3.3 Å structure of a plant geminivirus using cryo-EM. Nature communications. 9 (1), 2369 (2018).
- Malone, L. A., et al. Cryo-EM structure of the spinach cytochrome b6 f complex at 3.6 A resolution. Nature. 575 (7783), 535-539 (2019).
- Madej, M., et al. Structural and functional insights into oligopeptide acquisition by the RagAB transporter from Porphyromonas gingivalis. Nature Microbiology. , (2020).
- Gallardo, R., et al. Fibril structures of diabetes-related amylin variants reveal a basis for surface-templated assembly. Nature Structural and Molecular Biology. , (2020).
- Scarff, C., et al. Structure of the shutdown state of myosin-2. Nature. , (2020).
- Scarff, C. A., et al. Structure of the protective nematode protease complex H-gal-GP and its conservation across roundworm parasites. PLoS Pathogens. 16 (4), 1008465 (2020).
- Wu, M., Lander, G. C. How low can we go? Structure determination of small biological complexes using single-particle cryo-EM. Current Opinion in Structural Biology. , (2020).
- Khoshouei, M., Radjainia, M., Baumeister, W., Danev, R. Cryo-EM structure of haemoglobin at 3.2 Å determined with the Volta phase plate. Nature Communications. , (2017).
- Drulyte, I., et al. Approaches to altering particle distributions in cryo-electron microscopy sample preparation. Acta crystallographica. Section D, Structural biology. 74, 560-571 (2018).
- Thompson, R. F., Walker, M., Siebert, C. A., Muench, S. P., Ranson, N. A. An introduction to sample preparation and imaging by cryo-electron microscopy for structural biology. Methods. 100, 3-15 (2016).
- Cheng, Y., Grigorieff, N., Penczek, P. A., Walz, T. A primer to single-particle cryo-electron microscopy. Cell. 161 (3), 438-449 (2015).
- Scarff, C. A., Fuller, M. J. G., Thompson, R. F., Iadanza, M. G. Variations on negative stain electron microscopy methods: tools for tackling challenging systems. Journal of Visualized Experiments. (132), e57199 (2018).
- Ohi, M., Li, Y., Cheng, Y., Walz, T. Negative Staining and Image Classification – Powerful Tools in Modern Electron Microscopy. Biological procedures online. 6, 23-34 (2004).
- Baker, L. A., Rubinstein, J. L. Radiation Damage in Electron Cryomicroscopy. Methods in enzymology. 481, 371-388 (2010).
- Dubochet, J., et al. Cryo-electron microscopy of vitrified specimens. Quarterly Reviews of Biophysics. 21 (02), 129-228 (1988).
- Passmore, L. A., Russo, C. J. Specimen Preparation for High-Resolution Cryo-EM. Methods in enzymology. 579, 51-86 (2016).
- Carragher, B., et al. Current outcomes when optimizing ‘standard’ sample preparation for single-particle cryo-EM. Journal of Microscopy. , (2019).
- Naydenova, K., Jia, P., Russo, C. J. Cryo-EM with sub-1 Å specimen movement. Science. , (2020).
- Passmore, L. A., Russo, C. J. Specimen Preparation for High-Resolution Cryo-EM. Methods in Enzymology. , (2016).
- Thompson, R. F., Iadanza, M. G., Hesketh, E. L., Rawson, S., Ranson, N. A. Collection, pre-processing and on-the-fly analysis of data for high-resolution, single-particle cryo-electron microscopy. Nature protocols. 14 (1), 100-118 (2019).
- Suloway, C., et al. Automated molecular microscopy: the new Leginon system. Journal of Structural Biology. 151 (1), 41-60 (2005).
- Zhang, J., et al. JADAS: A customizable automated data acquisition system and its application to ice-embedded single particles. Journal of Structural Biology. , (2009).
- Mastronarde, D. N. SerialEM: A program for automated tilt series acquisition on Tecnai microscopes using prediction of specimen position. Microscopy and Microanalysis. , (2003).
- Schorb, M., Haberbosch, I., Hagen, W. J. H., Schwab, Y., Mastronarde, D. N. Software tools for automated transmission electron microscopy. Nature Methods. , (2019).
- Fernandez-Leiro, R., Scheres, S. H. W. A pipeline approach to single-particle processing in RELION. Acta crystallographica. Section D, Structural biology. 73, 496-502 (2017).
- Gómez-Blanco, J., et al. Using Scipion for stream image processing at Cryo-EM facilities. Journal of Structural Biology. , (2018).
- Wagner, T., et al. SPHIRE-crYOLO is a fast and accurate fully automated particle picker for cryo-EM. Communications biology. 2 (1), 213-218 (2019).
- Bepler, T., et al. TOPAZ: A Positive-Unlabeled Convolutional Neural Network CryoEM Particle Picker that can Pick Any Size and Shape Particle. Microscopy and Microanalysis. , (2019).
- Zivanov, J., et al. New tools for automated high-resolution cryo-EM structure determination in RELION-3. eLife. 7, 163 (2018).
- Zivanov, J., Nakane, T., Scheres, S. H. W. A Bayesian approach to beam-induced motion correction in cryo-EM single-particle analysis. IUCrJ. , (2019).
- Cianfrocco, M. A., Kellogg, E. H. What Could Go Wrong? A Practical Guide to Single-Particle Cryo-EM: From Biochemistry to Atomic Models. Journal of Chemical Information and Modeling. , (2020).
- Tagari, M., Newman, R., Chagoyen, M., Carazo, J. M., Henrick, K. New electron microscopy database and deposition system. Trends in Biochemical Sciences. , (2002).
- Berman, H. M., et al. The Protein Data Bank. Nucleic Acids Research. , (2000).
- Iudin, A., Korir, P. K., Salavert-Torres, J., Kleywegt, G. J., Patwardhan, A. EMPIAR: A public archive for raw electron microscopy image data. Nature Methods. , (2016).
- Punjani, A., Rubinstein, J. L., Fleet, D. J., Brubaker, M. A. CryoSPARC: Algorithms for rapid unsupervised cryo-EM structure determination. Nature Methods. , (2017).
- Tegunov, D., Cramer, P. Real-time cryo-electron microscopy data preprocessing with Warp. Nature Methods. , (2019).
- Goddard, T. D., et al. UCSF ChimeraX: Meeting modern challenges in visualization and analysis. Protein Science. 27 (1), 14-25 (2018).
- Klebl, D. P., et al. Need for Speed: Examining Protein Behavior during CryoEM Grid Preparation at Different Timescales. Structure. , (2020).
- Noble, A. J., et al. Routine single particle CryoEM sample and grid characterization by tomography. eLife. 7, 32 (2018).
- Danev, R., Buijsse, B., Khoshouei, M., Plitzko, J. M., Baumeister, W. Volta potential phase plate for in-focus phase contrast transmission electron microscopy. Proceedings of the National Academy of Sciences. , (2014).
- Zi Tan, Y., et al. Addressing preferred specimen orientation in single-particle cryo-EMthrough tilting. Nature Methods. , (2017).
- Armstrong, M., Han, B. -. G., Gomez, S., Turner, J., Fletcher, D. A., Glaeser, R. M. Microscale Fluid Behavior during Cryo-EM Sample Blotting. Biophysical Journal. 118 (3), 708-719 (2020).
- Arnold, S. A., et al. Blotting-free and lossless cryo-electron microscopy grid preparation from nanoliter-sized protein samples and single-cell extracts. Journal of Structural Biology. , (2017).
- Dandey, V. P., et al. Spotiton: New Features and Applications. Journal of Structural Biology. , (2018).
- Rubinstein, J. L., et al. Shake-it-off: a simple ultrasonic cryo-EM specimen-preparation device. Acta crystallographica. Section D, Structural biology. 75, 1063-1070 (2019).
- Tan, Y. Z., Rubinstein, J. L. Through-grid wicking enables high-speed cryoEM specimen preparation. bioRxiv. , (2020).
- Klebl, D. P., et al. Sample deposition onto cryo-EM grids: From sprays to jets and back. Acta Crystallographica Section D: Structural Biology. , (2020).

