Rask in Vivo-fiksering og isolering av translasjonskomplekser fra eukaryote celler
Summary
Vi presenterer en teknikk for raskt å stabilisere translasjonelle (proteinbiosyntese) komplekser med formaldehyd krysskobling i levende gjær og pattedyrceller. Tilnærmingen muliggjør dissekering av forbigående mellomprodukter og dynamiske RNA:proteininteraksjoner. De krysskoblede kompleksene kan brukes i flere nedstrømsapplikasjoner, for eksempel i dype sekvenseringsbaserte profileringsmetoder, mikroskopi og massespektrometri.
Abstract
Raske svar som involverer rask omfordeling av messenger(m)RNA og endringer av mRNA-oversettelse er relevante for pågående homeostatiske justeringer av cellene. Disse justeringene er avgjørende for eukaryotisk celleoverlevelse og “skadekontroll” under varierende nærings- og saltholdighetsnivåer, temperatur og ulike kjemiske og strålingsspenninger. På grunn av den svært dynamiske naturen til RNA-nivåresponsene, og ustabiliteten til mange av RNA: RNA og RNA: protein mellomprodukter, er det bare mulig å oppnå et meningsfullt øyeblikksbilde av den cytoplasmatiske RNA-tilstanden med et begrenset antall metoder. Transkripsjonsomfattende, RNA-seq-baserte ribosomeprofilerings-type eksperimenter er blant de mest informative datakildene for kontroll av oversettelse. Imidlertid kan fravær av en jevn RNA og RNA: protein mellomliggende stabilisering føre til forskjellige skjevheter, spesielt i de fartsfylte cellulære responsveiene. I denne artikkelen gir vi en detaljert protokoll for rask fiksering som gjelder for eukaryote celler med forskjellig permeabilitet, for å hjelpe til med RNA og RNA: protein mellomliggende stabilisering. Vi gir videre eksempler på isolasjon av de stabiliserte RNA:proteinkompleksene basert på deres co-sedimentering med ribosomale og poly (ribo)somale fraksjoner. Det separerte stabiliserte materialet kan senere brukes som en del av ribosomets profilerings-type eksperimenter, for eksempel i Translation Complex Profile sekvensering (TCP-seq) tilnærming og dets derivater. Allsidigheten til TCP-seq-stilmetodene er nå demonstrert av applikasjonene i en rekke organismer og celletyper. De stabiliserte kompleksene kan også i tillegg affinitetsrenses og avbildes ved hjelp av elektronmikroskopi, separert i forskjellige poly(ribo)somale fraksjoner og utsatt for RNA-sekvensering, på grunn av enkel krysskoblings reversering. Derfor kan metoder basert på snap-chilling og formaldehydfiksering, etterfulgt av sedimenteringsbasert eller annen type RNA: proteinkompleksberikelse, være av spesiell interesse i å undersøke finere detaljer om rask RNA: proteinkompleksdynamikk i levende celler.
Introduction
Levende organismer er utsatt for dynamiske intra- og ekstracellulære endringer gjennom hele levetiden, noe som krever raske svar for å opprettholde homeostase og sikre overlevelse. For å tillate miljøtilpasning justerer eukaryote celler stoffskiftet via genuttrykkskontroll. Genuttrykkskontroll kan utøves under transkripsjon og/eller oversettelse; oversettelsessvar som vanligvis forekommerraskere 1,2,3,4. For eksempel oppstår translasjonsendringer vanligvis innen 1-30 minutter etter stressde begynnelse, mens endringer på transkripsjonsnivå følger timer etter stresseksponering3,4,5. Endringer i oversettelsesutgangen oppnås raskere på grunn av vedvarende tilgjengelighet av messenger (m) RNA-molekyler i cytoplasma. Omvendt, på transkripsjonsnivå, må nye mRNA-molekyler syntetiseres, og i eukaryoter, behandles og eksporteres fra kjernen, og produserer omfattende forsinkelser i responstiden2,4,6,7,8.
Akutt translasjonell respons på stress er generelt preget av en generell reduksjon i oversettelsesproduksjonen, med selektiv oppregulering av proteiner som er nødvendige for celleoverlevelse1,3,4,9. Å redusere proteinproduksjonsproduksjonen antas å være avgjørende på grunn av den høye energikostnaden i prosessen.3,7. For å lette selektiv hemming og oppregulering, serveres translasjonsresponser av en rekke komplekse regulatoriske mekanismer. Regulering kan utøves på tvers av alle faser av oversettelsen: initiering, forlengelse, avslutning av polypeptidbiosyntese og ribosomal resirkulering10,11,12,13, men er utstilt sterkest i initieringsfasen5,7,9,10,13. Under initiering binder den lille ribosomale underenheten (SSU), assistert av eukaryote initieringsfaktorer (eIFer), til og skanner 5′ uoversatt region (UTR) av mRNA til en startkodon gjenkjennes2,5,6,8,11,12,13. Forskriftsmessige mekanismer retter seg ofte mot e-filer som påvirker vedlegg, skanning og start kodongjenkjenning. For eksempel initieringsfaktoren eIF2, en viktig oversettelsesfaktor som hjelper til med rekruttering av en initiativtaker Met-tRNAiMet SSU, er ofte målrettet i eukaryoter under stressforhold4,6,11. I gjær kan fosforylering av denne faktoren induseres under næringsmangel og osmotisk stress1,4,11,14,15, og i pattedyrceller kan aminosyre sult, endoplasmatisk retikulum (ER) stress, UV-stress, virusinfeksjon og endret oksygennivå utløse denne responsen8,9,11. Rask oppregulering av spesifikk mRNA-oversettelse er tydelig i pattedyrcelleresponsen på hypoksi, som viser en global rask oversettelseshemming og selektiv oppregulering av hypoksi-induserbare faktorer (HIFs) biosyntese. HIFer er transkripsjonsfaktorer, som deretter fremkaller langsiktig cellulær omprogrammering på DNA-transkripsjonsnivå8,9,16. Lignende responser har blitt observert i gjær under varmestress, med raskt translasjonsuttrykk av varmesjokkproteiner (HSP-er) etterfulgt av forsinkede transkripsjonsnivåresponser17,18. I tillegg til næringsmangel og varmesjokk har translasjonsresponser i gjær blitt studert under varierende oksygen8,19salinitet5, fosfat, svovel20,21 og nitrogen22,23 Nivåer. Denne forskningen har utbredte implikasjoner for industriell bruk av gjær, som baking og gjæring.24,25. Translasjonelle responser kan også være medvirkende til å fremme forståelse av sykdommer som nevrodegenerative lidelser og hjertesykdom, som er preget av intracellulære påkjenninger som oksidativt stress. Samlet sett er translasjonsresponser integrert i genuttrykkskontrollen og legger til rette for rask tilpasning til et bredt spekter av stressforhold i eukaryote organismer.
For å studere oversettelsessvar kreves det metoder som gir minimalt forvrengte øyeblikksbilder av oversettelseslandskapet. Polysomprofilering er en klassisk tilnærming som brukes i studiet av oversettelse på tvers av mRNA, som involverer separasjon av poly (ribo)somalfraksjoner av mRNA via ultracentrifugation gjennom sukrose gradienter26,27. Tilnærmingen kan brukes til å utforske oversettelsesnivåer for individuelle mRNAer (med deteksjonsmetoder som omvendt transkripsjon og polymerasekjedereaksjon, RT-PCR26), eller globalt i forbindelse med teknikker med høy gjennomstrømning (mikroarray eller RNA-seq28,29). En mer utviklet tilnærming er ribosomprofilering, som tillater studiet av posisjoner av forlengelse av ribosomer langs et mRNA-molekyl i genomomskala, samt inferens av effektivitet av oversettelse på tvers av transkripsjon og utnyttelse av de viktigste og alternative startstedene30,31. Ribosomprofilering innebærer isolering og sekvensering av mRNA-fragmenter beskyttet av ribosomal tilstedeværelse over dem. Ribosomprofilering har gitt betydelig innsikt i oversettelsesdynamikk på tvers av en rekke forhold, inkludert hypoksisk stress, varmesjokk og oksidativt stress31,32. Teknikken er tilpasset flere kildematerialetyper, inkludert gjær og pattedyrceller.
Mens polysom- og ribosomprofilering har vært grunnleggende for å utvide forskningens evner i oversettelse, inkluderer oversettelsesprosessen ulike oversettelsesmessige mellomprodukter og komplekser som er vanskelige å fange opp med disse metodene11,13. En ekstra begrensning stammer fra mangel på evne til å studere raske responstyper, da translasjonskomplekser enten stabiliseres in vivo ved tilsetning av spesifikke oversettelseshemmere (antibiotika), noe som fører til visse ribosomefordelingsartefakter, eller ex vivo på cellelys spesielt (antibiotika) eller uspesifisert (høyt salt eller magnesiumioner), noe som fører til deprivasjon av de kortere levde eller mindre stabile mellomprodukter33, 34,35.
Formaldehyd er mye brukt til å krysslinke nukleinsyrer og proteiner, for eksempel i kromatinimmunoprecipitation (ChIP) og crosslinking immunoprecipitation (CLIP) studier. Den lille størrelsen og utmerket cellegjennomtrengelighet gir mulighet for en rask in vivo-handling 36. Basert på den raske formaldehyd-krysskoblingen er ribosomets profileringsmetode utvidet med Translation Complex Profile Sequencing (TCP-seq)10,36,37,38,39,40. TCP-seq, som først ble utviklet i gjær, gjør det mulig å fange opp alle mellomliggende oversettelser, inkludert skanning eller SSU-komplekser etter avslutning og flere ribosomale konfigurasjoner37,38,41,42. Metoden har blitt brukt i flere studier10,38,39,41,42, hvorav noen bruker en kombinatorisk tilnærming til både oversettelseshemmere og formaldehyd krysskobling for å lette arrestasjonen av oversettelse. En ytterligere modifisert versjon av teknikken, selektiv TCP-seq39, har nylig blitt brukt til å inkludere immunopurifisering av krysskoblede komplekser, noe som utvider omfanget av TCP-seq-applikasjonene. Formaldehyd-krysskoblingens raske, effektive og reversible natur gjør disse tilnærmingene egnet for å studere forbigående mRNA:translation komplekse interaksjoner, spesielt i sammenheng med svært dynamiske responsveier på oversettelsesnivå.
Her beskriver vi prosessene med in vivo formaldehyd crosslinking med det formål å omfattende oversettelseskompleksstabilisering og isolasjon. Vi tilbyr separate protokoller nyansert for gjær og pattedyrceller (Figur 1). Vi skisserer videre eksempler på etterfølgende bruk av krysskoblingstabilisert materiale (figur 1), for eksempel for korenset proteinfaktordeteksjon ved hjelp av immunoblotting (western-blotting), immunassistert rensing (eller ‘immunrecipitation’; IP) og berikelse av translasjonskomplekser som inneholder spesifikke faktorer av interesse, elektronmikroskopi og RNA-sekvensering.
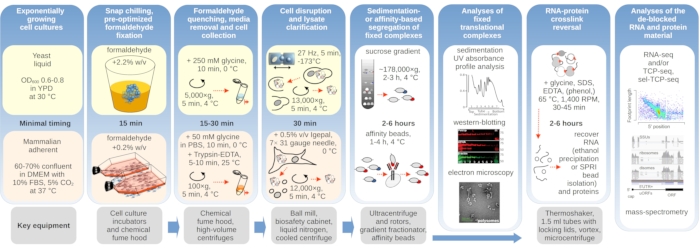
Figur 1: Skjematisk som viser en oversikt over det vanlige eksperimentelle oppsettet. Hovedtrinnene i in vivo formaldehydstabilisering av translasjonskomplekser er avbildet som et flytskjema, supplert med informasjon om de viktigste nødvendige instrumentene. Potensielle nedstrømsapplikasjoner av det krysskoblede materialet er skissert, inkludert eksempler som har blitt brukt, men ikke direkte dekket i denne protokollen, for eksempel SPRI-perlerensing av RNA, RNA-sekvensering og massespektrometri. Klikk her for å se en større versjon av denne figuren.
Protocol
Representative Results
Discussion
Formaldehydfiksering er en praktisk og populær metode for å oppnå rask in vivo-krysskobling av biomolekyler10,36,45,46,47,48. Sammenlignet med de andre potensielle biomolekylmålene, krever vellykket fangst av translasjonskomplekser en umiddelbar fiksering under snap-kjøling av cellene eller annet materiale. Uten den ubelagte stabiliseringen er det et potensial for at forskjellige oversettelsesrelaterte prosesser kan fortsette, og flytte den komplekse fordelingen bort fra den uforstyrrede in vivo-tilstanden 49. Sammenlignet med de andre metodene for translasjonell arrestasjon og ribosomal kompleks stabilisering, lover hurtigheten av formaldehydvirkning på tvers av cellemembraner og krysskoblingenes ukritiske natur bevaring av det maksimale mangfoldet av oversettelseskompleksets mellomprodukter nærmere deres opprinnelig distribuerte tilstander50.
Tilnærmingen som presenteres her er etablert og optimalisert i både gjær og pattedyrceller, og metoder er nå avledet av andre grupper for bruk på tvers av mer mangfoldig biologisk materiale, for eksempel i hele vertebrater (f.eks. sebrafiskembryoer)10,38,39,49,51,52 . Selv om disse verkene samlet beroliger allsidigheten og den brede anvendbarheten av tilnærmingen, kan rask formaldehyd krysskobling av oversettelseskomplekser betraktes som noe vanskelig å transponere til nye typer biologisk materiale på grunn av behovet for optimaliseringer og justeringer.
Et fremst krav til metodens suksess er reoptimalisering av konsentrasjonen av formaldehyd og cellesamlings- og forstyrrelsesteknikken. Mindre gjennomtrengelige, små og runde gjærceller krever mye høyere (minst 10 ganger) formaldehydkonsentrasjon og fysisk forstyrrelse av de faste cellene. I kontrast kan store og flate tilhengerpattedyrceller i kulturen lett overfaste og kreve skånsom håndtering ved fiksering, mens utvinningen av de faste kompleksene kan utføres kjemisk med membranforstyrrelser ved hjelp av vaskemidler. Under-crosslinking kan tillate mindre stabile eller mer kortvarige mellomprodukter å dissosiere eller lekke inn i en senere tilstand. Over-crosslinking kan påvirke evnen til å isolere og studere ribosomale fraksjoner negativt og kan skape selektive fordommer som dypere uttømming av tunge komplekser. I vår observasjon kan selv mindre endringer, for eksempel typen tilhenger av menneskelige celler som brukes, påvirke utbyttet av de gjenopprettede krysskoblede kompleksene og kan kreve reoptimalisering av krysskoblingsregimet. Vi kan også forutse at celler med vesentlig forskjellige permeabilitetsegenskaper, for eksempel planteceller, vil kreve ytterligere omfattende optimalisering av fikseringsbetingelsene52. Likevel er det vanskelig å forestille seg en type biologisk materiale som ville være helt uforenlig med tilnærmingen.
En vurdering som er relevant for pattedyrfikseringsprotokollen er tettheten og mengden cellemateriale som brukes som inngang. Det anbefales å la cellene kontinuerlig vokse uten re-seeding eller andre perturbasjoner i minst 2 dager for å unngå ytre påvirkninger på cellulær oversettelsesdynamikk. Gjelder for de fleste celletyper, men for de fleste tilhengerceller som konsekvent oppnås samløpsnivåer på ikke mer enn 70%, vil det sikre fravær av store kontakthemmingseffekter som kan påvirke oversettelsesraten negativt og uforutsigbart.
En annen interessant, og potensielt unikt praktisk, funksjon av formaldehydfiksering som stammer fra dens ukritiske reaktivitet, er stabiliseringseffekten på translasjonskomplekser i systemer med blandet taksonomi. Bakterielle, og enda mer så translasjonelle komplekser av mitokondrier, kloroplaster og forskjellige intracellulære parasitter, har vært notorisk vanskelig å målrette mot med spesifikke oversettelseshemmere. I TCP-seq-dataene er derimot fotavtrykk som tilordnes mitotranscriptomet, lett observerbare i dataene38,39,50. En interessant påfølgende utvikling kan være bruken av tilnærmingen til å undersøke oversettelse i hele mikrokommuniteter, for eksempel i jord-, vann- eller tarmprøver, der pålitelig rask translasjonell arrestasjon og kompleks stabilisering med andre midler ville være problematisk.
Det bør også nevnes at for det mest kompliserte materialet (som hardt og / eller klumpete vev), forhindrer ingenting bruk av formaldehydstabilisering umiddelbart ved celleforstyrrelser og materiell homogenisering. Denne tilnærmingen brukes allerede ofte for å fjerne celleinngangsforsinkelsen når du stabiliserer translasjonskomplekser med spesifikke små molekylhemmere33,53,54,55. Gitt at formaldehydfiksering tradisjonelt har blitt brukt med gode resultater for ex vivo / in vitro prøvestabilisering i applikasjoner som elektronmikroskopi45,56,57,58, kan vi forvente enda mindre negative effekter i dette tilfellet, spesielt de som er forbundet med dårlig utvinning av translasjonskompleksene fra de grundig faste cellene.
Våre funn bekrefter brukervennligheten til rask formaldehydfiksering for å stabilisere svært forbigående komplekser, for eksempel de som inkluderer eIF4A. Det er bemerkelsesverdig at gjær eIF4A i motsetning til pattedyr er mye mer svakt forbundet med hettebindingskomplekset eIF4F og som et resultat oversettelseskomplekser generelt. eIF4A går vanligvis tapt under omfattende rensing av ribosomalt materiale i gjær29,59,60,61,62,63. Likevel, i det in vivo-fastegjærmaterialet, er det mulig å oppnå pålitelig berikelse av eIF4A i alle brøkdeler av oversettelseskomplekser der dets tilstedeværelse ville forventes. De tidligere publiserte Sel-TCP-seq-dataene har vist berikelsen av eIF2 og eIF3 som sterkere forbinder med ribosomene (men også avslørt forbigående forekommende co-translational protein kompleks montering)39. Dermed er metoden egnet for påvisning av både sterkere og svakere tilknyttede bestanddeler av oversettelseskompleksene.
For å oppsummere har vi presentert en tilnærming som er nyttig for å få innsikt først og fremst i endringene som skjer i startfasen av oversettelsen, og når minimalt perturbert ribosomal distribusjon over mRNA er nødvendig. Det er viktig at tilnærmingen er egnet for stabilisering av relativt labile og dynamiske komponenter av translasjonskomplekser, for eksempel eIF4A, og kan brukes bredt utsatt for nødvendige optimaliseringer. Vi har også gitt bevis på nytten av formaldehydfiksering i scenariene for rask dynamisk oversettelsesendring, og åpner opp undersøkelsesområder som raske cellulære responser på miljøendringer eller stressforhold.
Divulgazioni
The authors have nothing to disclose.
Acknowledgements
Dette arbeidet ble støttet av Australian Research Council Discovery Project grant (DP180100111 til T.P. and N.E.S), National Health and Medical Research Council Investigator Grant (GNT1175388 til N.E.S.) og Research Fellowship (APP1135928 til T.P.). Forfatterne anerkjenner fasilitetene til Microscopy Australia ved Centre for Advanced Microscopy, Australian National University, et anlegg som er finansiert av Universitetet og den føderale regjeringen.
Materials
| Yeast extract | Merck, Sigma-Aldrich | 70161 | |
| Peptone | Merck, Sigma-Aldrich | 70178 | |
| D-Glucose (Dextrose) | Merck, Sigma-Aldrich | 49139 | |
| Adenine sulphate | Amresco | 0607-50G | |
| Formaldehyde solution | Merck Sigma-Aldrich | F11635-500ML | ACS reagent, 37 wt. % in H2O, contains 10-15% Methanol as stabiliser (to prevent polymerisation) |
| RNaseOUT™ Recombinant Ribonuclease Inhibitor | Invitrogen™ byThermo Fischer Scientific | 10777019 | |
| cOmplete™, EDTA-free Protease Inhibitor Cocktail | COEDTAF-RO Roche by Merck | 11873580001 | |
| Magnesium chloride solution | (Merck/Sigma-Aldrich) | M1028 | |
| Ethylenediaminetetraacetic acid solution | (Merck/Sigma-Aldrich) | E7889 | |
| Ambion™ RNase I, cloned, 100 U/µL | Ambion | AM2294 | |
| SUPERase•In™ RNase Inhibitor (20 U/μL) | Invitrogen™ by Thermo Fisher Scientific | AM2694 | |
| Acidic phenol:chlorophorm:isoamyl alcohol 125:24:1 (pH 4.0-5.0) | (Merck/Sigma-Aldrich) | P1944-100ML | |
| Dynabeads™ Goat Anti-Mouse IgG | Invitrogen™ by Thermo Fisher Scientific) | 11033 | |
| Sodium Acetate (3 M), pH 5.5 | Invitrogen™ by Thermo Fisher Scientific) | AM9740 | |
| Glycogen (5 mg/ml) | Invitrogen™ by Thermo Fisher Scientific) | AM9510 | |
| Ethyl alcohol, Pure | Merck; Sigma Aldrich | E7023 | |
| Amersham™ Hybond® P Western blotting membranes, PVDF | Merck | GE10600023 | PVDF membrane for western blotting |
| Bolt™ 4 to 12%, Bis-Tris, 1.0 mm, Mini Protein Gel | Invitrogen™ by ThermoFischer Sientific | NW04120BOX | Protein gel |
| 4X Bolt™ LDS Sample Buffer | Invitrogen™ by ThermoFischer Sientific | B0007 | LDS sample loading buffer |
| Precision Plus Protein™ Kaleidoscope™ Prestained Protein Standards | BioRad | 1610375 | Protein ladder |
| 20X Bolt™ MES SDS Running Buffer | ThermoFischer Scientific | B0002 | PAGE runninjg buffer |
| Intercept® (PBS) Blocking Buffer | LI-COR | 927-70001 | Odyssey Blcoking buffer (PBS) |
| IRDye® 800CW Goat anti-Mouse IgG Secondary Antibody | LI-COR | 92632210 | |
| IRDye® 800CW Goat anti-Rabbit IgG Secondary Antibody | LI-COR | 92632211 | |
| TAP Tag Polyclonal Antibody | Invitrogen™ by ThermoFischer Sientific | CAB1001 | |
| Anti-beta Actin antibody | Abcam | ab8227 | |
| Sucrose | (Merck/Sigma-Aldrich) | 84097 | BioUltra, for molecular biology, ≥99.5% (HPLC) |
| DL-Dithiothreitol solution | (Merck/Sigma-Aldrich) | 43816 | BioUltra, for molecular biology, ~1 M in H2O |
| Terumo Syringe 1CC/mL | Terumo Syringe | 878499 | |
| Potassium chloride | (Merck/Sigma-Aldrich) | 60128 | |
| HEPES | (Merck/Sigma-Aldrich) | H3375 | |
| Dulbecco's Modified Eagle's Medium – high glucose | Sigma Aldrich | D5796 | |
| Fetal Bovine Serum | Sigma Aldrich | 12003C | |
| Trypsin-EDTA (0.05%), phenol red | Gibco | 25300062 | |
| Dulbecco's Phosphate Buffered Saline with Calcium and magnesium | Sigma-Aldrich | D8662 | |
| Glycine | Sigma-Aldrich | G7126 | |
| Tris hydrochloride | Merck/Sigma-Aldrich | 10812846001 | |
| Sodium dodecyl sulfate | Merck/Sigma-Aldrich | 436143 | |
| IGEPAL CA-630 | Merck/Sigma-Aldrich | I3021 | |
| Rnasin Ribonuclease Inhibitor | Promega | N2111 | |
| Stainless steel grinding jar | Retsch | 02.462.0059 | |
| MM400 mixer mill | Retsch | 20.745.0001 | |
| Gradient Fractionator | Brandel | BRN-BR-188 | |
| Thermomixer R | Eppendorf | Z605271 | |
| Nanodrop spectrophotometer | Thermo Fisher Scientific | ND-2000 | |
| 0.5-ml microcentrifuge tubes with locking devices | Eppendorf Safe-Lock | 30121023 | |
| Mini Gel Tank | (Thermo Fisher Scientific) | A25977 | PAGE running tank |
| 5 mL, Open-Top Thinwall Ultra-Clear Tube, 13 x 51mm | Beckman-Coulter | 344057 | |
| 13.2 mL, Certified Free Open-Top Thinwall Polypropylene, 14 x 89mm – 50Pk | Beckman-Coulter | 331372 | |
| Amicon Ultra-0.5 ultrafiltration devices | Merck | UFC5030 | Ultracel-30 regenerated cellulose membrane, 0.5 mL sample volume |
| Thermo Sorvall Evolution RC Floor Super Speed Centrifuge | Cambridge Scientific | 15566 | |
| Beckman Coulter Optima L-90K | GMI | 8043-30-1191 | |
| Nunc EasYFlask 175cm2 | Thermofisher Scientific | 159910 | |
| Falcon 50 mL Conical Centrifuge Tubes | Thermofisher Scientific | 14-432-22 | |
| 25 mL Serological Pipette | Sigma-Aldrich | SIAL1250 | |
| 10 mL Serological Pipette | Sigma-Aldrich | SIAL1100 | |
| DNA lobind tubes | Eppendorf | 30108051 | |
| Cold Centrifuge 5810 R | Eppendorf | EP022628188 | for 50 mL tubes |
| Orbital Shaking Incubator | Ratek | OM11 | |
| Frezco 17 Microcentrifuge | Thermofisher Scientific | 75002402 | |
| Eppendorf DNA lo-bind tubes | Merck/Sigma-Aldrich | EP0030108051 | |
| Eppendorf® Protein LoBind tubes | Merck/Sigma-Aldrich | EP0030108116 | |
| SW 41 Ti Swinging bucket rotor | Beckman-Coulter | 331362 | |
| Heracell™ 150i CO2 Incubator, 150 L | Thermofisher Scientific | 51026282 | |
| 0,3 mL ultra-fine II short insulin syringe | BD Medical | 328822 | |
| 3 mL syringe with Luer Lok tip | BD Medical | 302113 | |
| 25 G x 16 mm Hypodermic Needle | Terumo | TUAN2516R1 |
Riferimenti
- Janapala, Y., Preiss, T., Shirokikh, N. E. Control of translation at the initiation phase during glucose starvation in yeast. International Journal of Molecular Sciences. 20 (16), 4043 (2019).
- Masvidal, L., Hulea, L., Furic, L., Topisirovic, I., Larsson, O. mTOR-sensitive translation: Cleared fog reveals more trees. RNA Biology. 14 (10), 1299-1305 (2017).
- Ashe, M. P., De Long, S. K., Sachs, A. B. Glucose depletion rapidly inhibits translation initiation in yeast. Molecular Biology of the Cell. 11 (3), 833-848 (2000).
- Crawford, R. A., Pavitt, G. D. Translational regulation in response to stress in Saccharomyces cerevisiae. Yeast. 36 (1), 5-21 (2019).
- Melamed, D., Pnueli, L., Arava, Y. Yeast translational response to high salinity: global analysis reveals regulation at multiple levels. RNA. 14 (7), 1337-1351 (2008).
- Hershey, J. W., Sonenberg, N., Mathews, M. B. Principles of translational control: An overview. Cold Spring Harbor Perspectives in Biology. 4 (12), 011528 (2012).
- Mata, J., Marguerat, S., Bähler, J. Post-transcriptional control of gene expression: a genome-wide perspective. Trends in Biochemical Sciences. 30 (9), 506-514 (2005).
- Spriggs, K. A., Bushell, M., Willis, A. E. Translational regulation of gene expression during conditions of cell stress. Molecular Cell. 40 (2), 228-237 (2010).
- Liu, B., Qian, S. B. Translational reprogramming in cellular stress response. Wiley Interdisciplinary Reviews RNA. 5 (3), 301-315 (2014).
- Archer, S. K., Shirokikh, N. E., Beilharz, T. H., Preiss, T. Dynamics of ribosome scanning and recycling revealed by translation complex profiling. Nature. 535 (7613), 570-574 (2016).
- Hinnebusch, A. G., Ivanov, I. P., Sonenberg, N. Translational control by 5′-untranslated regions of eukaryotic mRNAs. Science. 352 (6292), 1413-1416 (2016).
- Dever, T. E., Green, R. The elongation, termination, and recycling phases of translation in eukaryotes. Cold Spring Harbor Perspectives in Biology. 4 (7), 013706 (2012).
- Shirokikh, N. E., Preiss, T. Translation initiation by cap-dependent ribosome recruitment: Recent insights and open questions. Wiley Interdisciplinary Reviews RNA. 9 (4), 1473 (2018).
- Jiménez-Díaz, A., Remacha, M., Ballesta, J. P., Berlanga, J. J. Phosphorylation of initiation factor eIF2 in response to stress conditions is mediated by acidic ribosomal P1/P2 proteins in Saccharomyces cerevisiae. PLoS One. 8 (12), 84219 (2013).
- Sonenberg, N., Hinnebusch, A. G. Regulation of translation initiation in eukaryotes: mechanisms and biological targets. Cell. 136 (4), 731-745 (2009).
- Majmundar, A. J., Wong, W. J., Simon, M. C. Hypoxia-inducible factors and the response to hypoxic stress. Molecular Cell. 40 (2), 294-309 (2010).
- Barraza, C. E., et al. The role of PKA in the translational response to heat stress in Saccharomyces cerevisiae. PLoS One. 12 (10), 0185416 (2017).
- Richter, K., Haslbeck, M., Buchner, J. The heat shock response: Life on the verge of death. Molecular Cell. 40 (2), 253-266 (2010).
- Jamar, N. H., Kritsiligkou, P., Grant, C. M. The non-stop decay mRNA surveillance pathway is required for oxidative stress tolerance. Nucleic Acids Research. 45 (11), 6881-6893 (2017).
- Chen, Z., et al. The complete pathway for thiosulfate utilization in Saccharomyces cerevisiae. Applied and Environmental Microbiology. 84 (22), (2018).
- Marzluf, G. A. Molecular genetics of sulfur assimilation in filamentous fungi and yeast. Annual Review of Microbiology. 51, 73-96 (1997).
- Miller, D., Brandt, N., Gresham, D. Systematic identification of factors mediating accelerated mRNA degradation in response to changes in environmental nitrogen. PLoS Genetics. 14 (5), 1007406 (2018).
- Zhang, W., Du, G., Zhou, J., Chen, J. Regulation of sensing, transportation, and catabolism of nitrogen sources in Saccharomyces cerevisiae. Microbiology and Molecular Biology Reviews. 82 (1), (2018).
- Tokpohozin, S. E., Fischer, S., Becker, T. Selection of a new Saccharomyces yeast to enhance relevant sorghum beer aroma components, higher alcohols, and esters. Food Microbiology. 83, 181-186 (2019).
- Walker, G. M., Stewart, G. G. Saccharomyces cerevisiae in the production of fermented beverages. Beverages. 2 (4), 30 (2016).
- Chassé, H., Boulben, S., Costache, V., Cormier, P., Morales, J. Analysis of translation using polysome profiling. Nucleic Acids Research. 45 (3), 15 (2017).
- Jin, H. Y., Xiao, C. An integrated polysome profiling and ribosome profiling method to investigate in vivo translatome. Methods in Molecular Biology. 1712, 1-18 (2018).
- Arava, Y., et al. Genome-wide analysis of mRNA translation profiles in Saccharomyces cerevisiae. Proceedings of the National Academy of Sciences of the United States of America. 100 (7), 3889-3894 (2003).
- Lackner, D. H., et al. A network of multiple regulatory layers shapes gene expression in fission yeast. Molecular Cell. 26 (1), 145-155 (2007).
- Ingolia, N. T., Ghaemmaghami, S., Newman, J. R. S., Weissman, J. S. Genome-Wide Analysis in Vivo of Translation with Nucleotide Resolution Using Ribosome Profiling. Science. 324 (5924), 218-223 (2009).
- Ingolia, N. T., Hussmann, J. A., Weissman, J. S. Ribosome Profiling: Global Views of Translation. Cold Spring Harbor Perspectives in Biology. 11 (5), (2019).
- Gerashchenko, M. V., Lobanov, A. V., Gladyshev, V. N. Genome-wide ribosome profiling reveals complex translational regulation in response to oxidative stress. Proceedings of the National Academy of Sciences of the United States of America. 109 (43), 17394-17399 (2012).
- Hussmann, J. A., Patchett, S., Johnson, A., Sawyer, S., Press, W. H. Understanding biases in ribosome profiling experiments reveals signatures of translation dynamics in yeast. Proceedings of the National Academy of Sciences Genetics. 11 (12), 1005732 (2015).
- Santos, D. A., Shi, L., Tu, B. P., Weissman, J. S. Cycloheximide can distort measurements of mRNA levels and translation efficiency. Nucleic Acids Research. 47 (10), 4974-4985 (2019).
- Schneider-Poetsch, T., et al. Inhibition of eukaryotic translation elongation by cycloheximide and lactimidomycin. Nature Chemical Biology. 6 (3), 209-217 (2010).
- Hoffman, E. A., Frey, B. L., Smith, L. M., Auble, D. T. Formaldehyde crosslinking: A tool for the study of chromatin complexes. Journal of Biological Chemistry. 290 (44), 26404-26411 (2015).
- Kage, U., Powell, J. J., Gardiner, D. M., Kazan, K. Ribosome profiling in plants: What is not lost in translation. Journal of Experimental Botany. 71 (18), 5323-5332 (2020).
- Shirokikh, N. E., Archer, S. K., Beilharz, T. H., Powell, D., Preiss, T. Translation complex profile sequencing to study the in vivo dynamics of mRNA-ribosome interactions during translation initiation, elongation and termination. Nature Protocols. 12 (4), 697-731 (2017).
- Wagner, S., et al. Selective translation complex profiling reveals staged initiation and co-translational assembly of initiation factor complexes. Molecular Cell. 79 (4), 546-560 (2020).
- Zlotorynski, E. Profiling ribosome dynamics. Nature Reviews Molecular Cell Biology. 17 (9), 535-535 (2016).
- Sen, N. D., Gupta, N., S, K. A., Preiss, T., Lorsch, J. R., Hinnebusch, A. G. Functional interplay between DEAD-box RNA helicases Ded1 and Dbp1 in preinitiation complex attachment and scanning on structured mRNAs in vivo. Nucleic Acids Research. 47 (16), 8785-8806 (2019).
- Zhao, J., Qin, B., Nikolay, R., Spahn, C. M. T., Zhang, G. Translatomics: The global view of translation. International Journal of Molecular Sciences. 20 (1), 20010212 (2019).
- Luthe, D. S. A simple technique for the preparation and storage of sucrose gradients. Analytical Biochemistry. 135 (1), 230-232 (1983).
- Wang, Z., Gerstein, M., Snyder, M. RNA-Seq: A revolutionary tool for transcriptomics. Nature Review Genetics. 10 (1), 57-63 (2009).
- Orlando, V. Mapping chromosomal proteins in vivo by formaldehyde-crosslinked-chromatin immunoprecipitation. Trends in Biochemical Sciences. 25 (3), 99-104 (2000).
- Schmiedeberg, L., Skene, P., Deaton, A., Bird, A. A Temporal Threshold for Formaldehyde Crosslinking and Fixation. PLoS One. 4 (2), 4636 (2009).
- Solomon, M. J., Varshavsky, A. Formaldehyde-mediated DNA-protein crosslinking: A probe for in vivo chromatin structures. Proceedings of the National Academy of Sciences. 82 (19), 6470-6474 (1985).
- Solomon, M. J., Larsen, P. L., Varshavsky, A. Mapping proteinDNA interactions in vivo with formaldehyde: Evidence that histone H4 is retained on a highly transcribed gene. Cell. 53 (6), 937-947 (1988).
- Bohlen, J., Fenzl, K., Kramer, G., Bukau, B., Teleman, A. A. Selective 40S footprinting reveals cap-tethered ribosome scanning in human cells. Molecular Cell. 79 (4), 561-574 (2020).
- Shirokikh, N. E. Translation complex stabilization on messenger RNA and footprint profiling to study the RNA responses and dynamics of protein biosynthesis in the cells. Critical Reviews in Biochemistry and Molecular Biology. , (2021).
- Giess, A., et al. Profiling of small ribosomal subunits reveals modes and regulation of translation initiation. Cell Reports. 31 (3), 107534 (2020).
- Firmino, A. A. P., et al. Separation and paired proteome profiling of plant chloroplast and cytoplasmic ribosomes. Plants (Basel). 9 (7), (2020).
- Gerashchenko, M. V., Gladyshev, V. N. Translation inhibitors cause abnormalities in ribosome profiling experiments. Nucleic Acids Research. 42 (17), 134 (2014).
- Santos, D. A., Shi, L., Tu, B. P., Weissman, J. S. Cycloheximide can distort measurements of mRNA levels and translation efficiency. Nucleic Acids Research. 47 (10), 4974-4985 (2019).
- Schneider-Poetsch, T., et al. Inhibition of eukaryotic translation elongation by cycloheximide and lactimidomycin. Nature Chemical Biology. 6 (3), 209-217 (2010).
- Plénat, F., et al. Formaldehyde fixation in the third millennium. Annales De Pathologie. 21 (1), 29-47 (2001).
- Salic, A., Mitchison, T. J. A chemical method for fast and sensitive detection of DNA synthesis in vivo. Proceedings of the National Academy of Sciences. 105 (7), 2415-2420 (2008).
- Wang, N. S., Minassian, H. The formaldehyde-fixed and paraffin-embedded tissues for diagnostic transmission electron microscopy: A retrospective and prospective study. Human Pathology. 18 (7), 715-727 (1987).
- Grifo, J. A., et al. Characterization of eukaryotic initiation factor 4A, a protein involved in ATP-dependent binding of globin mRNA. Journal of Biological Chemistry. 257 (9), 5246-5252 (1982).
- Li, Y. Commonly used tag combinations for tandem affinity purification. Biotechnology and Applied Biochemistry. 55 (2), 73-83 (2010).
- Blum, S., et al. ATP hydrolysis by initiation factor 4A is required for translation initiation in Saccharomyces cerevisiae. Proceedings of the National Academy of Sciences. 89 (16), 7664-7668 (1992).
- Merrick, W. C. eIF4F: A Retrospective. Journal of Biological Chemistry. 290 (40), 24091-24099 (2015).
- Rogers, G. W., Komar, A. A., Merrick, W. C. eIF4A: The godfather of the DEAD box helicases. Progress in Nucleic Acid Research and Molecular Biology. 72, 307-331 (2002).

