Microtubule زائد نهاية ديناميات التصور في نموذج مرض هنتنغتون على أساس الخلايا الليفية الجلد الأساسية البشرية
Summary
هذا البروتوكول مخصص للتصور microtubule زائد نهاية بواسطة EB3 البروتين transfection لدراسة خصائصها الحيوية في ثقافة الخلايا الأولية. تم تنفيذ البروتوكول على الخلايا الليفية الجلدية الأولية البشرية التي تم الحصول عليها من مرضى مرض هنتنغتون.
Abstract
Transfection مع بروتين علامة المسمى fluorescently من الفائدة في تركيبة مع المجهر الفيديو الفاصل الزمني هو وسيلة كلاسيكية لدراسة الخصائص الديناميكية للهيكل الخلوي. يقدم هذا البروتوكول تقنية لإصابة الإنسان بالخلايا الليفية الأولية ، والتي يمكن أن تكون صعبة بسبب تفاصيل ظروف زراعة الخلايا الأولية. بالإضافة إلى ذلك، يتطلب الهيكل الخلوي صيانة الممتلكات الحيوية مستوى منخفض من العدوى للحصول على نسبة جيدة من الإشارة إلى الضوضاء دون التسبب في استقرار microtubule. من المهم اتخاذ تدابير لحماية الخلايا من الإجهاد الناجم عن الضوء وتلاشي الصبغة الفلورية. في سياق عملنا، اختبرنا طرق وبروتوكولات مختلفة للإصابة وكذلك ناقلات مختلفة لاختيار أفضل مزيج من الشروط المناسبة لدراسات الورم الليفي الأولي للإنسان. قمنا بتحليل مقاطع الفيديو الناتجة عن الفاصل الزمني وديناميكيات microtubule المحسوبة باستخدام ImageJ. ديناميات microtubules ‘زائد ينتهي في أجزاء الخلية المختلفة ليست متشابهة ، لذلك قسمنا التحليل إلى مجموعات فرعية — المنطقة المركزية ، ولاميلا ، وذيل الخلايا الليفية. وتجدر الإشارة إلى أن هذا البروتوكول يمكن استخدامه للتحليل المختبري لديناميكيات الهيكل الخلوي في عينات المرضى ، مما يتيح الخطوة التالية نحو فهم ديناميكيات تطور المرض المختلفة.
Introduction
مرض هنتنغتون (HD) هو مرض تنكسي عصبي غير قابل للشفاء ناجم عن بروتين ترميز الجينات الطفرة (HTT). ويرتبط HTT في المقام الأول مع الحويصلات والبيبوليتولات الصغيرة، وربما تشارك في عمليات النقل التي تعتمد على microtubule1،2. لدراسة تأثير HTT متحولة على ديناميات microtubule، استخدمنا في التصور المختبري للبروتين EB3، الذي ينظم الخصائص الديناميكية لل microtubules عن طريق ربط وتحقيق الاستقرار في النمو زائد ينتهي. لتحميل الفلورسنت المسمى EB3 في الخلايا الليفية الجلد البشري، تم تطبيق التراتوفيكيد البلازميد. استخدمنا ثقافة الخلايا الليفية الأولية التي تم الحصول عليها من خزعة جلد المرضى عالية الدقة لهذه الدراسة.
الطفرة في الجين البروتين HTT يؤدي إلى استطالة من البوليglutamine المسالك3. HTT له دور في عمليات خلوية مثل الغدد الصماء4، نقل الخلية1،2، تدهور البروتين5، إلخ. جزء كبير من هذه العمليات ينطوي على عناصر مختلفة من الهيكل الخلوي الخلية، بما في ذلك microtubules.
الخلايا الأولية البشرية هي أفضل نموذج لإعادة إنتاج الأحداث التي تحدث في خلايا المريض عن كثب قدر الإمكان. لإنشاء مثل هذه النماذج ، يحتاج المرء إلى عزل الخلايا عن مواد الخزعة البشرية (على سبيل المثال ، من العينات الجراحية). خط الخلية الأولية الناتجة مناسبة لدراسة الإمراض باستخدام مختلف الأساليب الوراثية والكيميائية الحيوية والجزيئية وبيولوجيا الخلايا. أيضا، ثقافات الخلايا الأولية البشرية بمثابة مقدمة لخلق مختلف الثقافات المتحولة وراثيا ومحورةوراثيا 6.
ومع ذلك ، على النقيض من ثقافات الخلايا الخالدة ، فإن العيب الكبير للخلايا الأولية هو قدرتها المحدودة على المرور. لذلك، نوصي باستخدام الخلايا في مرحلة الممرات المبكرة (حتى 15). الثقافات القديمة تتدهور بسرعة كبيرة، وتفقد خصائصها الفريدة. وبالتالي، ينبغي الاحتفاظ الخلايا الأولية التي تم الحصول عليها حديثا المجمدة للتخزين على المدى الطويل.
ثقافات الخلايا الأولية عرضة لظروف الزراعة. ولذلك، فإنها غالبا ما تتطلب نهجا فريدة من نوعها والاستفادة المثلى من ظروف النمو. على وجه الخصوص ، فإن الخلايا الليفية الأولية للبشرة البشرية المستخدمة في تجاربنا تتطلب على الركيزة. ومن ثم، استخدمنا مختلف الطلاء إضافية (على سبيل المثال، الجيلاتين أو فيبروكتين) اعتمادا على نوع التجربة.
يحدد الهيكل الخلوي الخلوي شكل الخلية وحركتها وحركتها. ديناميات الهيكل الخلوي حاسمة بالنسبة للعديد من العمليات داخل الخلايا على حد سواء في مرحلة ما بين المراحل والميتوسيس. على وجه الخصوص، والهيكل الخلوي بوليمر من توبولين، هي هياكل ديناميكية للغاية والقطبية، وتمكين النقل الحركي بوساطة البروتين الموجهة داخل الخلايا. نهايات microtubules هي في إعادة ترتيب مستمر، مراحل التجميع الخاصة بهم بالتناوب مع مراحل التفكيك، وهذا السلوك يسمى “عدم الاستقرار الديناميكي”7،8،9. تحول البروتينات المختلفة المرتبطة بها توازن تفاعل البلمرة ، مما يؤدي إما إلى تكوين البوليمر أو تكوين مونومر البروتين. إضافة وحدات توبولين الفرعية يحدث أساسا في نهاية زائد من microtubules10. تتكون عائلة البروتينات الملزمة النهائية (EB) من ثلاثة أعضاء: EB1 و EB2 و EB3. أنها بمثابة زائد نهاية تتبع البروتينات (+TIPs) وتنظيم الخصائص الديناميكية لل microtubules عن طريق ربط وتحقيق الاستقرار في النمو زائد ينتهي11.
تستخدم العديد من الدراسات الفلورسنت المسمى جزيء أنبوبولين microinjection أو العدوى مع التصوير الفاصل الزمني وتحليل الفيديو لتصور microtubules في المختبر. قد تكون هذه الطرق الغازية والضارة للخلايا، وخاصة الخلايا البشرية الأولية. الخطوة الأكثر تحديا هي إيجاد ظروف لإصابة الخلايا. حاولنا الوصول إلى أعلى مستوى ممكن من العدوى دون التأثير على الجدوى ومورفولوجيا الخلايا الأصلية. تطبق هذه الدراسة الطريقة الكلاسيكية لدراسة الاختلافات في ديناميات microtubule في الخلايا الليفية الجلدية من المتبرعين الأصحاء والمرضى الذين يعانون من مرض هنتنغتون.
Protocol
Representative Results
Discussion
يمكن الحصول على نتائج أفضل جودة لتحليل ديناميكيات microtubules من صور مجهرية عالية الجودة. من المهم مراقبة جميع الشروط اللازمة لتصوير الخلايا الحية بفارق زمني وضبط معلمات التصوير بشكل صحيح. استخدام أطباق خاصة ثقافة الخلية مع أسفل الزجاج (أطباق confocal) مهم، لأن الزجاج لديه مؤشر الانكسار مختلفة من …
Divulgazioni
The authors have nothing to disclose.
Acknowledgements
تم تمويل هذا البحث من قبل وزارة العلوم والتعليم العالي في الاتحاد الروسي، منحة رقم 075-15-2019-1669 (نقل الخلايا الليفية)، من قبل مؤسسة العلوم الروسية، منحة رقم 19-15-00425 (جميع الأعمال الأخرى على زراعة الخلايا الليفية في المختبر). وقد دعم جزئيا من قبل برنامج تطوير جامعة موسكو الحكومية لومونوسوف PNR5.13 (التصوير والتحليل). يعترف المؤلفون بدعم مركز نيكون للتميز في معهد أ. ن. بيلوزيرسكي للبيولوجيا الفيزيائية والكيميائية. نريد أن نقدم شكرنا الخاص لإيكاترينا تاران لمساعدتها في التمثيل الصوتي. كما يشكر المؤلفون بافل بيلكوف على مساعدته في تحرير الفيديو. تم إنشاء الأرقام في المخطوطة مع BioRender.com.
Materials
| Instrumentation | |||
| Camera iXon DU897 EMCCD | Andor Technology | ||
| Eppendorf Centrifuge 5804 R | Eppendorf Corporate | ||
| Fluorescence filter set HYQ FITC | Nikon | Alternative: Leica, Olympus, Zeiss | |
| LUNA-II Automated Cell Counte | Logos Biosystems | L40002 | |
| Microscope incubator for lifetime filming | Okolab | Temperature controller H301-T-UNIT-BL-PLUS | |
| Gas controller CO2-O2-UNIT-BL | |||
| Objective lens CFI Plan Apo Lambda 60x Oil 1.4 (WD 0.13) | Nikon | Alternative: Leica, Olympus, Zeiss | |
| Widefield fluorescence light microscope Eclipse Ti-E | Nikon | Alternative: Leica, Olympus, Zeiss | |
| Software | |||
| Fiji (Image J version 2.1.0/1.53c) | Open source image processing software | ||
| NIS Elements | Nikon | Alternative: Leica, Olympus, Zeiss | |
| Additional reagents | |||
| Mineral oil (Light white oil) | MP | 151694 | |
| Cell culture dish | |||
| Cell Culture Dish | SPL Lifesciences | 20035 | |
| Confocal Dish (glass thickness 170 µm) | SPL Lifesciences | 211350 | Alternative: MatTek |
| Conical Centrifuge tube | SPL Lifesciences | 50015 | |
| Cryogenic Vials | Corning-Costar | 430659 | |
| Microcentrifuge Tube | Nest | 615001 | |
| Cultivation | |||
| Lipofectamine 3000 Transfection Reagent | Thermo Fisher Scientific | L3000001 | |
| Dimethyl sulfoxide | PanEko | 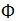 135 135 |
|
| DMEM (Dulbecco's Modified Eagle Media) | PanEko | C420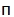 |
|
| DPBS (Dulbecco's phosphate-salt solution) | PanEko | P060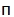 |
|
| Fetal bovine serum (FBS) | Hyclone | K053/SH30071.03 | |
| Gelatin (bovine skin) | PanEko | 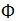 070 070 |
|
| GlutaMAX | Thermo Fisher Scientific | 35050038 | |
| Opti-MEM (1x) + Glutamax | Gibco | 519850026 | |
| Penicillin-streptomycin | PanEko | A063 |
|
| Trypsin-EDTA (0.25%) | Thermo Fisher Scientific | 25200072 | |
| Transfection | |||
| Plasmid DNA with EB3-GFP | Kind gift of Dr. I. Kaverina [Vanderbilt University, Nashville] with permission from Dr. A. Akhmanova [Erasmus University, Rotterdam] |
Stepanova et al., 2003 DOI: 10.1523/JNEUROSCI.23-07-02655.2003 |
Riferimenti
- Engelender, S., et al. Huntingtin-associated Protein 1 (HAP1) Interacts with the p150 Glued Bubunit of Dynactin. Human Molecular Genetics. 6 (13), 2205-2212 (1997).
- Caviston, J. P., Ross, J. L., Antony, S. M., Tokito, M., Holzbaur, E. L. Huntingtin facilitates dynein/dynactin-mediated vesicle transport. Proceedings of the National Academy of Sciences. 104 (24), 10045-10050 (2007).
- MacMillan, J. C., et al. Molecular analysis and clinical correlations of the Huntington’s disease mutation. The Lancet. 342 (8877), 954-958 (1993).
- Proskura, A. L., Vechkapova, S. O., Zapara, T. A., Ratushniak, A. S. Protein-protein interactions of huntingtin in the hippocampus. Biologia Molecolare. 51 (4), 647-653 (2017).
- Steffan, J. S., et al. The Huntington’s disease protein interacts with p53 and CREB-binding protein and represses transcription. Proceedings of the National Academy of Sciences. 97 (12), 6763-6768 (2000).
- Nekrasov, E. D., et al. Manifestation of Huntington’s disease pathology in human induced pluripotent stem cell-derived neurons. Molecular Neurodegeneration. 11 (1), 1-15 (2016).
- Mitchison, T., Kirschner, M. Dynamic instability of microtubule growth. Nature. 312 (5991), 237-242 (1984).
- Walker, R. A., et al. Dynamic instability of individual microtubules analyzed by video light microscopy: rate constants and transition frequencies. The Journal of Cell Biology. 107 (4), 1437-1448 (1988).
- Desai, A., Mitchison, T. J. Microtubule polymerization dynamics. Annual Review of Cell and Developmental Biology. 13 (1), 83-117 (1997).
- Allen, C., Borisy, G. G. Structural polarity and directional growth of microtubules of Chlamydomonas flagella. Journal of Molecular Biology. 90 (2), 381-402 (1974).
- Stepanova, T., et al. Visualization of microtubule growth in cultured neurons via the use of EB3-GFP (end-binding protein 3-green fluorescent protein). Journal of Neuroscience. 23 (7), 2655-2664 (2003).
- Shelden, E., Wadsworth, P. Observation and quantification of individual microtubule behavior in vivo: microtubule dynamics are cell-type specific. Journal of Cell Biology. 120 (4), 935-945 (1993).
- O’Brien, E. T., Salmon, E. D., Walker, R. A., Erickson, H. P. Effects of magnesium on the dynamic instability of individual microtubules. Biochimica. 29 (28), 6648-6656 (1990).
- Drechsel, D. N., Hyman, A. A., Cobb, M. H., Kirschner, M. W. Modulation of the dynamic instability of tubulin assembly by the microtubule-associated protein tau. Molecular Biology of the Cell. 3 (10), 1141-1154 (1992).
- Gildersleeve, R. F., Cross, A. R., Cullen, K. E., Fagen, A. P., Williams, R. C. Microtubules grow and shorten at intrinsically variable rates. Journal of Biological Chemistry. 267 (12), 7995-8006 (1992).
- Penazzi, L., Bakota, L., Brandt, R. Microtubule dynamics in neuronal development, plasticity, and neurodegeneration. International Review of Cell and Molecular Biology. 321, 89-169 (2016).
- van de Willige, D., Hoogenraad, C. C., Akhmanova, A. Microtubule plus-end tracking proteins in neuronal development. Cellular and Molecular Life Sciences. 73 (10), 2053-2077 (2016).
- Applegate, K. T., et al. plusTipTracker: Quantitative image analysis software for the measurement of microtubule dynamics. Journal of Structural Biology. 176 (2), 168-184 (2011).
- Komarova, Y. A., Vorobjev, I. A., Borisy, G. G. Life cycle of MTs: persistent growth in the cell interior, asymmetric transition frequencies and effects of the cell boundary. Journal of Cell Science. 115 (17), 3527-3539 (2002).
- Nahidiazar, L., Agronskaia, A. V., Broertjes, J., vanden Broek, B., Jalink, K. Optimizing imaging conditions for demanding multi-color super resolution localization microscopy. PLoS One. 11 (7), 0158884 (2016).
- Dixit, R., Cyr, R. Cell damage and reactive oxygen species production induced by fluorescence microscopy: effect on mitosis and guidelines for non-invasive fluorescence microscopy. The Plant Journal. 36 (2), 280-290 (2003).
- Grzelak, A., Rychlik, B., Bartosz, G. Light-dependent generation of reactive oxygen species in cell culture media. Free Radical Biology and Medicine. 30 (12), 1418-1425 (2001).

