Microtubule Plus-End Dynamics Visualisering i Huntingtons sykdomsmodell basert på humane primære hudfibroblaster
Summary
Denne protokollen er dedikert til mikrotubule plus-end visualisering av EB3 proteintransfeksjon for å studere deres dynamiske egenskaper i primærcellekulturen. Protokollen ble implementert på humane primære hudfibroblaster hentet fra pasienter med Huntington sykdom.
Abstract
Transfeksjon med et fluorescerende merket markørprotein av interesse i kombinasjon med tidsforløp videomikroskopi er en klassisk metode for å studere de dynamiske egenskapene til cytoskjelettet. Denne protokollen tilbyr en teknikk for menneskelig primær fibroblasttransfeksjon, noe som kan være vanskelig på grunn av spesifikasjonene til primære cellekultiveringsforhold. I tillegg krever cytoskeleton dynamisk egenskapsvedlikehold et lavt nivå av transfeksjon for å oppnå et godt signal-til-støy-forhold uten å forårsake mikrotubul stabilisering. Det er viktig å ta tiltak for å beskytte cellene mot lysindusert stress og fluorescerende fargestofffading. I løpet av vårt arbeid testet vi forskjellige transfeksjonsmetoder og protokoller, samt forskjellige vektorer for å velge den beste kombinasjonen av forhold som passer for menneskelige primære fibroblaststudier. Vi analyserte de resulterende intervallvideoene og beregnet mikrotubuldynamikk ved hjelp av ImageJ. Dynamikken i mikrotubulenes pluss-ender i de forskjellige celledelene er ikke like, så vi delte analysen i undergrupper – sentrosomområdet, lamellen og halen av fibroblaster. Spesielt kan denne protokollen brukes til in vitro-analyse av cytoskjelettdynamikk i pasientprøver, noe som muliggjør neste skritt mot å forstå dynamikken i de ulike sykdomsutviklingene.
Introduction
Huntingtons sykdom (HS) er en uhelbredelig nevrodegenerativ patologi forårsaket av et mutasjonsgenkodinghuntingtinprotein (HTT). HTT er primært forbundet med vesicles og mikrotubuler og er sannsynligvis involvert i mikrotubuleavhengige transportprosesser1,2. For å studere påvirkning av mutant HTT på mikrotubuldynamikken brukte vi in vitro-visualisering av EB3-proteinet, som regulerer mikrotubulens dynamiske egenskaper ved å binde og stabilisere de voksende pluss endene. For å laste fluorescerende merket EB3 inn i humane hudfibroblaster, ble plasmidtransfeksjon påført. Vi brukte den primære fibroblastkulturen hentet fra HS-pasientenes hudbiopsi for denne studien.
Mutasjonen i HTT-proteingenet fører til forlengelse av polyglutaminkanalen3. HTT har en rolle i slike cellulære prosesser som endokytose4, celletransport1,2, proteinforringelse5, etc. En betydelig del av disse prosessene involverer ulike elementer i cellecytoskjelettet, inkludert mikrotubulene.
Menneskelige primærceller er den beste modellen for å reprodusere hendelser som forekommer i pasientceller så nært som mulig. For å lage slike modeller må man isolere celler fra humant biopsimateriale (f.eks. fra kirurgiske prøver). Den resulterende primære cellelinjen er egnet til å studere patogenese ved hjelp av ulike genetiske, biokjemiske, molekylære og cellebiologiske metoder. Også menneskelige primære cellekulturer tjener som en forløper for å skape ulike transdifferensierte og transgene kulturer6.
Men i motsetning til udødelige cellekulturer er den betydelige ulempen ved primærceller deres begrensede passasjekapasitet. Derfor anbefaler vi å bruke celler i de tidlige passasjene (opptil 15). Eldre kulturer degener veldig raskt og mister sine unike egenskaper. Dermed bør de nylig oppnådde primærcellene holdes frosset for langsiktig lagring.
Primærcellekulturer er utsatt for dyrkingsforhold. Derfor krever de ofte unike tilnærminger og optimalisering av vekstforhold. Spesielt krever den menneskelige huden primære fibroblaster som brukes i våre eksperimenter på substratet. Derfor brukte vi forskjellige ekstra belegg (f.eks. gelatin eller fibronectin) avhengig av eksperimenttypen.
Cellecytoskjelettet bestemmer celleformen, mobiliteten og bevegelse. Dynamikken i cytoskjelettet er avgjørende for mange intracellulære prosesser både i interfase og mitose. Spesielt er cytoskjelettpolymerert fra tubulin svært dynamiske og polare strukturer, noe som muliggjør motorproteinmediert rettet intracellulær transport. Mikrotubulenes ender er i konstant omorganisering, monteringsfasene veksler med demonteringsfasene, og denne virkemåten kalles “dynamisk ustabilitet”7,8,9. Ulike tilknyttede proteiner skifter likevekten av polymerisasjonsreaksjonen, noe som fører enten til polymerformasjonen eller proteinmonomerformasjonen. Tilsetningen av tubulinunderenheter skjer hovedsakelig i pluss-enden av mikrotubuler10. End-bindende (EB) proteinfamilien består av tre medlemmer: EB1, EB2 og EB3. De tjener som plus-end-tracking proteiner (+TIPs) og regulerer de dynamiske egenskapene til mikrotubuler ved å binde og stabilisere deres voksende pluss-ender11.
Mange studier bruker fluorescerende molekyl-merket tubulin mikroinjeksjon eller transfeksjon med tidsforløp avbildning og videoanalyse for å visualisere mikrotubuler in vitro. Disse metodene kan være invasive og skadelige for celler, spesielt primære menneskelige celler. Det mest utfordrende trinnet er å finne forhold for celletransfeksjon. Vi prøvde å nå høyest mulig nivå av transfeksjon uten å påvirke levedyktighet og innfødt cellemorfologi. Denne studien bruker den klassiske metoden for å studere forskjellene i mikrotubuldynamikk i hudfibroblaster av friske donorer og pasienter med Huntingtons sykdom.
Protocol
Representative Results
Discussion
Bedre kvalitetsresultater for mikrotubules dynamikkanalyse kan fås fra mikroskopiske bilder av høy kvalitet. Det er viktig å observere alle nødvendige forhold for tidsforløpavbildning av levende celler og for å justere bildeparametrene riktig. Bruk av spesielle cellekulturretter med glassbunn (konfokale retter) er viktig, siden glass har en annen brytningsindeks av lys enn plast. Tykkelsen på glasset og dets ensartethet over hele området er også ekstremt viktig, siden disse parametrene er avgjørende for normal …
Divulgazioni
The authors have nothing to disclose.
Acknowledgements
Denne forskningen ble finansiert av Departementet for vitenskap og høyere utdanning i Russland, gi No. 075-15-2019-1669 (transfeksjon av fibroblaster), av Den russiske vitenskapsstiftelsen, gi Nr. 19-15-00425 (alle andre arbeider om dyrking av fibroblaster in vitro). Det ble delvis støttet av Lomonosov Moscow State University Development program PNR5.13 (avbildning og analyse). Forfatterne anerkjenner støtten fra Nikon Center of Excellence ved A. N. Belozersky Institute of Physico-Chemical Biology. Vi ønsker å tilby vår spesielle takk til Ekaterina Taran for hennes hjelp med stemmeskuespill. Forfatterne takker også Pavel Belikov for hans hjelp med videoredigering. Figurer i manuskriptet ble laget med BioRender.com.
Materials
| Instrumentation | |||
| Camera iXon DU897 EMCCD | Andor Technology | ||
| Eppendorf Centrifuge 5804 R | Eppendorf Corporate | ||
| Fluorescence filter set HYQ FITC | Nikon | Alternative: Leica, Olympus, Zeiss | |
| LUNA-II Automated Cell Counte | Logos Biosystems | L40002 | |
| Microscope incubator for lifetime filming | Okolab | Temperature controller H301-T-UNIT-BL-PLUS | |
| Gas controller CO2-O2-UNIT-BL | |||
| Objective lens CFI Plan Apo Lambda 60x Oil 1.4 (WD 0.13) | Nikon | Alternative: Leica, Olympus, Zeiss | |
| Widefield fluorescence light microscope Eclipse Ti-E | Nikon | Alternative: Leica, Olympus, Zeiss | |
| Software | |||
| Fiji (Image J version 2.1.0/1.53c) | Open source image processing software | ||
| NIS Elements | Nikon | Alternative: Leica, Olympus, Zeiss | |
| Additional reagents | |||
| Mineral oil (Light white oil) | MP | 151694 | |
| Cell culture dish | |||
| Cell Culture Dish | SPL Lifesciences | 20035 | |
| Confocal Dish (glass thickness 170 µm) | SPL Lifesciences | 211350 | Alternative: MatTek |
| Conical Centrifuge tube | SPL Lifesciences | 50015 | |
| Cryogenic Vials | Corning-Costar | 430659 | |
| Microcentrifuge Tube | Nest | 615001 | |
| Cultivation | |||
| Lipofectamine 3000 Transfection Reagent | Thermo Fisher Scientific | L3000001 | |
| Dimethyl sulfoxide | PanEko | 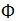 135 135 |
|
| DMEM (Dulbecco's Modified Eagle Media) | PanEko | C420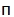 |
|
| DPBS (Dulbecco's phosphate-salt solution) | PanEko | P060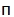 |
|
| Fetal bovine serum (FBS) | Hyclone | K053/SH30071.03 | |
| Gelatin (bovine skin) | PanEko | 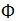 070 070 |
|
| GlutaMAX | Thermo Fisher Scientific | 35050038 | |
| Opti-MEM (1x) + Glutamax | Gibco | 519850026 | |
| Penicillin-streptomycin | PanEko | A063 |
|
| Trypsin-EDTA (0.25%) | Thermo Fisher Scientific | 25200072 | |
| Transfection | |||
| Plasmid DNA with EB3-GFP | Kind gift of Dr. I. Kaverina [Vanderbilt University, Nashville] with permission from Dr. A. Akhmanova [Erasmus University, Rotterdam] |
Stepanova et al., 2003 DOI: 10.1523/JNEUROSCI.23-07-02655.2003 |
Riferimenti
- Engelender, S., et al. Huntingtin-associated Protein 1 (HAP1) Interacts with the p150 Glued Bubunit of Dynactin. Human Molecular Genetics. 6 (13), 2205-2212 (1997).
- Caviston, J. P., Ross, J. L., Antony, S. M., Tokito, M., Holzbaur, E. L. Huntingtin facilitates dynein/dynactin-mediated vesicle transport. Proceedings of the National Academy of Sciences. 104 (24), 10045-10050 (2007).
- MacMillan, J. C., et al. Molecular analysis and clinical correlations of the Huntington’s disease mutation. The Lancet. 342 (8877), 954-958 (1993).
- Proskura, A. L., Vechkapova, S. O., Zapara, T. A., Ratushniak, A. S. Protein-protein interactions of huntingtin in the hippocampus. Biologia Molecolare. 51 (4), 647-653 (2017).
- Steffan, J. S., et al. The Huntington’s disease protein interacts with p53 and CREB-binding protein and represses transcription. Proceedings of the National Academy of Sciences. 97 (12), 6763-6768 (2000).
- Nekrasov, E. D., et al. Manifestation of Huntington’s disease pathology in human induced pluripotent stem cell-derived neurons. Molecular Neurodegeneration. 11 (1), 1-15 (2016).
- Mitchison, T., Kirschner, M. Dynamic instability of microtubule growth. Nature. 312 (5991), 237-242 (1984).
- Walker, R. A., et al. Dynamic instability of individual microtubules analyzed by video light microscopy: rate constants and transition frequencies. The Journal of Cell Biology. 107 (4), 1437-1448 (1988).
- Desai, A., Mitchison, T. J. Microtubule polymerization dynamics. Annual Review of Cell and Developmental Biology. 13 (1), 83-117 (1997).
- Allen, C., Borisy, G. G. Structural polarity and directional growth of microtubules of Chlamydomonas flagella. Journal of Molecular Biology. 90 (2), 381-402 (1974).
- Stepanova, T., et al. Visualization of microtubule growth in cultured neurons via the use of EB3-GFP (end-binding protein 3-green fluorescent protein). Journal of Neuroscience. 23 (7), 2655-2664 (2003).
- Shelden, E., Wadsworth, P. Observation and quantification of individual microtubule behavior in vivo: microtubule dynamics are cell-type specific. Journal of Cell Biology. 120 (4), 935-945 (1993).
- O’Brien, E. T., Salmon, E. D., Walker, R. A., Erickson, H. P. Effects of magnesium on the dynamic instability of individual microtubules. Biochimica. 29 (28), 6648-6656 (1990).
- Drechsel, D. N., Hyman, A. A., Cobb, M. H., Kirschner, M. W. Modulation of the dynamic instability of tubulin assembly by the microtubule-associated protein tau. Molecular Biology of the Cell. 3 (10), 1141-1154 (1992).
- Gildersleeve, R. F., Cross, A. R., Cullen, K. E., Fagen, A. P., Williams, R. C. Microtubules grow and shorten at intrinsically variable rates. Journal of Biological Chemistry. 267 (12), 7995-8006 (1992).
- Penazzi, L., Bakota, L., Brandt, R. Microtubule dynamics in neuronal development, plasticity, and neurodegeneration. International Review of Cell and Molecular Biology. 321, 89-169 (2016).
- van de Willige, D., Hoogenraad, C. C., Akhmanova, A. Microtubule plus-end tracking proteins in neuronal development. Cellular and Molecular Life Sciences. 73 (10), 2053-2077 (2016).
- Applegate, K. T., et al. plusTipTracker: Quantitative image analysis software for the measurement of microtubule dynamics. Journal of Structural Biology. 176 (2), 168-184 (2011).
- Komarova, Y. A., Vorobjev, I. A., Borisy, G. G. Life cycle of MTs: persistent growth in the cell interior, asymmetric transition frequencies and effects of the cell boundary. Journal of Cell Science. 115 (17), 3527-3539 (2002).
- Nahidiazar, L., Agronskaia, A. V., Broertjes, J., vanden Broek, B., Jalink, K. Optimizing imaging conditions for demanding multi-color super resolution localization microscopy. PLoS One. 11 (7), 0158884 (2016).
- Dixit, R., Cyr, R. Cell damage and reactive oxygen species production induced by fluorescence microscopy: effect on mitosis and guidelines for non-invasive fluorescence microscopy. The Plant Journal. 36 (2), 280-290 (2003).
- Grzelak, A., Rychlik, B., Bartosz, G. Light-dependent generation of reactive oxygen species in cell culture media. Free Radical Biology and Medicine. 30 (12), 1418-1425 (2001).

