Recopilación, expansión y diferenciación de modelos primarios de células epiteliales nasales humanas para la cuantificación de la frecuencia de latido de los cilios
Summary
Este protocolo describe la recolección, expansión y diferenciación de células epiteliales nasales a modelos organotípicos de células epiteliales de las vías respiratorias y la cuantificación de la frecuencia de latidos de los cilios a través de imágenes de células vivas y guiones personalizados.
Abstract
Las mediciones de la función de los cilios (frecuencia de latido, patrón) se han establecido como herramientas de diagnóstico para enfermedades respiratorias como la discinesia ciliar primaria. Sin embargo, la aplicación más amplia de estas técnicas está limitada por la extrema susceptibilidad de la función ciliar a los cambios en los factores ambientales, por ejemplo, temperatura, humedad y pH. En las vías respiratorias de los pacientes con fibrosis quística (FQ), la acumulación de moco impide el latido de los cilios. La función de los cilios se ha investigado en modelos de células primarias de las vías respiratorias como un indicador de la actividad del canal CF Transmembrane conductance Regulator (CFTR). Sin embargo, se ha encontrado una considerable variabilidad de paciente a paciente en la frecuencia de latidos de los cilios en respuesta a los fármacos moduladores de CFTR, incluso para pacientes con las mismas mutaciones de CFTR . Además, el impacto de la secreción disfuncional de cloruro regulada por CFTR en la función ciliar es poco conocido. Actualmente no existe un protocolo integral que demuestre la preparación de muestras de modelos de vías respiratorias in vitro , la adquisición de imágenes y el análisis de la frecuencia de latido de los cilios (CBF). Las condiciones de cultivo estandarizadas y la adquisición de imágenes realizadas en una condición ambientalmente controlada permitirían una cuantificación consistente y reproducible de CBF entre individuos y en respuesta a fármacos moduladores de CFTR. Este protocolo describe la cuantificación de CBF en tres sistemas diferentes de modelos de células epiteliales de las vías respiratorias: 1) láminas epiteliales nativas, 2) modelos de interfaz aire-líquido fotografiados en insertos de soporte permeables y 3) organoides tridimensionales incrustados en matriz extracelular. Los dos últimos replican la fisiología pulmonar in vivo , con cilios batidos y producción de moco. La función ciliar se captura utilizando una cámara de vídeo de alta velocidad en una cámara controlada por el entorno. Se utilizan scripts personalizados para el análisis de CBF. Se prevé que la traducción de las mediciones de CBF a la clínica sea una herramienta clínica importante para predecir la respuesta a los fármacos moduladores de CFTR por paciente.
Introduction
Las mediciones de la frecuencia de latido de los cilios (CBF) y el patrón se han establecido como herramientas de diagnóstico para enfermedades respiratorias como la discinesia ciliar primaria (PCD)1. En la fibrosis quística (FQ), la disfunción del canal de cloruro del regulador de conductancia transmembrana (CFTR) de la FQ causa deshidratación del líquido de la superficie de las vías respiratorias y alteración del aclaramiento mucociliar2. La función ciliar ha sido investigada in vitro en modelos de células primarias de la vía aérea como indicador de la actividad del canal CFTR3. Sin embargo, existe una considerable variabilidad paciente a paciente en la CBF en respuesta a los fármacos moduladores de CFTR, incluso para pacientes con las mismas mutaciones CFTR 3. Además, el impacto de la secreción disfuncional de cloruro regulada por CFTR en la función ciliar es poco conocido. Actualmente no existe un protocolo integral que demuestre la preparación de muestras de modelos de vías respiratorias in vitro , la adquisición de imágenes y el análisis de CBF.
Las láminas epiteliales nasales aisladas de cepillados de la mucosa nasal se utilizan directamente para la medición de la función ciliar para el diagnóstico de DCP4. Sin embargo, aunque no hay control sobre el tamaño o la calidad de las láminas epiteliales nasales obtenidas, el CBF varía dependiendo de si se mide en células individuales o láminas celulares y en bordes ciliados de láminas epiteliales que están interrumpidas o no interrumpidas5. Como tal, las discinesias secundarias causadas por el daño a las células durante la recolección de cepillados de la mucosa nasal pueden influir en la CBF. El cultivo celular primario de células epiteliales nasales y su diferenciación en la interfaz aire-líquido (LPA) o en la matriz tridimensional de la membrana basal en organoides epiteliales de las vías respiratorias ciliadas dan lugar a cilios libres de discinesias secundarias 4,6,7,8. Las células epiteliales de las vías respiratorias diferenciadas en ALI (en adelante denominadas modelos ALI) se han considerado una importante ayuda diagnóstica secundaria que replica los patrones de latido ciliar y la frecuencia de cepillados ex vivo de la mucosa nasal6 y permite el análisis de la ultraestructura ciliar, el patrón de latido y la frecuencia de latido, al tiempo que conserva defectos específicos del paciente9 . Sin embargo, existen discrepancias en las metodologías utilizadas para crear estos modelos celulares pseudoestratificados y mucociliares diferenciados. Diferentes protocolos de expansión o diferenciación del cultivo podrían inducir distintos fenotipos epiteliales (ciliados o secretores)10 y dar lugar a diferencias significativas en la CBF11. El CBF se ha cuantificado en cepillados epiteliales nasales 4,6,12,13,14,15,16, organoides epiteliales de la vía aérea 14,17,18 y modelos ALI 3,4,6,13,19,20, 21. Sin embargo, entre estos protocolos, existen grandes variabilidades, y a menudo muchos parámetros no están controlados. Por ejemplo, en algunos estudios, CBF se visualiza in situ mientras que las células del modelo ALI permanecen en el inserto de soporte permeable 3,19,20,21, y otros raspan las células del inserto de soporte permeable y las visualizan suspendidas en medios 4,6,13.
Además, la aplicación más amplia de técnicas que miden la función ciliar está limitada por la extrema susceptibilidad de la función ciliar a los cambios en los factores ambientales. Los factores ambientales como la temperatura 22, la humedad 23,24 y el pH 25,26 influyen en la función ciliar y deben regularse para cuantificar el CBF con precisión. Los diversos parámetros fisiológicos utilizados en diferentes laboratorios y cómo influyen en la CBF han sido revisados previamente27.
En la literatura se informan diversas tecnologías de imagen y enfoques para las mediciones de CBF. Para el diagnóstico de PCD, la microscopía de video se utiliza para medir la función ciliar28,29. Recientemente, se utilizó un algoritmo de análisis de video basado en microscopía dinámica diferencial para cuantificar la coordinación de CBF y cilios en modelos ALI de células epiteliales de las vías respiratorias 3,30. Este método permite caracterizar el latido ciliar en células epiteliales de la vía aérea de forma rápida y totalmente automatizada, sin necesidad de segmentar o seleccionar regiones. Varios métodos para la obtención de imágenes y la cuantificación del CBF pueden aumentar las diferencias reportadas en CBF en la literatura (Archivo complementario 1).
Un protocolo desde el cultivo hasta la cuantificación para racionalizar los métodos existentes, la estandarización de las condiciones de cultivo y la adquisición de imágenes, realizada en condiciones estrictamente controladas ambientalmente, permitiría una cuantificación consistente y reproducible de CBF dentro y entre individuos.
Este protocolo proporciona una descripción completa de la colección de células epiteliales, las condiciones de cultivo de expansión y diferenciación, y la cuantificación de CBF en tres sistemas diferentes de modelos de células epiteliales de las vías respiratorias de origen nasal: 1) láminas epiteliales nativas, 2) modelos ALI fotografiados en insertos de soporte permeables y 3) organoides tridimensionales incrustados en matriz extracelular (ECM) (Figura 1 ). Las células epiteliales nasales obtenidas de cepillados de cornetes nasales inferiores se utilizan como representantes del epitelio de la vía aérea, ya que son un sustituto eficaz de las células epiteliales bronquiales31 superando el procedimiento invasivo asociado a la recolección de cepillados bronquiales. El método de la célula de reprogramación condicional (CRC) se utiliza para expandir las células epiteliales primarias de las vías respiratorias para la creación de modelos ALI y organoides tridimensionales. La reprogramación condicional de las células epiteliales de las vías respiratorias a un estado similar al de las células madre es inducida por el cocultivo con el sistema de células alimentadoras de fibroblastos con detención del crecimiento y el inhibidor de la quinasa asociada a Rho (ROCK)32. Es importante destacar que el método del CCR aumenta la duplicación de la población en las células epiteliales de las vías respiratorias, al tiempo que conserva su potencial de diferenciación tisular específico33,34. En todos los modelos de células epiteliales de las vías respiratorias, la función ciliar se captura en una cámara de temperatura controlada utilizando una cámara de video de alta velocidad con ajustes estandarizados de adquisición de imágenes. Se emplean scripts personalizados para la cuantificación de CBF.
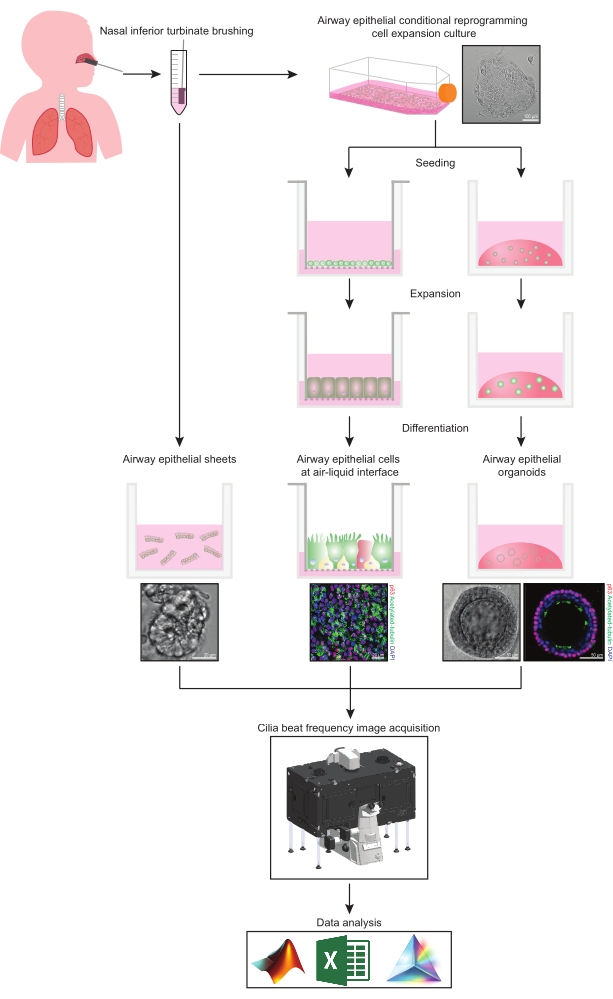
Figura 1: Esquema del flujo de trabajo. Después de cepillar el cornete nasal inferior de los participantes, las células epiteliales de las vías respiratorias se utilizan de una de dos maneras. O bien se aíslan las láminas epiteliales de las vías respiratorias y se obtiene una imagen inmediata de la frecuencia de latido de los cilios, o bien las células epiteliales de las vías respiratorias se expanden mediante el método de reprogramación condicional de las células. Las células epiteliales de las vías respiratorias expandidas por CCR se diferencian para establecer células epiteliales de las vías respiratorias en una interfaz aire-líquido o cultivos de organoides epiteliales de las vías respiratorias. Las imágenes de la frecuencia de latido ciliar se adquieren utilizando un microscopio de imagen de células vivas con una cámara ambiental de calentamiento y humedad y una cámara científica de velocidad de cuadro rápida (>100Hz). El análisis de datos se realiza utilizando scripts personalizados. Haga clic aquí para ver una versión más grande de esta figura.
Protocol
Representative Results
Discussion
Existen múltiples factores que podrían oscurecer la cuantificación de CBF en láminas epiteliales nasales. Las hojas epiteliales deben ser fotografiadas dentro de las 3-9 horas de la recolección de la muestra, ya que la función ciliar es más estable durante este tiempo37. Menos glóbulos rojos y desechos son los más óptimos para obtener imágenes, ya que interfieren con la adquisición de datos. Al seleccionar un ROI para la obtención de imágenes, es importante seleccionar una hoja epite…
Divulgazioni
The authors have nothing to disclose.
Acknowledgements
Agradecemos a los participantes del estudio y sus familias por sus contribuciones. Agradecemos la asistencia del departamento respiratorio de Randwick de Sydney Children’s Hospitals (SCH) en la organización y recolección de muestras biológicas de pacientes, un agradecimiento especial al Dr. John Widger, la Dra. Yvonne Belessis, Leanne Plush, Amanda Thompson y Rhonda Bell. Reconocemos la asistencia de Iveta Slapetova y Renee Whan del Centro de Microscopía de Luz Katharina Gaus dentro del Centro Analítico Mark Wainwright en UNSW Sydney. Este trabajo cuenta con el apoyo del Consejo Nacional de Salud e Investigación Médica (NHMRC) Australia (GNT1188987), CF Foundation Australia y Sydney Children’s Hospital Foundation. Los autores desean agradecer a Luminesce Alliance – Innovation for Children’s Health por su contribución y apoyo. Luminesce Alliance – Innovation for Children’s Health es una empresa conjunta cooperativa sin fines de lucro entre la Red de Hospitales Infantiles de Sídney, el Instituto de Investigación Médica Infantil y el Instituto de Cáncer Infantil. Se ha establecido con el apoyo del Gobierno de Nueva Gales del Sur para coordinar e integrar la investigación pediátrica. Luminesce Alliance también está afiliada a la Universidad de Sydney y la Universidad de Nueva Gales del Sur Sydney. KMA cuenta con el apoyo de una beca del Programa de Capacitación en Investigación del Gobierno de Australia. LKF cuenta con el apoyo del Club Rotario de Sydney Cove/Sydney Children’s Hospital Foundation y becas de posgrado de la Universidad UNSW.
Materials
| Adenine | Sigma-Aldrich | A2786 | 10 mg/mL |
| Advanced DMEM/F-12 | Thermo Fisher Scientific | 12634-010 | |
| Alanyl-glutamine | Sigma-Aldrich | G8541 | 200 mM |
| Andor Zyla 4.2 sCMOS | Oxford Instruments | Fast frame rate (>100 Hz) scientific camera | |
| Bottle-top vacuum filter system | Sigma-Aldrich | CLS431098 | |
| Ceftazidime hydrate | Sigma-Aldrich | A6987 | 50 mg/mL |
| Cell Culture Microscope | Olympus | CKX53 | |
| CFI S Plan Fluor ELWD 20XC | Nikon Instruments Inc. | MRH08230 | Long working distance objective lens. NA0.45 WD 8.2-6.9 |
| Cholera toxin | Sigma-Aldrich | C8052-1MG | 200 µg/mL |
| Corning Gel Strainer 40 UM | Sigma-Aldrich | CLS431750 | Pore size 40 μm |
| Corning Matrigel Matrix (Phenol red-free) | Corning | 356231 | Extracellular matrix (ECM) |
| Corning bottle-top vacuum filter system | Sigma-Aldrich | CLS431098 | |
| Corning CoolCell LX Cell Freezing Container | Sigma-Aldrich | CLS432002 | |
| Corning Transwell polyester membrane cell culture inserts | Sigma-Aldrich | CLS3470 | Permeable support inserts. 6.5 mm Transwell with 0.4 μm pore polyester membrane insert. |
| Countess Cell Counting Chamber Slides | Thermo Fisher Scientific | C10228 | |
| Countess II Automated Cell Counter | ThermoFisher Scientific | AMQAX1000 | Automated cell counter |
| Cytology brushes | McFarlane Medical | 33009 | |
| DMEM/F12-Ham | Thermo Fisher Scientific | 11330032 | |
| DMEM/F12-Ham | Thermo Fisher Scientific | 11330032 | |
| DMEM-High Glucose | Thermo Fisher Scientific | 11965-092 | |
| Dulbecco′s Phosphate Buffered Saline (PBS) | Sigma-Aldrich | D8537 | |
| Eclipse Ti2-E | Nikon | Live-cell imaging microscope. | |
| Fetal Bovine Serum, certified, heat inactivated, United States | Thermo Fisher Scientific | 10082147 | |
| Fungizone (Amphotericin B) | Thermo Fisher Scientific | 15290018 | 250 µg/mL |
| Gentamicin solution | Sigma-Aldrich | G1397 | 50 mg/mL |
| Graphpad Prism | Graphpad | Scientific analysis software | |
| Greiner Cryo.s vials | Sigma-Aldrich | V3135 | Cryogenic vials |
| HEPES solution | Sigma-Aldrich | H0887 | 1 M |
| HI-FBS | Thermo Fisher Scientific | 10082-147 | |
| Hydrocortisone | Sigma-Aldrich | H0888 | 3.6 mg/mL |
| Incubator NL Ti2 BLACK 2000 | PeCon | Microscope environmental chamber. Allows warm air incubation and local CO2 and O2 gassing | |
| Insulin | Sigma-Aldrich | I2643 | 2 mg/mL |
| Lab Armor 74220 706 Waterless Bead Bath 6L | John Morris Group | 74220 706 | Bead bath |
| Lab Armor Beads | Thermo Fisher Scientific | A1254302 | Thermal beads |
| MATLAB | MathWorks | Computing software | |
| Microsoft Excel | Microscoft | Spreadsheet software | |
| NIH/3T3 | American Type Culture Collection | CRL-1658 | Irradiated NIH-3T3 mouse embryonic feeder cells |
| NIS-Elements AR | Nikon Instruments Inc. | Image acquisition software | |
| Penicillin-Streptomycin | Sigma-Aldrich | P4333 | 10,000 units penicillin and 10 mg streptomycin/mL |
| Dulbecco′s Phosphate Buffered Saline (PBS) | Sigma-Aldrich | D8537 | |
| PneumaCult Airway Organoid Kit | StemCell Technologies | 5060 | Airway Organoid Kit |
| PneumaCult-ALI Medium | StemCell Technologies | 5001 | |
| PneumaCult-Ex Plus Medium | StemCell Technologies | 5040 | |
| PureCol-S | Advanced BioMatrix | 5015 | Type I Collagen solution |
| ReagentPack Subculture Reagents | Lonza | CC-5034 | |
| rhEGF (Epidermal Growth Factor, human) | Sigma-Aldrich | E9644 | 25 µg/mL |
| Y-27632 2HCl (ROCK inhibitor) | Selleckchem | S1049 | 10 mM |
| Tobramycin | Sigma-Aldrich | T4014 | 100 mg/mL |
| Trypan blue solution | Sigma-Aldrich | T8154 | 0.4% |
| UNO Stage Top Incubator | Okolab | Microscope incubator. Allows temperature, humidity and CO2 conditioning |
Riferimenti
- Barbato, A., et al. Primary ciliary dyskinesia: a consensus statement on diagnostic and treatment approaches in children. European Respiratory Journal. 34 (6), 1264-1276 (2009).
- Cutting, G. R. Cystic fibrosis genetics: from molecular understanding to clinical application. Nature Reviews Genetics. 16 (1), 45-56 (2015).
- Chioccioli, M., Feriani, L., Kotar, J., Bratcher, P. E., Cicuta, P. Phenotyping ciliary dynamics and coordination in response to CFTR-modulators in Cystic Fibrosis respiratory epithelial cells. Nature Communications. 10 (1), 1763 (2019).
- Hirst, R. A., Rutman, A., Williams, G., O’Callaghan, C. Ciliated air-liquid cultures as an aid to diagnostic testing of primary ciliary dyskinesia. Chest. 138 (6), 1441-1447 (2010).
- Thomas, B., Rutman, A., O’Callaghan, C. Disrupted ciliated epithelium shows slower ciliary beat frequency and increased dyskinesia. European Respiratory Journal. 34 (2), 401-404 (2009).
- Coles, J. L., et al. A revised protocol for culture of airway epithelial cells as a diagnostic tool for primary ciliary dyskinesia. Journal of Clinical Medicine. 9 (11), (2020).
- Pifferi, M., et al. Simplified cell culture method for the diagnosis of atypical primary ciliary dyskinesia. Thorax. 64 (12), 1077-1081 (2009).
- Pifferi, M., et al. Rapid diagnosis of primary ciliary dyskinesia: cell culture and soft computing analysis. European Respiratory Journal. 41 (4), 960-965 (2013).
- Lee, D. D. H., et al. Higher throughput drug screening for rare respiratory diseases: Readthrough therapy in primary ciliary dyskinesia. European Respiratory Journal. 58 (4), 2000455 (2021).
- Saint-Criq, V., et al. Choice of differentiation media significantly impacts cell lineage and response to CFTR modulators in fully differentiated primary cultures of cystic fibrosis human airway epithelial cells. Cells. 9 (9), (2020).
- Awatade, N. T., et al. Significant functional differences in differentiated Conditionally Reprogrammed (CRC)- and Feeder-free Dual SMAD inhibited-expanded human nasal epithelial cells. Journal of Cystic Fibrosis. 20 (2), 364-371 (2021).
- Dabrowski, M., Bukowy-Bieryllo, Z., Jackson, C. L., Zietkiewicz, E. Properties of non-aminoglycoside compounds used to stimulate translational readthrough of PTC mutations in primary ciliary dyskinesia. International Journal of Molecular Sciences. 22 (9), (2021).
- Hirst, R. A., et al. Culture of primary ciliary dyskinesia epithelial cells at air-liquid interface can alter ciliary phenotype but remains a robust and informative diagnostic aid. PloS One. 9 (2), 89675 (2014).
- Marthin, J. K., Stevens, E. M., Larsen, L. A., Christensen, S. T., Nielsen, K. G. Patient-specific three-dimensional explant spheroids derived from human nasal airway epithelium: a simple methodological approach for ex vivo studies of primary ciliary dyskinesia. Cilia. 6, 3 (2017).
- Chilvers, M. A., O’Callaghan, C. Analysis of ciliary beat pattern and beat frequency using digital high speed imaging: comparison with the photomultiplier and photodiode methods. Thorax. 55 (4), 314-317 (2000).
- Chilvers, M. A., Rutman, A., O’Callaghan, C. Functional analysis of cilia and ciliated epithelial ultrastructure in healthy children and young adults. Thorax. 58 (4), 333-338 (2003).
- Castillon, N., et al. Polarized expression of cystic fibrosis transmembrane conductance regulator and associated epithelial proteins during the regeneration of human airway surface epithelium in three-dimensional culture. Laboratory Investigation. 82 (8), 989-998 (2002).
- Jorissen, M., Bessems, A. Normal ciliary beat frequency after ciliogenesis in nasal epithelial cells cultured sequentially as monolayer and in suspension. Acta Oto-Laryngologica. 115 (1), 66-70 (1995).
- Conger, B. T., et al. Comparison of cystic fibrosis transmembrane conductance regulator (CFTR) and ciliary beat frequency activation by the CFTR Modulators Genistein, VRT-532, and UCCF-152 in primary sinonasal epithelial cultures. JAMA Otolaryngology-Head & Neck Surgery. 139 (8), 822-827 (2013).
- Pique, N., De Servi, B. Rhinosectan((R)) spray (containing xyloglucan) on the ciliary function of the nasal respiratory epithelium; results of an in vitro study. Allergy, Asthma & Clinical Immunology. 14, 41 (2018).
- Chen, Q., et al. Host antiviral response suppresses ciliogenesis and motile ciliary functions in the nasal epithelium. Frontiers in Cell and Developmental Biology. 8, 581340 (2020).
- Clary-Meinesz, C. F., Cosson, J., Huitorel, P., Blaive, B. Temperature effect on the ciliary beat frequency of human nasal and tracheal ciliated cells. Biology of the Cell. 76 (3), 335-338 (1992).
- Ballenger, J. J., Orr, M. F. Quantitative measurement of human ciliary activity. Annals of Otology, Rhinology and Laryngology. 72, 31-39 (1963).
- Mercke, U. The influence of varying air humidity on mucociliary activity. Acta Oto-Laryngologica. 79 (1-2), 133-139 (1975).
- Sutto, Z., Conner, G. E., Salathe, M. Regulation of human airway ciliary beat frequency by intracellular pH. Journal of Physiology. 560, 519-532 (2004).
- Salathe, M. Regulation of mammalian ciliary beating. Annual Review of Physiology. 69, 401-422 (2007).
- Kempeneers, C., Seaton, C., Garcia Espinosa, B., Chilvers, M. A. Ciliary functional analysis: Beating a path towards standardization. Pediatric Pulmonology. 54 (10), 1627-1638 (2019).
- Kempeneers, C., Seaton, C., Chilvers, M. A. Variation of ciliary beat pattern in three different beating planes in healthy subjects. Chest. 151 (5), 993-1001 (2017).
- Jackson, C. L., et al. Accuracy of diagnostic testing in primary ciliary dyskinesia. European Respiratory Journal. 47 (3), 837-848 (2016).
- Feriani, L., et al. Assessing the collective dynamics of motile cilia in cultures of human airway cells by multiscale DDM. Biophysical Journal. 113 (1), 109-119 (2017).
- Brewington, J. J., et al. Brushed nasal epithelial cells are a surrogate for bronchial epithelial CFTR studies. JCI Insight. 3 (13), (2018).
- Liu, X., et al. ROCK inhibitor and feeder cells induce the conditional reprogramming of epithelial cells. The American Journal of Pathology. 180 (2), 599-607 (2012).
- Suprynowicz, F. A., et al. Conditionally reprogrammed cells represent a stem-like state of adult epithelial cells. Proceedings of the National Academy of Sciences of the United States of America. 109 (49), 20035-20040 (2012).
- Martinovich, K. M., et al. Conditionally reprogrammed primary airway epithelial cells maintain morphology, lineage and disease specific functional characteristics. Scientific Reports. 7 (1), 17971 (2017).
- Wong, J. Y., Rutman, A., O’Callaghan, C. Recovery of the ciliated epithelium following acute bronchiolitis in infancy. Thorax. 60 (7), 582-587 (2005).
- Gentzsch, M., et al. Pharmacological rescue of conditionally reprogrammed cystic fibrosis bronchial epithelial cells. American Journal of Respiratory Cell and Molecular Biology. 56 (5), 568-574 (2017).
- Sommer, J. U., Gross, S., Hormann, K., Stuck, B. A. Time-dependent changes in nasal ciliary beat frequency. European Archives of Oto-Rhino-Laryngology. 267 (9), 1383-1387 (2010).
- Ratjen, F., et al. Cystic fibrosis. Nature Reviews Disease Primers. 1, 15010 (2015).
- Delmotte, P., Sanderson, M. J. Ciliary beat frequency is maintained at a maximal rate in the small airways of mouse lung slices. American Journal of Respiratory Cell and Molecular Biology. 35 (1), 110-117 (2006).
- Smith, C. M., et al. Cooling of cilia allows functional analysis of the beat pattern for diagnostic testing. Chest. 140 (1), 186-190 (2011).
- Raidt, J., et al. Ciliary beat pattern and frequency in genetic variants of primary ciliary dyskinesia. European Respiratory Journal. 44 (6), 1579-1588 (2014).

