Detektion av neutraliseringskänsliga epitoper i antigener som visas på virusliknande partikelbaserade vacciner (VLP) med hjälp av en capture-analys
Summary
Här presenterar vi ett protokoll för att upptäcka neutralisering epitoper på antigen-displaying virus-liknande partiklar (VLPs). Immunoprecipitation av humant immunbristvirus (HIV)-härledda VLPs utförs med hjälp av kuvert glykoproteiner-specifika monoklonala antikroppar kopplade till protein G-konjugerade magnetiska pärlor. Fångade VLPs utsätts därefter för SDS-PAGE och western blot-analys med viralt kärnprotein Gag-specifika antikroppar.
Abstract
Den virusliknande partikeln (VLP) capture assay är en immunoprecipitationsmetod, allmänt känd som en “pull-down assay” som används för att rena och isolera antigendisplay VLPs. På grund av deras höga affinitet till målantigenet kan dessa antikroppar fånga VLPs dekorerade med cognate antigen förankrade i membran kuvertet av VLPs. Detta protokoll beskriver bindning av antigenspecifika antikroppar till protein A- eller G-konjugerade magnetiska pärlor. I vår studie undersöks humant immunbristvirus (HIV)-härlett VLPs som bildas av det gruppspecifika antigenet (Gag) virala kärnprekursorproteinet p55 Gag och som visar kuvertglykoproteiner (Env) av HIV. VLPs fångas med hjälp av i stort sett neutraliserande antikroppar (bNAbs) riktade mot neutraliseringskänsliga epitoper i Env. Vlp-fångstanalysen som beskrivs här representerar en känslig och lätt att utföra metod för att visa att i) VLPs är dekorerade med respektive målantigen, ii) ytantigenet behöll sin strukturella integritet, vilket framgår av den epitopspecifika bindningen av bNAbs som används i analysen och iii) den strukturella integriteten hos VLPs som avslöjas genom påvisande av Gag proteiner i en efterföljande västerländsk blot-analys. Följaktligen underlättar användningen av bNAbs för immunprecipitation en förutsägelse om VLP-vacciner kommer att kunna framkalla ett neutraliserande B-cellssvar hos vaccinerade människor. Vi förväntar oss att detta protokoll kommer att ge andra forskare ett värdefullt och enkelt experimentellt tillvägagångssätt för att undersöka potentiella VLP-baserade vacciner.
Introduction
Virusliknande partiklar (VLPs) liknar den inhemska viruspartikelstrukturen samtidigt som de saknar det virala genomet, vilket ger en hög säkerhetsprofil1,2. VLP representerar en individuell klass av vacciner som utvecklas alltmer på grund av deras höga immunogenicitet3,4,5,6,7. Detta gäller särskilt membran-hölje VLPs, vilket möjliggör visning av inte bara homologa virala ytan antigener men också heterologous antigener såsom tumör antigener8,9,10. Figur 1 ger en föredömlig översikt över strukturen hos en omsluten antigendekorerad VLP. Under utvecklingsprocessen av VLP-baserade vacciner är analyser oumbärliga för att möjliggöra analys av respektive målantigen som visas på VLP-ytan. Sådana analyser bör vara avgörande för att klargöra sammansättningen av ett partikelvaccin: i) Är VLP dekorerade med respektive ytantigen? ii) Har ytantigenet behållit sin ursprungliga struktur, vilket framgår av epitopigenkänning av neutraliserande antikroppar (bNAbs) och iii) kan VLP:s strukturella integritet bekräftas på grund av påvisande av det virala protein som förmedlar VLP-bildandet?
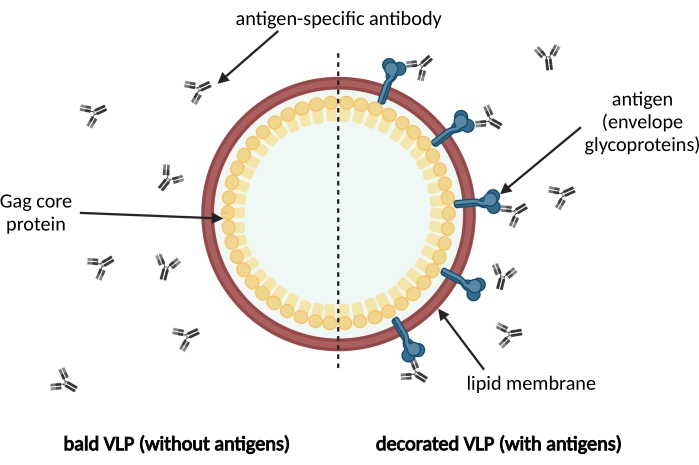
Bild 1: Schematisk illustration av en membransluten VLP. VLPs bildas av omogna prekursor Gag kärnproteiner och omges av ett lipidmembran som härrör från värdcellen. Antigenerna, t.ex. kuvertglykoproteiner, införlivas i lipidmembranet och visas på VLP:s yta (till höger). Antigenspecifika antikroppar känner igen antigenet. Till vänster visas en skallig VLP utan antigendekoration. Klicka här för att se en större version av den här figuren.
Särskilt VLPs bildas av viral gruppspecifik antigen (Gag) core precursor protein p55 av humant immunbristvirus typ 1 (HIV-1) är föredragna byggnadsställningar för antigen display i vaccin utveckling som många antikroppar, och ELISA kit finns tillgängliga, vilket möjliggör kvantifiering av dessa VLPs11,12. Hiv-1-kuvertet glykoproteiner (Env), nämligen transmembranproteinet gp41 (gp41-TM) och den lösliga ytanheten gp120 (gp120-SU) som bildar heterodimerer, införlivas i membranhöljet av partiklar och är viktiga målantigener för utveckling av vacciner mot HIV-infektion13,14,15 . Visning av neutraliseringskänsliga epitoper i dessa målantigener är en förutsättning för att framkalla ett i stort sett neutraliserande antikroppssvar i vacciner. Förutom ett T-cellssvar riktat mot Gag-proteinerna anses detta vara en viktig korrelat av skydd mot HIV-infektion16. Följaktligen, och vid utformning och produktion av VLP dekorerade med målantigenkandidater, utgör den efterföljande analysen av kvaliteten på de visade antigenerna ett kritiskt steg i processen för vaccinutveckling.
Immunoprecipitation (IP) är en allmänt använd teknik för detektion av protein-proteininteraktioner och rening av proteinkomplex i liten skala17. Barret et al. först rapporterades om utvecklingen av immateriella rättigheter 1960, men denna metod har ständigt förbättrats ytterligare. IP möjliggör avskiljning och isolering av ett målantigen (byte) från en lösning genom att använda en antigenspecifik antikropp (bete) immobiliserad genom koppling till pärlor18,19. I detta protokoll visar vi en variation av den klassiska IP-applikationen med membran-enveloped p55 Gag-formade VLPs som byte och bNAbs som känner igen neutraliserande känsliga epitoper i kuvertproteinerna som visas på ytan av VLPs som beteproteiner. Den framgångsrika tillämpningen av denna VLP-fångstanalys underlättar förutsägelsen om huruvida de testade antigenpositiva VLPs kommer att kunna framkalla en neutraliserande B-cellsrespons hos vaccinerade personer. Sådana immunogenica egenskaper hos VLP-baserade vaccinkandidater demonstreras ofta i smådjursmodeller20,21,22.
För att bedöma kvaliteten på den nyutvecklade VLP-vaccinkandidaten har VLP-insamlingsanalyser framgångsrikt använts5,23,24. Antalet publicerade metoder är dock begränsat. VLP fångst analys som presenteras här börjar med immobilisering av Env-specifika bNAbs på protein G-konjugerade pärlor, som binder till Fc regionen av däggdjur-härledda antikroppar. Typiska matriser för immobilisering av den antikropp som valts är agaros eller magnetiska pärlor. Magnetiska pärlor är dock gynnsamma för applikationer med hög genomströmning25. I nästa steg fångas VLP:er som visar målantigenet av bNAb-belagda pärlor. De bildade immunkomplexen bestående av Env-positiva VLPs och immobiliserade bNAbs berikas lätt med hjälp av en magnet. De isolerade immunkomplexen eluteras i det sista steget. Därefter kan VLPs biokemiskt karakteriseras. Här utförde vi western blot-analys med p55 Gag viral kärna protein-specifika antikroppar för att visa att det utfällda målet Env antigener inte bara hyser neutraliserande känsliga epitopes men visades också på Gag-bildade VLPs. Dessutom ökar upptäckten av viruskärnan Gag-proteiner känsligheten hos fångstanalysen eftersom Gag-proteiner är mer rikliga än Env i en VLP. I HIV-1 finns Env-proteiner endast på ett ensiffrigt eller tvåsiffrigt nummer26, medan mer än 3 500 gagmolekyler utgör kärnan i en partikel27.
Jämfört med andra tekniker för undersökning av interaktioner mellan protein och protein28,29 ger VLP-insamlingsanalysen en alternativ metod för forskningslaboratorier som inte har tillgång till dyra analysinstrument. Till exempel kan transmissionselektronmikroskopisk analys (TEM), ytplasmonresonansspektroskopi (SPR) och nanopartikelspårningsanalys (NTA) vara kostnadsintensiva. Den avskiljningsanalys som presenteras här tillåter också senare subjektering av fångade antigenpositiva VLP-prover till ytterligare proteinkarakterisering, t.ex. med hjälp av gelelektrofores, immunoblotting, elektronmikroskopi respektive masspektrometri (MS). Med tanke på att målantigenets ursprungliga struktur bevaras under VLP-fångstanalysen kan även prestandan hos en inbyggd SIDA och efterföljande immunblåsningstekniker användas.
VLP-fångstanalysen representerar en lättanvänd och känslig metod för att undersöka dekorationen av VLPs med målantigener som exponerar neutraliserande känsliga epitoper, och därmed deras användbarhet som framtida vaccinkandidater.
Protocol
Representative Results
Discussion
Före VLP-insamlingsanalysen, utvärdera bildandet av VLP och uttrycket av målantigenet i VLP-producentcelllinjerna. Instrumentella metoder är flödescytometrisk analys av antigenets cellytans uttryck samt antigen- och viral kärnproteinspecifik ELISA av CFSN och pelleterade VLPs.
Kritiska steg i VLP-fångstanalysen är beläggningen av pärlor med fångstantikroppar – här bNAbs – och den efterföljande fångsten av antigenpositiva VLPs av de antikroppsbelagda pärlorna. Framgångsrik beläggning av pärlor med antikroppar beror på valet av det konjugerade immunglobulinbindningsproteinet (Ig)-bindande proteinet. Donatorarten samt Ig-klassen av antikropparna avgör om protein G- eller protein A-konjugerade pärlor är att föredra. För de flesta arter och Ig klasser, protein G är ligand av val33. Som ett alternativ till protein A/G-konjugerade pärlor finns streptavidinpärlor för beläggningen med biotinylerade antikroppar tillgängliga. Pärlor kan också kovalent kopplas med antikroppar.
Avskiljningen av VLPs genom antikroppsbelagda pärlor beror på noggrann blandning, tillräcklig inkubationstid, antigen överflöd och affinitet av capture antikroppen. Enligt vår erfarenhet uppnås grundlig blandning av de antikroppsbelagda pärlor med VLP-proverna bäst genom användning av volymer >500 μL i 1,5 ml rör under rotation i minst 2 timmar vid rumstemperatur eller 4 °C. Ett annat potentiellt hinder är den för låga mängden VLPs i exemplet. För antikroppar som starkt binder målantigenet tillåter VLP-ingångar så låga som 15 ng Gag-protein vanligtvis lätt detekterbara mängder av de virala kärnproteiner som använder västerländsk blot-analys. Antikroppar med låg affinitet kräver dock högre inmatningsmängder, t.ex. 100 ng gagprotein, för att uppnå avgörande resultat (figur 3, bNAb 3).
Vissa ytantigener är benägna att proteasnedbrytning. Här rekommenderar vi tillsats av proteashämmare till VLP-proverna och inkubation vid 4 °C. Icke-specifik vidhäftning av värdcellsproteiner och VLPs till de pärlbundna antikropparna observeras sällan och bör uteslutas genom att använda lämpliga negativa kontroller, som vi här visade här med hjälp av mock och skalliga VLP-prover och isotyp kontroll antikroppar. Strategier för att minska icke-specifik bindning inkluderar förlängda tvättsteg och tillsats av kasein i tvättbufferten34. Dessutom kan infångningsanalysen också förbättras genom att bestämma det optimala förhållandet mellan antikroppar och antigendisplay VLP-mängd.
I det sista steget i VLP-fångstanalysen beskriver vi elutionen av immunkomplexen från pärlorna genom att koka för att minska Laemmli-bufferten. Under detta steg demonteras VLPs, och fångstantikroppar och målantigener separeras från pärlorna. I synnerhet måste donatorarten av den primära antikroppen som används i den efterföljande västerländska blot-analysen skilja sig från givaren av infångningsantikroppen för att undvika oavsiktlig detektion av infångningsantikroppen av de sekundära antidonatoriska IgG HRP- konjugerade antikropparna.
VLP-fångstanalysen som presenteras här ger en lättanvänd och känslig metod för att upptäcka neutraliseringskänsliga epitoper i strukturella intakta målantigener som visas på VLP-ytor. Insamlingsanalysen möjliggör dock inte direkt epitopkvantifiering. ELISA som utförs med bNAbs är avgörande för detta ändamål och bör utföras parallellt, särskilt om undersökta VLPs är avsedda att användas i prekliniska studier med användning av djurmodeller35. Detta är avgörande, eftersom mängden antigen direkt kan korrelera med elicitation av ett neutraliserande antikroppssvar hos immuniserade djur, vilket visas för porcin circovirus typ 2 (PCV2) vacciner36.
Ett idealiskt vaccin bör resultera i att bNAbs framkallas med inriktning på de neutraliserande känsliga epitoperna på virionytan. Analysen av dessa epitoper som särskilt hänvisar till deras fullständiga strukturella integritet på partikelvaccinytan är avgörande för att identifiera potentiella vaccinkandidater. Detta är inte bara fallet för hiv-härledda VLPs utan också för många andra VLP-vacciner under utveckling37. Framstående VLP-baserade vacciner härrör till exempel från icke-hölje eller kapsejsade föräldravirus som humant papillomvirus (HPV). Till skillnad från HIV-1-partiklar, som bildas av endast ett strukturellt kärnprotein, nämligen p55 Gag, och omsluts av membranet som härstammar från VLP-producentcellen, består HPV-partiklar av endast ett eller två strukturella kärnproteiner38,39. På samma sätt och som presenteras här för hölje vlps, VLP fångst analysen kan också tillämpas på påvisande av neutraliseringskänsliga epitoper av icke-hölje vlps.
Som ett alternativ till fångstanalysen kan VLP-prover direkt utsättas för inbyggt PAGE följt av western blot-analys med bNAbs och lämpliga sekundära antikroppar kopplade till HRP40. Men för analys av HIV Env-dekorerade VLPs är denna analys mindre känslig eftersom endast ett lågt antal antigenproteiner per VLP kan förväntas. Däremot underlättar fångstanalysen upptäckten av kärnproteinerna som är rikliga i stora mängder per VLP, när det gäller HIV-härledda VLPs mer än 3 500 Gag-proteiner bildar en VLP27. Detta möjliggör mycket känslig indirekt detektion av epitoper i Env som visas även vid låg densitet på VLPs.
Antalet väletablerade metoder för att undersöka neutraliseringskänsliga epitoper i ytantigener av VLPs är begränsat. Märkning av de antigener som visas på VLP: erna är möjlig med epitopspecifika antikropps-fluoroforkonjugat och efterföljande detektion genom nanopartikelspårningsanalys (NTA), vilket möjliggör detektion och kvantifiering av VLPs. Denna metod har också framgångsrikt utvecklats och optimerats för exosomer som presenterar cellytans markörer41. Ytplasmon resonans (SPR) spektroskopi möjliggör också analys av interaktioner mellan okonjugerade neutraliserande antikroppar och cognate epitopes presenteras på VLPs. Även om vlps inte är lämpliga för högre genomströmningsanalys kan de också märkas med bNAbs kopplade till guldpartiklar och efterföljande transmissionselektronmikroskopiska (TEM)-undersökning42.
Sammanfattningsvis ger vlp-fångstanalysen vissa betydande fördelar: i) Bedömning av den strukturella integriteten hos neutraliseringskänsliga epitoper på vlp:s yta, ii) känslig och indirekt detektion av antigener även när den visas vid låg densitet på VLP, och iii) metoden kräver inte kostnadsintensiv analysutrustning.
Divulgazioni
The authors have nothing to disclose.
Acknowledgements
Detta arbete stöddes av ett bidrag från det tyska federala ministeriet för utbildning och forskning, finansieringsprogram Forschung an Fachhochschulen, kontraktsnummer 13FH767IA6 och 13FH242PX6 till JS. Figurerna 1 och 2 skapades med BioRender.com.
Materials
| 1.5 mL reaction tubes | Eppendorf | ||
| 10x PBS | gibco | 70011044 | |
| 4%–15% Mini-PROTEAN TGX stain-free protein gels | BioRad | 4568085 | |
| Antibodies (bnAbs) | Polymun Scientic | ||
| Isotype control antibody | invitrogen (Thermo Fisher Scientific) | 02-7102 | |
| Chemidoc XRS+ imaging system | BioRad | 1708265 | |
| Chicken anti-rabbit IgG HRP-coupled | Life technologies | A15987 | 1:5000 in TBS-T + 2 % (w/v) powdered milk |
| Dynabeads Protein G Immunoprecipitation Kit | invitrogen (Thermo Fisher Scientific) | 10007D | includes buffers and washing solutions |
| FreeStyle 293-F cells | invitrogen (Thermo Fisher Scientific) | R790-07 | |
| FreeStyle 293 Expression Medium | invitrogen (Thermo Fisher Scientific) | 12338026 | |
| Gel blotting papers | Whatman | GB005 | |
| Glycine | Carl Roth | 0079 | blotting buffer |
| Magnetic separation rack | New England Biolabs | S1509S | for 12 x 1.5 mL or 6 x 1.5 mL tubes |
| Methanol | Carl Roth | 4627 | blotting buffer |
| Mini-PROTEAN Tetra Cell electrophoresis system | BioRad | ||
| Optima XE-90 ultracentrifuge | Beckman Coulter | ||
| PageRuler prestained protein ladder | Thermo Scientific | 26616 | |
| Polyvinylidene fluoride (PVDF) syringe filters, 0.45 µm | Carl Roth | KC89.1 | |
| Powdered milk | Carl Roth | T145 | blocking buffer |
| PVDF transfermembrane, 0.45 µm | Carl Roth | T830.1 | |
| QuickTiter HIV p24 ELISA | Cell Biolabs | VPK-108-H | |
| Rabbit polyclonal to HIV1 p55 + p24 + p17 | abcam | ab63917 | 1:2000 in TBS-T + 2 % (w/v) powdered milk |
| Rotator | Heidolph | REAX2 | |
| ROTI Load 1 (laemmli buffer) | Carl Roth | K929.1 | 4x concentrated reducing protein gel loading buffer |
| ROTIPHORESE 10x SDS-PAGE | Carl Roth | 3060 | |
| Sodium chloride | Carl Roth | 3957 | TBS-T buffer |
| SuperSignal West Pico PLUS chemiluminescent substrate | Thermo Scientific | 34579 | |
| SW28 rotor | Beckman Coulter | ||
| Thermomixer | Cel Media | basic | |
| Trans-Blot Turbo | BioRad | ||
| Trehalose dihydrate | Carl Roth | 8897.2 | |
| TRIS | Carl Roth | 5429 | blotting buffer |
| TRIS hydrochloride | Carl Roth | 9090 | TBS-T buffer |
| Tween-20 | Carl Roth | 9127 | TBS-T buffer |
| Ultra Clear centrifuge tubes | Beckman Coulter | 344058 |
Riferimenti
- Roldão, A., Mellado, M. C. M., Castilho, L. R., Carrondo, M. J. T., Alves, P. M. Virus-like particles in vaccine development. Expert Review of Vaccines. 9 (10), 1149-1176 (2010).
- Noad, R., Roy, P. Virus-like particles as immunogens. Trends in Microbiology. 11 (9), 438-444 (2003).
- Qian, C., et al. Recent progress on the versatility of virus-like particles. Vaccines. 8 (1), 139 (2020).
- Zabel, F., Kündig, T. M., Bachmann, M. F. Virus-induced humoral immunity: On how B cell responses are initiated. Current Opinion in Virology. 3 (3), 357-362 (2013).
- Garg, H., Mehmetoglu-Gurbuz, T., Joshi, A. Virus Like Particles (VLP) as multivalent vaccine candidate against Chikungunya, Japanese Encephalitis, Yellow Fever and Zika Virus. Scientific Reports. 10 (1), 4017 (2020).
- Hodgins, B., Pillet, S., Landry, N., Ward, B. J. A plant-derived VLP influenza vaccine elicits a balanced immune response even in very old mice with co-morbidities. PLoS ONE. 14 (1), 0210009 (2019).
- Lai, C. C., et al. Process development for pandemic influenza VLP vaccine production using a baculovirus expression system. Journal of Biological Engineering. 13, 78 (2019).
- Caldeira, J. C., Perrine, M., Pericle, F., Cavallo, F. Virus-like particles as an immunogenic platform for cancer vaccines. Viruses. 12 (5), 488 (2020).
- Nika, L., et al. An HER2-displaying virus-like particle vaccine protects from challenge with mammary carcinoma cells in a mouse model. Vaccines. 7 (2), 41 (2019).
- Mohsen, M. O., Zha, L., Cabral-Miranda, G., Bachmann, M. F. Major findings and recent advances in virus-like particle (VLP)-based vaccines. Seminars in Immunology. 34, 123-132 (2017).
- Fontana, D., Garay, E., Cevera, L., Kratje, R., Prieto, C., Gòdia, F. Chimeric VLPs based on hiv-1 gag and a fusion rabies glycoprotein induce specific antibodies against rabies and foot-and-mouth disease virus. Vaccines. 9 (3), 251 (2021).
- Cervera, L., et al. Production of HIV-1-based virus-like particles for vaccination: achievements and limits. Applied Microbiology and Biotechnology. 103 (18), 7367-7384 (2019).
- Gonelli, C. A., King, H. A. D., Mackenzie, C., Sonza, S., Center, R. J., Purcell, D. F. J. Immunogenicity of HIV-1-based virus-like particles with increased incorporation and stability of membrane-bound env. Vaccines. 9 (3), 1-36 (2021).
- Trkola, A. HIV not as simple as one, two, three. Nature. 568, 321-322 (2019).
- Berman, P. W., et al. Protection of chimpanzees from infection by HIV-1 after vaccination with recombinant glycoprotein gp120 but not gp160. Nature. 345 (6276), 622-625 (1990).
- Barouch, D. H. Challenges in the development of an HIV-1 vaccine. Nature. 455 (7213), 613-619 (2008).
- DeCaprio, J., Kohl, T. O. Immunoprecipitation. Cold Spring Harbor Protocols. 2020 (11), 449-461 (2020).
- Barret, B., Wood, P. A., Volwiler, W. Quantitation of gamma globulins in human serum by immunoprecipitation. Journal of Laboratory and Clinical Medicine. 55, 605-615 (1960).
- Kaboord, B., Perr, M. Isolation of proteins and protein complexes by immunoprecipitation. Methods in Molecular Biology. 424, 349-364 (2008).
- Lee, S. H., Chu, K. B., Kang, H. J., Quan, F. S. Virus-like particles containing multiple antigenic proteins of Toxoplasma gondii induce memory T cell and B cell responses. PLoS ONE. 14 (8), 0220865 (2019).
- Lee, Y. T., et al. Intranasal vaccination with M2e5x virus-like particles induces humoral and cellular immune responses conferring cross-protection against heterosubtypic influenza viruses. PLoS ONE. 13 (1), 0190868 (2018).
- Wang, J., et al. Large-scale manufacture of VP2 VLP vaccine against porcine parvovirus in Escherichia coli with high-density fermentation. Applied Microbiology and Biotechnology. 104 (9), 3847-3857 (2020).
- Swenson, D. L., et al. Generation of Marburg virus-like particles by co-expression of glycoprotein and matrix protein. FEMS Immunology and Medical Microbiology. 40 (1), 27-31 (2004).
- Latham, T., Galarza, J. M. Formation of wild-type and chimeric influenza virus-like particles following simultaneous expression of only four structural proteins. Journal of Virology. 75 (13), 6154-6165 (2001).
- Doyle, J., Ray, M., Ouyang, A., Benton, B., Bell, P. A. Abstract 4877: High throughput proteomic applications using protein A/G magnetic beads. Association for Cancer Research (AACR) 102nd Annual Meeting. 20, 4877 (2011).
- Zhu, P., et al. Electron tomography analysis of envelope glycoprotein trimers on HIV and simian immunodeficiency virus virions. Proceedings of the National Academy of Sciences of the United States of America. 100 (26), 15812-15817 (2003).
- Lavado-García, J., Jorge, I., Boix-Besora, A., Vázquez, J., Gòdia, F., Cervera, L. Characterization of HIV-1 virus-like particles and determination of Gag stoichiometry for different production platforms. Biotechnology and Bioengineering. 118 (7), 2660-2675 (2021).
- Miura, K. An overview of current methods to confirm protein-protein interactions. Protein & Peptide Letters. 25 (8), 728-733 (2018).
- Rao, V. S., Srinivas, K., Sujini, G. N., Kumar, G. N. Advances in molecular techniques to study diversity. Plant Biotechnology, Volume 1: Principles, Techniques, and Applications. , 341-365 (2017).
- Rosengarten, J. F., Schatz, S., Wolf, T., Barbe, S., Stitz, J. Components of a HIV-1 vaccine mediate virus-like particle (VLP)-formation and display of envelope proteins exposing broadly neutralizing epitopes. Virology. , 41-48 (2022).
- JoVE, Grundlegende Methoden in der Zell- und Molekularbiologie. Separating Protein with SDS-PAGE. JoVE Science Education Database. , (2021).
- Eslami, A., Lujan, J. Western blotting: sample preparation to detection. Journal of Visualized Experiments: JoVE. (44), e2359 (2010).
- Sheng, S., Kong, F. Separation of antigens and antibodies by immunoaffinity chromatography. Pharmaceutical Biology. 50 (8), 1038-1044 (2012).
- Guzzo, C., et al. Virion incorporation of integrin 47 facilitates HIV-1 infection and intestinal homing. Science Immunology. 2 (11), (2017).
- Wei, M., et al. Bacteria expressed hepatitis E virus capsid proteins maintain virion-like epitopes. Vaccine. 32 (24), 2859-2865 (2014).
- Jin, J., Park, C., Cho, S. H., Chung, J. The level of decoy epitope in PCV2 vaccine affects the neutralizing activity of sera in the immunized animals. Biochemical and Biophysical Research Communications. 496 (3), 846-851 (2018).
- Zhang, X., et al. Lessons learned from successful human vaccines: Delineating key epitopes by dissecting the capsid proteins. Human Vaccines and Immunotherapeutics. 11 (5), 1277-1292 (2015).
- DiGiuseppe, S., Bienkowska-Haba, M., Guion, L. G. M., Keiffer, T. R., Sapp, M. Human papillomavirus major capsid protein L1 remains associated with the incoming viral genome throughout the entry process. Journal of Virology. 91 (16), 00537 (2017).
- Wang, J. W., Roden, R. B. S. L2, the minor capsid protein of papillomavirus. Virology. 445 (1-2), 175-186 (2013).
- Binley, J. M., et al. Profiling the specificity of neutralizing antibodies in a large panel of plasmas from patients chronically infected with human immunodeficiency virus type 1 subtypes B and C. Journal of Virology. 82 (23), 11651-11668 (2008).
- Thane, K. E., Davis, A. M., Hoffman, A. M. Improved methods for fluorescent labeling and detection of single extracellular vesicles using nanoparticle tracking analysis. Scientific Reports. 9 (1), 12295 (2019).
- Mulder, A. M., et al. Toolbox for non-intrusive structural and functional analysis of recombinant VLP based vaccines: A case study with hepatitis B vaccine. PLoS ONE. 7 (4), 0033235 (2012).

