सरलीकृत, उच्च थ्रूपुट विश्लेषण एकल-सेल संकुचितता का उपयोग कर Micropatterned Elastomers का उपयोग कर
Summary
यह काम फ्लोरोसेंट प्रोटीन माइक्रोपैटर्न के विज़ुअलाइज़्ड विस्थापन के आधार पर एकल-सेल संकुचनशील बलों के सरलीकृत, हाथों से परिमाणीकरण के लिए माइक्रोवेल प्रारूप में फ्लोरोसेंटली लेबल वाले इलास्टोमेरिक अनुबंधयोग्य सतहों (FLECS) प्रौद्योगिकी का उपयोग करने के लिए एक लचीला प्रोटोकॉल प्रस्तुत करता है।
Abstract
सेलुलर संकुचनशील बल उत्पादन लगभग सभी कोशिकाओं द्वारा साझा की जाने वाली एक मौलिक विशेषता है। ये संकुचनशील बल उचित विकास के लिए महत्वपूर्ण हैं, दोनों सेलुलर और ऊतक स्तरों पर कार्य करते हैं, और शरीर में यांत्रिक प्रणालियों को विनियमित करते हैं। कई जैविक प्रक्रियाएं बल-निर्भर हैं, जिनमें गतिशीलता, आसंजन और एकल-कोशिकाओं का विभाजन, साथ ही हृदय, मूत्राशय, फेफड़े, आंतों और गर्भाशय जैसे अंगों का संकुचन और विश्राम शामिल है। उचित शारीरिक कार्य को बनाए रखने में इसके महत्व को देखते हुए, सेलुलर संकुचन भी अतिरंजित या बाधित होने पर रोग प्रक्रियाओं को चला सकता है। अस्थमा, उच्च रक्तचाप, अपरिपक्व श्रम, फाइब्रोटिक स्कारिंग, और अंडरएक्टिव मूत्राशय यांत्रिक रूप से संचालित रोग प्रक्रियाओं के सभी उदाहरण हैं जिन्हें संभावित रूप से सेलुलर संकुचनशील बल के उचित नियंत्रण के साथ कम किया जा सकता है। यहां, हम एक उपन्यास माइक्रोप्लेट-आधारित संकुचन परख प्रौद्योगिकी का उपयोग करने के लिए एक व्यापक प्रोटोकॉल प्रस्तुत करते हैं जिसे फ्लोरोसेंटली लेबल वाले इलास्टोमेरिक अनुबंध योग्य सतहों (FLECS) के रूप में जाना जाता है, जो बड़े पैमाने पर स्केल किए गए तरीके से एकल-सेल संकुचन का सरलीकृत और सहज ज्ञान युक्त विश्लेषण प्रदान करता है। यहां, हम दो छह-बिंदु खुराक-प्रतिक्रिया घटता प्राप्त करने के लिए एक चरण-वार प्रोटोकॉल प्रदान करते हैं जो प्राथमिक मानव मूत्राशय चिकनी मांसपेशी कोशिकाओं के संकुचन पर दो संकुचनशील अवरोधकों के प्रभावों का वर्णन करते हैं, जो एक सरल प्रक्रिया में केवल एक ही FLECS परख माइक्रोप्लेट का उपयोग करते हैं, विधि के उपयोगकर्ताओं के लिए उचित तकनीक का प्रदर्शन करने के लिए। FLECS प्रौद्योगिकी का उपयोग करते हुए, बुनियादी जैविक प्रयोगशालाओं और फ्लोरोसेंट माइक्रोस्कोपी सिस्टम वाले सभी शोधकर्ताओं को इस मौलिक लेकिन मुश्किल-से-मात्रा में कार्यात्मक सेल फेनोटाइप का अध्ययन करने के लिए पहुंच प्राप्त होती है, जो बल जीव विज्ञान के क्षेत्र में प्रवेश बाधा को प्रभावी ढंग से कम करती है और संकुचनशील सेल बल की फेनोटाइपिक स्क्रीनिंग करती है।
Introduction
कोशिका-जनित यांत्रिक बल पूरे शरीर में विभिन्न अंगों जैसे आंतों, मूत्राशय, हृदय और अन्य में उचित कार्य करने के लिए आवश्यक हैं। इन अंगों को आंतरिक होमोस्टेटिक स्थिति को बनाए रखने के लिए सेल संकुचन और विश्राम के स्थिर पैटर्न उत्पन्न करना चाहिए। असामान्य चिकनी मांसपेशी कोशिका (एसएमसी) संकुचन विभिन्न विकारों की शुरुआत का कारण बन सकता है, उदाहरण के लिए, आंतों की डिस्मोटिलिटी, आंतों के चिकनी मांसपेशियों के संकुचन 1 के असामान्य पैटर्न की विशेषता है, साथ ही साथ ओवरएक्टिव 2 या अंडरएक्टिव मूत्राशय 3 की यूरोलॉजिक स्थितियां। वायुमार्ग के भीतर, एसएमसी जो अनियमित संकुचन पैटर्न प्रदर्शित करते हैं, अस्थमा के हाइपररेस्पॉन्सिबिलिटी 4 को ट्रिगर कर सकते हैं, संभावित रूप से वायुमार्ग को कस सकते हैं और फेफड़ों में ऑक्सीजन के एयरफ्लो को कम कर सकते हैं। एक और व्यापक शारीरिक स्थिति, उच्च रक्तचाप, रक्त वाहिकाओं के भीतर चिकनी मांसपेशियों के संकुचन में उतार-चढ़ाव के कारण होता है5। स्पष्ट रूप से, कोशिकाओं और ऊतकों के भीतर संकुचनशील तंत्र उन बीमारियों को जन्म दे सकते हैं जिनके लिए उपचार के विकल्पों की आवश्यकता होती है। जैसा कि ये स्थितियां स्पष्ट रूप से कोशिकाओं के बेकार संकुचनशील व्यवहारों से स्टेम करती हैं, संभावित दवा उम्मीदवारों की स्क्रीनिंग करते समय सेल संकुचनशील फ़ंक्शन को मापने के लिए तार्किक और आवश्यक हो जाता है।
सेलुलर संकुचन बल का अध्ययन करने के लिए उपकरणों की आवश्यकता को पहचानते हुए, कई मात्रात्मक संकुचन परख विधियों को शैक्षिक शोधकर्ताओं द्वारा विकसित किया गया है, जिसमें कर्षण बल माइक्रोस्कोपी (टीएफएम) 6, माइक्रोपैटर्न्ड टीएफएम 7, फ्लोटिंग जेल assays8, और इलास्टोमेरिक माइक्रोपोस्ट assays9 शामिल हैं। इन प्रौद्योगिकियों का उपयोग कई अध्ययनों में एकल-डिश प्रारूप के साथ-साथ बहु-अच्छी तरह से प्लेट प्रारूप में किया गया है और यहां तक कि तीन आयामी बल माप 10,11,12,13,14 के लिए भी प्रस्तावित किया गया है। हालांकि इन प्रौद्योगिकियों ने सेल फोर्स जीव विज्ञान के विशाल क्षेत्र के भीतर अग्रणी अनुसंधान को सक्षम किया है, वे सभी काफी हद तक विशिष्ट क्षमताओं और संसाधनों वाले प्रयोगशालाओं तक सीमित हैं, विशेष रूप से: टीएफएम सब्सट्रेट बनाने की क्षमता, टीएफएम विस्थापन मानचित्रों को हल करने के लिए जटिल और गैर-सहज ज्ञान युक्त एल्गोरिदम को ठीक से लागू करने की क्षमता, और अपेक्षाकृत सटीक माइक्रोस्कोपी सिस्टम जो मंच से नमूना हटाने से पहले और बाद में ली गई छवियों को पंजीकृत कर सकते हैं (सेल पृथक्करण के लिए)। इस प्रकार, एक अप्रशिक्षित शोधकर्ता के लिए, इन तरीकों का उपयोग करने के लिए प्रवेश बाधा इन प्रौद्योगिकियों को लागू करने के लिए आवश्यकताओं के व्यापक सेट को देखते हुए काफी अधिक हो सकती है। इसके अलावा, कई मौजूदा प्रौद्योगिकियों (40x उद्देश्यों या उससे अधिक) के लिए आवश्यक इमेजिंग रिज़ॉल्यूशन प्रयोगात्मक थ्रूपुट को काफी सीमित कर सकता है, जबकि थोक माप प्रौद्योगिकियां बाहरी कोशिकाओं से योगदान को मुखौटा कर सकती हैं और हल्के संकुचनशील मतभेदों की खोज को रोक सकती हैं। ध्यान दें, जहां तक लेखकों को पता है, केवल कम थ्रूपुट और अर्ध-मात्रात्मक फ्लोटिंग जेल परख दृष्टिकोण शोधकर्ताओं के लिए उपलब्ध होने के लिए पर्याप्त रूप से परिपक्व हो गया है (चित्रा 1 देखें)।
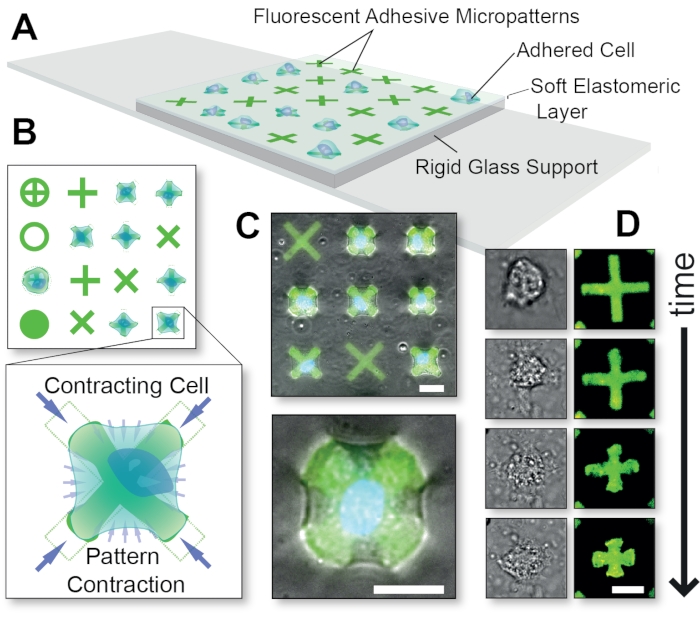
चित्र1: FLECS प्रौद्योगिकी विधि की समग्र योजनाबद्ध. (A) कोशिकाओं को चिपकने वाले प्रोटीन माइक्रोपैटर्न का पालन किया जाता है जो कांच द्वारा समर्थित एक पतली इलास्टोमेरिक परत में सहसंयोजक रूप से एम्बेडेड होते हैं। (बी) विभिन्न संभावित माइक्रोपैटर्न आकृतियों का शीर्ष दृश्य और एक ‘एक्स’ के आकार के माइक्रोपैटर्न को अनुबंधित करने वाले सेल का एक झटका। (सी) फ्लोरोसेंट माइक्रोपैटर्न का ओवरले और एक अनुबंधित सेल की चरण कंट्रास्ट छवियां। (डी) एक एकल अनुबंध सेल की समय-पाठ्यक्रम छवियां। स्केल सलाखों = 25 μm. यह आंकड़ा पुष्करस्की एट अल 15 से अनुमति के साथ अनुकूलित किया गया था। कृपया इस आंकड़े का एक बड़ा संस्करण देखने के लिए यहाँ क्लिक करें.
माइक्रोटेक्नोलॉजी में हाल की प्रगति के बाद, लेखकों ने एक माइक्रोप्लेट-आधारित तकनीक विकसित की है जो सैकड़ों हजारों कोशिकाओं में एकल-सेल संकुचन के मात्रात्मक माप को सक्षम करती है जिसे FLECS कहा जाता है (फ्लोरोसेंटली लेबल वाली इलास्टोमेरिक अनुबंध योग्य सतहें)15,16,17,18,19,20 , टीएफएम के विकल्प के रूप में। इस दृष्टिकोण में, फ्लोरोसेंट प्रोटीन माइक्रोपैटर्न को नरम फिल्मों में एम्बेडेड किया जाता है जो विकृत और सिकुड़ते हैं जब कोशिकाएं उन पर कर्षण बलों को लागू करती हैं, एक सहज और औसत दर्जे के तरीके से। महत्वपूर्ण रूप से, प्रोटीन माइक्रोपैटर्न कोशिका की स्थिति, आकार और प्रसार क्षेत्र को बाधित करते हैं, जिससे समान परीक्षण की स्थिति होती है। ये केवल अपने आयामी परिवर्तनों के आधार पर सरल माप की अनुमति देते हैं, जो 4x आवर्धन छवियों में भी स्थानिक रूप से अत्यधिक हल किए जाते हैं। इस विधि में एक ब्राउज़र-आधारित छवि विश्लेषण मॉड्यूल शामिल है और नाजुक हैंडलिंग प्रक्रियाओं या प्रत्ययी मार्करों के पंजीकरण की आवश्यकता के बिना संकुचनशील सेल बल के सीधे विश्लेषण को सक्षम बनाता है, जैसे कि इसे किसी भी शोधकर्ता द्वारा एक बुनियादी सेल संस्कृति सुविधा और कम आवर्धन के साथ सरल फ्लोरोसेंट माइक्रोस्कोप के साथ संचालित किया जाना चाहिए (चित्रा 2) ). यह तकनीक, जो शेल्फ-तैयार और व्यावसायिक रूप से उपलब्ध है, को अंतिम उपयोगकर्ता को ध्यान में रखते हुए डिज़ाइन किया गया था और इसका उद्देश्य सेलुलर बल जीव विज्ञान का अध्ययन करने के लिए किसी भी प्रयोगशाला वैज्ञानिक के लिए प्रवेश बाधा को कम करना है।

चित्रा 2: एकल सेल contractility परख के लिए 24 अच्छी तरह से प्लेट प्रारूप की योजनाबद्ध. इस प्रारूप का उपयोग यहां वर्णित प्रयोगों में किया गया था और लेख के वीडियो भाग में चित्रित किया गया था। स्केल बार = 25 μm. कृपया इस आकृति का एक बड़ा संस्करण देखने के लिए यहाँ क्लिक करें।
इस काम में, हम प्राथमिक मूत्राशय चिकनी मांसपेशी कोशिकाओं में सेलुलर संकुचन पर बल-मॉड्यूलेटिंग दवाओं के प्रभावों को मापने के लिए FLECS प्रौद्योगिकी मंच के 24 अच्छी तरह से प्लेट प्रारूप को लागू करने के लिए एक प्रोटोकॉल प्रस्तुत करते हैं। इस सामान्य उद्देश्य प्रोटोकॉल को विभिन्न अन्य टाइमस्केल, सेल-प्रकार, और ब्याज की उपचार स्थितियों के लिए खाते में आवश्यक रूप से अनुकूलित और संशोधित किया जा सकता है, और बल जीव विज्ञान में अन्य प्रश्नों के उत्तर देने के लिए स्केल किया जा सकता है।
Protocol
Representative Results
Discussion
विभिन्न उपचार स्थितियों के तहत एक समय में सैकड़ों हजारों कोशिकाओं में संकुचन को मात्रात्मक रूप से मापने और केवल मानक माइक्रोस्कोपी उपकरणों का उपयोग करने के लिए यह सरलीकृत विधि शोधकर्ताओं को सेलुलर बल जीव विज्ञान का अध्ययन करने के लिए पारंपरिक टीएफएम के लिए एक सुलभ विकल्प प्रदान करती है। क्योंकि प्रस्तुत तकनीक नियमित रूप से आकार के फ्लोरोसेंट माइक्रोपैटर्न में परिवर्तनों का विश्लेषण करके सेल संकुचन का एक दृश्य प्रदर्शन प्रदान करती है, किसी भी दिए गए सेल द्वारा उत्पादित संकुचन के परिमाण को सहजता से समझा जाता है – माइक्रोपैटर्न जितना छोटा होता है, सेल द्वारा लगाए जाने वाले संकुचन बल उतना ही बड़ा होता है।
विशेष रूप से, आकार, प्रसार-क्षेत्र और आसंजन अणु जैसे कारकों पर नियंत्रण की पेशकश करके, जिसमें माइक्रोपैटर्न शामिल हैं (सेल संकुचन 22,23,24 को विनियमित करने के लिए जाने जाने वाले सभी कारक), प्रस्तुत तकनीक व्यवस्थित रूप से अतिरिक्त चर को समाप्त कर देती है जो सेल संकुचन अध्ययनों की व्याख्याओं को भ्रमित कर सकती है।
इस प्रयोग में, जेल में 10 केपीए कठोरता का उपयोग किया गया था और एक 70 μm (विकर्ण लंबाई) माइक्रोपैटर्न का उपयोग किया गया था जिसमें टाइप IV कोलेजन शामिल था। इन मापदंडों के अलावा, चिपकने वाले अणु को विभिन्न कोलेजन, फाइब्रोनेक्टिन, जिलेटिन और अन्य एक्स्ट्रासेल्युलर मैट्रिक्स (ईसीएम) के साथ प्रतिस्थापित किया जा सकता है। जेल की कठोरता को 0.1 kPa तक ट्यून किया जा सकता है, और MPa रेंज में ऊपर। माइक्रोपैटर्न ज्यामिति को ~ 5 μm के न्यूनतम सुविधा आकार के साथ किसी भी आकार के लिए डे नोवो डिज़ाइन किया जा सकता है। इन मापदंडों decoupled हैं और स्वतंत्र रूप से एक विशेष जैविक संदर्भ के लिए अनुकूलित किया जा सकता है।
इस तकनीक को विभिन्न चिकनी मांसपेशी कोशिका प्रकारों (प्राथमिक मानव मूत्राशय, आंतों, श्वासनली, ब्रोन्कियल, गर्भाशय, महाधमनी और धमनी), मेसेनकाइमल स्टेम कोशिकाओं और उनके विभेदित संतानों, विभिन्न फाइब्रोब्लास्ट्स (फुफ्फुसीय, त्वचीय और हृदय), मायोफाइब्रोब्लास्ट्स और एंडोथेलियल कोशिकाओं सहित मेसेनकाइमल फेनोटाइप के अत्यधिक चिपकने वाले और संकुचनशील सेल प्रकारों के साथ संगत होने के लिए बड़े पैमाने पर मान्य किया गया है। इसके अलावा, मोनोसाइट-व्युत्पन्न मैक्रोफेज भी माइक्रोपैटर्न पर बड़े औसत दर्जे के फागोसाइटिक बल का उत्पादन करेंगे, खासकर यदि माइक्रोपैटर्न में एक ज्ञात ऑप्सोनिन होता है। विभिन्न कैंसर लाइनों को भी विधि का उपयोग करके परखा जा सकता है।
यह विधि उन कोशिकाओं के साथ उपयोग के लिए कुछ चुनौतियां पैदा कर सकती है जो या तो अपेक्षाकृत छोटे होते हैं जैसे कि टी-कोशिकाएं और न्यूट्रोफिल, या मुख्य रूप से उपकला फेनोटाइप के साथ सेल प्रकार। इसका मुख्य कारण यह है कि विधि मापने योग्य संकुचनशील संकेत उत्पन्न करने के लिए माइक्रोपैटर्न पर मजबूत आसंजन और कोशिकाओं के पूर्ण प्रसार पर निर्भर करती है। कोशिकाएं जो कमजोर रूप से बांधती हैं, एक-दूसरे से बंधती हैं, या पूरी तरह से फैलती नहीं हैं, वे औसत दर्जे के संकुचनशील संकेतों का उत्पादन नहीं करेंगी। ये व्यवहार, जो अपेक्षाकृत दुर्लभ हैं, को माइक्रोपैटर्न आकार को छोटा होने के लिए समायोजित करके, या माइक्रोपैटर्न के भीतर वैकल्पिक चिपकने वाले अणुओं का उपयोग करके कम किया जा सकता है जो उन कोशिकाओं में आसंजन और प्रसार को बेहतर ढंग से बढ़ावा देगा।
प्रौद्योगिकी के उपयोगकर्ताओं को अपने विशेष सेल प्रकार के ब्याज के लिए विभिन्न संभावित सेल संस्कृति माध्यम योगों का सावधानीपूर्वक मूल्यांकन करना चाहिए, क्योंकि विभिन्न घटक, विकास कारक, सीरम स्तर और पीएच संवेदनशीलता विभिन्न कोशिकाओं में चर व्यवहार को चला सकती हैं। प्रोटोकॉल का अनुकूलन किसी भी प्रयोगात्मक वर्कफ़्लो के स्केलिंग से पहले होना चाहिए, और मीडिया घटकों को हमेशा ताजा, बाँझ और पूर्व बैचों के अनुरूप होना चाहिए।
आखिरकार, यदि एकल-सेल रिज़ॉल्यूशन उपयोगकर्ता के लक्ष्यों के लिए आवश्यक नहीं है, या यदि लक्ष्य सेल प्रकार में न्यूनतम प्रसार क्षमता है, तो पारंपरिक टीएफएम ऐसे प्रयोगों के लिए समान रूप से या अधिक उपयुक्त हो सकता है। लेखकों का उद्देश्य और आशा यह है कि यह उपकरण सेल जीवविज्ञानियों को सेलुलर संकुचन का अध्ययन करने के लिए एक अतिरिक्त एवेन्यू प्रदान करता है, विशेष रूप से स्वचालित उच्च-थ्रूपुट फेनोटाइपिक दवा स्क्रीन के संदर्भ में।
दवा स्क्रीन में भविष्य के उपयोग के लिए विशिष्ट, 384-अच्छी तरह से FLECS प्लेट जैसे उच्च थ्रूपुट प्लेटों का उपयोग किया जा सकता है। ऐसी प्लेटों में, कई माइक्रोस्कोप पर 4x उद्देश्य अपने दृश्य के क्षेत्र में एक पूरे एकल कुएं पर कब्जा कर सकते हैं, यह सुनिश्चित करते हुए कि सभी सेलुलर संकुचनशील प्रतिक्रियाओं पर कब्जा कर लिया गया है। एक उच्च-थ्रूपुट इमेजिंग सिस्टम का उपयोग करके, एक पूरे 384-वेल प्लेट को लगभग 5 मिनट में चित्रित किया जा सकता है, जिससे यह प्रणाली अन्य विकल्पों की तुलना में नाटकीय रूप से तेज हो जाती है, और इसलिए, उच्च-थ्रूपुट फेनोटाइपिक दवा खोज के लिए उपयुक्त होती है। दरअसल, लेखक नियमित रूप से स्वचालन का उपयोग करके ~ 50 384-वेलप्लेट (कुल मिलाकर 19,000 से अधिक कुओं) पर साप्ताहिक दवा स्क्रीन चलाते हैं।
Divulgazioni
The authors have nothing to disclose.
Acknowledgements
प्रयोगशाला का काम यूसीएलए आणविक साझा स्क्रीनिंग संसाधन (एमएसएसआर) के समर्थन से आयोजित किया गया था, जहां फोर्साइट अनुसंधान गतिविधियों को प्रायोजित कर रहा है, और कैलिफोर्निया नैनोसिस्टम्स इंस्टीट्यूट (सीएनएसआई) में आवर्धक इनक्यूबेटर, जहां फोर्ट बायो टेक्नोलॉजीज, इंक एक निवासी कंपनी है। लेखक अनुरोध पर सभी अकादमिक शोधकर्ताओं को Biodock.ai FLECS विश्लेषण मॉड्यूल तक पहुंच प्रदान करेंगे। एल.एच. और आई.पी. ने इस काम में समान रूप से योगदान दिया।
Materials
| Bladder smooth muscle cell culture | Sciencell | #4310 | |
| Blebbistatin | Sigma-Aldrich | B0560 | |
| Cell culture media | Thermofisher | 11765054 | Ham's F12 medium supplemented with 10% FBS and 1% p/s |
| Cell strainer | Fisher Scientific | 7201432 | |
| Conical Tube | Fisher Scientific | 05-539-13 | |
| Culture flask | Fisher Scientific | FB012941 | |
| Cytochalasin D | Sigma-Aldrich | C8273 | |
| DMSO (Dimethyl sulfoxide) | Fisher Scientific | D1284 | |
| Eppendorf tubes | Fisher Scientific | 05-402-31 | |
| Fluorescent microscope | Molecular Devices | ImageXpress Confocal | |
| Forcyte-manufactured 24-well plate | Forcyte Biotechnologies | 24-HC4R-X1-QB12 | |
| Hoescht 3342 Live Nuclear Stain | Thermofisher | 62249 | |
| Phosphate Buffered Saline (PBS) | Fisher Scientific | BP39920 |
Riferimenti
- Ohama, T., Hori, M., Ozaki, H. Mechanism of abnormal intestinal motility in inflammatory bowel disease: How smooth muscle contraction is reduced. Journal of Smooth Muscle Research. 43 (2), 43-54 (2007).
- Peyronnet, B., et al. A comprehensive review of overactive bladder pathophysiology: On the way to tailored treatment. European Urology. 75 (6), 988-1000 (2019).
- Aldamanhori, R., Osman, N. I., Chapple, C. R. Underactive bladder: Pathophysiology and clinical significance. Asian Journal of Urology. 5 (1), 17-21 (2018).
- Sanderson, M. J., Delmotte, P., Bai, Y., Perez-Zogbhi, J. F. Regulation of airway smooth muscle cell contractility by Ca2+ signaling and sensitivity. Proceedings of the American Thoracic Society. 5 (1), 23-31 (2008).
- Brozovich, F. V., et al. Mechanisms of vascular smooth muscle contraction and the basis for pharmacologic treatment of smooth muscle disorders. Pharmacological Reviews. 68 (2), 476-532 (2016).
- Munevar, S., Wang, Y., Dembo, M. Traction force microscopy of migrating normal and H-ras transformed 3T3 fibroblasts. Biophysical Journal. 80 (4), 1744-1757 (2001).
- Tseng, Q., et al. A new micropatterning method of soft substrates reveals that different tumorigenic signals can promote or reduce cell contraction levels. Lab on a Chip. 11 (13), 2231-2240 (2011).
- Bell, E., Ivarsson, B., Merrill, C. Production of a tissue-like structure by contraction of collagen lattices by human fibroblasts of different proliferative potential in vitro. Proceedings of the National Academy of Sciences. 76 (3), 1274-1278 (1979).
- Tan, J. L., et al. Cells lying on a bed of microneedles: an approach to isolate mechanical force. Proceedings of the National Academy of Sciences. 100 (4), 1484-1489 (2003).
- Rokhzan, R., et al. high-throughput measurements of cell contraction and endothelial barrier function. Laboratory Investigation. 99 (1), 138-145 (2019).
- Park, C. Y., et al. High-throughput screening for modulators of cellular contractile force. Integrative Biology. 7 (10), 1318-1324 (2015).
- Kaylan, K. B., Kourouklis, A. P., Underhill, G. H. A high-throughput cell microarray platform for correlative analysis of cell differentiation and traction forces. Journal of Visualized Experiments. (121), e55362 (2017).
- Huang, Y., et al. Traction force microscopy with optimized regularization and automated Bayesian parameter selection for comparing cells. Scientific Reports. 9, 539 (2019).
- Franck, C., Maskarinec, S. A., Tirrell, D. A., Ravichandran, G. Three-dimensional traction force microscopy: A new tool for quantifying cell-matrix interactions. PLOS ONE. 6, 17833 (2011).
- Pushkarsky, I., et al. Elastomeric sensor surfaces for high-throughput single-cell force cytometry. Nature Biomedical Engineering. 2 (2), 124-137 (2018).
- Pushkarsky, I. FLECS technology for high-throughput single-cell force biology and screening. ASSAY and Drug Development Technologies. 16 (1), 7-11 (2017).
- Koziol-White, C. J., et al. Inhibition of PI3K promotes dilation of human small airways in a rho kinase-dependent manner. British Journal of Pharmacology. 173 (18), 2726-2738 (2016).
- Orfanos, S., et al. Obesity increases airway smooth muscle responses to contractile agonists. American Journal of Physiology-Lung Cellular and Molecular Physiology. 315 (5), 673-681 (2018).
- Tseng, P., Pushkarsky, I., Carlo, D. D. Metallization and biopatterning on ultra-flexible substrates via dextran sacrificial layers. PLOS ONE. 9, 106091 (2014).
- Yoo, E. J., et al. Gα12 facilitates shortening in human airway smooth muscle by modulating phosphoinositide 3-kinase-mediated activation in a RhoA-dependent manner. British Journal of Pharmacology. 174 (4), 4383-4395 (2017).
- MacGlashan, D., Vilariño, N. Polymerization of actin does not regulate desensitization in human basophils. Journal of Leukocyte Biology. 85 (4), 627-637 (2009).
- Hocking, D. C., Sottile, J., Langenbach, K. J. Stimulation of integrin-mediated cell contractility by fibronectin polymerization. Journal of Biological Chemistry. 275 (14), 10673-10682 (2000).
- Tolić-Nørrelykke, I. M., Wang, N. Traction in smooth muscle cells varies with cell spreading. Journal of Biomechanics. 38 (7), 1405-1412 (2005).
- Ye, G. J. C., et al. The contractile strength of vascular smooth muscle myocytes is shape dependent. Integrative Biology. 6 (2), 152-163 (2014).

