Forenklet analyse med høj gennemstrømning af enkeltcellekontraktilitet ved hjælp af mikromønstrede elastomerer
Summary
Dette arbejde præsenterer en fleksibel protokol til anvendelse af fluorescerende mærkede elastomeriske kontraktbare overflader (FLECS) Teknologi i mikrobrøndformat til forenklet, hands-off kvantificering af enkeltcellekontraktile kræfter baseret på visualiserede forskydninger af fluorescerende proteinmikromønstre.
Abstract
Cellulær kontraktil kraftgenerering er et grundlæggende træk, der deles af stort set alle celler. Disse kontraktile kræfter er afgørende for korrekt udvikling, fungerer på både celle- og vævsniveau og regulerer de mekaniske systemer i kroppen. Talrige biologiske processer er kraftafhængige, herunder bevægelighed, vedhæftning og opdeling af enkeltceller samt sammentrækning og afslapning af organer som hjerte, blære, lunger, tarme og livmoder. I betragtning af dets betydning for at opretholde korrekt fysiologisk funktion kan cellulær kontraktilitet også drive sygdomsprocesser, når de overdrives eller forstyrres. Astma, hypertension, for tidlig fødsel, fibrotisk ardannelse og underaktiv blære er alle eksempler på mekanisk drevne sygdomsprocesser, der potentielt kan lindres med korrekt kontrol af cellulær kontraktil kraft. Her præsenterer vi en omfattende protokol til brug af en ny mikropladebaseret kontraktilitetsanalyseteknologi kendt som fluorescerende mærkede elastomeriske kontraktbare overflader (FLECS), der giver forenklet og intuitiv analyse af enkeltcellekontraktilitet på en massivt skaleret måde. Heri giver vi en trinvis protokol til opnåelse af to sekspunkts dosisresponskurver, der beskriver virkningerne af to kontraktile hæmmere på sammentrækningen af primære humane blæreglat muskelceller i en simpel procedure, der kun anvender en enkelt FLECS-assaymikroplade for at demonstrere korrekt teknik til brugere af metoden. Ved hjælp af FLECS-teknologi får alle forskere med grundlæggende biologiske laboratorier og fluorescerende mikroskopisystemer adgang til at studere denne grundlæggende, men vanskelige at kvantificere funktionelle cellefænotype, hvilket effektivt sænker adgangsbarrieren inden for kraftbiologi og fænotypisk screening af kontraktil cellekraft.
Introduction
Cellegenererede mekaniske kræfter er afgørende for korrekt funktion i forskellige organer i hele kroppen, såsom tarmene, blæren, hjertet og andre. Disse organer skal generere stabile mønstre af cellekontraktion og afslapning for at opretholde den indre homeostatiske tilstand. Unormal sammentrækning af glatte muskelceller (SMC) kan føre til udbrud af forskellige lidelser, herunder for eksempel intestinal dysmotilitet, der er karakteriseret ved unormale mønstre af intestinal glat muskelkontraktion1, samt de urologiske tilstande af overaktiv2 eller underaktiv blære3. Inden for luftvejene kan SMC’er, der udviser uregelmæssige sammentrækningsmønstre, udløse astmatisk hyperresponsivitet4, potentielt stramme luftvejene og mindske luftstrømmen af ilt ind i lungerne. En anden udbredt fysisk tilstand, hypertension, er forårsaget af udsving i sammentrækningen af glatte muskler i blodkarrene5. Det er klart, at kontraktile mekanismer i celler og væv kan føre til sygdomme, der kræver behandlingsmuligheder. Da disse tilstande umiskendeligt stammer fra cellernes dysfunktionelle kontraktile adfærd, bliver det logisk og nødvendigt at måle selve cellekontraktilfunktionen, når man screener potentielle lægemiddelkandidater.
I erkendelse af behovet for værktøjer til at studere cellulær kontraktil kraft er der udviklet flere kvantitative sammentrækningsassaymetoder af akademiske forskere, herunder trækkraftmikroskopi (TFM)6, mikromønstret TFM7, flydende gelassays8 og elastomeriske mikropostassays9. Disse teknologier er blevet brugt i enkeltskålsformat såvel som multi-well-plate-format i adskillige undersøgelser og er endda blevet foreslået til tredimensionelle kraftmålinger10,11,12,13,14. Mens disse teknologier har muliggjort banebrydende forskning inden for det ekspansive område af cellekraftbiologi, har de alle stort set været begrænset til laboratorier, der besidder specifikke evner og ressourcer, især: evne til at fremstille TFM-substrater, evne til korrekt at anvende komplekse og ikke-intuitive algoritmer til at løse TFM-forskydningskort og relativt præcise mikroskopisystemer, der kan registrere billeder taget før og efter prøvefjernelse fra scenen (til celledisociation). For en uuddannet forsker kan adgangsbarrieren for at anvende disse metoder således være ret høj i betragtning af det omfattende sæt krav til anvendelse af disse teknologier. Derudover kan den billedopløsning, der kræves for mange eksisterende teknologier (40x mål eller derover), betydeligt begrænse eksperimentel gennemstrømning, mens bulkmålingsteknologier kan maskere bidrag fra afvigende celler og forhindre opdagelse af mildere kontraktile forskelle. Det bemærkes, så vidt forfatterne ved, at kun den lave gennemstrømning og semi-kvantitative flydende gelassay-tilgang er modnet tilstrækkeligt til at blive tilgængelig for forskere (se figur 1).
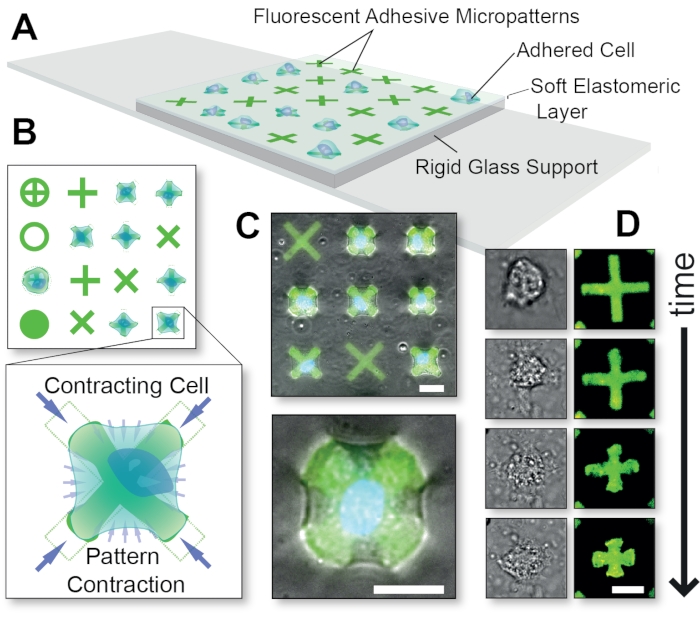
Figur 1: Overordnet skematisk oversigt over FLECS-teknologimetoden. (A) Celler klæbes til klæbende proteinmikromønstre, der er kovalent indlejret i et tyndt elastomerisk lag understøttet af glas. (B) Top-view af forskellige mulige mikromønsterformer og en sprængning af en celle, der kontraherer en »X«-formet mikromønster. (C) Overlejring af fluorescerende mikromønstre og fasekontrastbilleder af en kontraherende celle. (D) Tidsforløbsbilleder af en enkelt kontraherende celle. Skalastænger = 25 μm. Denne figur blev tilpasset med tilladelse fra Pushkarsky et al15. Klik her for at se en større version af denne figur.
Efter de seneste fremskridt inden for mikroteknologi udviklede forfatterne en mikropladebaseret teknologi, der muliggør kvantitative målinger af enkeltcellekontraktion i hundredtusinder af celler kaldet FLECS (fluorescerende mærkede elastomeriske kontraktbare overflader)15,16,17,18,19,20 , som et alternativ til TFM. I denne tilgang er fluorescerende proteinmikromønstre indlejret i bløde film, der deformeres og krymper, når celler anvender trækkraft på dem på en intuitiv og målbar måde. Det er vigtigt, at proteinmikromønstrene begrænser celleposition, form og spredningsområde, hvilket fører til ensartede testbetingelser. Disse tillader enkle målinger, der kun er baseret på deres dimensionelle ændringer, som er meget løst rumligt, selv i 4x forstørrelsesbilleder. Metoden omfatter et browserbaseret billedanalysemodul og muliggør enkel analyse af kontraktil cellekraft uden at kræve delikate håndteringsprocedurer eller registrering af tillidsmarkører, således at den bør kunne betjenes af enhver forsker med en grundlæggende cellekulturfacilitet og simpelt fluorescerende mikroskop med lav forstørrelse (figur 2 ). Denne teknologi, som er hyldeklar og kommercielt tilgængelig, blev designet med slutbrugeren i tankerne og har til formål at reducere adgangsbarrieren for enhver laboratorieforsker til at studere cellulær kraftbiologi.

Figur 2: Skematisk oversigt over pladeformatet med 24 brønde til enkeltcellekontraktilitetsassayet. Dette format blev brugt i de eksperimenter, der er beskrevet heri og afbildet i videodelen af artiklen. Skalabjælker = 25 μm. Klik her for at se en større version af dette tal.
I dette arbejde præsenterer vi en protokol til anvendelse af FLECS Technology-platformens 24 brøndpladeformat for at kvantificere virkningerne af kraftmodulerende lægemidler på cellulær kontraktilitet i primære blæreglatmuskelceller. Denne protokol til generelle formål kan tilpasses og ændres efter behov for at tage højde for forskellige andre tidsskalaer, celletyper og behandlingsbetingelser af interesse og skaleres til at besvare andre spørgsmål i gældende biologi.
Protocol
Representative Results
Discussion
Denne forenklede metode til kvantitativt at måle sammentrækning i hundredtusinder af celler ad gangen under forskellige behandlingsbetingelser og kun ved hjælp af standardmikroskopiinstrumenter giver et tilgængeligt alternativ til traditionel TFM for forskere til at studere cellulær kraftbiologi. Fordi den præsenterede teknologi giver en visuel visning af cellekontraktion ved at analysere ændringer i regelmæssigt formede fluorescerende mikromønstre, forstås størrelsen af sammentrækningen produceret af en given celle intuitivt – jo mindre mikromønsteret er, desto større er den kontraktile kraft, der udøves af cellen.
Især ved at tilbyde kontrol over faktorer som form, spredningsområde og vedhæftningsmolekyle, der omfatter mikromønstrene (alle faktorer, der vides at regulere cellekontraktilitet22,23,24), eliminerer den præsenterede teknologi systematisk yderligere variabler, der kan forvirre fortolkninger af cellekontraktionsundersøgelser.
I dette eksperiment blev der anvendt 10 kPa stivhed i gelen, og der blev anvendt et mikromønster på 70 μm (diagonal længde) bestående af type IV kollagen. Udover disse parametre kan klæbemiddelmolekylet erstattes med forskellige kollagener, fibronectin, gelatine og anden ekstracellulær matrix (ECM). Gelens stivhed kan indstilles ned til 0,1 kPa og op i MPa-området. Mikromønstergeometrien kan designes de novo til at være enhver form med minimal funktionsstørrelse på ~ 5 μm. Disse parametre er afkoblet og kan uafhængigt optimeres til en bestemt biologisk sammenhæng.
Denne teknologi er blevet grundigt valideret til at være kompatibel med stærkt klæbende og kontraktile celletyper af en mesenkymal fænotype, herunder forskellige glatte muskelcelletyper (primær human blære, tarm, trakeal, bronchial, livmoder, aorta og arteriel), mesenkymale stamceller og deres differentierede afkom, forskellige fibroblaster (lunge, dermal og hjerte), myofibroblaster og endotelceller. Derudover vil monocytafledte makrofager også producere stor målbar fagocytisk kraft på mikromønstrene, især hvis mikromønsteret består af et kendt opsonin. Forskellige kræftlinjer kan også analyseres ved hjælp af metoden.
Metoden kan give nogle udfordringer for brugen med celler, der enten er relativt små, såsom T-celler og neutrofiler, eller celletyper med en overvejende epitelfænotype. Hovedårsagen til dette er, at metoden er afhængig af stærk vedhæftning og fuldstændig spredning af celler over mikromønsteret for at generere det målbare kontraktile signal. Celler, der binder svagt, binder sig til hinanden eller ikke spredes fuldstændigt, vil ikke producere målbare kontraktile signaler. Denne adfærd, som er relativt sjælden, kan afbødes ved at justere mikromønsterstørrelsen til at være mindre eller ved at anvende alternative klæbemiddelmolekyler i mikromønstrene, der bedre fremmer vedhæftning og spredning i disse celler.
Brugere af teknologien skal omhyggeligt evaluere forskellige mulige cellekulturmedieformuleringer for deres særlige celletype af interesse, da forskellige komponenter, vækstfaktorer, serumniveauer og pH-følsomheder kan drive variabel adfærd i forskellige celler. Optimering af protokollen bør gå forud for skalering af eventuelle eksperimentelle arbejdsgange, og mediekomponenter skal altid være friske, sterile og i overensstemmelse med tidligere batches.
I sidste ende, hvis enkeltcelleopløsning ikke er nødvendig for en brugers mål, eller hvis målcelletypen har minimal spredningskapacitet, kan traditionel TFM være lige så eller mere egnet til sådanne eksperimenter. Forfatternes mål og håb er, at dette værktøj giver en ekstra mulighed for cellebiologer til at studere cellulær sammentrækning, især i forbindelse med automatiserede fænotypiske lægemiddelskærme med høj gennemstrømning.
Specifikt for fremtidige anvendelser i lægemiddelskærme kan der anvendes plader med højere gennemstrømning såsom en FLECS-plade med 384 brønde. I sådanne plader kan 4x mål på mange mikroskoper fange en hel enkelt brønd i deres synsfelt, hvilket sikrer, at alle cellulære kontraktile reaktioner fanges. Ved at bruge et billedbehandlingssystem med høj gennemstrømning kan en hel plade med 384 brønde afbildes på cirka 5 minutter, hvilket gør dette system dramatisk hurtigere end andre muligheder og derfor velegnet til fænotypisk lægemiddelopdagelse med høj gennemstrømning. Faktisk kører forfatterne rutinemæssigt ugentlige lægemiddelskærme på ~ 50 384-brøndplader (i alt mere end 19.000 brønde) ved hjælp af automatisering.
Divulgazioni
The authors have nothing to disclose.
Acknowledgements
Laboratoriearbejdet blev udført med støtte fra UCLA Molecular Shared Screening Resource (MSSR), hvor Forcyte sponsorerer forskningsaktiviteter, og Magnify Incubator ved California NanoSystems Institute (CNSI), hvor Forcyte Biotechnologies, Inc. er et hjemmehørende selskab. Forfatterne vil give adgang til Biodock.ai FLECS-analysemodulet til alle akademiske forskere efter anmodning. L.H. og I.P. bidrog ligeligt til dette arbejde.
Materials
| Bladder smooth muscle cell culture | Sciencell | #4310 | |
| Blebbistatin | Sigma-Aldrich | B0560 | |
| Cell culture media | Thermofisher | 11765054 | Ham's F12 medium supplemented with 10% FBS and 1% p/s |
| Cell strainer | Fisher Scientific | 7201432 | |
| Conical Tube | Fisher Scientific | 05-539-13 | |
| Culture flask | Fisher Scientific | FB012941 | |
| Cytochalasin D | Sigma-Aldrich | C8273 | |
| DMSO (Dimethyl sulfoxide) | Fisher Scientific | D1284 | |
| Eppendorf tubes | Fisher Scientific | 05-402-31 | |
| Fluorescent microscope | Molecular Devices | ImageXpress Confocal | |
| Forcyte-manufactured 24-well plate | Forcyte Biotechnologies | 24-HC4R-X1-QB12 | |
| Hoescht 3342 Live Nuclear Stain | Thermofisher | 62249 | |
| Phosphate Buffered Saline (PBS) | Fisher Scientific | BP39920 |
Riferimenti
- Ohama, T., Hori, M., Ozaki, H. Mechanism of abnormal intestinal motility in inflammatory bowel disease: How smooth muscle contraction is reduced. Journal of Smooth Muscle Research. 43 (2), 43-54 (2007).
- Peyronnet, B., et al. A comprehensive review of overactive bladder pathophysiology: On the way to tailored treatment. European Urology. 75 (6), 988-1000 (2019).
- Aldamanhori, R., Osman, N. I., Chapple, C. R. Underactive bladder: Pathophysiology and clinical significance. Asian Journal of Urology. 5 (1), 17-21 (2018).
- Sanderson, M. J., Delmotte, P., Bai, Y., Perez-Zogbhi, J. F. Regulation of airway smooth muscle cell contractility by Ca2+ signaling and sensitivity. Proceedings of the American Thoracic Society. 5 (1), 23-31 (2008).
- Brozovich, F. V., et al. Mechanisms of vascular smooth muscle contraction and the basis for pharmacologic treatment of smooth muscle disorders. Pharmacological Reviews. 68 (2), 476-532 (2016).
- Munevar, S., Wang, Y., Dembo, M. Traction force microscopy of migrating normal and H-ras transformed 3T3 fibroblasts. Biophysical Journal. 80 (4), 1744-1757 (2001).
- Tseng, Q., et al. A new micropatterning method of soft substrates reveals that different tumorigenic signals can promote or reduce cell contraction levels. Lab on a Chip. 11 (13), 2231-2240 (2011).
- Bell, E., Ivarsson, B., Merrill, C. Production of a tissue-like structure by contraction of collagen lattices by human fibroblasts of different proliferative potential in vitro. Proceedings of the National Academy of Sciences. 76 (3), 1274-1278 (1979).
- Tan, J. L., et al. Cells lying on a bed of microneedles: an approach to isolate mechanical force. Proceedings of the National Academy of Sciences. 100 (4), 1484-1489 (2003).
- Rokhzan, R., et al. high-throughput measurements of cell contraction and endothelial barrier function. Laboratory Investigation. 99 (1), 138-145 (2019).
- Park, C. Y., et al. High-throughput screening for modulators of cellular contractile force. Integrative Biology. 7 (10), 1318-1324 (2015).
- Kaylan, K. B., Kourouklis, A. P., Underhill, G. H. A high-throughput cell microarray platform for correlative analysis of cell differentiation and traction forces. Journal of Visualized Experiments. (121), e55362 (2017).
- Huang, Y., et al. Traction force microscopy with optimized regularization and automated Bayesian parameter selection for comparing cells. Scientific Reports. 9, 539 (2019).
- Franck, C., Maskarinec, S. A., Tirrell, D. A., Ravichandran, G. Three-dimensional traction force microscopy: A new tool for quantifying cell-matrix interactions. PLOS ONE. 6, 17833 (2011).
- Pushkarsky, I., et al. Elastomeric sensor surfaces for high-throughput single-cell force cytometry. Nature Biomedical Engineering. 2 (2), 124-137 (2018).
- Pushkarsky, I. FLECS technology for high-throughput single-cell force biology and screening. ASSAY and Drug Development Technologies. 16 (1), 7-11 (2017).
- Koziol-White, C. J., et al. Inhibition of PI3K promotes dilation of human small airways in a rho kinase-dependent manner. British Journal of Pharmacology. 173 (18), 2726-2738 (2016).
- Orfanos, S., et al. Obesity increases airway smooth muscle responses to contractile agonists. American Journal of Physiology-Lung Cellular and Molecular Physiology. 315 (5), 673-681 (2018).
- Tseng, P., Pushkarsky, I., Carlo, D. D. Metallization and biopatterning on ultra-flexible substrates via dextran sacrificial layers. PLOS ONE. 9, 106091 (2014).
- Yoo, E. J., et al. Gα12 facilitates shortening in human airway smooth muscle by modulating phosphoinositide 3-kinase-mediated activation in a RhoA-dependent manner. British Journal of Pharmacology. 174 (4), 4383-4395 (2017).
- MacGlashan, D., Vilariño, N. Polymerization of actin does not regulate desensitization in human basophils. Journal of Leukocyte Biology. 85 (4), 627-637 (2009).
- Hocking, D. C., Sottile, J., Langenbach, K. J. Stimulation of integrin-mediated cell contractility by fibronectin polymerization. Journal of Biological Chemistry. 275 (14), 10673-10682 (2000).
- Tolić-Nørrelykke, I. M., Wang, N. Traction in smooth muscle cells varies with cell spreading. Journal of Biomechanics. 38 (7), 1405-1412 (2005).
- Ye, G. J. C., et al. The contractile strength of vascular smooth muscle myocytes is shape dependent. Integrative Biology. 6 (2), 152-163 (2014).

