Forenklet, høygjennomstrømningsanalyse av encellet kontraktilitet ved hjelp av mikropatternede elastomerer
Summary
Dette arbeidet presenterer en fleksibel protokoll for bruk av fluorescerende merket elastomerisk kontraktable overflater (FLECS) Teknologi i mikrowellformat for forenklet, hands-off kvantifisering av encellede kontraktilkrefter basert på visualiserte forskyvninger av fluorescerende proteinmikropatterner.
Abstract
Cellulær kontraktil kraftgenerering er et grunnleggende trekk som deles av praktisk talt alle celler. Disse kontraktile kreftene er avgjørende for riktig utvikling, fungerer både på cellulært og vevsnivå, og regulerer de mekaniske systemene i kroppen. Tallrike biologiske prosesser er kraftavhengige, inkludert motilitet, vedheft og oppdeling av enkeltceller, samt sammentrekning og avslapning av organer som hjerte, blære, lunger, tarmer og livmor. Gitt sin betydning for å opprettholde riktig fysiologisk funksjon, kan cellulær kontraktilitet også drive sykdomsprosesser når overdrevet eller forstyrret. Astma, hypertensjon, preterm labor, fibrotisk arrdannelse og underaktiv blære er alle eksempler på mekanisk drevne sykdomsprosesser som potensielt kan lindres med riktig kontroll av cellulær kontraktil kraft. Her presenterer vi en omfattende protokoll for bruk av en ny mikroplatebasert kontraktilitetsanalyseteknologi kjent som fluorescerende merket elastomeriske kontraktbare overflater (FLECS), som gir forenklet og intuitiv analyse av encellet kontraktilitet på en massivt skalert måte. Heri gir vi en trinnvis protokoll for å oppnå to sekspunkts doseresponskurver som beskriver effekten av to kontraktile hemmere på sammentrekning av primære menneskelige blære glatte muskelceller i en enkel prosedyre ved hjelp av bare en enkelt FLECS analysemikroplate, for å demonstrere riktig teknikk for brukere av metoden. Ved hjelp av FLECS Technology får alle forskere med grunnleggende biologiske laboratorier og fluorescerende mikroskopisystemer tilgang til å studere denne grunnleggende, men vanskelig å kvantifisere funksjonelle cellefenotypen, og effektivt senke inngangsbarrieren innen kraftbiologi og fenotypisk screening av kontraktil cellekraft.
Introduction
Cellegenererte mekaniske krefter er avgjørende for at de skal fungere riktig i ulike organer i hele kroppen, for eksempel tarmene, blæren, hjertet og andre. Disse organene må generere stabile mønstre for cellekontraksjon og avslapning for å opprettholde den indre homeostatiske tilstanden. Unormal glatt muskelcelle (SMC) sammentrekning kan føre til utbruddet av ulike lidelser, inkludert for eksempel intestinal dysmotility, preget av unormale mønstre av tarm glatt muskelkontraksjon1, samt de urologiske forholdene til overaktiv2 eller underaktiv blære3. Innenfor luftveiene kan SMB-er som har uregelmessige sammentrekningsmønstre utløse astmatisk hyperresponsivitet4, potensielt stramme luftveiene og redusere oksygenstrømmen inn i lungene. En annen utbredt fysisk tilstand, hypertensjon, er forårsaket av svingninger i den glatte muskelsammentrekningen i blodårene5. Det er klart at kontraktile mekanismer i celler og vev kan føre til sykdommer som krever behandlingsalternativer. Ettersom disse forholdene umiskjennelig stammer fra cellenes dysfunksjonelle kontraktile oppførsel, blir det logisk og nødvendig å måle selve cellekontraktilfunksjonen når du screener potensielle narkotikakandidater.
Ved å erkjenne behovet for verktøy for å studere cellulær sammentrekningskraft, er flere kvantitative sammentrekningsanalysemetoder utviklet av akademiske forskere, inkludert trekkraftmikroskopi (TFM)6, mikropatterned TFM7, flytende gelanalyser8 og elastomeriske mikropostanalyser9. Disse teknologiene har blitt brukt i enkeltrettsformat samt multi-well-plate format i mange studier og har til og med blitt foreslått for tredimensjonale kraftmålinger10,11,12,13,14. Selv om disse teknologiene har gjort det mulig for banebrytende forskning innen det ekspansive feltet cellekraftbiologi, har de alle i stor grad vært begrenset til laboratorier som har spesifikke evner og ressurser, spesielt: evne til å fremstille TFM-substrater, evne til å bruke komplekse og ikke-intuitive algoritmer riktig for å løse TFM-forskyvningskart, og relativt presise mikroskopisystemer som kan registrere bilder tatt før og etter prøvefjerning fra scenen (for celledissosiasjon). For en utrent forsker kan derfor inngangsbarrieren for å bruke disse metodene være ganske høy gitt det omfattende settet med krav for å bruke disse teknologiene. I tillegg kan bildeoppløsningen som kreves for mange eksisterende teknologier (40x mål eller høyere), begrense eksperimentell gjennomstrømning betydelig, mens massemålingsteknologier kan maskere bidrag fra ytre celler og forhindre oppdagelse av mildere kontraktilforskjeller. Vær oppmerksom på at så vidt forfatterne er klar over, er det bare lavgjennomstrømningen og den semi-kvantitative flytende gelanalysetilnærmingen som har modnet tilstrekkelig til å bli tilgjengelig for forskere (se figur 1).
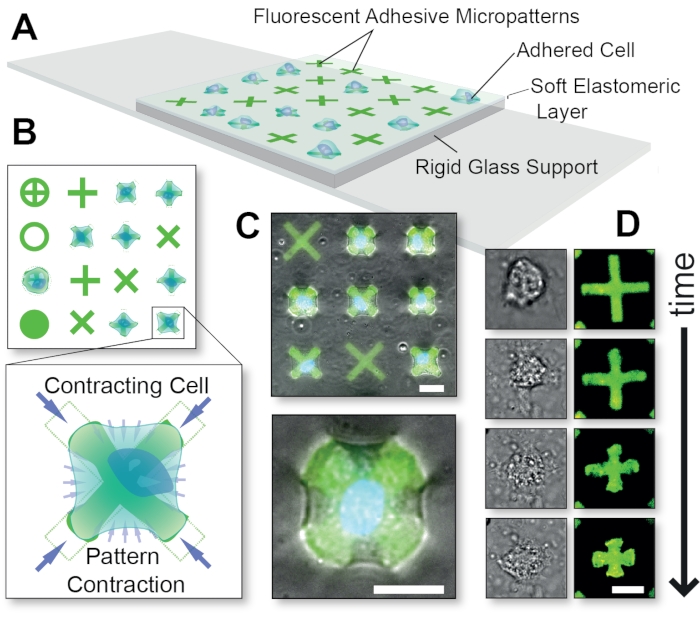
Figur 1: Samlet skjematisk for FLECS Technology-metoden. (A) Celler følges av limproteinmikropatterner som er kovalent innebygd i et tynt elastomerisk lag støttet av glass. (B) Toppvisning av ulike mulige mikropatternformer og en oppblåsning av en celle som trekker sammen en “X”-formet mikropattern. (C) Overlegg av fluorescerende mikropatterner og fasekontrastbilder av en kontraherende celle. (D) Tidsforløpbilder av en enkelt kontraherende celle. Skalastenger = 25 μm. Denne figuren ble tilpasset med tillatelse fra Pushkarsky et al15. Klikk her for å se en større versjon av denne figuren.
Etter nylige fremskritt innen mikroteknologi utviklet forfatterne en mikroplatebasert teknologi som muliggjør kvantitative målinger av encellet sammentrekning i hundretusenvis av celler kalt FLECS (fluorescerende merket elastomeriske kontraktbare overflater)15,16,17,18,19,20 , som et alternativ til TFM. I denne tilnærmingen er fluorescerende proteinmikropatterner innebygd i myke filmer som deformerer og krymper når celler bruker trekkraftkrefter på dem, på en intuitiv og målbar måte. Det er viktig at proteinmikropatternene begrenser celleposisjon, form og spredningsområde, noe som fører til ensartede testforhold. Disse tillater enkle målinger basert bare på deres dimensjonale endringer, som er svært løst romlig selv i 4x forstørrelsesbilder. Metoden inkluderer en nettleserbasert bildeanalysemodul og muliggjør enkel analyse av kontraktilcellekraft uten å kreve delikate håndteringsprosedyrer eller registrering av fiduciary markører, slik at den skal fungere av enhver forsker med et grunnleggende cellekulturanlegg og enkelt fluorescerende mikroskop med lav forstørrelse (figur 2 ). Denne teknologien, som er hylleklar og kommersielt tilgjengelig, ble designet med sluttbrukeren i tankene og tar sikte på å redusere inngangsbarrieren for enhver laboratorieforsker for å studere cellulær kraftbiologi.

Figur 2: Skjematisk for 24-brønns plateformatet for encellet kontraktilitetsanalyse. Dette formatet ble brukt i eksperimentene beskrevet heri og avbildet i videodelen av artikkelen. Skalastenger = 25 μm. Klikk her for å se en større versjon av denne figuren.
I dette arbeidet presenterer vi en protokoll for å bruke 24 brønnplateformatet til FLECS Technology-plattformen for å kvantifisere effekten av kraftmodulerende legemidler på cellulær kontraktilitet i primære blære glatte muskelceller. Denne generelle protokollen kan tilpasses og modifiseres etter behov for å ta hensyn til ulike andre tidsskalaer, celletyper og behandlingsbetingelser av interesse, og skaleres for å svare på andre spørsmål i kraftbiologi.
Protocol
Representative Results
Discussion
Denne forenklede metoden for kvantitativt å måle sammentrekning i hundretusenvis av celler om gangen under ulike behandlingsforhold og bruk av bare standard mikroskopiinstrumenter gir et tilgjengelig alternativ til tradisjonell TFM for forskere å studere cellulær kraftbiologi. Fordi den presenterte teknologien gir en visuell visning av cellekontraksjon ved å analysere endringer i regelmessig formede fluorescerende mikropatterner, er størrelsen på sammentrekningen produsert av en gitt celle intuitivt forstått – jo mindre mikropattern, desto større er kontraktilkraften som utøves av cellen.
Spesielt ved å tilby kontroll over faktorer som form, spredningsområde og vedheftsmolekyl som består av mikropatternene (alle faktorer som er kjent for å regulere cellekontraktilitet22,23,24), eliminerer den presenterte teknologien systematisk ytterligere variabler som kan forvirre tolkninger av cellekontraksjonsstudier.
I dette eksperimentet ble 10 kPa stivhet brukt i gelen og en 70 μm (diagonal lengde) mikropattern ble brukt bestående av type IV kollagen. I tillegg til disse parametrene kan limmolekylet erstattes med ulike kollagener, fibronektin, gelatin og annen ekstracellulær matrise (ECM). Gelens stivhet kan stilles ned til 0,1 kPa, og opp i MPa-serien. Mikropatterngeometrien kan utformes de novo til å være en hvilken som helst form med minimal funksjonsstørrelse på ~ 5 μm. Disse parametrene er frakoplet og kan optimaliseres uavhengig for en bestemt biologisk kontekst.
Denne teknologien har blitt grundig validert for å være kompatibel med svært klebende og kontraktile celletyper av en mesenchymal fenotype, inkludert ulike glatte muskelcelletyper (primær menneskelig blære, tarm-, trakeal-, bronkial-, livmor-, aorta- og arteriell), mesenchymale stamceller og deres differensierte avkom, ulike fibroblaster (lunge-, dermal- og hjerte-), myofibroblaster og endotelceller. I tillegg vil monocytt-avledede makrofager også produsere stor målbar fagocytisk kraft på mikropatternene, spesielt hvis mikropattern består av et kjent opsonin. Ulike kreftlinjer kan også analyses ved hjelp av metoden.
Metoden kan utgjøre noen utfordringer for bruk med celler som enten er relativt små som T-celler og nøytrofiler, eller celletyper med en overveiende epitel fenotype. Hovedårsaken til dette er at metoden er avhengig av sterk vedheft og fullstendig spredning av celler over mikropatternet for å generere det målbare kontraktilsignalet. Celler som binder seg svakt, binder seg til hverandre eller ikke sprer seg helt, vil ikke produsere målbare kontraktilsignaler. Disse atferdene, som er relativt sjeldne, kan reduseres ved å justere mikropatternstørrelsen for å være mindre, eller ved å bruke alternative limmolekyler i mikropatternene som bedre vil fremme vedheft og spredning i disse cellene.
Brukere av teknologien må nøye vurdere forskjellige mulige cellekulturelle middels formuleringer for deres spesielle celletype, da forskjellige komponenter, vekstfaktorer, serumnivåer og pH-følsomheter kan drive variabel oppførsel i forskjellige celler. Optimalisering av protokollen bør komme før skalering av eksperimentelle arbeidsflyter, og mediekomponenter bør alltid være friske, sterile og i samsvar med tidligere grupper.
Til syvende og sist, hvis encellet oppløsning ikke er nødvendig for en brukers mål, eller hvis målcelletypen har minimal spredningskapasitet, kan tradisjonell TFM være like eller mer egnet for slike eksperimenter. Forfatternes mål og håp er at dette verktøyet gir en ekstra mulighet for cellebiologer til å studere cellulær sammentrekning, spesielt i sammenheng med automatiserte høygjennomstrømning fenotypiske narkotikaskjermer.
Høyere gjennomstrømningsplater som en 384-brønns FLECS-plate kan brukes spesielt for fremtidig bruk i legemiddelskjermer. I slike plater kan 4x mål på mange mikroskoper fange en hel brønn i sitt synsfelt, og sikre at alle cellulære kontraktilresponser fanges opp. Ved å bruke et bildesystem med høy gjennomstrømning kan en hel 384-brønnsplate avbildes på ca. 5 minutter, noe som gjør dette systemet dramatisk raskere enn andre alternativer, og derfor egnet for høygjennomstrømning fenotypisk legemiddeloppdagelse. Faktisk kjører forfatterne rutinemessig ukentlige narkotikaskjermer på ~ 50 384 brønnplater (totalt mer enn 19.000 brønner) ved hjelp av automatisering.
Divulgazioni
The authors have nothing to disclose.
Acknowledgements
Laboratoriearbeidet ble utført med støtte fra UCLA Molecular Shared Screening Resource (MSSR) hvor Forcyte sponser forskningsaktiviteter, og Magnify Incubator ved California NanoSystems Institute (CNSI), hvor Forcyte Biotechnologies, Inc. er et hjemmehørende selskap. Forfatterne vil gi tilgang til Biodock.ai FLECS analysemodul til alle akademiske forskere på forespørsel. L.H. og I.P. bidro likt til dette arbeidet.
Materials
| Bladder smooth muscle cell culture | Sciencell | #4310 | |
| Blebbistatin | Sigma-Aldrich | B0560 | |
| Cell culture media | Thermofisher | 11765054 | Ham's F12 medium supplemented with 10% FBS and 1% p/s |
| Cell strainer | Fisher Scientific | 7201432 | |
| Conical Tube | Fisher Scientific | 05-539-13 | |
| Culture flask | Fisher Scientific | FB012941 | |
| Cytochalasin D | Sigma-Aldrich | C8273 | |
| DMSO (Dimethyl sulfoxide) | Fisher Scientific | D1284 | |
| Eppendorf tubes | Fisher Scientific | 05-402-31 | |
| Fluorescent microscope | Molecular Devices | ImageXpress Confocal | |
| Forcyte-manufactured 24-well plate | Forcyte Biotechnologies | 24-HC4R-X1-QB12 | |
| Hoescht 3342 Live Nuclear Stain | Thermofisher | 62249 | |
| Phosphate Buffered Saline (PBS) | Fisher Scientific | BP39920 |
Riferimenti
- Ohama, T., Hori, M., Ozaki, H. Mechanism of abnormal intestinal motility in inflammatory bowel disease: How smooth muscle contraction is reduced. Journal of Smooth Muscle Research. 43 (2), 43-54 (2007).
- Peyronnet, B., et al. A comprehensive review of overactive bladder pathophysiology: On the way to tailored treatment. European Urology. 75 (6), 988-1000 (2019).
- Aldamanhori, R., Osman, N. I., Chapple, C. R. Underactive bladder: Pathophysiology and clinical significance. Asian Journal of Urology. 5 (1), 17-21 (2018).
- Sanderson, M. J., Delmotte, P., Bai, Y., Perez-Zogbhi, J. F. Regulation of airway smooth muscle cell contractility by Ca2+ signaling and sensitivity. Proceedings of the American Thoracic Society. 5 (1), 23-31 (2008).
- Brozovich, F. V., et al. Mechanisms of vascular smooth muscle contraction and the basis for pharmacologic treatment of smooth muscle disorders. Pharmacological Reviews. 68 (2), 476-532 (2016).
- Munevar, S., Wang, Y., Dembo, M. Traction force microscopy of migrating normal and H-ras transformed 3T3 fibroblasts. Biophysical Journal. 80 (4), 1744-1757 (2001).
- Tseng, Q., et al. A new micropatterning method of soft substrates reveals that different tumorigenic signals can promote or reduce cell contraction levels. Lab on a Chip. 11 (13), 2231-2240 (2011).
- Bell, E., Ivarsson, B., Merrill, C. Production of a tissue-like structure by contraction of collagen lattices by human fibroblasts of different proliferative potential in vitro. Proceedings of the National Academy of Sciences. 76 (3), 1274-1278 (1979).
- Tan, J. L., et al. Cells lying on a bed of microneedles: an approach to isolate mechanical force. Proceedings of the National Academy of Sciences. 100 (4), 1484-1489 (2003).
- Rokhzan, R., et al. high-throughput measurements of cell contraction and endothelial barrier function. Laboratory Investigation. 99 (1), 138-145 (2019).
- Park, C. Y., et al. High-throughput screening for modulators of cellular contractile force. Integrative Biology. 7 (10), 1318-1324 (2015).
- Kaylan, K. B., Kourouklis, A. P., Underhill, G. H. A high-throughput cell microarray platform for correlative analysis of cell differentiation and traction forces. Journal of Visualized Experiments. (121), e55362 (2017).
- Huang, Y., et al. Traction force microscopy with optimized regularization and automated Bayesian parameter selection for comparing cells. Scientific Reports. 9, 539 (2019).
- Franck, C., Maskarinec, S. A., Tirrell, D. A., Ravichandran, G. Three-dimensional traction force microscopy: A new tool for quantifying cell-matrix interactions. PLOS ONE. 6, 17833 (2011).
- Pushkarsky, I., et al. Elastomeric sensor surfaces for high-throughput single-cell force cytometry. Nature Biomedical Engineering. 2 (2), 124-137 (2018).
- Pushkarsky, I. FLECS technology for high-throughput single-cell force biology and screening. ASSAY and Drug Development Technologies. 16 (1), 7-11 (2017).
- Koziol-White, C. J., et al. Inhibition of PI3K promotes dilation of human small airways in a rho kinase-dependent manner. British Journal of Pharmacology. 173 (18), 2726-2738 (2016).
- Orfanos, S., et al. Obesity increases airway smooth muscle responses to contractile agonists. American Journal of Physiology-Lung Cellular and Molecular Physiology. 315 (5), 673-681 (2018).
- Tseng, P., Pushkarsky, I., Carlo, D. D. Metallization and biopatterning on ultra-flexible substrates via dextran sacrificial layers. PLOS ONE. 9, 106091 (2014).
- Yoo, E. J., et al. Gα12 facilitates shortening in human airway smooth muscle by modulating phosphoinositide 3-kinase-mediated activation in a RhoA-dependent manner. British Journal of Pharmacology. 174 (4), 4383-4395 (2017).
- MacGlashan, D., Vilariño, N. Polymerization of actin does not regulate desensitization in human basophils. Journal of Leukocyte Biology. 85 (4), 627-637 (2009).
- Hocking, D. C., Sottile, J., Langenbach, K. J. Stimulation of integrin-mediated cell contractility by fibronectin polymerization. Journal of Biological Chemistry. 275 (14), 10673-10682 (2000).
- Tolić-Nørrelykke, I. M., Wang, N. Traction in smooth muscle cells varies with cell spreading. Journal of Biomechanics. 38 (7), 1405-1412 (2005).
- Ye, G. J. C., et al. The contractile strength of vascular smooth muscle myocytes is shape dependent. Integrative Biology. 6 (2), 152-163 (2014).

