Tipo de fibra e análise subcelular-específica do conteúdo de gotícula lipídica no músculo esquelético
Summary
Evidências crescentes indicam que a infiltração excessiva de lipídios dentro do músculo esquelético resulta em lipotoxicidade e diabetes. Aqui, apresentamos um protocolo completo, incluindo processamento de tecidos, coloração com Bodipy, aquisição de imagens e análise, para quantificar o tamanho, densidade e distribuição subcelular de gotículas lipídicas de forma específica do tipo fibra.
Abstract
A infiltração de lipídios musculares esqueléticos, conhecida como micosteatose, aumenta com obesidade e envelhecimento. A miostetose também foi descoberta recentemente como um fator prognóstico negativo para vários outros transtornos, como doenças cardiovasculares e câncer. A infiltração excessiva de lipídios diminui a massa e a força muscular. Também resulta em lipotoxicidade e resistência à insulina, dependendo do teor total de lipídio intramialcelular, morfologia de gotícula lipídica (LD) e distribuição subcelular. O tipo de fibra (oxidativo versus glicolítico) também é importante, uma vez que as fibras oxidativas têm maior capacidade de utilizar lipídios. Devido às suas implicações cruciais na fisiopatologia, estudos aprofundados sobre a dinâmica ld e função de forma específica do tipo de fibra são justificados.
Aqui, é apresentado um protocolo completo para a quantificação do conteúdo lipídudo intramyocelular e análise da morfologia LD e distribuição subcelular de forma específica do tipo de fibra. Para isso, as crioseções musculares em série foram manchadas com o corante fluorescente Bodipy e anticorpos contra isoformas de cadeia pesada de miosina. Este protocolo permite o processamento simultâneo de diferentes músculos, economizando tempo e evitando possíveis artefatos e, graças a uma macro personalizada criada em Fiji, a automatização da análise LD também é possível.
Introduction
A infiltração de lipídios musculares esqueléticos, conhecida como micosteatose, aumenta com obesidade e envelhecimento. A miostetose está negativamente correlacionada com massa muscular e força e com sensibilidade à insulina1. Além disso, estudos recentes indicam que o grau de mostetose poderia ser usado como fator prognóstico para outras condições como doença cardiovascular2, doença hepática gordurosa não alcoólica3 ou câncer4. Lipídios podem se acumular no músculo esquelético entre as fibras musculares como lipídios extramyocelulares ou dentro das fibras, como lipídios intramyocelulares (IMCLs). Os IMCLs são predominantemente armazenados como triglicérides em gotículas lipídicas (LDs) que são usadas como combustível metabólico durante o exercício físico 5,6. No entanto, quando a oferta lipídica excede a demanda, ou quando as mitocôndrias se tornarem disfuncionais, os IMCLs serão implicados na resistência à insulina muscular, como visto em indivíduos metabolicamente insalubres, obesos e em pacientes com diabetes tipo 27. Curiosamente, os atletas de resistência têm níveis semelhantes, se não mais elevados, de IMCLs aos encontrados em pacientes obesos com diabetes mellitus tipo 2, mantendo alta sensibilidade à insulina. Esse fenômeno é descrito como o “paradoxo do atleta”8,9, e é explicado por uma avaliação mais matizada de LDs musculares, relacionadas ao seu tamanho, densidade, localização, dinâmica e composição de espécies lipídicas.
Primeiro, o tamanho do LD está inversamente correlacionado à sensibilidade à insulina e ao condicionamento físico10,11. De fato, LDs menores exibem uma área de superfície relativamente maior para a ação de lipase e, portanto, potencialmente têm maior capacidade de mobilizar lipídios12. Em segundo lugar, a densidade LD (número/superfície) desempenha um papel controverso na ação de insulina 8,10; ainda, parece ser aumentado em atletas. Em terceiro lugar, a localização subcelular de LDs é importante, uma vez que os LDs localizados logo abaixo da membrana superficial (subsarcolemmal ou periférico) exercem um efeito mais deletério sobre a sensibilidade à insulina do que os centrais 8,9,13. Estas últimas fornecem combustível para mitocôndrias centrais, que possuem maior atividade respiratória e são mais especializadas para atender à alta demanda energética necessária para a contração14. Em contrapartida, os LDs periféricos fornecem mitocôndrias subsarcolemmal, que estão envolvidas nos processos relacionados à membrana8. Finalmente, além dos triglicérides, lipídios complexos específicos dentro do músculo podem ser mais deletérios do que outros. Por exemplo, diaciglicerol, acicl-CoA de cadeia longa e ceramidas podem se acumular em músculos quando a taxa de rotatividade de triglicérides é baixa, prejudicando assim a sinalização de insulina 9,15. Voltando ao “paradoxo do atleta”, os atletas de resistência têm um alto número de LDs centrais menores com taxas de rotatividade elevadas nas fibras tipo I (oxidativa), enquanto pacientes obesos e diabéticos têm LDs periféricos maiores com baixas taxas de rotatividade nas fibras tipo II (glicolítico) 8,15,16. Além de seu papel no armazenamento e liberação de energia, os LDs via ácidos graxos derivados (FA) e uma proteína de casaco (perilipin 5) também poderiam funcionar como atores críticos envolvidos na regulação transcricional da oxidação da FA e biogênese mitocondrial8. Devido às suas implicações cruciais na fisiologia e na fisiopatologia, estudos aprofundados sobre dinâmicas e funções de LDs são justificados.
Embora existam várias técnicas para estudar IMCLs, elas não são todas adequadas para quantificar com precisão o tamanho, a densidade e a distribuição de LD de forma específica. Por exemplo, a avaliação de IMCLs por espectroscopia de ressonância magnética, embora não invasiva, oferece um nível de resolução que não é suficiente para estudar o tamanho e a localização precisa de LDs dentro da fibra, e não é específica do tipo fibra 17,18. Da mesma forma, técnicas bioquímicas realizadas em homogeneizadores muscularesinteiros 19 não podem avaliar a localização e o tamanho dos lipídios. Consequentemente, o método mais adequado para analisar a morfologia e localização de LD é a microscopia eletrônica de transmissão quantitativa13, mas essa técnica é cara e demorada. Portanto, a fluorescência confocal em preparações com corantes como Oil Red O (ORO)20,21, monodansylpentane (MDH)22, ou Bodipy 23,24,25, emergiu como a melhor ferramenta para esses estudos.
Aqui, é descrito um protocolo completo, incluindo amostragem e processamento de tecidos, coloração bodipy e aquisição e análise de imagem confocal para quantificar o tamanho, o número e a localização de LD em crioseções musculares de camundongos. Uma vez que as IMCLs não são distribuídas uniformemente entre fibras oxidativas e glicolíticas, e cada tipo de fibra regula a dinâmica LD de forma diferente, o estudo das IMCLs deve ser específico do tipo fibra 16,25,26,27. Portanto, este protocolo utiliza imunofluorescência em seções seriais para identificar isoform(s) de cadeia pesada de miosina (MyHC) expressa por cada fibra. Outra vantagem deste protocolo é o processamento simultâneo de um músculo glicolítico (extensor digitorum longus, EDL) e um músculo oxidativo (soleus) colocado lado a lado antes de congelar (Figura 1). Esse processamento simultâneo não só economiza tempo, mas também evita a variabilidade devido ao processamento separado das amostras.
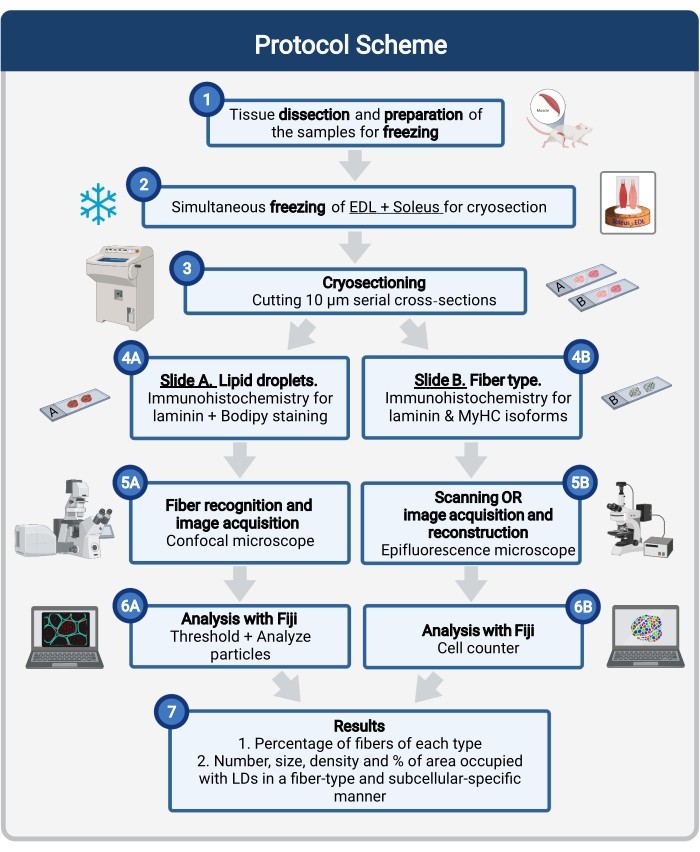
Figura 1: Visão geral do procedimento. Após dissecção muscular (1), músculos selecionados de tamanho semelhante são preparados e congelados juntos (2). Seções transversais em série de 10 μm são obtidas usando um criostat e montadas diretamente em slides de adesão (3). A partir de dois slides seriais, o primeiro (4A) é imunolabeled para laminina e manchado com Bodipy para reconhecer LDs e o segundo (4B) é imunossumado com anticorpos contra MyHCs para o reconhecimento de tipos de fibras musculares. As imagens são adquiridas usando um microscópio confocal para Bodipy (5A) e um microscópio de epifluorescência para tipos de fibras musculares (5B). As imagens são analisadas em Fiji aplicando um limiar e quantificando partículas (6A) para obter o número, tamanho médio, densidade e percentual da área total ocupada por LDs (7) ou células de contagem (6B) para obter a porcentagem de fibras de cada tipo na seção (7). Abreviaturas: LDs = gotículas lipídicas; EDL = extensor digitorum longus; MyHCs = isoforms de cadeia pesada de miosina. Clique aqui para ver uma versão maior desta figura.
Protocol
Representative Results
Discussion
O protocolo aqui detalhado descreve um método eficiente para quantificar LDs marcados com Bodipy em uma base tipo de fibra e subcelular específico. Nos últimos anos, corantes lipídicos clássicos, como ORO ou Sudan Black B, foram substituídos por uma nova matriz de corantes celulares permeáveis, lipofílicos, fluorescentes que se ligam a lipídios neutros (por exemplo, Bodipy). Disponível como diferentes conjugados, Bodipy tem se mostrado muito eficaz na marcação de LDs para estudar sua morfologia, dinâmica e i…
Divulgazioni
The authors have nothing to disclose.
Acknowledgements
Este trabalho foi apoiado por subvenções da Fonds National de la Recherche Scientifique (FNRS-Crédit de Recherche J.0022.20) e da Société Francophone du Diabète (SFD-Roche Diabetes Care).C.M.S. é o beneficiário de uma bolsa de doutorado da FRIA (FNRS). M.A.D.-L.d.C. recebeu uma bolsa do Programa internacional de Excelência Wallonie-Bruxelles.
Os autores agradecem a Alice Monnier por sua contribuição para o desenvolvimento deste protocolo e Caroline Bouzin por sua expertise e ajuda técnica no processo de aquisição de imagens. Agradecemos também à plataforma de imagem 2IP-IREC pelo acesso ao criostat e aos microscópios (2IP-IREC Imaging Platform, Institute of Experimental and Clinical Research, Université Catholique de Louvain, 1200 Bruxelas, Bélgica). Por fim, os autores gostariam de agradecer Nicolas Dubuisson, Romain Versele e Michel Abou-Samra pela crítica construtiva ao manuscrito. Algumas das figuras deste artigo foram criadas com BioRender.com.
Materials
| Equipment | |||
| AxioCam 506 mono 6 Mpix camera | Zeiss | ||
| AxioCam MRm 1.4MPix CCD camera | Zeiss | ||
| Chemical hood | Potteau Labo | EN-14175 | |
| Confocal microscope | Zeiss | LSM800 | |
| Cork discs (ø 20 mm, 3 mm thick) | Electron Microscopy Sciences | 63305 | |
| Cryo-Gloves | Tempshield | 16072252 | |
| Cryostat | Thermo Scientific | Microm Cryo Star HM 560 | |
| Dissecting Stereo Microscope SMZ745 | Nikon | ||
| Dry Ice | |||
| Dumont Forceps | F.S.T | 11295-10 | |
| Epifluorescence microscope | Zeiss | AxioImage-Apotome Z1 | |
| Extra Fine Bonn Scissors | F.S.T | 14084-08 | |
| FisherBrand Disposable Base Molds (0.7 x 0.7 cm) | ThermoFisher | 22-363-552 | Used to cut a piece to hold the muscle on the cork for freezing |
| Glass petri dish (H 25 mm, ø 150 mm) | BRAND Petri dish, MERK | BR455751 | Used to place the muscles on ice during dissection |
| ImmEdge Hydrophobic barrier PAP Pen | Vector Labs | H-4000 | Used to create an hidrophobic barrier around the muscle sections |
| Incubator | MMM Medcenter | Incucell 707 | |
| Microscope Cover Glasses (24×50 mm) | Assistent | 40990151 | |
| Microscope Slide Boxes | Kartell | 278 | Used as humid chambers for immunohistochemistry |
| Neck holder | Linie zwo | SB-035X-02 | Used as strap to hold the stainless steel tumbler |
| No 15 Sterile Carbon Steel Scalpel Blade | Swann-Morton | 0205 | |
| Paint brushes | Van Bleiswijck | Amazon B07W7KJQ2X | Used to handle cryosections |
| Permanent Marker Pen Black | Klinipath/VWR | 98307-R | Used to label slides |
| Pierce Fixation Forceps | F.S.T | 18155-13 | |
| Polystyrene Box | H 12 cm x L 25 cm x W 18 cm, used as a liquid nitrogen container and to transport the samples to the cryostat | ||
| Scalpel Handle, 125 mm (5"), No. 3 | Aesculap | BB073R | |
| Stainless Steel Cup 10oz | Eboxer | B07GFCBPFH | Tumbler to fill with isopentene for muscle freezing |
| Superfrost Ultra Plus slides | ThermoFisher | J1800AMNZ | |
| Surgical tweezers 1/2 teeth | Medische Vakhandel | 1303152 | Also called "Rat teeth tweezers" |
| Vannas Spring Scissors – 3 mm Cutting Edge | F.S.T | 15000-00 | |
| Weighing boats | VWR international | 611-2249 | |
| Whole-Slide Scanner for Fluorescence | Zeiss | Axio Scan.Z1 | |
| Reagents | |||
| Alexa Fluor 405 Goat Anti-Mouse IgG2b | Sigma-Aldrich | SAB4600477 | Used at a final concentration of 1:500 |
| Alexa Fluor 488 Goat Anti-Mouse IgG1 | ThermoFisher | A-21121 | Used at a final concentration of 1:500 |
| Alexa Fluor 568 Goat Anti-Mouse IgM | Abcam | ab175702 | Used at a final concentration of 1:1,000 |
| Alexa Fluor 647 goat anti rat-IgG (H+L) secondary antibody | ThermoFisher | A-21247 | Used at a final concentration of 1:500 |
| BODIPY-493/503 (4,4-difluoro-1,3,5,7,8-pentametil-4-bora-3a,4a-diaza-s-indaceno) | ThermoFisher | D3922 | Used at a final concentration of 1 µg/mL |
| BODIPY-558/568 C12 (4,4-Difluoro-5-(2-Thienyl)-4-Bora-3a,4a-Diaza-s-Indacene-3-Dodecanoic Acid) | ThermoFisher | D3835 | Used at a final concentration of 1 µg/mL |
| DAPI (4',6-diamidino-2-phenylindole) | ThermoFisher | D1306 | Used at a final concentration of 0.5 µg/mL |
| Dimethyl Sulfoxide (DMSO) | Sigma-Aldrich | D-8418 | Used to solve Bodipy for the 1 mg/mL stock solution. CAUTION: Toxic and flammable. Vapors may cause irritation. Manipulate in a fume hood. Avoid direct contact with skin. Wear rubber gloves, protective eye goggles. |
| Formaldehyde solution 4%, buffered, pH 6.9 | Sigma-Aldrich | 1004969011 | CAUTION: May cause an allergic skin reaction. Suspected of causing genetic defects. May cause cancer. Manipulate in a fume hood. Avoid direct contact with skin. Wear rubber gloves, protective eye goggles. |
| Isopentane GPR RectaPur | VWR international | 24872.298 | CAUTION: Extremely flammable liquid and vapor. May be fatal if swallowed and enters airways. May cause drowsiness or dizziness. Repeated exposure may cause skin dryness or cracking. Wear protective gloves/protective clothing/eye protection/face protection. |
| Liquid Nitrogen | CAUTION: Extremely cold. Wear gloves. Handle slowly to minimize boiling and splashing and in well ventilated areas. Use containers designed for low-temperature liquids. | ||
| Mouse on mouse Blocking Reagent | Vector Labs | MKB-2213-1 | Used at concentration of 1:30 |
| Myosin heavy chain Type I (BA-D5-s Primary Antibody) Gene: MYH7, monoclonal bovine anti mouse IgG2b | DSHB University of Iowa | BA-D5-supernatant | Used at a final concentration of 1:10 |
| Myosin heavy chain Type IIA (SC-71-s Primary Antibody) Gene: MYH2, Monoclonal bovine anti mouse IgG1 | DSHB University of Iowa | SC-71-supernatant | Used at a final concentration of 1:10 |
| Myosin heavy chain Type IIX (6H1-s Primary Antibody), Gene: MYH1, Monoclonal rabbit anti mouse IgM | Developmental Studies Hybridoma Bank, University of Iowa | 6H1-supernatant | Used at a final concentration of 1:5 |
| Normal Goat Serum (NGS) | Vector Labs | S-1000 | |
| PBS 0.1 M | Commonly used on histology laboratories | ||
| ProLong Gold Antifade Mountant | Invitrogen | P36930 | |
| Rat anti-Laminin-2 (α-2 Chain) primary antibody (monoclonal) | Sigma-Aldrich | L0663 | Used at a final concentration of 1:1,000 |
| Tissue-Tek O.C.T compound | Sakura | 4583 | |
| Software | |||
| Adobe Illustrator CC | Adobe Inc. | Used to design the figures | |
| Adobe Photoshop | Adobe Inc. | Confocal software | |
| BioRender | https://biorender.com/ | Used to design the figures | |
| Fiji/ImageJ | https://imagej.net/software/fiji/ | Used to analyse the acquired images | |
| Microsoft PowerPoint | Microsoft | Used to reconstruct the histology of the whole muscle after scanning the fiber types | |
| Zen Blue 2.6 | Zeiss | Used to reconstruct the histology of the whole muscle after scanning the fiber types |
Riferimenti
- Correa-de-Araujo, R., et al. Myosteatosis in the context of skeletal muscle function deficit: an interdisciplinary workshop at the National Institute on Aging. Frontiers in Physiology. 11, 963 (2020).
- Miljkovic, I., et al. Greater skeletal muscle fat infiltration is associated with higher all-cause and cardiovascular mortality in older men. Journals of Gerontology Series A: Biomedical Sciences and Medical Sciences. 70 (9), 1133-1140 (2015).
- Nachit, M., et al. Myosteatosis rather than sarcopenia associates with non-alcoholic steatohepatitis in non-alcoholic fatty liver disease preclinical models. Journal of Cachexia, Sarcopenia, and Muscle. 12 (1), 144-158 (2021).
- Aleixo, G. F. P., et al. Myosteatosis and prognosis in cancer: Systematic review and meta-analysis. Critical Reviews in Oncology/Hematolgoy. 145, 102839 (2020).
- Gemmink, A., Schrauwen, P., Hesselink, M. K. C. Exercising your fat (metabolism) into shape: a muscle-centred view. Diabetologia. 63 (8), 1453-1463 (2020).
- van Loon, L. J. Use of intramuscular triacylglycerol as a substrate source during exercise in humans. Journal of Applied Physiology. 97 (4), 1170-1187 (2004).
- Coen, P. M., Goodpaster, B. H. Role of intramyocelluar lipids in human health. Trends in Endocrinology and Metabolism. 23 (8), 391-398 (2012).
- Seibert, J. T., Najt, C. P., Heden, T. D., Mashek, D. G., Chow, L. S. Muscle lipid droplets: cellular signaling to exercise physiology and beyond. Trends in Endocrinology and Metabolism. 31 (12), 928-938 (2020).
- Bergman, B. C., Goodpaster, B. H. Exercise and muscle lipid content, composition, and localization: influence on muscle insulin sensitivity. Diabetes. 69 (5), 848-858 (2020).
- Nielsen, J., Christensen, A. E., Nellemann, B., Christensen, B. Lipid droplet size and location in human skeletal muscle fibers are associated with insulin sensitivity. American Journal of Physiology-Endocrinology and Metabolism. 313 (6), 721-730 (2017).
- Covington, J. D., et al. Intramyocellular lipid droplet size rather than total lipid content is related to insulin sensitivity after 8 weeks of overfeeding. Obesity (Silver Spring). 25 (12), 2079-2087 (2017).
- Bosma, M. Lipid droplet dynamics in skeletal muscle). Experimental Cell Research. 340 (2), 180-186 (2016).
- Nielsen, J., et al. Increased subsarcolemmal lipids in type 2 diabetes: effect of training on localization of lipids, mitochondria, and glycogen in sedentary human skeletal muscle. American Journal of Physiology-Endocrinology and Metabolism. 298 (3), 706-713 (2010).
- Ferreira, R., et al. Subsarcolemmal and intermyofibrillar mitochondria proteome differences disclose functional specializations in skeletal muscle. Proteomics. 10 (17), 3142-3154 (2010).
- Barrett, J. S., Whytock, K. L., Strauss, J. A., Wagenmakers, A. J. M., Shepherd, S. O. High intramuscular triglyceride turnover rates and the link to insulin sensitivity: influence of obesity, type 2 diabetes and physical activity. Applied Physiology, Nutrition and Metabolism. , 1-14 (2022).
- Daemen, S., et al. Distinct lipid droplet characteristics and distribution unmask the apparent contradiction of the athlete’s paradox. Molecular Metabolism. 17, 71-81 (2018).
- Bredella, M. A., Ghomi, R. H., Thomas, B. J., Miller, K. K., Torriani, M. Comparison of 3.0 T proton magnetic resonance spectroscopy short and long echo-time measures of intramyocellular lipids in obese and normal-weight women. Journal of Magnetic Resonance Imaging. 32 (2), 388-393 (2010).
- Schrauwen-Hinderling, V. B., Hesselink, M. K., Schrauwen, P., Kooi, M. E. Intramyocellular lipid content in human skeletal muscle. Obesity (Silver Spring). 14 (3), 357-367 (2006).
- De Bock, K., et al. Evaluation of intramyocellular lipid breakdown during exercise by biochemical assay, NMR spectroscopy, and Oil Red O staining. American Journal of Physiology-Endocrinology and Metabolism. 293 (1), 428-434 (2007).
- Koopman, R., Schaart, G., Hesselink, M. K. Optimisation of oil red O staining permits combination with immunofluorescence and automated quantification of lipids. Histochemistry and Cell Biology. 116 (1), 63-68 (2001).
- Gueugneau, M., et al. Skeletal muscle lipid content and oxidative activity in relation to muscle fiber type in aging and metabolic syndrome. Journal of Gerontology Series A: Biomedical Sciences and Medical Sciences. 70 (5), 566-576 (2015).
- Gemmink, A., et al. Super-resolution microscopy localizes perilipin 5 at lipid droplet-mitochondria interaction sites and at lipid droplets juxtaposing to perilipin 2. Biochimica et Biophysica Acta-Molecular and Cell Biology of Lipids. 1863 (11), 1423-1432 (2018).
- Spangenburg, E. E., Pratt, S. J. P., Wohlers, L. M., Lovering, R. M. Use of BODIPY (493/503) to visualize intramuscular lipid droplets in skeletal muscle. Journal of Biomedicine and Biotechnology. 598358, (2011).
- Prats, C., et al. An optimized histochemical method to assess skeletal muscle glycogen and lipid stores reveals two metabolically distinct populations of type I muscle fibers. PLoS One. 8 (10), 77774 (2013).
- Strauss, J. A., Shepherd, D. A., Macey, M., Jevons, E. F. P., Shepherd, S. O. Divergence exists in the subcellular distribution of intramuscular triglyceride in human skeletal muscle dependent on the choice of lipid dye. Histochemistry and Cell Biology. 154 (4), 369-382 (2020).
- Shepherd, S. O., et al. Sprint interval and traditional endurance training increase net intramuscular triglyceride breakdown and expression of perilipin 2 and 5. Journal of Physiology. 591 (3), 657-675 (2013).
- Whytock, K. L., et al. A 7-day high-fat, high-calorie diet induces fibre-specific increases in intramuscular triglyceride and perilipin protein expression in human skeletal muscle. Journal of Physiology. 598 (6), 1151-1167 (2020).
- Wang, C., Yue, F., Kuang, S. Muscle histology characterization using h&e staining and muscle fiber type classification using immunofluorescence staining. Bio-Protocol. 7 (10), (2017).
- Meng, H., et al. Tissue triage and freezing for models of skeletal muscle disease. Journal of Visualized Experiments: JoVE. (89), e51586 (2014).
- Kumar, A., Accorsi, A., Rhee, Y., Girgenrath, M. Do’s and don’ts in the preparation of muscle cryosections for histological analysis. Journal of Visualized Experiments: JoVE. (99), e52793 (2015).
- Leiva-Cepas, F., et al. Laboratory methodology for the histological study of skeletal muscle. Archivos de Medicina del Deporte. 35 (186), 254-262 (2018).
- Schindelin, J., et al. Fiji: an open-source platform for biological-image analysis. Nature Methods. 9 (7), 676-682 (2012).
- Schiaffino, S., et al. Three myosin heavy chain isoforms in type 2 skeletal muscle fibres. Journal of Muscle Research & Cell Motility. 10 (3), 197-205 (1989).
- Komiya, Y., et al. Mouse soleus (slow) muscle shows greater intramyocellular lipid droplet accumulation than EDL (fast) muscle: fiber type-specific analysis. Journal of Muscle Research & Cell Motility. 38 (2), 163-173 (2017).
- Andrich, D. E., et al. Altered lipid metabolism impairs skeletal muscle force in young rats submitted to a short-term high-fat diet. Frontiers in Physiology. 9, 1327 (2018).
- Schiaffino, S. Fibre types in skeletal muscle: a personal account. Acta Physiologica. 199 (4), 451-463 (2010).
- Bloemberg, D., Quadrilatero, J. Rapid determination of myosin heavy chain expression in rat, mouse, and human skeletal muscle using multicolor immunofluorescence analysis. PLoS One. 7 (4), 35273 (2012).
- Gemmink, A., et al. Decoration of intramyocellular lipid droplets with PLIN5 modulates fasting-induced insulin resistance and lipotoxicity in humans. Diabetologia. 59 (5), 1040-1048 (2016).
- Askinas, C., et al. . Biophotonics Congress: Biomedical Optics Congress 2018 (Microscopy/Translational/Brain/OTS). , (2018).
- Morén, B., et al. EHD2 regulates adipocyte function and is enriched at cell surface-associated lipid droplets in primary human adipocytes. Molecular Biology of the Cell. 30 (10), 1147-1159 (2019).
- Benador, I. Y., et al. Mitochondria bound to lipid droplets have unique bioenergetics, composition, and dynamics that support lipid droplet expansion. Cell Metabolism. 27 (4), 869-885 (2018).
- de la Rosa Rodriguez, M. A., et al. Hypoxia-inducible lipid droplet-associated induces DGAT1 and promotes lipid storage in hepatocytes. Molecular Metabolism. 47, 101168 (2021).
- Jevons, E. F. P., Gejl, K. D., Strauss, J. A., Ørtenblad, N., Shepherd, S. O. Skeletal muscle lipid droplets are resynthesized before being coated with perilipin proteins following prolonged exercise in elite male triathletes. American Journal of Physiology-Endocrinology and Metabolism. 318 (3), 357-370 (2020).
- Ohsaki, Y., Maeda, T., Fujimoto, T. Fixation and permeabilization protocol is critical for the immunolabeling of lipid droplet proteins. Histochemistry and Cell Biology. 124 (5), 445-452 (2005).
- Prats, C., et al. Decrease in intramuscular lipid droplets and translocation of HSL in response to muscle contraction and epinephrine. Journal of Lipid Research. 47 (11), 2392-2399 (2006).
- Listenberger, L. L., Brown, D. A. Fluorescent detection of lipid droplets and associated proteins. Current Protocols in Cell Biology. , (2007).
- Xue, Y., Lim, S., Bråkenhielm, E., Cao, Y. Adipose angiogenesis: quantitative methods to study microvessel growth, regression and remodeling in vivo. Nature Protocols. 5 (5), 912-920 (2010).
- Muliyil, S., et al. ADAM17-triggered TNF signalling protects the ageing Drosophila retina from lipid droplet-mediated degeneration. The EMBO Journal. 39 (17), 104415 (2020).
- Yan, Q., et al. Autophagy activation contributes to lipid accumulation in tubular epithelial cells during kidney fibrosis. Cell Death Discovery. 4, 2 (2018).
- Coassin, S., et al. Investigation and functional characterization of rare genetic variants in the adipose triglyceride lipase in a large healthy working population. PLoS Genetics. 6 (12), 1001239 (2010).
- Daemen, S., van Zandvoort, M., Parekh, S. H., Hesselink, M. K. C. Microscopy tools for the investigation of intracellular lipid storage and dynamics. Molecular Metabolism. 5 (3), 153-163 (2016).
- Chen, Q., et al. Rab8a deficiency in skeletal muscle causes hyperlipidemia and hepatosteatosis by impairing muscle lipid uptake and storage. Diabetes. 66 (9), 2387-2399 (2017).
- Gemmink, A., et al. Decoration of myocellular lipid droplets with perilipins as a marker for in vivo lipid droplet dynamics: A super-resolution microscopy study in trained athletes and insulin resistant individuals. Biochimica et Biophysica Acta (BBA)-Molecular and Cell Biology of Lipids. 1866 (2), 158852 (2021).
- Bergman, B. C., Hunerdosse, D. M., Kerege, A., Playdon, M. C., Perreault, L. Localisation and composition of skeletal muscle diacylglycerol predicts insulin resistance in humans. Diabetologia. 55 (4), 1140-1150 (2012).

