뼈 유사체 생성을 위한 세포 함유 현탁액의 세라믹 전방향 바이오프린팅
Summary
이 프로토콜은 젤라틴 기반 과립 지지체에 인산 칼슘 잉크를 증착하여 뼈와 같은 구조를 제조하는 3D 프린팅 기술을 설명합니다. 인쇄된 뼈 유사체는 다상 구축물을 위한 살아있는 세포 매트릭스 내에서 인쇄물의 직접 수확 또는 가교를 위한 유연성과 함께 자유 형태로 증착됩니다.
Abstract
구조적으로 뼈 조직은 계층적이고 고도로 광물화된 매트릭스 내에 내장된 대사 활성 세포를 포함하는 무기-유기 복합체입니다. 이 조직은 뼈의 이질적인 환경으로 인해 복제하기가 어렵습니다. 세포 현탁액의 세라믹 전 방향 바이오 프린팅 (COBICS)은 뼈의 미네랄 및 세포 구조를 독특하게 복제하는 마이크로 젤 기반 바이오 프린팅 기술입니다. COBICS는 뼈 모방 구조물의 적층 제조에서 가장 큰 두 가지 과제인 희생 지지 재료나 가혹한 후처리 단계(예: 방사선 및 고온 소결)가 필요 없이 복잡하고 생물학적으로 관련된 구조물을 인쇄합니다. 이 기술은 젤라틴 기반 마이크로겔 현탁액 내에서 새로운 인산칼슘 기반 잉크의 자유형 압출을 통해 가능합니다. 현탁액의 항복 응력 특성은 증착을 허용하고 인쇄된 뼈 구조를 지지합니다. UV 가교 및 나노 침전은 제자리에 “고정”됩니다. 세포가 함유된 생체 재료 내에서 나노 구조의 뼈 모방 세라믹을 인쇄하는 기능은 거시적 및 미시적 아키텍처에 대한 시공간 제어를 제공하고 임상 환경에서 복잡한 뼈 구조의 실시간 제조를 용이하게 합니다.
Introduction
뼈는 내인성 치유능력이 손상되었을 때 치명적인 결함 크기까지 정상적인 세포 구성, 방향 및 기계적 강도를 재현하여 치유할 수 있는 신체의 몇 안 되는 구조 중 하나로서 놀라운 재생 능력을 가지고 있습니다1. 뼈는 연골 및 인대와 함께 신체 움직임을 지원하고 촉진하는 동시에 미네랄과 지방을 저장하고 혈액 세포를 생성합니다. 단단하고 조밀 한 결합 조직으로서 뼈는 주로 무기상, 물 및 콜라겐 섬유로 주로 구성된 유기 물질로 구성됩니다2. 세포는 콜라겐 I 섬유와 수산화인회석(HA) 결정의 고도로 광물화된 매트릭스 내에 내장되어 계층적 구조3를 형성합니다.
이 조직의 복잡한 조직은 이질적인 뼈 마이크로 및 나노 환경을 복제하기 위한 합성 대안의 제조를 매우 어렵게 만듭니다3. 이를 위해 바이오 세라믹, 세포 함유 하이드로 겔 및 합성 재료를 포함한 다양한 재료가 뼈 매트릭스를 만드는 솔루션으로 제안되었습니다. 비계 제조 기술 중 3D 프린팅 기반 기술이 최근에 등장하여 환자 맞춤형 치료의 큰 가능성을 가진 매우 정교하고 정밀한 구조의 제조를 허용하는 놀라운 능력으로 인해 조직 공학 커뮤니티에서 많은 관심을 받았습니다.4,5,6 . 하이드로겔은 매트릭스 모조물 및 바이오잉크의 가장 인기 있는 선택이었으며, 이는 이들이 세포 및 생리활성 분자와 함께 인쇄되어 기능적 구축물6을 생성할 수 있기 때문이다. 그러나 하이드로겔은 기계적 강도와 대사 활성 세포를 포함하는 고도로 석회화된 무기상과 같은 뼈의 기능적 특성이 부족합니다.
3D 인쇄 된 세라믹 스캐 폴드는 일반적으로 소결, 고온 처리 또는 시험관 내 또는 생체 내 응용 프로그램 전에 철저히 세척해야하는 가혹한 화학 물질 사용을 포함한 후 처리 단계가 필요합니다5. 이러한 한계를 해결하기 위해 Lode et al.7 은 최근 생리적 조건에서 인쇄 및 설정할 수 있는 하이드록시아파타이트로 형성된 α-인산삼칼슘 기반 페이스트를 개발했습니다. 그러나 이 물질은 습한 환경에서 후처리가 필요하고 장기간 수용액에 담가야 하기 때문에 여전히 살아있는 세포와 함께 인쇄할 수 없습니다.
대안적으로, 무기 입자가 혼입된 세포 함유 하이드로겔이 3D 뼈 매트릭스 8,9의 대체물로서 제안되었다. 세포 생존력을 지원하는 뛰어난 능력에도 불구하고 조밀하게 광물화된 뼈 조직 환경을 요약할 수 없습니다. Thrivikarman et al.10은 나노 스케일 아파타이트 침착을 더 잘 모방하기 위해 비 콜라겐 단백질 유사체와 함께 과포화 칼슘 및 인산염 배지를 사용하는 생체 모방 접근법을 채택했다. 그러나 이들의 구조는 여전히 뼈대와 유사한 마이크로 및 매크로 스케일 아키텍처를 가진 견고한 3D 구조를 생성할 수 없습니다.
본 연구는 세포와 성장 인자11을 모두 통합 할 수있는 무기 및 유기 단계에서 뼈 모방 구조물을 제조하기위한 인쇄 전략의 개발을 통해 이러한 단점을 해결합니다. COBICS는 마이크로젤 기반 바이오프린팅 기술을 사용하여 뼈의 미네랄 및 세포 구조를 독특하게 요약합니다. 본원의 프로토콜은 세라믹 본-잉크 및 젤라틴-기반 마이크로겔을 합성하고, 이어서 COBICS를 가능하게 하는 세포를 조합하는 과정을 설명한다. 이 공정은 뼈 잉크의 주요 전구체 물질의 합성으로 시작됩니다. 그런 다음 가교성 하이드로겔을 합성하여 마이크로겔로 형성합니다. 마지막으로, 뼈 잉크는 세포가 담긴 마이크로젤의 지지 수조에 전방향으로 증착됩니다(그림 1).
본-잉크는 적절한 항복-응력 특성, 즉 특정 전단 속도에서 유동화하고 후속적으로 증착된 구조를 지지하는 능력을 갖는 마이크로겔의 임의의 현탁액에 인쇄될 수 있다. 두 가지 유연한 접근법이 입증되었습니다 : 젤라틴 마이크로 겔로 구성된 현탁액과 젤라틴 메타 크릴 레이트 (GelMA) 마이크로 겔로 구성된 현탁액. 전자의 현탁액은 온도가 37°C로 상승될 때, 부유된 하이드로겔의 자유형 가역적 임베딩(FRESH) 기술(12)에서 용해되는 반면, 후자는 인쇄 후에 광가교결합될 수 있고, 마이크로겔을 효과적으로 “스티칭”하고 인쇄된 뼈-잉크를 제자리에 고정시킬 수 있다. 본 연구는 복잡한 뼈 모방 구조의 현장 인쇄로 세포 성장을 지원할 수 있다는 독특한 이점을 제공하기 때문에 GelMA를 매트릭스로 사용하는 데 중점을 둡니다. 궁극적으로 이 접근 방식은 질병 모델링, 약물 발견 및 재생 공학에 대한 높은 수준의 생체 모방과 광범위한 영향을 가진 복잡한 조직 모델의 생성을 가능하게 합니다.
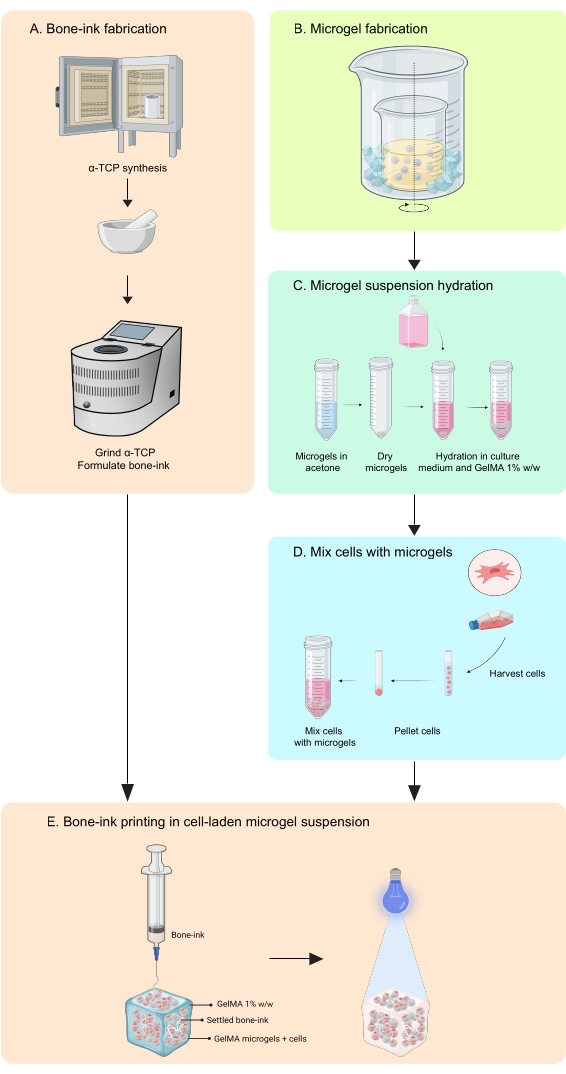
그림 1: 워크플로의 개략도 . (A) 뼈 잉크는 α-인산 삼칼슘 합성과 글리세롤, 폴리소르베이트 80 및 인산이염기성 암모늄과의 후속 조합에서 시작하여 합성됩니다. (B) GelMA 마이크로젤은 유중수 에멀젼 방법으로 제조됩니다. 수득 된 마이크로 겔은 (C) 수화되고 (D) 세포와 결합된다. 세포-마이크로겔 복합체는 뼈-잉크가 증착되는 과립 욕조로 사용됩니다. (E) 그런 다음 전체 구축물을 UV 가교하여 배양을 위해 인큐베이터로 옮깁니다. 약어 : α-TCP = α- 인산 삼 칼슘; 겔마 = 젤라틴 메타크릴레이트. 이 그림의 더 큰 버전을 보려면 여기를 클릭하십시오.
Protocol
Representative Results
Discussion
3D 프린팅 기술 COBICS는 압출을 통해 살아있는 세포를 포함하는 가교 결합 가능한 마이크로 겔 현탁액으로 광물화 된 뼈와 같은 구조를 제조 할 수 있도록 개발되었습니다. 상기 기술은 분해가능한 마이크로겔 현탁액에 적용되었고, 세포는 시스템(11) 내에서 양호한 생존력, 확산 및 골형성 분화 능력을 나타낸다. 이 기술을 사용하여 생성 된 구문의 성공을 결정하는 핵심 요소는 α…
Divulgazioni
The authors have nothing to disclose.
Acknowledgements
저자는 국립 보건 및 의학 연구위원회 (보조금 번호. GNT1111694 및 GNT1141602) 및 호주 연구위원회 (보조금 번호. FT180100417, FL150100060 및 CE14100036). 저자는 뉴 사우스 웨일즈 대학의 생물 의학 이미징 시설을 인정하고자합니다. 피규어는 Biorender.com, 어도비 포토샵, 어도비 일러스트레이터로 제작되었으며 유료 구독으로 내보내졌습니다.
Materials
| 3D Printer Extruder | Hyrel3D | EMO-25 | |
| 50 mL centrifuge tubes | Falcon | BDAA352070 | |
| Absolute Ethanol 100% Denatured | Chem-Supply | ||
| Acetone | Chem-Supply | 154871 | |
| Alumina crucible | Coors | ||
| Ammonium phosphate dibasic (NaHPO4) | Sigma | A5764 | |
| Autodesk Fusion 360 | Autodesk | ||
| Biosafety cabinet level 2 | |||
| Calcium carbonate | Sigma | 239216 | |
| Calcium hydrogen phosphate (CaHPO4) | Sigma | C7263 | |
| Cell culture flasks | Corning | various volumes used | |
| Cellulose Dialysis Tubes, 14 kDa cut-off | Sigma | D9777 | |
| Centrifuge | Eppendorf | 5430R | |
| Centrifuge | Sigma | 3-16KL | |
| Dispensing Tip, 23 G | Nordson | 7018302 | |
| DMEM, low glucose, pyruvate | Thermo FIsher | 11885084 | |
| DPBS, no calcium, no magnesium | Thermo FIsher | 14190144 | |
| Elevator furnace | Labec | ||
| Engine HR Multihead Printer | Hyrel3D | ||
| Fetal Bovine Serum | Bovogen | ||
| Gelatin type A, from porcine skin | Sigma | G2500 | |
| General Purpose Stainless Steel Tips | Nordson EF | ||
| Glycerol | Sigma | G9012 | |
| Human adipose derived stem cells | ATCC | PCS-500-011 | |
| LSM 800 Confocal Microscope | ZEISS | ||
| Lyophilizer (Alpha 1-4 LDplus) | Christ | 101541 | |
| Magnetic hot plate and stirrer | |||
| Methacrylic anhydride | Sigma | 276685 | |
| Mini 2 Desktop 3D Printer | LulzBot | ||
| Parafilm sealing film | Parafilm | PM996 | |
| Penicillin-Streptomycin | Thermo FIsher | 15140122 | |
| Planetary ball mill | |||
| Planetary ball mill jar | |||
| Polyoxyethylenesorbitan monooleate Tween-80 | Sigma | P6224 | |
| Scanning electron microscope | FEI Nova NanoSEM 450 FE-SEM | ||
| Science Kimwipes Delicate Task Wipers | Kimtech | 18813156 | |
| Stainless steel standard test sieve | |||
| Sunflower Oil | Community Co | ||
| Trypsin-EDTA 0.25% phenol red | Thermo FIsher | 25200056 | |
| ZEN Microscope Software | ZEISS | ||
| Live/Dead viability/ cytotoxicity kit for mammalian cells | Invitrogen | L3224 | |
| DMEM, low glucose, no phenol red | Thermo Fisher | 11054020 |
Riferimenti
- Bates, P., Ramachandran, M. Bone injury, healing and grafting. Basic Orthopaedic Sciences. The Stanmore Guide. , 123-134 (2007).
- Lin, X., et al. The bone extracellular matrix in bone formation and regeneration. Frontiers in Pharmacology. 11, 757 (2020).
- Reznikov, N., et al. A materials science vision of extracellular matrix mineralization. Nature Reviews Materials. 1, 16041 (2016).
- Kang, H. W., et al. A 3D bioprinting system to produce human-scale tissue constructs with structural integrity. Nature Biotechnology. 34 (3), 312-319 (2016).
- Lin, K., et al. 3D printing of bioceramic scaffolds-Barriers to the clinical translation: From promise to reality, and future perspectives. Materials. 12 (17), 2660 (2019).
- Qu, M., et al. Multi-dimensional printing for bone tissue engineering. Advanced Healthcare Materials. 10 (11), 2001986 (2021).
- Lode, A., et al. Fabrication of porous scaffolds by three-dimensional plotting of a pasty calcium phosphate bone cement under mild conditions. Journal of Tissue Engineering and Regenerative Medicine. 8 (9), 682-693 (2014).
- Bernal, P. N., et al. Volumetric bioprinting of complex living-tissue constructs within seconds. Advanced Materials. 31 (42), 1904209 (2019).
- Diloksumpan, P., et al. Combining multi-scale 3D printing technologies to engineer reinforced hydrogel-ceramic interfaces. Biofabrication. 12 (2), 025014 (2020).
- Thrivikraman, G., et al. Rapid fabrication of vascularized and innervated cell-laden bone models with biomimetic intrafibrillar collagen mineralization. Nature Communications. 10 (1), 3520 (2019).
- Romanazzo, S., et al. Synthetic bone-like structures through omnidirectional ceramic bioprinting in cell suspensions. Advanced Functional Materials. 31 (13), 2008216 (2021).
- Hinton, T. J., et al. Three-dimensional printing of complex biological structures by freeform reversible embedding of suspended hydrogels. Science Advances. 1 (9), 1500758 (2015).
- Phromsopha, T., Baimark, Y. Preparation of starch/gelatin blend microparticles by a water-in-oil emulsion method for controlled release drug delivery. International Journal of Biomaterials. 2014, 829490 (2014).
- Moreno, D., et al. Solid-state synthesis of alpha tricalcium phosphate for cements used in biomedical applications. Boletín de la Sociedad Española de Cerámica y Vidrio. 59 (5), 193-200 (2020).

