Isolering av bronkiale epitelceller fra resektert lungevev for biobanking og etablering av godt differensierte luft-væske-grensesnittkulturer
Summary
Presentert her er en reproduserbar, rimelig og robust metode for isolering og utvidelse av primære bronkiale epitelceller for langsiktig biobanking og generering av differensierte epitelceller ved kultur ved luft-væske-grensesnittet.
Abstract
Luftveisepitelcellelaget danner den første barrieren mellom lungevev og ytre miljø og utsettes dermed konstant for innåndede stoffer, inkludert smittestoffer og luftforurensende stoffer. Luftveisepitellaget spiller en sentral rolle ved en lang rekke akutte og kroniske lungesykdommer, og ulike behandlinger rettet mot dette epitelet gis ved innånding. Å forstå epitelets rolle i patogenesen og hvordan det kan målrettes mot terapi krever robuste og representative modeller. In vitro epitelkulturmodeller blir i økende grad brukt og gir fordelen av å utføre eksperimenter i et kontrollert miljø, utsette cellene for forskjellige typer stimuli, toksiske stoffer eller smittsomme stoffer. Bruken av primære celler i stedet for immortaliserte eller tumorcellelinjer har fordelen at disse cellene skiller seg i kultur til et pseudostratifisert polarisert epitelcellelag med en bedre representasjon av epitelet sammenlignet med cellelinjer.
Presentert her er en robust protokoll, som har blitt optimalisert de siste tiårene, for isolasjon og kultur av luftveisepitelceller fra lungevev. Denne prosedyren tillater vellykket isolering, ekspansjon, kultur og mukociliær differensiering av primære bronkiale epitelceller (PBECs) ved dyrking ved luft-væskegrensesnittet (ALI) og inkluderer en protokoll for biobanking. Videre beskrives karakteriseringen av disse kulturene ved hjelp av cellespesifikke markørgener. Disse ALI-PBEC kulturer kan brukes til en rekke applikasjoner, inkludert eksponering for hele sigarettrøyk eller inflammatoriske mediatorer, og co-kultur / infeksjon med virus eller bakterier.
Protokollen i dette manuskriptet, som illustrerer prosedyren trinnvis, forventes å gi grunnlag og/eller referanse for de som er interessert i å implementere eller tilpasse slike kultursystemer i sitt laboratorium.
Introduction
Luftveisepitelets rolle i en rekke akutte og kroniske lungesykdommer er beskrevet i ulike vurderinger 1,2,3,4,5,6,7. Godt differensierte kulturer av luftveisepitelceller er et viktig verktøy for å løse rollen til luftveisepitelet. Luft-væske-grensesnitt (ALI) luftveis epitelcellekultur brukes bredt for å fremme differensiering av luftveis basale epitelceller og derved studere luftveisepitelet pålitelig in vitro 8,9. De siste årene har bruken av slike modeller økt ytterligere som følge av nye forskningsinitiativer knyttet til COVID-19-pandemien og en verdensomspennende overgang til dyrefri forskning. Derfor understreker den økte bruken av denne modellcellelinjen behovet for delingsprosedyrer og erfaringer for å oppnå robuste resultater. Dette vil også gjøre det mulig å sammenligne resultater mellom forskningsgrupper. Prosedyrens robusthet er nøkkelegenskapen og må derfor underkastes kvalitetskontroll. Flere laboratorier har investert i å utvikle protokoller for dyrking av primære luftveisepitelceller ved ALI. Tiden, innsatsen og det nødvendige budsjettet kan reduseres når disse prosedyrene deles i detalj. Disse detaljene inkluderer for eksempel valg av cellekulturplast og media levert av forskjellige produsenter, siden dette ble funnet å påvirke egenskapene til kulturene oppnådd10,11,12. Dette understreker viktigheten av å dele erfaringer og detaljer om kulturprosedyrer, siden i fravær av slik innsikt kan resultatene bli påvirket og / eller valideringsarbeidet på tvers av ulike laboratorier kan bli hindret.
Det menneskelige lungeepitelet består av forskjellige celletyper, inkludert hovedtyper som basale celler, cilierte celler, begerceller og klubbceller. For å kunne etterligne epitelcellelaget i luftveiene in vitro på en pålitelig måte, må disse celletypene være representert i kulturmodellene, og deres polarisering og funksjon opprettholdes13,14,15,16. Realiseringen av at donoregenskaper (inkludert sykdomstilstand) og cellens anatomiske opprinnelse (dvs. nese-, trakeal-, store og små luftveier) kan påvirke cellekulturens cellulære sammensetning og funksjonelle responser er like viktig. Relevant kompetanse og praksis er en forutsetning for vellykket dyrkning av primære luftveisepitelceller og vurdering av kulturens kvalitet både intuitivt (ved visuell inspeksjon under dyrkning) og kvantifiserbart. Målet med dette bidraget er å gi en kostnadseffektiv og tidseffektiv metode for isolering og kultur av primære humane bronkialepitelceller (PBECs) som også kan brukes på kulturen av trakeale og små luftveisepitelceller. I tillegg til å beskrive en metode for isolering av slike celler fra resektert lungevev, presenteres og diskuteres en metode for ekspansjon og biobanking, og til slutt for etablering og karakterisering av en godt differensiert ALI-kultur innenfor en rimelig kostnad og tidsperiode.
Protocol
Representative Results
Discussion
Protokollen som presenteres her beskriver isolering av humane bronkialepitelceller fra resektert lungevev, en metode for optimal ekspansjon av celler uten tap av differensieringspotensial, en kryopreserveringsprosedyre og en prosedyre for å generere godt differensierte ALI-PBEC-kulturer. Videre gis en beskrivelse av kvalitetskontrollen, samt instruksjoner for overvåking og evaluering av de differensierte ALI-PBECene.
Den beskrevne protokollen starter med en makroskopisk normal, tumorfri bronkialring som resekteres fra en lungelapp fra pasienter som gjennomgår kirurgi relatert til lungekreftdiagnosen. Det må derfor bemerkes at disse ringene strengt tatt ikke kan betraktes som sunt vev, noe som derfor kan påvirke cellekulturegenskaper. Alternative kilder for å skaffe bronkial epitelceller inkluderer bruk av bronkial biopsier, bronkial børsting, eller vev fra en transplantasjon donor eller mottaker lunger. Uavhengig av kilden, ved bruk av lungevev, bør en risiko for mikrobiell kontaminering vurderes, og derfor brukes antibiotika i de forskjellige kulturmediene for å redusere risikoen for mikrobiell kontaminering av cellekulturen. Spesielt er mykoplasma en høy og vanlig risiko i cellekultur, på grunn av sin store variasjon av effekter på cellekultur, resistens mot antibiotika som vanligvis brukes i cellekultur, og det faktum at mykoplasmaforurensning kun kan bekreftes ved mykoplasmadeteksjonsanalyser. Derfor, i den første fasen av cellekultur etter isolering av celler fra lungevev, brukes den bredspektrede antimikrobielle formuleringen Primocin, og under kulturprosessen testes tilfeldig utvalgte prøver for tilstedeværelse av mykoplasma.
Isolasjonsprosedyren som starter med en bronkialring gir tilstrekkelig utgangsmateriale for å tillate graden av ekspansjon av disse primære cellene som trengs for å starte kulturer ved ALI uten at det går ut over differensieringskapasiteten. Å starte utvidelsen av de isolerte epitelcellene med et begrenset antall celler kan imidlertid by på problemer med å oppnå et tilstrekkelig antall innlegg med nok celler som kan sås for ALI-kultur. Utvidet kultur og gjentatt passering av primære celler kan resultere i replikativ senescens. Det er foreslått ulike løsninger for å overvinne denne begrensningen. Horani et al. viste at Rho-kinasehemmeren (ROCK) Y-27632 økte spredningen av basale celler30, Mou et al. brukte dobbel Smad-hemming for å utvide basale stamceller samtidig som egenskapene til det differensierte epitelcellelaget 31 opprettholdes, og Sachs et al. har utviklet et luftveisorganoidsystem som kan brukes til å utvide luftveisepitelceller og opprettholde deres differensieringspotensial i løpet av flere passasjer32. Sistnevnte metode ble også brukt til å utvide celler fra kilder med svært lave celletall, for eksempel trakealaspirater (TA) fra premature spedbarn (<28 ukers svangerskapsalder) og bronkoalveolær skylling (BAL) væske, før overføring til ALI-kulturen som beskrevet her33. Det ble funnet at celler isolert fra BAL og TA viste en differensieringskapasitet som var lik celler generert fra bronkialvev, selv om forskjeller ble observert når differensieringen var skjev mot mer cilierte eller mer begercelleholdige kulturer ved bruk av Notch-signalinhibering eller Th2-cytokinet IL-1333. Det anbefales derfor at hvis ALI-PBECer dyrkes fra et utgangsmateriale med lavt epitelcelletall med lignende tilnærminger, alltid kontrollerer kulturene for de grunnleggende kvalitetskriteriene, som diskutert i avsnitt 6 i protokollen. Det er viktig at bruken av materceller også kan bidra til å oppnå større celletall, noe som er viktig i en setting for transplanterbar stillasteknikk der tid og cellenummer er avgjørende. Dette illustreres av en studie hvor autologe epitelceller ble dyrket fra biopsier avledet fra en pasient med trakealsykdom, og celler ble raskt utvidet i nærvær av et murine embryonalt materlag (mitotisk inaktiverte 3T3-J2 fibroblaster) og den ovennevnte inhibitoren av Rho / ROCK-banen (Y-27632) 34. Den resulterende cellekulturen ble funnet å være nyttig for repopulasjon av trakealstillas, og dette kunne derfor betraktes som en egnet protokoll for en transplantasjonsmodell.
Ved bruk av protokollen beskrevet i dette bidraget, men også ved bruk av andre kulturprotokoller, introduseres uunngåelig en seleksjonsskjevhet. Det er viktig å innse at forskjeller i protokolldetaljer, for eksempel opprinnelsen til celler som brukes til å initiere kulturer, mediumsammensetning og andre protokolldetaljer, kan føre til endringer i cellulær sammensetning av kulturene og dermed endringer i responsen til ALI-kulturen33,35. I tillegg har forskjeller i celleegenskaper også blitt observert ved sammenligning av forskjellige medier for differensiering av luftveiscellene10,11. Ved sammenligning av PneumaCult og cBD-medium ble det observert forskjeller i begercelle- og klubbcelle-mRNA-markører, TEER-verdier og cellelagtykkelse. Basert på disse observasjonene, til tross for mangelen på statistisk understøttelse, på grunn av det lave antallet donorer som brukes, er mediesammensetningen ukjent for kundene, og høyere kostnader for PneumaCult-mediet, ble beslutningen tatt i vårt laboratorium om å bruke cBD-medium.
Som diskutert kan celler først utvides ved hjelp av organoidkultur og deretter overføres til 2D ALI-innsatssystemet. Dette er viktig, siden luftveisepitelorganoider ikke er egnet for eksponering for luftbårne stoffer, mens bruk av ALI 2D-systemet tillater evaluering av virkningen av luftbårne stoffer som sigarettrøyk23,36 på dyrkede luftveisepitelceller. En annen tilnærming for å etablere ALI-epitelcellekulturer i luftveiene er å generere luftveisepitelceller ved differensiering av humane pluripotente stamceller (hiPSCs)37. I slike protokoller, i sluttfasen av differensieringsprotokollen etter differensiering til proksimale luftveisprogenitorer, kan celler differensieres etter kultur til ALI ved hjelp av prosedyrer som ligner de som er beskrevet her.
I den nåværende protokollen brukes cBD-medium til kultur ved ALI. cBD-medium er et serumfritt medium som fremstilles ved å legge til en blanding av forskjellige kosttilskudd, inspirert av Fulcher et al.38 , samt andre studier. Tilleggsløsningen inneholder 52 μg/ml bovint hypofyseekstrakt (BPE), 0,5 μg/ml hydrokortison, 0,5 ng/ml human EGF, 0,5 μg/ml adrenalin, 10 μg/ml transferrin, 5 μg/ml insulin, 6,5 ng/ml trijodtyronin og 0,1 ng/ml RA39. Siden BPE er et vevekstrakt og blir utsatt for batchvis variasjon, kan mediet ikke betraktes som et fullt definert medium, og det er heller ikke dyrefritt. Cellekulturmedium som er fullstendig definert, foretrekkes for å minimere batch-til-batch-forskjeller. I lys av overgangen til dyrefri forskning er det viktig at det arbeides for å produsere definerte medier som ikke inneholder animalske produkter og som er rimelige for det vitenskapelige samfunnet.
Ulike eksperimentelle oppsett kan brukes basert på ALI-modellen, avhengig av forskningsspørsmålet. For eksempel, for å undersøke virkningen av forbindelser som kan påvirke differensieringsprosessen, kan dette løses ved å tilsette forbindelsene til kulturen under de forskjellige stadier av nedsenket kultur, under differensiering eller på det godt differensierte stadiet. Den cellulære sammensetningen av ALI-PBEC-kulturen kan påvirkes ved å tilsette spesifikke forbindelser; for eksempel genererer differensiering av ALI-PBECs i nærvær av IL-13 en kultur med flere begerceller og færre cilierte celler, mens behandling med γ-sekretasehemmeren DAPT (brukes til å blokkere Notch-signalering) under differensiering resulterer i en kultur med flere cilierte celler på bekostning av begerceller 23,40,41,42.
Videre kan agenter for å stimulere celler eller blokkere visse prosesser enten påføres basalrommet eller (i et svært lite volum) til kulturens apikale rom. Celler kan også bli utsatt for luftbårne stoffer fra den apikale siden. Slike eksponeringsdesign har blitt brukt til å studere effekten av dieseleksos eller hel sigarettrøyk på PBEC23,43,44. Mediet kan høstes hver gang mediet endres for å overvåke utskilte proteiner på basalsiden; det samme gjelder for den apikale siden av cellene som vaskes med PBS mens basalmediet forfriskes. Den såkalte apikale vasken høstes og valgfri dithioerythritol (DTE) tilsettes for å dissosiere slimet som produseres av begercellene mer effektivt. Cellelysater kan oppnås for isolering av totalt protein, RNA og kromosomalt og mitokondrielt DNA. Cellene kan studeres videre ved hjelp av antistoffer for spesifikke markører, ved å kutte polyetylentereftalatmembranen (PET) fra plastinnsatsen og videre kutte denne membranen i mindre biter for flere immunfluorescensfarginger45. Videre kan flowcytometri eller FACS også brukes etter trypsinisering av cellene i innleggene. Under ALI-stadiet kan utviklingen av den cellulære barrieren overvåkes ved å måle den elektriske motstanden og deretter beregne TEER, hvor den elektriske motstanden er omvendt proporsjonal med overflaten av membraninnsatsen. Beregningen er basert på Ohms lov ved å bruke følgende formel: 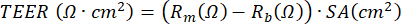 , hvor Rm er den målte elektriske motstanden, Rb er den grunnleggende elektriske motstanden til en innsats uten belegg og celler, og SA er overflaten av membranen til innsatsen. Måling av elektrisk motstand ved hjelp av EVOM2 og STX / spisepinne elektroder er enkelt, men svært avhengig av håndteringsprosedyrer ved innføring i brønnen. Formen på elektroden har også blitt foreslått å påvirke målingen av barrierefunksjonen til det relativt store overflatearealet17.
, hvor Rm er den målte elektriske motstanden, Rb er den grunnleggende elektriske motstanden til en innsats uten belegg og celler, og SA er overflaten av membranen til innsatsen. Måling av elektrisk motstand ved hjelp av EVOM2 og STX / spisepinne elektroder er enkelt, men svært avhengig av håndteringsprosedyrer ved innføring i brønnen. Formen på elektroden har også blitt foreslått å påvirke målingen av barrierefunksjonen til det relativt store overflatearealet17.
Ytterligere forbedring i ALI-cellekultursystemet, med sikte på å øke nøyaktig vevsrepresentasjon, inkluderer kokultur av ytterligere celletype, som leukocytter, fibroblaster eller endotelceller46,47,48. Det har blitt observert at den samkulturen av ALI-PBEC med granulocytt-makrofagkolonistimulerende faktor (GM-CSF) eller M-CSF-differensierte makrofager påvirker medfødte epitelresponser og reparasjon48. Det er viktig å merke seg at i slike kokulturmodeller kan mediumkompatibilitet være et problem. Siden mediet som brukes til epitelcellekulturen i luftveiene er utviklet spesielt for PBEC og kanskje ikke er optimalt egnet for andre celletyper, er optimalisering nødvendig. En annen type fremskritt sett innen luftveisbiologi som isolerte PBECer kan brukes til, er bruken av Organs-on-Chips (OoC) teknologi49,50. Ved hjelp av denne teknologien kan påvirkningen av de mekaniske kreftene til pust og blodstrøm, som strekk, luft og middels strømning, studeres 29.
Interdonorvariabilitet kan være signifikant ved bruk av PBEC fra ulike donorer, og det er derfor viktig å vurdere å bruke celler fra flere donorer for å ta hensyn til denne variasjonen i epitelcellekulturstudier. Siden kulturen av ALI-PBECs er tidkrevende og forbundet med betydelige kostnader, undersøkes muligheten til å etablere ALI-PBEC-kulturer ved å blande celler fra forskjellige donorer i en cellekulturinnsats. På denne måten kan piloteksperimenter lett utføres ved hjelp av primære celler, før analysere responsene til kulturer avledet fra ulike individuelle givere . I tillegg kan donorer med ulike karakteristika (f.eks. ulik alderskategori eller kjønn) grupperes for eksplorative studier. Ved bruk av donorblandinger er det viktig å sørge for at det er likt antall donorer til stede, for å forhindre muligheten for at en donor dominerer utfallet som følge av en høyere spredningsrate. Derfor utvides celler fra individuelle donorer separat og sås med en høyere tetthet i innsatsen sammenlignet med såceller fra en individuell donor, for å minimere spredning i innsatsen før overgang til ALI. Respons fra donorblandinger og korresponderende enkeltdonorer ble sammenlignet ved å studere infeksjonskinetikken til SARS-CoV-2. Ved hjelp av RT-qPCR og immunfluorescensfarging ble det observert at donorblandingen ga en god representasjon av de ulike enkeltdonorene, ved å vise tilsvarende antall produserte viruspartikler og tilsvarende antall infiserte celler28.
For å bli et akseptabelt alternativ for dyremodeller, bør genredigering av dyrkede bronkiale epitelceller være mulig51. RNA-interferensteknologi ved bruk av små forstyrrende RNA (siRNA) i ALI-PBECs undersøkes, men siden cellene må transfekteres med siRNA under den nedsenkede fasen av kulturen, opprettholdes ikke knockdown tilstrekkelig under ALI-kulturen på grunn av den lange kulturvarigheten, med mindre siRNA-transfeksjon ofte gjentas under kultur52. Likevel kan siRNA med hell brukes til å modifisere genuttrykk i nedsenkede basalceller. Andre har med hell brukt CRISPR / Cas9-teknologi for å oppnå genredigering i primære ALI-luftveisepitelcellekulturer med ribonukleoprotein (RNP) levering 53. Ved bruk av slike teknikker er det viktig at cellene opprettholder sin fulle differensieringskapasitet. Fordi primære luftveiscellekulturer ikke kan passeres på ubestemt tid, er klonal ekspansjon av genredigerte celler ikke lett, og tilsetning av medium for å velge transfekterte celler er tungvint. Derfor er det vanskelig å oppnå den ønskelige knockdown i alle dyrkede celler. Et alternativ til å generere knockout-kloner er bruken av knock-out-strategier i hiPSCs54 og bruken av disse cellene for å generere luftveisepitelceller. Et annet, om enn suboptimalt, alternativ er å etablere en udødeliggjort PBEC-linje for å klonalt utvide genredigerte celler55.
Protokollen som presenteres her er en måte å generere en godt differensiert pseudostratifisert ALI-PBEC, men andre protokoller har også blitt funnet å etablere en slik kultur, med mindre og større forskjeller i forhold til den presenterte protokollen. Etter vår mening er laboratorievalidering av kulturmetoder og streng kvalitetskontroll avgjørende for at ALI-PBEC-systemet og lignende kultursystemer av luftveisepitelceller, skal bli et gyldig alternativ for dyreforsøk.
Divulgazioni
The authors have nothing to disclose.
Acknowledgements
Studiene som bruker modellen beskrevet i dette bidraget har blitt støttet av en rekke finansieringsorganisasjoner, inkludert Lung Foundation Nederland, Nederlands organisasjon for helseforskning og utvikling (ZonMw, COVID-19 MKMD-stipend), Dutch Society for the Replacement of Animal Testing (Stichting Proefdiervrij, stipend #114025007), samt forskningstilskudd fra selskaper som Boehringer Ingelheim og Galapagos. Figur 1 ble laget med BioRender.com.
Materials
| 1,000 ohm test resistor | World Precision Instruments | N/A | Used to calibrate the EVOM2 Epithelial Voltohmmeter |
| 4-[2-(5,6,7,8-Tetrahydro-5,5,8,8-tetramethyl-2-naphthalenyl)ethynyl)-benzoic acid (EC 23) | Tocris | 4011 | Used in cBD medium |
| 6-well Clear TC-treated Multiple Well Plates | Corning | 3506 | Used in the first step to grow the cells isolated form the bronchial ring |
| Airway Epithelial Cell Growth Medium Kit | PromoCell | C-21160 | Used to compare to cBD medium |
| Bead Bath 20 Liter | Lab Armor | 74220-720 | Used to pre-warm cell culture solutions |
| BEGM Bronchial Epithelial Cell Growth Medium BulletKit | LONZA | CC-3170 | Used to compare to cBD medium |
| Bovine albumin fraction V (BSA) | Thermo Fisher Scientific | 15260037 | Used in coating solution |
| Bovine pituitary extract (BPE) | Thermo Fisher Scientific | 37000-015 | Used in c-KSFM |
| Bronchial epithelial cell growth supplement (BEpiCGS) | ScienCell Research Laboratories | 3262 | Used in cBD medium |
| Bronchial epithelial cell medium-basal (BEpiCM-b) | ScienCell Research Laboratories | SCC3211-b | Used in cBD medium |
| Cell culture inserts; 12 mm Transwell with 0.4 µm pore polyester membrane insert | Corning | 3460 | Cell culture inserts used in the protocol |
| Cell culture inserts; 12-well inserts, 0.4 µm PET clear | CellQART made by SABEU | 9310412 | Cell culture inserts used to compare with Corning cell culture inserts |
| Cell culture inserts; 12-well ThinCert Tissue culture Inserts | Greiner Bio-One | 82050-032 | Cell culture inserts used to compare with Corning cell culture inserts |
| CELLSTAR flask, TC, PS, 250 ml, 75 cm2 | Greiner Bio-One | 658170 | Used to expand the number cells |
| CFX Maestro 1.0 | Bio-Rad | N/A | Software program for analyzing qPCR data generated with the CFX384 System |
| CFX384 Touch Real-Time PCR Detection System | Bio-Rad | 1855484 | qPCR detection system |
| Chopstick electrode set | World Precision Instruments | STX2 | Used to measure electrical resistance in ALI-PBEC |
| CO2-Incubator | PHCbi | MCO-170AICUV-PE | Cell culture incubator used for mycplasma free cell cultures |
| CO2-Incubator | Hereaus | Heracell 150 | Cell culture incubator used for possibly mycplasma infected cell cultures |
| Coolcell Container | Corning | 432006 | Used to cryopreserve cells at -80 °C before transfer to liquid N2 |
| Countess 3 Automated cell counter | Thermo Fisher Scientific | AMQAX2000 | Used to count cells and determine the cell concentration |
| Cryovials | Nalgene | 479-3224 | Used to cryopreserve cells in |
| D-Glucose | Avantor VWR BDH CHEMICALS | 101174Y | Used in soft trypsin |
| Dimethyl sulfoxide (DMSO) | Avantor VWR | 0231 | Used in cell freeze medium |
| dNTP (10 mM) | Promega | U1515 | Used in the synthesis of cDNA |
| Dulbecco's Modified Eagle's Medium (DMEM) + 4500 mg/l D-Glucose | STEMCELL Technologies | 36250 | Used in cBD medium |
| Dulbecco's Modified Eagle's Medium (DMEM) 4.5 g/l glucose with l-glutamine | LONZA | LOBE12-604F | Used in cBD medium to compare with DMEM from other manufacturers |
| Dulbecco's Modified Eagle's Medium (DMEM), high glucose, pyruvate | Thermo Fisher Scientific | 41966029 | Used in cBD medium to compare with DMEM from other manufacturers |
| Epidermal growth factor (EGF) | Thermo Fisher Scientific | 37000-015 | Used in c-KSFM |
| Ethylenediaminetetraacetic acid (EDTA) | Avantor VWR BDH CHEMICALS | 443885J | Used in soft trypsin |
| EVOM2 Epithelial Voltohmmeter | World Precision Instruments | 91799 | Used with the chopstick electrode set to measure electrical resistance in ALI-PBEC |
| Fibronectin solution, Human | PromoCell | C-43060 | Used in coating solution |
| Glutamax | Thermo Fisher Scientific | 35050038 | Used in cBD medium |
| Hanks balanced salt solution (HBSS) | ScienCell Research Laboratories | SCC0313 | Used to dissolve protease XIV |
| IQ SYBR Green Super mix | Bio-Rad | 170887 | qPCR reagent |
| Isoproterenol hydrochloride, (-)- | Sigma-Aldrich | I-6504 | Used in c-KSFM |
| Keratinocyte-SFM (KSFM) | Thermo Fisher Scientific | 17005-034 | Used in c-KSFM |
| Maxwell RSC Instrument | Promega | AS4500 | Automated RNA isolation system |
| Maxwell RSC simplyRNA Tissue Kit | Promega | AS1340 | Used to isolate total RNA with the Maxwell RSC Instrument |
| M-MLV Reverse transcriptase | Promega | M5301 | Used in the synthesis of cDNA |
| M-MLV Reverse transcriptase 5X reaction buffer | Promega | M531A | Used in the synthesis of cDNA |
| MycoStrip | InvivoGen | rep-mys-10 | Used to detect the presence of mycoplasma in cell culture samples |
| N-2-hydroxyethylpiperazine-N-2-ethane sulfonic acid (HEPES) | Thermo Fisher Scientific | 15630056 | Used in cBD medium |
| Oligo(dT)15 | Qiagen | 79237 | Used in the synthesis of cDNA |
| Penicillin/Streptomycin solution (Pen/Strep) | ScienCell Research Laboratories | SCC0513 | Used as antibiotic in c-KSFM and cBD medium |
| Phosphate buffered saline (PBS) | LUMC pharmacy | N/A | Used in different steps of the protocol |
| Pneumacult-ALI Medium | STEMCELL Technologies | 05002 | Used to grow cells in the differentiation stage to compare to cBD medium |
| Pneumacult-Ex Plus Medium | STEMCELL Technologies | 05040 | Used to grow cells in the submerged stage to compare to cBD medium |
| Primer, ATP5B, forward | Integrated DNA Technologies | N/A | Nucleotide sequence: TCACCCAGGCTGGTTCAGA |
| Primer, ATP5B, reverse | Integrated DNA Technologies | N/A | Nucleotide sequence: AGTGGCCAGGGTAGGCTGAT |
| Primer, FOXJ1, forward | Integrated DNA Technologies | N/A | Nucleotide sequence: GGAGGGGACGTAAATCCCTA |
| Primer, FOXJ1, reverse | Integrated DNA Technologies | N/A | Nucleotide sequence: TTGGTCCCAGTAGTTCCAGC |
| Primer, MUC5AC, forward | Integrated DNA Technologies | N/A | Nucleotide sequence: CCTTCGACGGACAGAGCTAC |
| Primer, MUC5AC, reverse | Integrated DNA Technologies | N/A | Nucleotide sequence: TCTCGGTGACAACACGAAAG |
| Primer, MUC5B, forward | Integrated DNA Technologies | N/A | Nucleotide sequence: GGGCTTTGACAAGAGAGT |
| Primer, MUC5B, reverse | Integrated DNA Technologies | N/A | Nucleotide sequence: AGGATGGTCGTGTTGATGCG |
| Primer, RPL13A, forward | Integrated DNA Technologies | N/A | Nucleotide sequence: AAGGTGGTGGTCGTACGCTGTG |
| Primer, RPL13A, reverse | Integrated DNA Technologies | N/A | Nucleotide sequence: CGGGAAGGGTTGGTGTTCATCC |
| Primer, SCGB1A1, forward | Integrated DNA Technologies | N/A | Nucleotide sequence: ACATGAGGGAGGCAGGGGCTC |
| Primer, SCGB1A1, reverse | Integrated DNA Technologies | N/A | Nucleotide sequence: ACTCAAAGCATGGCAGCGGCA |
| Primer, TP63, forward | Integrated DNA Technologies | N/A | Nucleotide sequence: CCACCTGGACGTATTCCACTG |
| Primer, TP63, reverse | Integrated DNA Technologies | N/A | Nucleotide sequence: TCGAATCAAATGACTAGGAGGGG |
| Primocin | InvivoGen | ant-pm-2 | Used as antimicrobial agent against bacteria, mycoplasma, and fungi in c-KSFM medium |
| Protease XIV | Sigma-Aldrich | P5147 | Used for the enzymatic treatment of the bronchial ring |
| RNAsin Recombinant Ribonuclease inhibitor | Promega | N2515 | Used in the synthesis of cDNA |
| Soybean trypsin inhibitor (SBTI) | Sigma-Aldrich | T9128 | Used to inhibit the action of soft trypsin |
| T100 Thermal Cycler | Bio-Rad | 1861096 | Used in the synthesis of cDNA |
| TissueSAFE plus | MILESTONE MEDICAL | N/A | Vacuum transfer system for biological specimens |
| Trypan blue solution | Thermo Fisher Scientific | 15250061 | Used to count live- and dead cells |
| Trypsin 1:250 | Thermo Fisher Scientific | 27250-018 | Used in soft trypsin |
| Type I collagen solution (PureCol) | Advanced BioMatrix | 5005-B | Used in coating solution |
| Universal container, PP, with PE screw cap | Avantor VWR | 216-2053 | Used in the protocol for the Protease XIV treatment of the bronchial ring |
Riferimenti
- Aghapour, M., et al. Role of air pollutants in airway epithelial barrier dysfunction in asthma and COPD. European Respiratory Review. 31 (163), 210112 (2022).
- de Waal, A. M., Hiemstra, P. S., Ottenhoff, T. H., Joosten, S. A., vander Does, A. M. Lung epithelial cells interact with immune cells and bacteria to shape the microenvironment in tuberculosis. Thorax. 77 (4), 408-416 (2022).
- Duchesne, M., Okoye, I., Lacy, P. Epithelial cell alarmin cytokines: Frontline mediators of the asthma inflammatory response. Frontiers in Immunology. 13, 975914 (2022).
- Hewitt, R. J., Lloyd, C. M. Regulation of immune responses by the airway epithelial cell landscape. Nature Reviews Immunology. 21 (6), 347-362 (2021).
- Ruysseveldt, E., Martens, K., Steelant, B. Airway basal cells, protectors of epithelial walls in health and respiratory diseases. Frontiers in Allergy. 2, 787128 (2021).
- Alysandratos, K. D., Herriges, M. J., Kotton, D. N. Epithelial stem and progenitor cells in lung repair and regeneration. Annual Review of Physiology. 83, 529-550 (2021).
- Hammad, H., Lambrecht, B. N. Barrier epithelial cells and the control of type 2 immunity. Immunity. 43 (1), 29-40 (2015).
- Hynds, R. E., Bonfanti, P., Janes, S. M. Regenerating human epithelia with cultured stem cells: feeder cells, organoids and beyond. EMBO Molecular Medicine. 10 (2), 139-150 (2018).
- Hiemstra, P. S., Tetley, T. D., Janes, S. M. Airway and alveolar epithelial cells in culture. The European Respiratory Journal. 54 (5), 1900742 (2019).
- Saint-Criq, V., et al. Choice of differentiation media significantly impacts cell lineage and response to CFTR modulators in fully differentiated primary cultures of cystic fibrosis human airway epithelial cells. Cells. 9 (9), 2137 (2020).
- Leung, C., Wadsworth, S. J., Yang, S. J., Dorscheid, D. R. Structural and functional variations in human bronchial epithelial cells cultured in air-liquid interface using different growth media. American Journal of Physiology. Lung Cellular and Molecular Physiology. 318 (5), L1063-L1073 (2020).
- Morgan, R., et al. A medium composition containing normal resting glucose that supports differentiation of primary human airway cells. Scientific Reports. 12 (1), 1540 (2022).
- Ghosh, B., et al. Strong correlation between air-liquid interface cultures and in vivo transcriptomics of nasal brush biopsy. American Journal of Physiology. Lung Cellular and Molecular Physiology. 318 (5), L1056-L1062 (2020).
- Pezzulo, A. A., et al. The air-liquid interface and use of primary cell cultures are important to recapitulate the transcriptional profile of in vivo airway epithelia. American Journal of Physiology. Lung Cellular and Molecular Physiology. 300 (1), L25-L31 (2011).
- Dvorak, A., Tilley, A. E., Shaykhiev, R., Wang, R., Crystal, R. G. Do airway epithelium air-liquid cultures represent the in vivo airway epithelium transcriptome. American Journal of Respiratory Cell and Molecular Biology. 44 (4), 465-473 (2011).
- Legebeke, J., et al. Temporal whole-transcriptomic analysis of characterized in vitro and ex vivo primary nasal epithelia. Frontiers in Cell and Developmental Biology. 10, 907511 (2022).
- Srinivasan, B., et al. TEER measurement techniques for in vitro barrier model systems. Journal of Laboratory Automation. 20 (2), 107-126 (2015).
- van Wetering, S., et al. Regulation of secretory leukocyte proteinase inhibitor (SLPI) production by human bronchial epithelial cells: increase of cell-associated SLPI by neutrophil elastase. Journal of Investigative Medicine. 48 (5), 359-366 (2000).
- Balk, S. D. Calcium as a regulator of the proliferation of normal, but not of transformed, chicken fibroblasts in a plasma-containing medium. Proceedings of the National Academy of Sciences. 68 (2), 271-275 (1971).
- Gail, M. H., Boone, C. W., Thompson, C. S. A calcium requirement for fibroblast motility and prolifertion. Experimental Cell Research. 79 (2), 386-390 (1973).
- Dulbecco, R., Elkington, J. Induction of growth in resting fibroblastic cell cultures by Ca. Proceedings of the National Academy of Sciences. 72 (4), 1584-1588 (1975).
- van Wetering, S., et al. Epithelial differentiation is a determinant in the production of eotaxin-2 and -3 by bronchial epithelial cells in response to IL-4 and IL-13. Molecular Immunology. 44 (5), 803-811 (2007).
- Amatngalim, G. D., et al. Aberrant epithelial differentiation by cigarette smoke dysregulates respiratory host defence. The European Respiratory Journal. 51 (4), 1701009 (2018).
- Christie, V. B., et al. Retinoid supplementation of differentiating human neural progenitors and embryonic stem cells leads to enhanced neurogenesis in vitro. Journal of Neuroscience Methods. 193 (2), 239-245 (2010).
- Schrumpf, J. A., Ninaber, D. K., vander Does, A. M., Hiemstra, P. S. TGF-β1 impairs vitamin D-induced and constitutive airway epithelial host defense mechanisms. Journal of Innate Immunity. 12 (1), 74-89 (2020).
- Schrumpf, J. A., et al. Proinflammatory cytokines impair vitamin D-induced host defense in cultured airway epithelial cells. American Journal of Respiratory Cell and Molecular Biology. 56 (6), 749-761 (2017).
- Boei, J. J. W. A., et al. Xenobiotic metabolism in differentiated human bronchial epithelial cells. Archives of Toxicology. 91 (5), 2093-2105 (2017).
- Wang, Y., et al. Impact of human airway epithelial cellular composition on SARS-CoV-2 infection biology. bioRxiv. , (2021).
- Nawroth, J. C., et al. Breathing on Chip: Dynamic flow and stretch tune cellular composition and accelerate mucociliary maturation of airway epithelium in vitro. bioRxiv. , (2022).
- Horani, A., Nath, A., Wasserman, M. G., Huang, T., Brody, S. L. Rho-associated protein kinase inhibition enhances airway epithelial Basal-cell proliferation and lentivirus transduction. American Journal of Respiratory Cell and Molecular Biology. 49 (3), 341-347 (2013).
- Mou, H., et al. Dual SMAD signaling inhibition enables long-term expansion of diverse epithelial basal cells. Cell Stem Cell. 19 (2), 217-231 (2016).
- Sachs, N., et al. Long-term expanding human airway organoids for disease modeling. The EMBO Journal. 38 (4), 100300 (2019).
- Eenjes, E., et al. Disease modeling following organoid-based expansion of airway epithelial cells. American Journal of Physiology. Lung Cellular and Molecular Physiology. 321 (4), L775-L786 (2021).
- Butler, C. R., et al. Rapid expansion of human epithelial stem cells suitable for airway tissue engineering. American Journal of Respiratory and Critical Care Medicine. 194 (2), 156-168 (2016).
- Amatngalim, G. D., et al. Antibacterial defense of human airway epithelial cells from chronic obstructive pulmonary disease patients induced by acute exposure to nontypeable Haemophilus influenzae: modulation by cigarette smoke. Journal of Innate Immunity. 9 (4), 359-374 (2017).
- Plebani, R., et al. 3D lung tissue models for studies on SARS-CoV-2 pathophysiology and therapeutics. International Journal of Molecular Sciences. 23 (17), 10071 (2022).
- Wong, A. P., et al. Directed differentiation of human pluripotent stem cells into mature airway epithelia expressing functional CFTR protein. Nature Biotechnology. 30 (9), 876-882 (2012).
- Fulcher, M. L., Gabriel, S., Burns, K. A., Yankaskas, J. R., Randell, S. H. Well-differentiated human airway epithelial cell cultures. Methods in Molecular Biology. 107, 183-206 (2005).
- Cao, J., Wong, C. K., Yin, Y., Lam, C. W. K. Activation of human bronchial epithelial cells by inflammatory cytokines IL-27 and TNF-alpha: implications for immunopathophysiology of airway inflammation. The Journal of Cellular Physiology. 223 (3), 788-797 (2010).
- Tsao, P. N., et al. Notch signaling controls the balance of ciliated and secretory cell fates in developing airways. Development. 136 (13), 2297-2307 (2009).
- Laoukili, J., et al. IL-13 alters mucociliary differentiation and ciliary beating of human respiratory epithelial cells. The Journal of Clinical Investigation. 108 (12), 1817-1824 (2001).
- Mertens, T. C. J., et al. Cigarette smoke differentially affects IL-13-induced gene expression in human airway epithelial cells. Physiological Reports. 5 (13), e13347 (2017).
- Zarcone, M. C., et al. Effect of diesel exhaust generated by a city bus engine on stress responses and innate immunity in primary bronchial epithelial cell cultures. Toxicology in Vitro. 48, 221-231 (2018).
- vander Does, A. M., et al. Early transcriptional responses of bronchial epithelial cells to whole cigarette smoke mirror those of in-vivo exposed human bronchial mucosa. Respiratory Research. 23 (1), 227 (2022).
- Wang, Y., Ninaber, D. K., van Schadewijk, A., Hiemstra, P. S. Tiotropium and fluticasone inhibit rhinovirus-induced mucin production via multiple mechanisms in differentiated airway epithelial cells. Frontiers in Cellular and Infection Microbiology. 10, 278 (2020).
- Ronaghan, N. J., et al. M1-like, but not M0- or M2-like, macrophages, reduce RSV infection of primary bronchial epithelial cells in a media-dependent fashion. PLoS One. 17 (10), 0276013 (2022).
- Gindele, J. A., et al. Opposing effects of in vitro differentiated macrophages sub-type on epithelial wound healing. PLoS One. 12 (9), e0184386 (2017).
- van Riet, S., et al. Modulation of airway epithelial innate immunity and wound repair by M(GM-CSF) and M(M-CSF) macrophages. Journal of Innate Immunity. 12 (5), 410-421 (2020).
- Huh, D., et al. Reconstituting organ-level lung functions on a chip. Science. 328 (5986), 1662-1668 (2010).
- Stucki, A. O., et al. A lung-on-a-chip array with an integrated bio-inspired respiration mechanism. Lab on a Chip. 15 (5), 1302-1310 (2015).
- Peters-Hall, J. R., et al. Long-term culture and cloning of primary human bronchial basal cells that maintain multipotent differentiation capacity and CFTR channel function. American Journal of Physiology. Lung Cellular and Molecular Physiology. 315 (2), L313-L327 (2018).
- Bartman, C. M., Stelzig, K. E., Linden, D. R., Prakash, Y. S., Chiarella, S. E. Passive siRNA transfection method for gene knockdown in air-liquid interface airway epithelial cell cultures. American Journal of Physiology. Lung Cellular and Molecular Physiology. 321 (1), L280-L286 (2021).
- Koh, K. D., et al. Efficient RNP-directed human gene targeting reveals SPDEF is required for IL-13-induced mucostasis. American Journal of Respiratory Cell and Molecular Biology. 62 (3), 373-381 (2020).
- Bhargava, N., et al. Development of an efficient single-cell cloning and expansion strategy for genome edited induced pluripotent stem cells. Molecular Biology Reports. 49 (8), 7887-7898 (2022).
- Angelopoulou, A., Papaspyropoulos, A., Papantonis, A., Gorgoulis, V. G. CRISPR-Cas9-mediated induction of large chromosomal inversions in human bronchial epithelial cells. STAR Protocols. 3 (2), 101257 (2022).

