Daglige overføringer, arkivering av populasjoner og måling av kondisjon i det langsiktige evolusjonseksperimentet med Escherichia coli
Summary
Denne protokollen beskriver hvordan man opprettholder Escherichia coli Long-Term Evolution Experiment (LTEE) ved å utføre daglige overføringer og periodiske nedfrysninger, og hvordan man gjennomfører konkurranseanalyser for å måle kondisjonsforbedringer i utviklede bakterier. Disse prosedyrene kan tjene som en mal for forskere som starter sine egne mikrobielle evolusjonseksperimenter.
Abstract
Long-Term Evolution Experiment (LTEE) har fulgt tolv populasjoner av Escherichia coli som de har tilpasset seg et enkelt laboratoriemiljø i mer enn 35 år og 77.000 bakteriegenerasjoner. Oppsettet og prosedyrene som brukes i LTEE illustrerer pålitelige og reproduserbare metoder for å studere mikrobiell evolusjon. I denne protokollen beskriver vi først hvordan LTEE-populasjonene overføres til ferskt medium og dyrkes hver dag. Deretter beskriver vi hvordan LTEE-populasjonene regelmessig kontrolleres for mulige tegn på forurensning og arkiveres for å gi en permanent frossen “fossilpost” for senere studier. Flere sikkerhetstiltak som er inkludert i disse prosedyrene, er utformet for å forhindre forurensning, oppdage ulike problemer når de oppstår, og gjenopprette fra forstyrrelser uten å sette tilbake fremdriften i eksperimentet nevneverdig. En måte at det generelle tempoet og karakteren av evolusjonære endringer overvåkes i LTEE, er ved å måle konkurransedyktigheten til populasjoner og stammer fra eksperimentet. Vi beskriver hvordan samkulturkonkurranseanalyser gjennomføres og gir både et regneark og en R-pakke (fitnessR) for beregning av relativ kondisjon fra resultatene. I løpet av LTEE har oppførselen til enkelte populasjoner endret seg på interessante måter, og nye teknologier som helgenomsekvensering har gitt ytterligere veier for å undersøke hvordan populasjonene har utviklet seg. Vi avslutter med å diskutere hvordan de opprinnelige LTEE-prosedyrene har blitt oppdatert for å imøtekomme eller dra nytte av disse endringene. Denne protokollen vil være nyttig for forskere som bruker LTEE som et modellsystem for å studere sammenhenger mellom evolusjon og genetikk, molekylærbiologi, systembiologi og økologi. Mer bredt gir LTEE en prøvd og sann mal for de som begynner sine egne evolusjonseksperimenter med nye mikrober, miljøer og spørsmål.
Introduction
I februar 1988 inokulerte Richard Lenski tolv kolber som inneholdt et definert glukosebegrenset vekstmedium med klonale kulturer av Escherichia coli ved University of California, Irvine1. Dagen etter overførte han 1% av kulturen fra hver kolbe til et sett med nye kolber som inneholdt friskt vekstmedium. Denne 1:100-fortynningen tillot bakteriepopulasjonene å ekspandere 100 ganger før den tilgjengelige glukosen ble uttømt, tilsvarende omtrent 62/3 generasjoner av celledelinger. Denne prosedyren ble gjentatt dagen etter og har vært hver dag siden, med noen få avbrudd. Disse daglige overføringene har fortsatt, selv om eksperimentet ble flyttet, først til Michigan State University i 1992, og deretter til University of Texas i Austin i 2022. Hele tiden har nye mutasjoner kontinuerlig generert genetisk variasjon i disse E. coli-populasjonene , og naturlig utvalg har ført til at utviklede celler utkonkurrerer sine forfedre.
Lenski designet dette eksperimentet, nå kjent som Long-Term Evolution Experiment (LTEE), for å undersøke evolusjonens dynamikk og repeterbarhet. For å svare på disse spørsmålene inkluderte han flere viktige funksjoner i utformingen av det eksperimentelle oppsettet og dets protokoller2. En av disse funksjonene var det forsiktige valget av en modellorganisme. De opprinnelige tolv populasjonene ble alle startet fra enkeltkolonier som delte en umiddelbar felles stamfar, Escherichia coli B-stammen REL606. Denne stammen ble valgt fordi den allerede hadde blitt vanlig brukt i laboratorieinnstillinger, reprodusert helt aseksuelt, og inneholdt ingen plasmider eller intakte profager 3,4 – som alle gjør det enklere å studere utviklingen. Et annet valg som forenklet forsøket var å bruke en svært lav konsentrasjon av glukose i vekstmediet for å begrense tettheten av celler i hver kolbe etter vekst. Bruk av lav celletetthet var ment å gjøre det lettere å analysere endringer i populasjonskondisjon ved å redusere potensialet for utvikling av økologiske interaksjoner i populasjoner (f.eks. ved kryssmating)5.
REL606 kan ikke bruke ʟ-arabinose som karbon- og energikilde (Ara−) på grunn av en punktmutasjon i araA-genet. Før oppstart av LTEE ble en spontan mutant med en gjenopprettet araA-sekvens, betegnet REL607, isolert fra REL6066. REL607 er i stand til å vokse på ʟ-arabinose (Ara+). REL606 ble brukt til å starte seks av LTEE-populasjonene, og REL607 ble brukt til å starte de andre seks. Arabinose er ikke tilstede i vekstmediet som brukes under LTEE, så REL607 oppfører seg på samme måte som REL606 under disse forholdene. Men når de er belagt på tetrazolium arabinose (TA) agar, danner Ara– og Ara+-celler henholdsvis røde og hvite kolonier. Denne metoden for å diskriminere mellom de to forfedre E. coli-stammene og deres etterkommere er ganske nyttig. Den kan brukes til å oppdage krysskontaminering mellom LTEE-populasjoner. Det hjelper også med å måle kondisjonen til en Ara-stamme eller befolkning i forhold til en Ara+ når de konkurrerer mot hverandre. Kondisjon måles ved å sette opp en samkultur av motsatt markerte konkurrenter og deretter overvåke hvordan frekvensene til røde og hvite kolonier (oppnådd ved å spre fortynninger av kulturen på TA-plater) endres mellom når konkurrentene først blandes og etter en eller flere vekstsykluser under samme forhold som LTEE. Representasjonen av den mer tilpassede celletypen vil øke i løpet av hver vekstsyklus.
Et annet kritisk trekk ved LTEE er at prøver av de utviklende populasjonene periodisk arkiveres. Når det blandes med et kryobeskyttelsesmiddel som glyserol, kan E. coli-celler fryses og senere gjenopplives7. Som en del av LTEE-protokollen, hver 75. dag (som tilsvarer omtrent 500 generasjoner), blandes en del av hver populasjon som ikke ble overført til en ny kolbe med glyserol, deles opp mellom flere hetteglass og lagres i en fryser. Denne frosne “fossilposten” gjorde det mulig for forskere å utføre de første studiene av LTEE, der de gjenopplivet de utviklede E. coli-populasjonene fra forskjellige tidspunkter og konkurrerte dem mot forfedrenes stammer for å spore hvor raskt kondisjonen økte1. Kondisjonsutviklingen har blitt målt på nytt med jevne mellomrom etter hvert som flere “lag” av den frosne “fossilposten” har blitt bevart. Den overordnede konklusjonen fra disse målingene er at kondisjonen fortsetter å forbedre seg i LTEE til denne dagen, selv etter så mange generasjoner med evolusjon i samme miljø 8,9,10.
Hva har gjort det mulig for LTEE å fortsette så lenge? Mange av de samme funksjonene som gjorde det mulig å stille og besvare de opprinnelige spørsmålene, har også fungert som sikkerhetstiltak og feilsikring mot uunngåelige forstyrrelser på grunn av uflaks, menneskelig feil og verdenshendelser. Hver dag, når kulturene overføres til et nytt vekstmedium, veksler forskeren som utfører overføringene mellom Ara− og Ara+ populasjoner. Deretter, når populasjonene er frosset, kan de bli belagt på selektiv og indikatoragar for å sjekke om noen “nabo” populasjoner ved et uhell har blitt kryssforurenset eller blandet opp (f.eks. Hvite kolonier er i en populasjon som bare skal danne røde kolonier) eller forurenset med fremmede mikrober (f.eks. Uventede kolonimorfologier eller celletettheter). I tilfelle en befolkning har blitt kompromittert, kan dens forfedre gjenopplives fra fryseren og føres videre på sin plass. Ara-markørene og det frosne arkivet tjener dermed to formål både som eksperimentelle ressurser og sikkerhetstiltak.
Fordi historien er så godt bevart og lett tilgjengelig, har LTEE-prøver blitt studert ved hjelp av teknologier som ikke eksisterte da eksperimentet begynte. For eksempel har helgenomsekvensering blitt brukt til å undersøke dynamikken til mutasjoner i LTEE-populasjonene 11,12,13,14,15, og transkriptomikk og ribosomal profilering har blitt brukt til å undersøke endringer i genuttrykk 16,17. Genetiske verktøy har blitt brukt til å rekonstruere stammer som varierer ved enkeltmutasjoner eller kombinasjoner av flere utviklede mutasjoner for å forstå deres effekter på kondisjon og ulike fenotyper 18,19,20,21. Prøver fra den frosne “fossilposten” blir enkelt etterfylt slik at deler av eller hele kopier av eksperimentets historie kan sendes til andre laboratorier. LTEE-prøver finnes nå på alle kontinenter unntatt Antarktis, og de blir studert av forskere som er yngre enn selve eksperimentet. De robuste metodene til LTEE og utviklede E. coli-prøver og stammer fra dens historiske rekord har også tjent som utgangspunkt for evolusjonseksperimenter som undersøker andre spørsmål og miljøer 22,23,24,25,26,27,28,29.
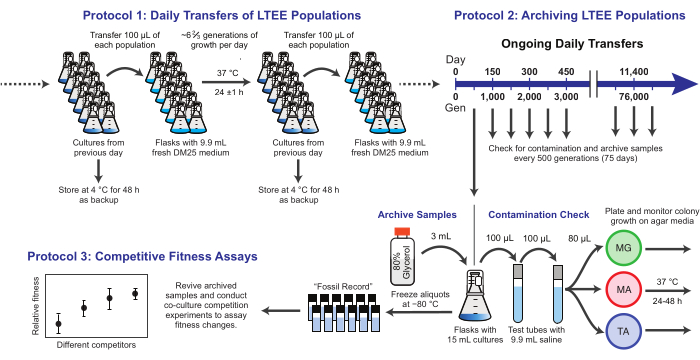
Figur 1: Oversikt over LTEE-prosedyrer. Klikk her for å se en større versjon av denne figuren.
Her demonstrerer vi tre kjerneprotokoller brukt i E. coli Long-Term Evolution Experiment (figur 1). Vi beskriver: (1) hvordan man utfører de daglige overføringene, (2) hvordan man arkiverer populasjonsprøver og klonale isolater, og (3) hvordan man utfører og analyserer samarbeidskonkurranseanalyser for å måle kondisjonsforskjeller. Vårt håp er at disse protokollene fremmer fortsatt bruk av LTEE-ressurser og informerer utformingen av nye mikrobielle evolusjonseksperimenter.
Protocol
Representative Results
Discussion
Langsiktig motstandskraft av LTEE og dens metoder
E. coli Long-Term Evolution Experiment (LTEE) er nå inne i sitt fjerde tiår. For et mikrobielt evolusjonseksperiment av hvilken som helst varighet er det avgjørende å opprettholde et reproduserbart miljø, unngå forurensning, arkivere prøver og måle kondisjon nøyaktig. LTEE demonstrerer flere tidstestede strategier for å oppnå disse målene, inkludert bruk av godt ristede kolber som skaper et homogent miljø og et kjemisk definert vekstmedium som støtter en lav celletetthet. Videre bruker LTEE forfedrestammer som er forskjellige i en genetisk markør som gir en fenotype (kolonifarge) som både er lett screenet og selektivt nøytral i evolusjonsmiljøet. Denne eksperimentelle designfunksjonen gjør det mulig å identifisere intern og ekstern kontaminering og forenkler måling av kondisjon. Imidlertid har ikke alle prosedyrene og sikkerhetstiltakene som har blitt brukt av LTEE siden 1988 vist seg å være like robuste. Noen metoder som var pålitelige da LTEE begynte, har blitt mindre effektive etter hvert som E. coli-populasjonene har utviklet seg. Heldigvis kan disse problematiske metodene nå utvides eller erstattes ved hjelp av teknologier utviklet siden eksperimentets begynnelse.
Oppdage forurensning
Påvisning av forurensning er kritisk for LTEE. Forurensning kan være av to typer: mellom LTEE-populasjoner (krysskontaminering) og med mikrober fra miljøet (ekstern forurensning). For det meste forhindrer forsiktig bruk av aseptiske teknikker og nøye oppmerksomhet under medieforberedelse og de daglige overføringene begge typer forurensning, men de skjer. Tidlig i forsøket kunne plating på TA-agar brukes til å oppdage tilfeller av krysskontaminering fordi overføringer alltid har vekslet mellom Ara− og Ara + populasjoner. Fingeravtrykket av følsomhet og motstand av disse E. coli til visse bakteriofager var også ment å være en designfunksjon som kunne skille LTEE-populasjonene fra vanlige E. coli-laboratoriestammer som kan forurense dem4. Imidlertid har disse genetiske markørene blitt upålitelige etter hvert som eksperimentet har utviklet seg (f.eks. Noen populasjoner danner ikke lenger kolonier på TA-agar)10,35. Heldigvis har populasjonene genetisk divergert da de har opplevd separate evolusjonære historier under forsøket, noe som har skapt nye genetiske markører som nå kan brukes til å oppdage krysskontaminering. For eksempel har hver populasjon utviklet en unik kombinasjon av mutasjoner i pykF– og nadR-genene 14,36,37. Noen ganger forsterker PCR og Sanger-sekvenserer disse to genene for å teste om kolonier med uvanlige morfologier eller farger skyldes krysskontaminering. Etter hvert som kostnadene ved helgenom- og helpopulasjonssekvensering fortsetter å falle, kan rutinemessig sekvensering av LTEE-populasjonene snart være mulig, og dermed presentere nye muligheter til å overvåke dem for tegn på forurensning.
Måling av konkurransedyktig kondisjon
Et annet tilfelle der LTEE har vokst ut av sine opprinnelige metoder, er at kondisjonen til den utviklede E. coli har økt i det eksperimentelle miljøet i en slik grad at man ikke lenger direkte kan måle kondisjonen til dagens populasjoner i forhold til deres forfedre ved hjelp av protokollen beskrevet her. De utviklede populasjonene utkonkurrerer forfedrene i en slik grad at få eller ingen forfedrekolonier gjenstår å telle etter en en-dags konkurranse. En tilnærming for å håndtere denne store kondisjonsforskjellen er å bruke ulike startforhold mellom stammene, og vekte de innledende volumene som blandes mot den mindre spreke konkurrenten (f.eks. 90 μL forfedre og 10 μL utviklet konkurrent). En annen tilnærming er å identifisere en utviklet Ara−-klon som har høyere kondisjon enn LTEE-forfedre, isolere en spontan Ara+ revertant mutant av den ved å velge på MA-agar, og deretter verifisere at revertantstammen har samme kondisjon som foreldrene ved å bruke en konkurranseanalyse 6,38. Dette nye Ara−/Ara+-paret kan deretter brukes som et sett med vanlige konkurrerende stammer i stedet for REL606/REL607. Ideelt sett vil den utviklede Ara−-klonen valgt som en felles konkurrent (og dens Ara+ revertant) ha middels kondisjon i forhold til alle stammer av interesse i et eksperiment. I løpet av de første 50 000 generasjonene av LTEE produserte ikke disse to tilnærmingene (ved bruk av ulike startforhold eller en felles konkurrent) meningsfullt forskjellige kondisjonsmålinger i forhold til den typiske tilnærmingen39.
Disse endringene i konkurranseprotokollen gjør visse forenklende forutsetninger som kanskje ikke alltid er sanne. Det ene er at kondisjonsmålinger er transitive. Det vil si at hvis vi konkurrerer to populasjoner hver mot en felles konkurrentstamme separat, kan vi utlede den relative kondisjonen til de to populasjonene til hverandre. Dette forholdet har vist seg å være sant for LTEE40, for det meste, men det er ikke for andre eksperimenter41. En årsak til dette avviket kan være utviklingen av negative frekvensavhengige kondisjonseffekter. Denne situasjonen oppstår når stammer isolert fra to forskjellige divergerte linjer fra populasjon A-2 av LTEE konkurreres mot hverandre19,42. Hver har en fordel når det er sjeldent, på grunn av kryssfôring, noe som stabiliserer deres sameksistens. Sekvenseringsdata som viser langsiktig sameksistens av linjer med forskjellige sett med mutasjoner antyder at lignende interaksjoner også kan ha oppstått i andre LTEE-populasjoner14,43, selv om det ikke er klart om de er sterke nok til å merkbart endre kondisjonsestimater. Endelig betyr utviklingen av aerob vekst på citrat i populasjon A-3 av LTEE32 at kondisjonen til disse cellene nå inkorporerer bruken av en “privat” ressurs når de konkurreres mot celler som ikke kan bruke citrat, noe som kompliserer tolkningen av disse resultatene. Til tross for disse unntakene har bruken av lav glukosekonsentrasjon og godt rystet miljø utvilsomt forenklet kondisjonssammenligninger mellom LTEE-stammer og populasjoner.
Ved senere generasjoner danner noen av LTEE-populasjonene ikke lenger kolonier på TA-agar, noe som gjør det vanskelig eller umulig å utføre konkurranseeksperimenter ved hjelp av selv modifiserte protokoller10. Alternative metoder som ikke krever kolonivekst kan potensielt brukes til å bestemme den relative representasjonen av to konkurrenter, for eksempel FREQ-seq som bruker neste generasjons sekvensering for å telle andelen avlesninger som inneholder to alternative alleler i en amplikon44. Denne metoden eller en lignende kan potensielt brukes med Ara-allelene eller med nyutviklede mutasjoner, som de i pykF og nadR, versus forfedresekvensen. Å utføre genetiske modifikasjoner som introduserer andre typer nøytrale markører, kan også brukes til å måle relativ kondisjon. For eksempel har fluorescerende proteingener blitt satt inn i kromosomene til celler i LTEE-avleggereksperimenter, slik at konkurrenter kan telles ved hjelp av flowcytometri45. En annen tilnærming, som åpner muligheten for å blande sammen mer enn to stammer i samme konkurransekolbe, er å sette inn strekkoder som kan PCR-forsterkes og sekvenseres i genomene til forskjellige konkurrenter. Denne tilnærmingen har blitt brukt til avstamningssporing i evolusjonseksperimenter46. Både flowcytometri og strekkodesekvensering kan nøyaktig måle mye mer ekstreme forhold mellom to stammer versus kolonitelling (fordi de kan spørre > 10.000 celler / genomer mot < 500 som kan telles på en agarplate), så bruk av disse metodene lover også å øke det dynamiske området når det gjelder kondisjonsforskjeller som kan måles i forhold til en vanlig konkurrent.
Alternative design for langsiktige mikrobielle evolusjonseksperimenter
For alle sine dyder er LTEE ikke perfekt. Visse aspekter av designen gjør den arbeidsintensiv og utsatt for menneskelige feil. For eksempel må en forsker hver dag komme inn i laboratoriet og pipette mellom Erlenmeyer-kolber for å fortsette eksperimentet. Konkurranseeksperimenter kan også utgjøre skremmende logistiske hindringer, gitt at krav til sterilt glass, media, inkubatorplass og kolonitelling raskt eskalerer når selv et lite antall konkurrenter blir testet med beskjeden replikering. Vi blir ofte spurt om hvorfor vi ikke utnytter laboratorieautomatiseringssystemer, for eksempel pipetteringsroboter som opererer på mikroplater med 96 brønner, eller kontinuerlige kultursystemer, som kjemostater eller turbidomstater. Svaret er enkelt: LTEE er på en måte en fange av sin egen lange historie. Vi tør ikke avvike fra 10 ml kulturer som rister med en bestemt hastighet i 50 ml Erlenmeyer-kolber fordi dette ville risikere å endre eksperimentet fundamentalt. Subtile aspekter av miljøet som disse populasjonene har tilpasset seg i flere tiår (f.eks. mengden lufting), vil bli endret i mikroplater eller kontinuerlige kultursystemer. Populasjonens flaskehals ved hver overføring kan også være forskjellig (mindre i mikroplater, for eksempel), noe som endrer evolusjonsdynamikken. Kort sagt, avvik fra metodene beskrevet her ville gjøre LTEE til et annet eksperiment, eller i det minste risikere å introdusere en diskontinuitet som ville forstyrre evolusjonære baner.
Forskere som designer nye evolusjonseksperimenter, bør vurdere disse andre måtene å forplante mikrobielle populasjoner på, samtidig som de er klar over deres potensielle fordeler og ulemper. Bruk av pipetteringsroboter for å overføre populasjoner i mikrobrønnplater er logistisk enklere på noen måter og kan vise seg å være ganske kraftig på grunn av det høye antallet replikerende populasjoner som kan forplantes på denne måten47,48,49. Automatiserte overføringer i de fleste nåværende oppsett skjer imidlertid ikke under helt sterile forhold, noe som øker sannsynligheten for ekstern forurensning. For å forhindre forurensning blir vekstmediet ofte supplert med antibiotika, som blir et trekk ved miljøet som påvirker evolusjonen. Overføringer i mikrobrønnplater er også mer utsatt for krysskontamineringshendelser. Til slutt har miljøet til mikrobrønnplater – spesielt hvis de ikke ristes – en tendens til å velge for veggvekst, aggregering og andre fenomener som kan komplisere utviklingen ved å skape flere nisjer i en brønn. Bruk av rike medier eller høye konsentrasjoner av næringsstoffer for å holde populasjonsstørrelsene store i små brønner vil sannsynligvis forverre disse kompleksitetene. Hvis slike interaksjoner oppstår, kan de gjøre måling og tolking av kondisjon mye vanskeligere.
Kontinuerlige kultursystemer for mikrobiell evolusjon inkluderer kjemostater, hvor friskt medium pumpes kontinuerlig inn og kultur pumpes ut, og turbidostater, hvor kulturer periodisk fortynnes gjennom automatisert sensing og pumping for å opprettholde celler i en tilstand av konstant vekst. Disse systemene er svært nyttige når man ønsker å modellere mikrobiell fysiologi og evolusjon fordi de unngår at mikrober overgår mellom vekst og sult ved å holde dem i et miljø som alltid har næringsstoffer50. Man kan til og med legge til sensorer som gjør sanntidsmålinger av optisk tetthet, O2-forbruk, pH og andre aspekter av en kulturs miljø og vekst. Imidlertid krever nåværende kontinuerlige kultursystemer enten dyre utstyrskjøp eller spesialisert ekspertise for å bygge tilpassede oppsett51,52,53,54. Også veggvekst, der celler unnslipper fortynning ved å feste seg til kulturkammeret, bedevils evolusjonær dynamikk i kontinuerlige kultursystemer med mindre de periodisk steriliseres. På grunn av disse begrensningene har de fleste chemostat- og turbidostat-evolusjonseksperimenter hittil vært av begrenset varighet og/eller involvert relativt få populasjoner under utvikling uavhengig sammenlignet med serieoverføringsevolusjonseksperimenter.
Konklusjon
Metodene vi demonstrerer her for LTEE er avgjørende for å studere sin unike historiske rekord og fortsette den åpne utviklingen av disse E. coli-populasjonene. De gir også et utgangspunkt for andre som vurderer nye evolusjonseksperimenter som kan dra nytte av laboratorieautomatisering eller legge tilbake ulike elementer av kompleksiteten som finnes i naturlige miljøer som bevisst ble utelatt fra LTEE. Siden 1988 har eksperimentell evolusjon blomstret som et felt. I løpet av denne tiden har forskere i laboratorier over hele verden demonstrert den enorme fleksibiliteten i denne tilnærmingen for å studere evolusjon, innovere ved å introdusere kreative eksperimentelle design og overvåke resultatene ved hjelp av ny teknologi. Metodene til LTEE representerer ikke et endepunkt, men vi håper de vil fortsette å inspirere og gi grunnlag for feltet langt inn i fremtiden.
Divulgazioni
The authors have nothing to disclose.
Acknowledgements
Vi takker Richard Lenski og de mange forskerne som har studert og bidratt til å opprettholde Long-Term Evolution Experiment med E. coli, inkludert spesielt Neerja Hajela. LTEE støttes for tiden av National Science Foundation (DEB-1951307).
Materials
| 2,3,5-Triphenyltetrazolium chloride (TTC) | Sigma-Aldrich | T8877 | |
| 20 mL Glass Beaker | Sigma-Aldrich | CLS100020 | |
| 50 mL Erlenmeyer Flasks | Sigma-Aldrich | CLS498050 | |
| Agar | Sigma-Aldrich | A1296 | |
| Ammonium Sulfate | Sigma-Aldrich | AX1385 | |
| Antifoam | Sigma-Aldrich | A5757 | |
| Arabinose | Sigma-Aldrich | A3256 | |
| Freezer Box (2") | VWR | 82007-142 | |
| Freezer Box (3") | VWR | 82007-144 | |
| Freezer Box Cell Divider (49-place) | VWR | 82007-150 | |
| Freezer Box Cell Divider (81-place) | VWR | 82007-154 | |
| Freezer Vials (1/2-Dram) | VWR | 66009-816 | |
| Freezer Vials (2-Dram) | VWR | 66010-560 | |
| Glucose | Sigma-Aldrich | G8270 | |
| Glycerol | Fisher Scientific | G33 | |
| Magnesium Sulfate | Sigma-Aldrich | M7506 | |
| Metal Tray | Winco | SPJP-202 | |
| Petri Dish | Fisher Scientific | FB0875712 | |
| Potassium Phosphate Dibasic Trihydrate | Sigma-Aldrich | P5504 | |
| Potassium Phosphate Monobasic | Sigma-Aldrich | P5379 | |
| Sodium Chloride | Sigma-Aldrich | M7506 | |
| Sodium Citrate Tribasic Dihydrate | Sigma-Aldrich | C7254 | |
| Test Tube Cap (18mm) | VWR | 10200-142 | |
| Test Tube Rack (18mm, steel) | Adamas-Beta | N/A | Test Tube Racks Stainless Steel Grid Arrangement 72 Holes (17-19 mm) |
| Test Tubes (18 x 150 mm) | VWR | 47729-583 | |
| Thiamine, Hydrochloride | Millipore | 5871 | |
| Tryptone | Gibco | 211705 | |
| Yeast Extract | Gibco | 212750 |
Riferimenti
- Lenski, R. E., Rose, M. R., Simpson, S. C., Tadler, S. C. Long-term experimental evolution in Escherichia coli. I. Adaptation and divergence during 2,000 generations. The American Naturalist. 138 (6), 1315-1341 (1991).
- Fox, J. W., Lenski, R. E. From here to eternity-the theory and practice of a really long experiment. PLoS Biology. 13 (6), e1002185 (2015).
- Daegelen, P., Studier, F. W., Lenski, R. E., Cure, S., Kim, J. F. Tracing ancestors and relatives of Escherichia coli B, and the derivation of B strains REL606 and BL21(DE3). Journal of Molecular Biology. 394 (4), 634-643 (2009).
- Studier, F. W., Daegelen, P., Lenski, R. E., Maslov, S., Kim, J. F. Understanding the differences between genome sequences of Escherichia coli B strains REL606 and BL21(DE3) and comparison of the E. coli B and K-12 genomes. Journal of Molecular Biology. 394 (4), 653-680 (2009).
- Barrick, J. E., Lenski, R. E. Genome dynamics during experimental evolution. Nature Reviews Genetics. 14 (12), 827-839 (2013).
- Lenski, R. E. Experimental studies of pleiotropy and epistasis in Escherichia coli. II. Compensation for maladaptive pleiotropic effects associated with resistance to virus T4. Evolution. 42 (3), 425-432 (1988).
- Calcott, P. H., Gargett, A. M. Mutagenicity of freezing and thawing. FEMS Microbiology Letters. 10 (2), 151-155 (1981).
- Lenski, R. E., Travisano, M. Dynamics of adaptation and diversification: a 10,000-generation experiment with bacterial populations. Proceedings of the National Academy of Sciences of the United States of America. 91 (15), 6808-6814 (1994).
- Wiser, M. J., Ribeck, N., Lenski, R. E. Long-term dynamics of adaptation in asexual populations. Science. 342 (6164), 1364-1367 (2013).
- Lenski, R. E., et al. Sustained fitness gains and variability in fitness trajectories in the long-term evolution experiment with Escherichia coli. Proceedings of the Royal Society B: Biological Sciences. 282 (1821), 20152292 (2015).
- Barrick, J. E., et al. Genome evolution and adaptation in a long-term experiment with Escherichia coli. Nature. 461 (7268), 1243-1247 (2009).
- Blount, Z. D., Barrick, J. E., Davidson, C. J., Lenski, R. E. Genomic analysis of a key innovation in an experimental Escherichia coli population. Nature. 489 (7417), 513-518 (2012).
- Tenaillon, O., et al. Tempo and mode of genome evolution in a 50,000-generation experiment. Nature. 536 (7615), 165-170 (2016).
- Good, B. H., McDonald, M. J., Barrick, J. E., Lenski, R. E., Desai, M. M. The dynamics of molecular evolution over 60,000 generations. Nature. 551 (7678), 45-50 (2017).
- Consuegra, J., et al. Insertion-sequence-mediated mutations both promote and constrain evolvability during a long-term experiment with bacteria. Nature Communications. 12 (1), 980-980 (2021).
- Cooper, T. F., Rozen, D. E., Lenski, R. E. Parallel changes in gene expression after 20,000 generations of evolution in Escherichia coli. Proceedings of the National Academy of Sciences of the United States of America. 100 (3), 1072-1077 (2003).
- Favate, J. S., Liang, S., Cope, A. L., Yadavalli, S. S., Shah, P. The landscape of transcriptional and translational changes over 22 years of bacterial adaptation. eLife. 11, e81979 (2022).
- Khan, A. I., Dinh, D. M., Schneider, D., Lenski, R. E., Cooper, T. F. Negative epistasis between beneficial mutations in an evolving bacterial population. Science. 332 (6034), 1193-1196 (2011).
- Plucain, J., et al. Epistasis and allele specificity in the emergence of a stable polymorphism in Escherichia coli. Science. 343 (6177), 1366-1369 (2014).
- Quandt, E. M., Deatherage, D. E., Ellington, A. D., Georgiou, G., Barrick, J. E. Recursive genomewide recombination and sequencing reveals a key refinement step in the evolution of a metabolic innovation in Escherichia coli. Proceedings of the National Academy of Sciences of the United States of America. 111 (6), 2217-2222 (2014).
- Leon, D., D’Alton, S., Quandt, E. M., Barrick, J. E. Innovation in an E. coli evolution experiment is contingent on maintaining adaptive potential until competition subsides. PLoS Genetics. 14 (4), e1007348 (2018).
- Bennett, A. F., Lenski, R. E., Mittler, J. E. Evolutionary adaptation to temperature. I. Fitness responses of Escherichia coli to changes in its thermal environment. Evolution. 46 (1), 16-30 (1992).
- Kibota, T. T., Lynch, M. Estimate of the genomic mutation rate deleterious to overall fitness in E. coli. Nature. 381 (6584), 694-696 (1996).
- Friesen, M. L., Saxer, G., Travisano, M., Doebeli, M. Experimental evidence for sympatric ecological diversification due to frequency-dependent competition in Escherichia coli. Evolution. 58 (2), 245-260 (2004).
- Cooper, T. F. Recombination speeds adaptation by reducing competition between beneficial mutations in populations of Escherichia coli. PLoS Biology. 5 (9), e225 (2007).
- Cooper, T. F., Lenski, R. E. Experimental evolution with E. coli in diverse resource environments. I. Fluctuating environments promote divergence of replicate populations. BMC Evolutionary Biology. 10, 11 (2010).
- Quan, S., et al. Adaptive evolution of the lactose utilization network in experimentally evolved populations of Escherichia coli. PLoS Genetics. 8 (1), e1002444 (2012).
- Deatherage, D. E., Kepner, J. L., Bennett, A. F., Lenski, R. E., Barrick, J. E. Specificity of genome evolution in experimental populations of Escherichia coli evolved at different temperatures. Proceedings of the National Academy of Sciences of the United States of America. 114 (10), E1904-E1912 (2017).
- Izutsu, M., Lake, D. M., Matson, Z. W. D., Dodson, J. P., Lenski, R. E. Effects of periodic bottlenecks on the dynamics of adaptive evolution in microbial populations. BioRixv. , 4457 (2021).
- Chavarria-Palma, J. E., Blount, Z. D., Barrick, J. E. . LTEE Media Recipes. , (2022).
- Barrick, J. E., Lake, D. M. fitnessR: fitnessR-v1.0.0. barricklab. , (2023).
- Blount, Z. D., Borland, C. Z., Lenski, R. E. Historical contingency and the evolution of a key innovation in an experimental population of Escherichia coli. Proceedings of the National Academy of Sciences of the United States of America. 105 (23), 7899-7906 (2008).
- Grant, N. A., Magid, A. A., Franklin, J., Dufour, Y., Lenski, R. E. Changes in cell size and shape during 50,000 generations of experimental evolution with Escherichia coli. Journal of Bacteriology. 203 (10), 22 (2021).
- Wickham, H. . ggplot2: Elegant Graphics for Data Analysis. , (2016).
- Meyer, J. R., et al. Parallel changes in host resistance to viral infection during 45,000 generations of relaxed selection. Evolution. 64 (10), 3024-3034 (2010).
- Woods, R., Schneider, D., Winkworth, C. L., Riley, M. A., Lenski, R. E. Tests of parallel molecular evolution in a long-term experiment with Escherichia coli. Proceedings of the National Academy of Sciences of the United States of America. 103 (24), 9107-9712 (2006).
- . LTEE-Ecoli: genomics resources for the Long-Term Evolution Experiment with Escherichia coli Available from: https://github.com/barricklab/LTEE-Ecoli (2022)
- Izutsu, M., Lenski, R. E. Experimental test of the contributions of initial variation and new mutations to adaptive evolution in a novel environment. Frontiers in Ecology and Evolution. 10, 958406 (2022).
- Wiser, M. J., Lenski, R. E. A comparison of methods to measure fitness in Escherichia coli. PLoS One. 10 (5), 0126210 (2015).
- de Visser, J. A. G. M., Lenski, R. E. Long-term experimental evolution in Escherichia coli. XI. Rejection of non-transitive interactions as cause of declining rate of adaptation. BMC Evolutionary Biology. 2 (1), 19 (2002).
- Paquin, C. E., Adams, J. Relative fitness can decrease in evolving asexual populations of S. cerevisiae. Nature. 306 (5941), 368-371 (1983).
- Rozen, D. E., Lenski, R. E. Long-Term Experimental Evolution in Escherichia coli. VIII. Dynamics of a balanced polymorphism. The American Naturalist. 155 (1), 24-35 (2000).
- Quandt, E. M., Gollihar, J., Blount, Z. D., Ellington, A. D., Georgiou, G., Barrick, J. E. Fine-tuning citrate synthase flux potentiates and refines metabolic innovation in the Lenski evolution experiment. eLife. 4, e09696 (2015).
- Chubiz, L. M., Lee, M. -. C., Delaney, N. F., Marx, C. J. FREQ-Seq: a rapid, cost-effective, sequencing-based method to determine allele frequencies directly from mixed populations. PLoS One. 7 (10), e47959 (2012).
- Gallet, R., Cooper, T. F., Elena, S. F., Lenormand, T. Measuring selection coefficients below 10-3: method, questions, and prospects. Genetica. 190 (1), 175-186 (2012).
- Levy, S. F., et al. Quantitative evolutionary dynamics using high-resolution lineage tracking. Nature. 519 (7542), 181-186 (2015).
- Lang, G. I., Botstein, D., Desai, M. M. Genetic variation and the fate of beneficial mutations in asexual populations. Genetica. 188 (3), 647-661 (2011).
- Frenkel, E. M., et al. Crowded growth leads to the spontaneous evolution of semistable coexistence in laboratory yeast populations. Proceedings of the National Academy of Sciences. 112 (36), 11306-11311 (2015).
- Jordt, H., et al. Coevolution of host-plasmid pairs facilitates the emergence of novel multidrug resistance. Nature Ecology and Evolution. 4 (6), 863-869 (2020).
- Gresham, D., Dunham, M. J. The enduring utility of continuous culturing in experimental evolution. Genomics. 104 (6), 399-405 (2014).
- Miller, A. W., Befort, C., Kerr, E. O., Dunham, M. J. Design and use of multiplexed chemostat arrays). Journal of Visualized Experiments. (72), e50262 (2013).
- Toprak, E., et al. Building a morbidostat: an automated continuous-culture device for studying bacterial drug resistance under dynamically sustained drug inhibition. Nature Protocols. 8 (3), 555-567 (2013).
- Wong, B. G., Mancuso, C. P., Kiriakov, S., Bashor, C. J., Khalil, A. S. Precise, automated control of conditions for high-throughput growth of yeast and bacteria with eVOLVER. Nature Biotechnology. 36 (7), 614-623 (2018).
- Ekkers, D. M., Branco Dos Santos, F., Mallon, C. A., Bruggeman, F., Van Doorn, G. S. The omnistat: A flexible continuous-culture system for prolonged experimental evolution. Methods in Ecology and Evolution. 11 (8), 932-942 (2020).

