एक स्वचालित सेल प्रोसेसर पर चिमेरिक एंटीजन रिसेप्टर टी सेल विनिर्माण
Summary
यह लेख नैदानिक उपयोग के लिए चिमेरिक एंटीजन रिसेप्टर टी कोशिकाओं के लिए विनिर्माण प्रक्रिया का विवरण देता है, विशेष रूप से एक स्वचालित सेल प्रोसेसर का उपयोग करके जो वायरल ट्रांसडक्शन और टी कोशिकाओं की खेती करने में सक्षम है। हम सिफारिशें प्रदान करते हैं और उन नुकसानों का वर्णन करते हैं जिन्हें प्रारंभिक चरण के नैदानिक परीक्षण की प्रक्रिया विकास और कार्यान्वयन के दौरान माना जाना चाहिए।
Abstract
चिमेरिक एंटीजन रिसेप्टर (सीएआर) -टी कोशिकाएं विभिन्न घातक और गैर-घातक रोगों के उपचार के लिए एक आशाजनक इम्यूनोथेराप्यूटिक दृष्टिकोण का प्रतिनिधित्व करती हैं। सीएआर-टी कोशिकाएं आनुवंशिक रूप से संशोधित टी कोशिकाएं हैं जो एक चिमेरिक प्रोटीन को व्यक्त करती हैं जो सेल सतह लक्ष्य को पहचानती है और बांधती है, जिसके परिणामस्वरूप लक्ष्य सेल की हत्या होती है। पारंपरिक सीएआर-टी सेल विनिर्माण विधियां श्रम-गहन, महंगी हैं, और संदूषण का खतरा उठा सकती हैं। क्लिनीएमएसीएस प्रोडिजी, एक स्वचालित सेल प्रोसेसर, एक बंद प्रणाली में नैदानिक पैमाने पर सेल थेरेपी उत्पादों के निर्माण की अनुमति देता है, संदूषण के जोखिम को कम करता है। प्रसंस्करण एक कंप्यूटर के नियंत्रण में अर्ध-स्वचालित रूप से होता है और इस प्रकार प्रक्रिया में मानव भागीदारी को कम करता है, जो समय बचाता है और परिवर्तनशीलता और त्रुटियों को कम करता है।
यह पांडुलिपि और वीडियो इस प्रोसेसर का उपयोग करके सीएआर-टी कोशिकाओं के निर्माण के लिए टी सेल ट्रांसडक्शन (टीसीटी) प्रक्रिया का वर्णन करता है। टीसीटी प्रक्रिया में सीडी 4 + / सीडी 8 + टी सेल संवर्धन, सक्रियण, वायरल वेक्टर के साथ पारगमन, विस्तार और फसल शामिल है। गतिविधि मैट्रिक्स का उपयोग करते हुए, एक कार्यक्षमता जो इन चरणों के आदेश और समय की अनुमति देती है, टीसीटी प्रक्रिया को बड़े पैमाने पर अनुकूलित किया जा सकता है। हम वर्तमान अच्छे विनिर्माण अभ्यास (सीजीएमपी) के अनुपालन में सीएआर-टी सेल विनिर्माण का वॉक-थ्रू प्रदान करते हैं और आवश्यक रिलीज परीक्षण और प्रीक्लिनिकल प्रयोगों पर चर्चा करते हैं जो एक जांच नई दवा (आईएनडी) आवेदन का समर्थन करेंगे। हम व्यवहार्यता का प्रदर्शन करते हैं और नैदानिक सीएआर-टी सेल विनिर्माण के लिए अर्ध-स्वचालित प्रक्रिया का उपयोग करने के फायदे और नुकसान पर चर्चा करते हैं। अंत में, हम एक चल रहे अन्वेषक-शुरू किए गए नैदानिक परीक्षण का वर्णन करते हैं जो बाल चिकित्सा बी-सेल दुर्भावनाओं को लक्षित करता है [NCT05480449] एक उदाहरण के रूप में कि इस विनिर्माण प्रक्रिया को नैदानिक सेटिंग में कैसे लागू किया जा सकता है।
Introduction
एक चिमेरिक एंटीजन रिसेप्टर (सीएआर) को व्यक्त करने के लिए इंजीनियर टी कोशिकाओं के दत्तक हस्तांतरण ने दुर्दम्य बी-सेल विकृतियों 1,2,3,4,5 के रोगियों के इलाज में उल्लेखनीय प्रभावकारिता दिखाई है। हालांकि, सीएआर-टी कोशिकाओं के लिए पारंपरिक विनिर्माण विधियां श्रम-गहन, समय लेने वाली हैं, और अत्यधिक विशिष्ट चरणों को पूरा करने के लिए अत्यधिक प्रशिक्षित तकनीशियनों की आवश्यकता होती है। उदाहरण के लिए, एक ऑटोलॉगस सीएआर-टी सेल उत्पाद की पारंपरिक विनिर्माण प्रक्रिया में टी कोशिकाओं को समृद्ध करने के लिए घनत्व ढाल सेंट्रीफ्यूजेशन, एल्यूट्रिएशन या चुंबकीय पृथक्करण, एक बाँझ फ्लास्क में वायरल वेक्टर के साथ सक्रियण और पारगमन और फसल और सूत्रीकरण से पहले बायोरिएक्टर में विस्तार शामिल है। विभिन्न प्रणालियां हाल ही में उभरी हैं जिनका उद्देश्य इस प्रक्रिया को आंशिक रूप से स्वचालित करना है। उदाहरण के लिए, Miltenyi CliniMACS Prodigy (इसके बाद “प्रोसेसर” के रूप में संदर्भित) एक स्वचालित सेल प्रोसेसिंग डिवाइस है जो इनमें से कई चरणों को स्वचालित फैशन 6,7,8,9 में कर सकता है। पारंपरिक और स्वचालित सीएआर-टी विनिर्माण विधियों की गहन चर्चा हाल ही में समीक्षा लेख10 में प्रस्तुत की गई है।
प्रोसेसर हेमटोपोइएटिक पूर्वज कोशिकाओं के प्रसंस्करण के लिए एक अमेरिकी खाद्य और औषधि प्रशासन (एफडीए) -अनुमोदित चिकित्सा उपकरण क्लिनीएमएसीएस प्लस की कार्यक्षमता पर बनाता है। प्रोसेसर में एक सेल खेती इकाई शामिल है जो कोशिकाओं की स्वचालित धुलाई, विभाजन और खेती की अनुमति देती है (चित्रा 1)। टी सेल ट्रांसडक्शन (टीसीटी) प्रक्रिया प्रोसेसर डिवाइस के भीतर एक पूर्व निर्धारित कार्यक्रम है जो बड़े पैमाने पर मैनुअल सीएआर-टी सेल निर्माण को दोहराता है। टीसीटी एक ग्राफिकल यूजर इंटरफेस (“गतिविधि मैट्रिक्स,” चित्रा 2) का उपयोग करके अनुकूलन योग्य सेल प्रसंस्करण की अनुमति देता है। क्योंकि प्रोसेसर कई चरणों को स्वचालित करता है और एक मशीन में कई उपकरणों की कार्यक्षमता को समेकित करता है, इसके लिए प्रौद्योगिकीविदों से कम प्रशिक्षण और विशेष समस्या निवारण कौशल की आवश्यकता होती है। चूंकि सभी चरण एक बंद, एकल-उपयोग ट्यूबिंग सेट के भीतर किए जाते हैं, प्रोसेसर को खुली विनिर्माण प्रक्रिया के लिए स्वीकार्य माने जाने की तुलना में कम कठोर एयर-हैंडलिंग बुनियादी ढांचे वाली सुविधाओं में संचालित किया जा सकता है। उदाहरण के लिए, हम आईएसओ कक्षा 8 (ईयू ग्रेड सी के बराबर) के रूप में प्रमाणित सुविधा में प्रोसेसर का संचालन कर रहे हैं।
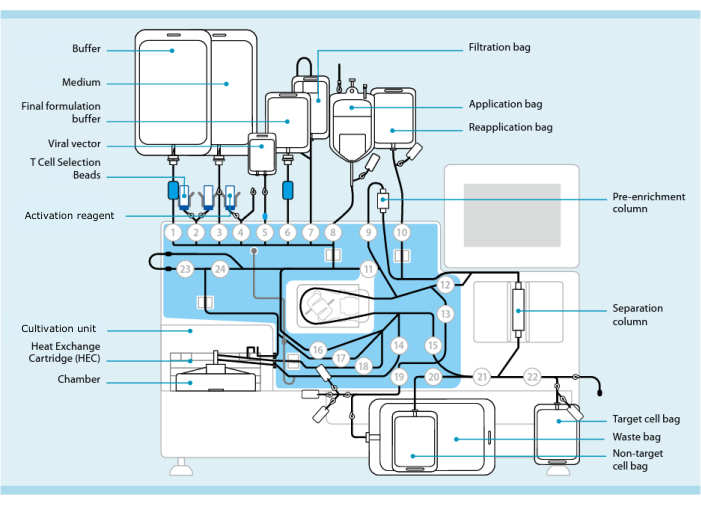
चित्रा 1: टी सेल ट्रांसडक्शन सिस्टम का उपयोग करके सीएआर-टी सेल विनिर्माण। ट्यूबिंग सेट स्थापित प्रोसेसर दिखाया गया है। ट्यूबिंग सेट बाँझ वेल्डिंग के माध्यम से प्रसंस्करण बफर, कल्चर माध्यम और लेंटिवायरल वेक्टर युक्त बैग जैसे अन्य घटकों को जोड़ने की अनुमति देता है। एक बार जब ल्यूकाफेरेसिस उत्पाद को एप्लिकेशन बैग में जोड़ा जाता है, तो इसे टी सेल चयन मोतियों के साथ लेबल किया जा सकता है, पृथक्करण कॉलम के माध्यम से पारित किया जा सकता है, और फिर पुन: आवेदन बैग में स्थानांतरित किया जा सकता है। चयनित कोशिकाओं को तब संस्कृति के लिए उपकरण की खेती इकाई में निर्देशित किया जाता है और सक्रियण अभिकर्मक के साथ सक्रिय किया जाता है (सामग्री की तालिका देखें)। अंतिम उत्पाद लक्ष्य सेल बैग में एकत्र किया जाता है। प्रक्रिया के दौरान, गुणवत्ता नियंत्रण के लिए नमूने निकालना संभव है। सर्कल के अंदर ग्रे नंबर प्रोसेसर पर क्रमांकित वाल्व का प्रतिनिधित्व करते हैं जो टयूबिंग सेट के माध्यम से तरल पथ को निर्देशित करते हैं। 11 से अनुमति के साथ पुन: प्रस्तुत किया गया। कृपया इस आंकड़े का एक बड़ा संस्करण देखने के लिए यहाँ क्लिक करें.
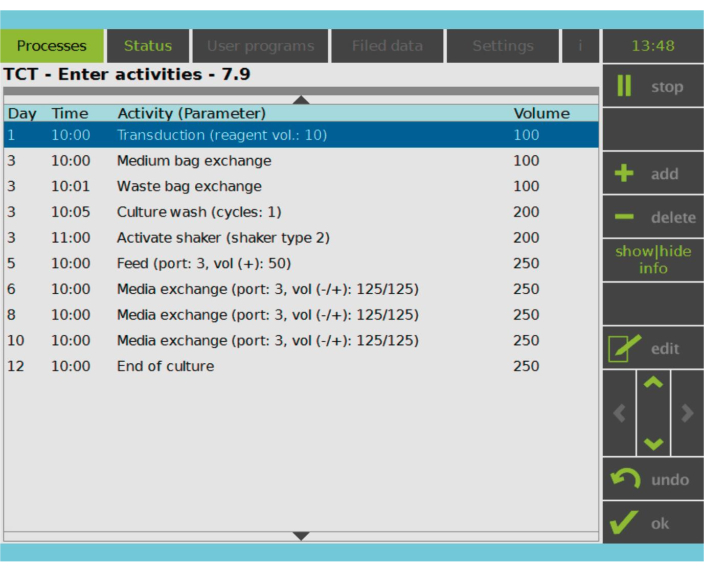
चित्र 2: गतिविधि मैट्रिक्स। टी सेल चयन और सक्रियण के बाद, सीएआर-टी सेल विनिर्माण प्रक्रिया का शेष पूरी तरह से अनुकूलन योग्य है। गतिविधियों को जोड़ा या हटाया जा सकता है और उचित दिन और समय के लिए शेड्यूल किया जा सकता है, और गतिविधि के बाद संस्कृति वॉल्यूम निर्दिष्ट किया जा सकता है (वॉल्यूम)। उदाहरण के लिए, ट्रांसडक्शन गतिविधि को दिन 1 पर सुबह 10:00 बजे शुरू करने के लिए कॉन्फ़िगर किया गया था, और गतिविधि के अंत में संस्कृति की मात्रा 100 एमएल के रूप में सेट की गई थी। गतिविधि मैट्रिक्स को खेती की अवधि के दौरान संपादित किया जा सकता है। प्रसंस्करण उपकरण की एकीकृत स्क्रीन पर प्रक्रिया की स्थिति की निगरानी की जा सकती है। कृपया इस आंकड़े का एक बड़ा संस्करण देखने के लिए यहाँ क्लिक करें.
इस पांडुलिपि का उद्देश्य प्रोसेसर का उपयोग करके सीएआर-टी कोशिकाओं के निर्माण का एक विस्तृत वॉक-थ्रू प्रदान करना है और इसके अतिरिक्त इन-प्रोसेस और उत्पाद रिलीज परीक्षण पर मार्गदर्शन प्रदान करना है जो नियामकों द्वारा एक जांच नई दवा (आईएनडी) आवेदन को मंजूरी देने के लिए आवश्यक होगा। प्रस्तुत प्रोटोकॉल विक्रेता के अनुशंसित दृष्टिकोण के करीब रहता है और आईएनडी 28617 के लिए अंतर्निहित प्रोटोकॉल है, जिसका वर्तमान में एकल-केंद्र अन्वेषक-शुरू किए गए चरण I / II नैदानिक परीक्षण में मूल्यांकन किया जा रहा है। इस परीक्षण का उद्देश्य बी सेल तीव्र लिम्फोब्लास्टिक ल्यूकेमिया (बी-एएलएल) या बी-वंश लिम्फोब्लास्टिक लिम्फोमा (बी-एलएलवाई) के रोगियों के लिए मानवकृत सीडी 19-निर्देशित ऑटोलॉगस सीएआर-टी कोशिकाओं के निर्माण के लिए इस प्रोसेसर का उपयोग करने की सुरक्षा और प्रभावकारिता निर्धारित करना NCT05480449 है। परीक्षण सितंबर 2022 में शुरू हुआ और बी-एएलएल या बी-एलएलवाई के साथ 0-29 वर्ष की आयु के 89 रोगियों को भर्ती करने की योजना है। हम पांडुलिपि में परीक्षण से कुछ विनिर्माण परिणामों की रिपोर्ट करते हैं।
हम यह बताना चाहते हैं कि यद्यपि पांडुलिपि को पालन करने के चरणों के साथ एक प्रोटोकॉल के रूप में प्रस्तुत किया गया है, लेकिन इसे दूसरों के लिए अपनी सीएआर-टी सेल विनिर्माण प्रक्रिया को अनुकूलित करना शुरू करने के लिए एक प्रारंभिक बिंदु माना जाना चाहिए। प्रस्तुत प्रोटोकॉल में संभावित विविधताओं की एक गैर-व्यापक सूची में शामिल हैं: शुरुआती सामग्री के रूप में क्रायोसंरक्षित टी कोशिकाओं के बजाय ताजा का उपयोग करना; टी सेल संवर्धन की एक अलग विधि का उपयोग करना या इसे पूरी तरह से छोड़ना; आईएल 2 के बजाय आईएल 7 / आईएल 15 जैसे विभिन्न मीडिया और साइटोकिन कॉकटेल का उपयोग करना; मानव एबी सीरम की एकाग्रता को बदलना या इसे पूरी तरह से छोड़ना; पारगमन का समय; “मल्टी-हिट” ट्रांसडक्शन का उपयोग करना; अलग-अलग आंदोलन, संस्कृति की मात्रा, और भोजन अनुसूची; न्यूक्लिक एसिड या गैर-लेंटिवायरल वैक्टर के इलेक्ट्रोपोरेशन सहित आनुवंशिक हस्तांतरण के विभिन्न तरीकों का उपयोग करना; एक अलग अंतिम फॉर्मूलेशन बफर और / या क्रायोप्रोटेक्टेंट का उपयोग करना; और बाद में जलसेक के लिए क्रायोप्रिजर्वकरने के बजाय सीएआर-टी कोशिकाओं को ताजा करना। इन विविधताओं का चिकित्सीय उत्पाद की सेलुलर संरचना और शक्ति पर महत्वपूर्ण प्रभाव पड़ सकता है।
| समग्र प्रक्रिया चरण | प्रक्रिया दिवस | तकनीकी विवरण | |||
| सेल संवर्धन। | दिन 0 | CD4+/CD8+T कक्षों का चयन | |||
| कक्ष सक्रियण | टी सेल कल्चर सीडिंग और सक्रियण। | ||||
| सेल ट्रांसडक्शन | दिन 1 | लेंटिवायरल ट्रांसडक्शन (100 एमएल कल्चर वॉल्यूम) | |||
| सेल विस्तार (सेल फॉर्मूलेशन के बाद) | दिन 2 | — | |||
| दिन 3 | कल्चर वॉश (1 चक्र); शेकर सक्रिय; संस्कृति की मात्रा 200 एमएल तक बढ़ जाती है | ||||
| दिन 4 | — | ||||
| दिन 5 | फ़ीड (50 एमएल); संस्कृति की मात्रा 250 एमएल की अंतिम मात्रा तक पहुंचती है | ||||
| दिन 6 | इन-प्रोसेस नमूना; मीडिया एक्सचेंज (-125 एमएल / + 125 एमएल) | ||||
| दिन 7 | मीडिया एक्सचेंज (-150 एमएल / + 150 एमएल) या हार्वेस्ट | ||||
| दिन 8 | इन-प्रोसेस नमूना; मीडिया एक्सचेंज (-150 एमएल / + 150 एमएल) या हार्वेस्ट | ||||
| दिन 9 | मीडिया एक्सचेंज (-180 एमएल / + 180 एमएल) या हार्वेस्ट | ||||
| 10वां दिन | इन-प्रोसेस नमूना; मीडिया एक्सचेंज (-180 एमएल / + 180 एमएल) या हार्वेस्ट | ||||
| दिन 11 | मीडिया एक्सचेंज (-180 एमएल / + 180 एमएल) या हार्वेस्ट | ||||
| दिन 12 | मीडिया एक्सचेंज (-180 एमएल / + 180 एमएल) या हार्वेस्ट | ||||
| दिन 13 | उपज | ||||
तालिका 1: प्रक्रिया समयरेखा और अवलोकन। यह तालिका वर्तमान नैदानिक परीक्षण में नियोजित टीसीटी प्रक्रिया चरणों को सारांशित करती है [NCT05480449]। यह प्रक्रिया सीडी 4 + / सीडी 8 + चयन, कल्चर सीडिंग और दिन 0 पर सक्रियण द्वारा टी सेल संवर्धन के साथ शुरू होती है, इसके बाद दिन 1 पर पारगमन होता है। कोशिकाएं 48 घंटे तक आराम करती हैं, इसके बाद एक कल्चर वॉश, कल्चर वॉल्यूम में 200 एमएल की वृद्धि होती है, और एक हिलाने वाले तंत्र का उपयोग करके आंदोलन होता है। 6 वें दिन, पहला इन-प्रोसेस नमूना लिया जाता है। सीएआर-टी कोशिकाओं की कम से कम तीन पूर्ण खुराक (5 × 10 6 सीएआर-टी कोशिकाओं / किग्रा के लिए पर्याप्त कोशिकाएं उपलब्ध होने के बाद कोशिकाओं की कटाई की जाती है यदि रोगी <50 किलोग्राम है, अन्यथा 2.5 × 108 सीएआर-टी कोशिकाएं) और गुणवत्ता नियंत्रण परीक्षण (~ 2 × 106 सीएआर-टी कोशिकाएं); या एक बार संस्कृति कुल 4-5 x 109 कोशिकाओं तक पहुंच जाती है। संक्षेप: टीसीटी = टी सेल ट्रांसडक्शन; सीएआर-टी = चिमेरिक एंटीजन रिसेप्टर टी कोशिकाएं; एमएसीएस = चुंबकीय-सक्रिय सेल सॉर्टिंग।
Protocol
Representative Results
Discussion
सीएआर-टी सेल थेरेपी बी-सेल और अन्य विकृतियों के लिए एक आशाजनक उपचार दृष्टिकोण के रूप में उभरा है। हालांकि, पारंपरिक सीएआर-टी सेल विनिर्माण विधियों में कई सीमाएं हैं, जैसे कि उच्च लागत, श्रम-गहन उत्पादन, ?…
Divulgazioni
The authors have nothing to disclose.
Acknowledgements
लेखक इस काम में कई व्यक्तियों और संगठनों के योगदान को स्वीकार करना चाहते हैं। सेल और जीन थेरेपी प्रयोगशाला और पेन ट्रांसलेशनल और कोररिलेटिव स्टडीज लेबोरेटरी ने आईएनडी सबमिशन के लिए प्रक्रिया विकास और तैयारी के साथ मूल्यवान सहायता प्रदान की। मेलिसा वर्गीज और अमांडा डिनोफिया ने इस पांडुलिपि के तहत आईएनडी प्रस्तुतियों के लिए प्रक्रिया विकास और तैयारी में योगदान दिया। इस काम को फिलाडेल्फिया के बच्चों के अस्पताल के सेल और जीन थेरेपी सहयोगी के त्वरण अनुदान द्वारा समर्थित किया गया था। लेखक अपने तकनीकी और अनुसंधान समर्थन के लिए मिल्टेनी बायोटेक को भी धन्यवाद देना चाहते हैं। चित्रा 1 कॉपीराइट © 2023 मिल्टेनी बायोटेक बीवी एंड कंपनी केजी द्वारा कवर किया गया है; सभी अधिकार सुरक्षित.
Materials
| 12 x 75 borosilicate tubes | Charles River | TL1000 | |
| 20 mL Reagent Bag | Miltenyi Biotec | 170-076-631 | |
| 50 mL Conical Tube | Fisher | 05-539-10 | |
| 150 mL Transfer Set | Fenwal | 4R2001 | |
| 2,000 mL Transfer Set | Fenwal | 4R2041 | |
| 7AAD | Fisher Scientific | BDB559925 | |
| Alcohol Prep | Tyco/Healthcare | ||
| Bag Access | Medline | 2300E-0500 | |
| CD19 APC-Vio770 REAfinity | Miltenyi Biotec | 130-113-643 | |
| CD19 CAR Detection Reagent Biotin | Miltenyi Biotec | 130-129-550 | |
| CD19 PE | BD | 555413 | |
| CD3 APC | BD | 340440 | |
| CD4 VioBright FITC REAfinity | Miltenyi Biotec | 130-113-229 | |
| CD45 VioBlue REAfinity | Miltenyi Biotec | 130-110-637 | |
| CD8 APC-Vio770 REAfinity | Miltenyi Biotec | 130-110-681 | |
| Cellometer Reference Beads 10um | Nexcelom | B10-02-020 | |
| Cellometer Reference Beads 15um | Nexcelom | B15-02-010 | |
| Cellometer Reference Beads 5um | Nexcelom | B05-02-050 | |
| Cellometer Slides | Nexcelom | CHT4-SD100-002 | |
| CliniMACS CD4 GMP MicroBeads | Miltenyi Biotec | 276-01 | The CD4 reagent |
| CliniMACS CD8 GMP MicroBeads | Miltenyi Biotec | 275-01 | The CD8 reagent |
| CliniMACS PBS/EDTA Buffer | Miltenyi Biotec | 130-021-201 | The buffer |
| DMSO | Origen | CP-10 | |
| Freezing Bag 50 mL | Miltenyi Biotec | 200-074-400 | |
| Freezing Vial, 1.8 mL | Nunc | 12565171N | |
| Freezing Vial, 4.5 mL | Nunc | 12565161N | |
| Human AB serum | Valley Biomedical | Sterile filtered, heat inactivated | |
| Human Serum Albumin 25% | Grifols | 68516-5216-1 | |
| Human Serum Albumin 5% | Grifols | 68516-5214-1 | |
| MACS GMP Recombinant Human IL-2 | Miltenyi Biotec | 170-076-148 | The cytokines |
| MACS GMP T Cell TransAct | Miltenyi Biotec | 200-076-202 | The activation reagent |
| MycoSeq Mycoplasma Detection Kit | Life Technologies | 4460623 | |
| Needles, Hypodermic 14G | Medline | SWD200573 | |
| Needles, SlideSafe 18G | BD | B-D305918 | |
| Pipet tips, 2-200 μL, individually wrapped | Eppendorf | 022492209 | |
| Pipet tips, 50-1000 μL, individually wrapped | Eppendorf | 022492225 | |
| Pipets 10 mL | Fisher | 13-678-27F | |
| Pipets 25 mL | Fisher | 13-675-30 | |
| Pipets 5 mL | Fisher | 13-678-27E | |
| Plasmalyte-A | Baxter | 2B2544X | The electrolyte solution |
| Prodigy TS520 Tubing Set | Miltenyi Biotec | 170-076- 600 | The tubing set |
| Sterile Field | Medline | NON21001 | |
| Streptavidin PE-Vio770 | Miltenyi Biotec | 130-106-793 | |
| Syringe 1 mL | BD | 309628 | |
| Syringe 10 mL | BD | 302995 | |
| Syringe 3 mL | BD | 309657 | |
| Syringe 30 mL | BD | 302832 | |
| Syringe 50 mL | BD | 309653 | |
| TexMACS GMP Medium | Miltenyi Biotec | 170-076-306 | The medium |
| Triple Sampling Adapter | Miltenyi Biotec | 170-076-609 | |
| Viral Vector | CHOP Clinical Vector Core | huCART19 | |
| Equipment | |||
| Biological Safety Cabinet | The Baker Co | ||
| Cellometer Auto 2000 | Nexcelom | ||
| CliniMACS Prodigy | Miltenyi Biotec | 200-075-301 | The processor |
| Controlled Rate Freezer | Planer/Kryosave | ||
| Endosafe nexgen-PTS150K | Charles River | ||
| Mettler Balance | Mettler | ||
| Refrigerated Centrifuge | Thermo Fisher | ||
| Refrigerated Centrifuge | Fisher Sci | ||
| SCD Sterile Tubing Welder | Terumo | ||
| Sebra Tube Sealer | Sebra | ||
| Varitherm | Barkey | The dry thaw device | |
| XN-330 Hematology Analyzer | Sysmex |
Riferimenti
- Maude, S. L., et al. Tisagenlecleucel in children and young adults with B-cell lymphoblastic leukemia. New England Journal of Medicine. 378 (5), 439-448 (2018).
- Shah, N. N., et al. Bispecific anti-CD20, anti-CD19 CAR T cells for relapsed B cell malignancies: A phase 1 dose escalation and expansion trial. Nature Medicine. 26 (10), 1569-1575 (2020).
- Maude, S. L., et al. Chimeric antigen receptor T cells for sustained remissions in leukemia. New England Journal of Medicine. 371 (16), 1507-1517 (2014).
- Grupp, S. A., et al. Chimeric antigen receptor-modified T cells for acute lymphoid leukemia. New England Journal of Medicine. 368 (16), 1509-1518 (2013).
- Maude, S. L., et al. Efficacy of humanized CD19-targeted chimeric antigen receptor (CAR)-modified T cells in children and young adults with relapsed/refractory acute lymphoblastic leukemia. Blood. 128 (22), 217 (2016).
- Mock, U., et al. Automated manufacturing of CAR-T cells for adoptive immunotherapy using CliniMACS Prodigy. Cytotherapy. 18 (8), 1002-1011 (2016).
- Fernández, L., et al. GMP-compliant manufacturing of NKG2D CAR memory T cells using CliniMACS Prodigy. Frontiers in Immunology. 10 (10), 2361 (2019).
- Zhu, F., et al. Closed-system manufacturing of CD19 and dual-targeted CD20/19 chimeric antigen receptor T Cells using CliniMACS Prodigy device at an academic medical center. Cytotherapy. 20 (3), 394-406 (2018).
- Zhang, W., Jordan, K. R., Schulte, B., Purev, E. Characterization of clinical grade CD19 chimeric antigen receptor T cells produced using automated CliniMACS prodigy system. Drug Design, Development and Therapy. 12 (12), 3343-3356 (2018).
- Abou-El-Enein, M., et al. Scalable manufacturing of CAR T cells for cancer immunotherapy. Blood Cancer Discovery. 2 (5), 408-422 (2021).
- Miltenyi Biotec. . CliniMACS Prodigy User Manual. , (2021).
- Ghassemi, S., et al. Rapid manufacturing of non-activated potent CAR T cells. Nature Biomedical Engineering. 6 (2), 118-128 (2022).
- U.S. Department of Health and Human Services, Food and Drug Administration. . Chemistry, manufacturing, and control (CMC) information for human gene therapy investigational new drug applications (INDs) guidance for industry. , (2020).
- U.S. Department of Health and Human Services, Food and Drug Administration. . Considerations for the development of chimeric antigen receptor (CAR) T cell products draft guidance for industry. , (2022).

