Højkvalitets hjerne- og knoglemarvskerneforberedelse til enkeltkerner multiomassays
Summary
Succesen med enkeltcelle/enkeltkerner transkriptomics og multi-omics afhænger i høj grad af kvaliteten af celler/kerner. Derfor skal isolering af celler / kerner fra væv og deres oprensning være stærkt standardiseret. Denne protokol beskriver fremstillingen af kerner fra hjernen og knoglemarven til nedstrøms enkeltkerne multiomassay.
Abstract
Enkeltcelleanalyse er blevet den valgte tilgang til at afsløre kompleksiteten af biologiske processer, der kræver vurdering af variabiliteten af individuelle cellulære reaktioner på behandling eller infektion med enkeltcelleopløsning.
Mange teknikker til encelle molekylær profilering er blevet udviklet i løbet af de sidste 10 år, og flere dedikerede teknologier er blevet kommercialiseret. Den 10X Genomics dråbebaserede enkeltcelleprofilering er en udbredt teknologi, der tilbyder brugsklare reagenser til transkriptomisk og multiomisk enkeltcelleprofilering. Teknologien omfatter arbejdsgange til enkeltcelle- og enkeltkerne-RNA-sekventering (henholdsvis scRNA-Seq og snRNA-Seq), scATAC-Seq, enkeltcelleimmunprofilering (BCR/TCR-sekventering) og multiome. Sidstnævnte kombinerer transkriptionel (scRNA-Seq) og epigenetisk information (scATAC-Seq), der kommer fra den samme celle.
Kvaliteten (levedygtighed, integritet, renhed) af enkeltcelle- eller enkeltkernesuspensioner isoleret fra væv og analyseret ved hjælp af en af disse tilgange er afgørende for at generere data af høj kvalitet. Prøveforberedelsesprotokollerne bør derfor tilpasses de særlige forhold, der gør sig gældende for hvert biologisk væv, og sikre, at der dannes celle- og kernesuspensioner af høj kvalitet.
Denne artikel beskriver to protokoller til forberedelse af hjerne- og knoglemarvsprøver til downstream multiome 10X Genomics-pipelinen. Protokollerne udføres trinvis og dækker vævsdissociation, cellesortering, kerneisolering og kvalitetskontrol af forberedt kernesuspension, der bruges som udgangsmateriale til celledeling og stregkodning, biblioteksforberedelse og sekventering. Disse standardiserede protokoller producerer kernebiblioteker af høj kvalitet og robuste og pålidelige data.
Introduction
I mange år har enkeltcelleteknikker været guldstandarden til analyse af biologiske processer. De var oprindeligt begrænset til enkeltcellefænotypning gennem mikroskopi, flowcytometri og lignende assays. Et gennembrud inden for enkeltcelleanalyse kom med udviklingen af tilgange til enkeltcellemolekylær profilering, især enkeltcelle RNA-sekventering (scRNA-Seq), der muliggjorde karakterisering af hele transkriptomet af individuelle celler. Meget kraftfuld, scRNA-Seq genererer information om transkriptionsstatus for en celle i en bestemt tilstand og tid. Det giver dog ikke synlighed om genreguleringen, der driver transkription, eller om de molekylære modifikationer, der opstår over tid. For at overvinde denne begrænsning er der investeret mange bestræbelser i udviklingen af enkeltcelle multi-omics-assays, der muliggør analyse af flere faktorer og processer fra den samme celle 1,2,3,4. Den første vellykkede måling af to modaliteter inden for enkeltceller kom ved at forbinde multiplexoverfladeproteinekspressionsmønstre med det fulde transkriptom af individuelle celler i CITE-Seq-tilgangen5. Nyere evolutioner kombinerer genekspression med kromatintilgængelighed (Assay for Transposase-Accessible Chromatin ved hjælp af sekventering, ATAC-Seq) og fanger derved samtidig transkriptomiske og epigenomiske modaliteter i de samme celler (f.eks. sci-CAR)6. De første kommercielle løsninger, der tillod at forbinde transkriptomik med cellefænotype eller med epigenetiske ændringer af den samme celle, kom fra 10X Genomics.
Forsøg med encellede molekylære profilering indeholder følgende trin: (1) vævsdissociation eller fremstilling af encellede suspensioner; 2) cellerensning og/eller kerneisolering (3) opdeling og stregkodning; 4) bibliotekskonstruktion og kvalitetskontrol 5) næste generations sekventering (6) dataanalyse. Mens trin (3)-(6) kan variere betydeligt afhængigt af den anvendte teknologi, er de indledende trin generelt fælles for dem alle. Kvaliteten af den fremstillede celle/kerner suspension vil bestemme det samlede resultat af forsøget. Afhængigt af vævstypen kan det være udfordrende at opnå højkvalitets enkeltcelle / kernesuspensioner. De særlige forhold ved nogle væv, såsom hjertet, musklen, hjernen, lungen, tarmen og andre, kræver metoder til vævsforstyrrelse og kerneisolering tilpasset hver type prøve for at garantere produktionen af kerner af høj kvalitet til molekylær analyse 7,8,9,10 . Vævsforstyrrelsesmetoderne og dissociationsprotokollerne kan være mekaniske, enzymatiske (f.eks. En blanding af collagenaser og DNase) eller en kombination af de to og kan udføres manuelt eller med instrumenter (f.eks. Qiagen DSC-400, gentleMACS).
Enkeltcelleteknikker er blevet et valg af værktøj til biomedicinsk forskning. I neurobiologi kræver cellediversiteten i hjernen og kompleksiteten af deres funktioner analyse med høj opløsning og høj gennemstrømning til visualisering af sjældne cellepopulationer og til vurdering af deres heterogenitet 11,12,13,14. Sammenkædning af cellulær identitet og genregulerende mekanismer i individuelle celler giver indsigt i hjernens udvikling og fysiologi. Et andet eksempel er undersøgelser af immunrespons i forbindelse med infektiøse, autoimmune eller kræftsygdomme, som er stærkt afhængige af enkeltcelleanalyser. Heterogeniteten af immuncelleundergrupper og kompleksiteten af deres aktivitet og interaktioner med andre celletyper kræver enkeltcelleopløsning ved dechifrering af mekanismerne bag immunrespons. Immuncellerne stammer fra knoglemarven, hvor hæmatopoietiske forfædre består af gradvist differentierende celler, der erhverver og mister celleoverflademarkører gennem en trinvis proces, inden knoglemarven forlader hjemmet i periferien. Enkeltcelleanalyse giver mulighed for minutkarakterisering af cellulære udviklingsstadier. Det kan opnås gennem enkeltcellefænotypning, konventionelt udført ved multiparameterflowcytometri. Imidlertid har enkeltcelle transkriptomiske signaturer vist sig at afsløre en mere præcis identifikation af stamcelleundertyper, da disse celler fordeles i klynger, der falder ind i hinanden og derfor kan fejlidentificeres, når der anvendes en grov celleoverflademarkørmetode15. Et stigende antal undersøgelser afdækker de epigenetiske modifikationer, som hæmatopoietiske stamceller og stamceller (HSPC’er) kan erhverve ved eksponering for forskellige midler, hvilket fører til en betydelig indvirkning på immunsystemets langsigtede responsivitet 16,17,18,19. De nye multi-omics-teknologier gør det muligt at studere disse processer med enkeltcelleopløsning.
Mange protokoller for celle- og kerneisolering er blevet beskrevet for hjerne 11,20,21,22 og knoglemarvsprøver 23,24. For at minimere bias på grund af eksperimentel variabilitet er det nødvendigt at validere optimerede enkeltkerneforberedelsesprotokoller til fælles enkeltcelletranskriptomisk og epigenomisk sekventering og derved sikre reproducerbarheden af enkeltcellede multiomiske assays.
Her beskrives to robuste protokoller for kernepræparation fra (1) friskfrosset hjernevæv og (2) frisk knoglemarv HSPC’er til nedstrøms enkeltcelle Multiome-analyse (figur 1).
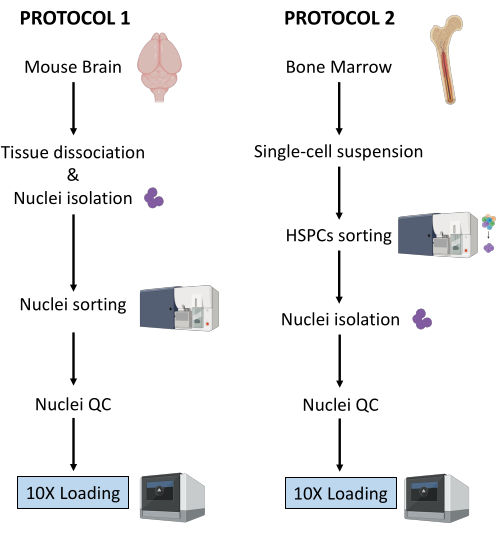
Figur 1: Skematisk gengivelse af protokoller for kerneisolering fra friskfrosset hjerne- og knoglemarvsvæv. Klik her for at se en større version af denne figur.
Protocol
Representative Results
Discussion
Forberedelse af højkvalitets celle- eller kernesuspension er af afgørende betydning for succesen med enkeltcelle eller enkeltkerner RNA-Seq og enkeltcelle multi-omiske analyser 29,30,31. Her har vi beskrevet protokoller til prøveforberedelse og kerneisolering for multiomassays fra to typer væv: hjerne og knoglemarv.
Hjerneprotokollen beskrevet i dette papir tillader genopretning af kerner af høj kvalitet fra friskfrosset hjernevæv. Det omfatter følgende trin: frosset vævsforstyrrelse, isolering af kerner, oprensning af kerner og kvalitetskontrol af det fremstillede materiale. Hjernevævet består af mange forskellige celletyper, og proceduren for vævsdissociation og kerneisolering bør bevare proportionerne af cellepopulationer som til stede i det oprindelige væv. Her blev lysisbuffersammensætningen og inkubationstiden optimeret til at muliggøre fuldstændig og skånsom lysering af alle cellepopulationer, der udgør vævet.
HSPC-protokollen for knoglemarv er noget anderledes, da det kræver et ekstra trin i begyndelsen af eksperimentet at isolere cellepopulationen af interesse fra en heterogen cellulær suspension. Efter indsamling af frisk væv lyseres røde blodlegemer, og prøven beriges til celledelmængden af interesse. De målrettede celler lyseres, kernerne isoleres, og kvaliteten af det fremstillede materiale kontrolleres.
10X Genomics giver flere protokoller valideret til kerneisolering i mange forskellige væv32,33. Virksomheden kommercialiserer også et kerneisoleringssæt med en ligetil pipeline til isolering af kerner fra valideret væv34. Disse protokoller har dog brug for yderligere optimering for at skræddersy de særlige forhold ved visse prøver. Et eksempel er de prøver, der kræver arbejde med lav celleindgang. For disse prøver er de mest udfordrende trin centrifugeringer, der skal være tilstrækkeligt strenge til at rense prøven og skånsomme nok til at undgå tab af celle / kerner. Med den her beskrevne protokol har vi tilpasset 10X Genomics Proven Protocol – Nuclei Isolation for Single Cell Multiome ATAC + GEX Sequencing (CG000365 – Rev C)27 for at finde en fin balance mellem disse to krav. Som påvist i eksemplet med fremstilling af kerner fra sorterede HSPC’er har vi forbedret genvindingen af kerner uden nogen indvirkning på prøvens kvalitet.
En yderligere udfordring er trinnet med lysering af oprensede celler til kerneisolering. Hårdere lyseringsbetingelser og længere inkubationstider kan beskadige kerner og dermed påvirke kvaliteten af sekventeringsdata. Figur 5 viser repræsentativ kernebilleddannelse fra knoglemarvsprøver ved forskellige inkubationstider med lysisbuffer og illustrerer, hvor forskellig tilstanden af kerner kan være afhængigt af cellelysen. I eksemplet med HSPC’erne har vi identificeret 3 minutters lysis som den tilstand, der resulterer i den højeste andel af sunde udseende, intakte kerner og den laveste andel af beskadigede kerner. Lysisinkubationstiderne bør optimeres for hver ny type prøve.
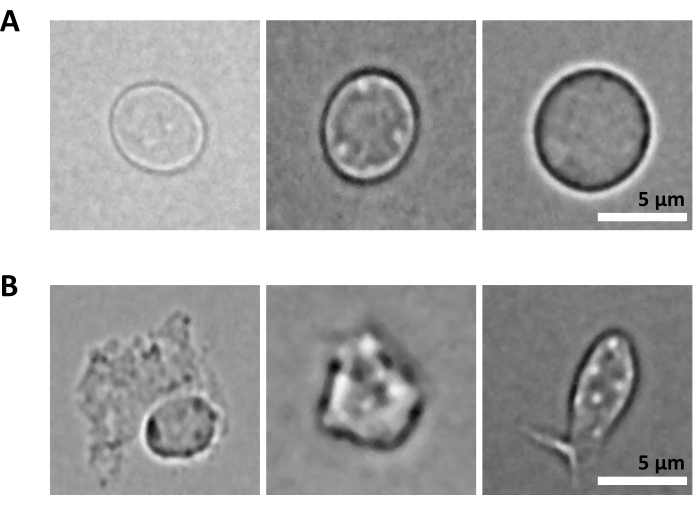
Figur 5: Kernekvalitetskontrol ved mikroskopi. Der vises repræsentative brightfield-billeder af isolerede kerner fra museknoglemarv med (A) intakte og (B) beskadigede kerner. Skala bar 5 μm. Billeder blev taget med et omvendt mikroskop ved hjælp af en 40x ELWD NA 0,60 objektiv og 1,5x digital zoom. Klik her for at se en større version af denne figur.
Begge protokoller, der er beskrevet i dette arbejde, er afhængige af rensning af målrettede celler eller kerner ved hjælp af FACS-instrumenter med høj kapacitet. Dette trin er af afgørende betydning for enkeltcelle-/kernepræparationsprotokoller, hvor sjældne delmængder af celler skal isoleres fra heterogene suspensioner. I disse, som i eksemplet vist her for HSPC-sortering, kan et højdimensionelt flowcytometripanel være nødvendigt for at muliggøre “gating” på cellepopulationen af interesse. Sorteringen er ekstremt hurtig og nøjagtig, hvilket fører til over 95% renhed af de sorterede celleundergrupper. Denne fremgangsmåde udsætter den cellulære suspension for et tryk på op til 70 psi og kan derfor være begrænsende for sortering af skrøbelige celler (f.eks. Dendritiske celler, neutrofiler), da det kan forårsage brud på deres cellemembran. I disse tilfælde bør der vælges alternative løsninger til cellulær rensning, herunder magnetisk sortering, anvendelse af nye generationsinstrumenter (f.eks. CellenOne, Cellenion; MACSQuant Tyto, Miltenyi)35,36 eller dråbebaserede systemer (f.eks. ODIN, Sensific)37. Ikke desto mindre er den langsomme sorteringshastighed for disse teknologier med cellesortering, der varer i timer i stedet for minutter, en stærk begrænsende faktor for anvendelsen af disse tilgange til fremstilling af levedygtige celler til Multiome og andre enkeltcelleapplikationer baseret på analyse af store celletal.
Til oprensning af kerner isoleret fra vævet er FACS den valgte metode på grund af dets gennemstrømning og renheden af det isolerede materiale. Kerner er ikke følsomme over for tryk, og filtrerede vævsisolater kan let renses gennem cellesortereren. Hvis laboratoriet ikke er udstyret med et FACS-instrument, findes der andre alternativer, noget mindre effektive, men tilstrækkeligt gode. Eksempler inkluderer ultracentrifugering eller brug af lille udstyr såsom MARS (Applied Cell), der adskiller partikler baseret på deres forskel i størrelse ved hjælp af akustiske bølger; CURIOX laminær skive, der bruger hydrofobe egenskaber af celle-/kernesuspensioner; eller LEVITAS bio, der er afhængig af fysiske egenskaber af celler (levitation) for at adskille dem fra affaldet.
Her beskriver vi protokoller for at opnå et højt antal kerner og den bedste renhed for downstream Multiome-protokollen. FACS-sortering og gentagne centrifugeringstrin resulterer i et betydeligt tab af det oprindelige materiale. Af denne grund kræver protokollen for kerneforberedelse fra hjernen, som vi beskriver her, tilstrækkeligt rigeligt udgangsmateriale til at resultere i indsamling af mindst 500.000 kerner efter FACS-sorteringen. Der bør anvendes alternative protokoller, hvis dette kriterium ikke kan opfyldes. Når man arbejder med sjældne cellepopulationer eller små vævssektioner, kan den tilgængelige mængde indledende materiale være en begrænsende faktor. For at løse dette problem er det muligt at forbedre gendannelsen af kerner ved (a) at reducere lysisvolumenet, (b) at reducere vaskevolumenet, (c) at bruge en enkelt vask med forlænget centrifugeringstid for at forsøge at forbedre restitutionen som angivet i 10X genomics-protokoller til isolering af kerner med lavt celleinput. Til multiomisk analyse af materiale med lavt indhold er det værd at overveje pladebaserede applikationer som scNMT, SNARE-seq og Paired-seq38 , der kræver meget færre inputprøver.
Sammenfattende har vi beskrevet to robuste protokoller til fremstilling af kerner fra hjernen og knoglemarven HSPC’er til downstream Multiome-analyse. Disse protokoller kan anvendes i ethvert videnskabeligt projekt, der kræver enkeltkernesuspensioner af høj kvalitet fra disse to vævstyper, uanset det videnskabelige spørgsmål, der stilles. Vores gruppe har anvendt hjernekerneisolationsprotokollen i studier af hjernens udvikling ved inaktivering af forskellige målrettede gener og i undersøgelser af immunrespons i forbindelse med neurologiske sygdomme. Vi bruger knoglemarvskerneisoleringsprotokollen til at dechiffrere deltagelsen af forskellige hæmatopoietiske subpopulationer i etableringen af immunsystemet.
Divulgazioni
The authors have nothing to disclose.
Acknowledgements
Ana Jeemin Choi blev støttet af et stipendium fra Pasteur – Paris University (PPU) International Ph.D. Program.
Materials
| 18 G x 1 ½ (1.2 mm x 38 mm) Agani needles | Terumo | AN*1838S1 | |
| 15 mL tubes | Falcon | 352097 | |
| 5 mL round bottom FACS tube with cell strainer cap 35 µm | falcon | 352235 | |
| 50 mL tubes | Falcon | 352070 | |
| 7-AAD | BD pharmagen | 559925 | |
| ACK Lysing Buffer | Gibco | A10492-01 | |
| APC anti-mouse CD117 (c-Kit) | BioLegend | 105812 | Clone: 2B8 |
| APC/Cyanine 7 anti-mouse CD16/32 (FcγR) | BioLegend | 101328 | Clone: 93 |
| BD FACSAria III | BD Biosciences | non-applicable | |
| BD FACSDiva Software v8.0.1 | BD Biosciences | non-applicable | |
| Bovine Serum Albumin stock solution 10% | Miltenyi Biotec | 130-091-376 | |
| Cell staining buffer | Biolegend | 420201 | |
| CFI Suprplan Fluor ELWD 40XC ON 0.6 | Nikon | non-applicable | |
| CMOS camera Prime 95B 25 mm | Photometrix | non-applicable | |
| Countess II FL Automated Cell Counter | Invitrogen | AMQAF1000 | |
| Countess cell counting chamber slide | Invitrogen | C10283 | |
| Coverglass 24 mm x 24 mm 0.13-0.17 mm | Brand | BR470819 | |
| Digitonine 5% | Invitrogen | BN2006 | |
| Disposable Scalpels | Swann-Morton | 0508 | |
| DMEM (1x) + GlutaMAX-I | Gibco | 31966-021 | |
| DPBS (10x) | Gibco | 14200-067 | |
| DTT | Sigma aldrich | 646563 | |
| Epifluorescence inverted microscope Nikon Ti2 -E | Nikon | non-applicable | |
| Eppendorf Safe-Lock Tubes 0.5 mL | Eppendorf | 30123603 | |
| Ethanol 70% | VWR | 83801.290 | |
| FITC anti-mouse CD34 | Invitrogen | 11-0341-85 | Clone: RAM34 |
| Forceps for dissection | FST | 11152-10 | |
| Heat-inactivated Fetal Bovine Serum (FBS) | Gibco | 11533387 | |
| Dounce Homogeniser 2 mL | Bellco glass | 1984-10002 | Pestle “A” Large Clearance: .0030-.0050″ and Pestle “B” Small Clearance: .0005-.0025″ |
| LIVE/DEAD fixable aqua dead cell stain kit | Invitrogen | L34957 | |
| Magnesium chloride solution 1 M | Sigma aldrich | M1028 | |
| Microcentrifuge | Eppendorf | 5424R | |
| Mounting medium Fluoromount-G | invitrogen | 00-4958-02 | |
| Nonidet P40 substitute | Sigma aldrich | 74385 | |
| Nuclease free water | ThermoFischer | AM9932 | |
| Nuclei buffer 20x | 10X Genomics | 2000153/2000207 | |
| Nuclei isolation kit EZ prep | Sigma Aldrich | NUC-101 | |
| OneComp eBeads compensation beads | Invitrogen | 01-1111-41 | |
| Pacific Blue anti-mouse lineage cocktail (including anti-mouse CD3, Ly-6G/Ly-6C, CD11b, CD45R/B220, TER-119) |
BioLegend | 133310 | Clones (in the same order as the antibodies listed): 17A2, RB6-8C5, M1/70, RA3-6B2, Ter-119 |
| PCR Tube Strips 0.2 mL | Eppendorf | 951010022 | |
| PE anti-mouse Ly-6A/E (Sca-1) | BioLegend | 122507 | Clone: E13-161.7 |
| Petri dish 100 mm x 20 mm OPTILUX | Falcon | 353003 | |
| Ply-L-lysine 0.01% sterile-filtered suitable for cell culture | Sigma | P4707 | |
| Printed microscope slides 8 well 6 mm numbered | Epredia | ER-301B-CE24 | |
| Protein LoBind Tubes 1.5 mL | Eppendorf | 30108116 | |
| Recombinant Rnase inhibitor 5000 U | Takara | 2313A | |
| Scissors for dissection | FST | 14090-09 | |
| Sodium chloride solution 5 M | Sigma aldrich | 59222C | |
| Syringe filters, PES, 0.2 µm | Fisher Scientific | 15206869 | |
| Transparent nail polish | any | non-applicable | |
| Trizma Hydrochloride solution pH 7.4 | Sigma aldrich | T2194 | |
| Trypan Blue 0.4% | gibco | 15250061 | |
| Tween 20 | Biorad | 1662404 | |
| UltraPure Distilated Water Dnase/Rnase Free | Invitrogen | 10977-035 |
Riferimenti
- Clark, S. J., et al. scNMT-seq enables joint profiling of chromatin accessibility DNA methylation and transcription in single cells. Nature Communications. 9 (1), 781 (2018).
- Lee, J., Hyeon, D. Y., Hwang, D. Single-cell multiomics: technologies and data analysis methods. Experimental & Molecular Medicine. 52 (9), 1428-1442 (2020).
- Cerrizuela, S., et al. High-throughput scNMT protocol for multiomics profiling of single cells from mouse brain and pancreatic organoids. STAR Protocols. 3 (3), 101555 (2022).
- Dimitriu, M. A., Lazar-Contes, I., Roszkowski, M., Mansuy, I. M. Single-cell multiomics techniques: From conception to applications. Frontiers in Cell and Developmental Biology. 10, 854317 (2022).
- Stoeckius, M., et al. Simultaneous epitope and transcriptome measurement in single cells. Nature Methods. 14 (9), 865-868 (2017).
- Cao, J., et al. . Joint profiling of chromatin accessibility and gene expression in thousands of single cells. 361 (6409), 1380-1385 (2018).
- Narayanan, A., et al. Nuclei Isolation from Fresh Frozen Brain Tumors for Single-Nucleus RNA-seq and ATAC-seq.Journal of Visualized Experiments. JoVE. 162, 61542 (2020).
- Kim, M., et al. Single-nucleus transcriptomics reveals functional compartmentalization in syncytial skeletal muscle cells. Nature Communications. 11 (1), 6375 (2020).
- Santos, M. D., et al. Extraction and sequencing of single nuclei from murine skeletal muscles. STAR Protocols. 2 (3), 100694 (2021).
- Safabakhsh, S., et al. Isolating nuclei from frozen human heart tissue for single-nucleus RNA sequencing. Current Protocols. 2 (7), (2022).
- Lau, S. -. F., Cao, H., Fu, A. K. Y., Ip, N. Y. Single-nucleus transcriptome analysis reveals dysregulation of angiogenic endothelial cells and neuroprotective glia in Alzheimer’s disease. Proceedings of the National Academy of Sciences of the United States of America. 117 (41), 25800-25809 (2020).
- Armand, E. J., Li, J., Xie, F., Luo, C., Mukamel, E. A. Single-cell sequencing of brain cell transcriptomes and epigenomes. Neuron. 109 (1), 11-26 (2021).
- Morabito, S., et al. Single-nucleus chromatin accessibility and transcriptomic characterization of Alzheimer’s disease. Nature Genetics. 53 (8), 1143-1155 (2021).
- Chen, S., et al. Spatially resolved transcriptomics reveals genes associated with the vulnerability of middle temporal gyrus in Alzheimer’s disease. Acta Neuropathologica Communications. 10 (1), (2022).
- Paul, F., et al. Transcriptional heterogeneity and lineage commitment in myeloid progenitors. Cell. 163 (7), 1663-1677 (2015).
- Kaufmann, E., et al. BCG educates hematopoietic stem cells to generate protective innate immunity against tuberculosis. Cell. 172 (1-2), 176-190 (2018).
- Christ, A., et al. diet triggers NLRP3-dependent innate immune reprogramming. Cell. 172 (1-2), 162-175 (2018).
- Moorlag, S. J. C. F. M., et al. β-Glucan Induces protective trained immunity against mycobacterium tuberculosis infection: A key role for IL-1. Cell Reports. 31 (7), 107634 (2020).
- de Laval, B., et al. C/EBPβ-dependent epigenetic memory induces trained immunity in hematopoietic stem cells. Cell Stem Cell. 26 (5), 657-674 (2020).
- Renthal, W., et al. Characterization of human mosaic Rett syndrome brain tissue by single-nucleus RNA sequencing. Nature Neuroscience. 21 (12), 1670-1679 (2018).
- Yang, A. C., et al. A human brain vascular atlas reveals diverse mediators of Alzheimer’s risk. Nature. 603 (7903), 885-892 (2022).
- Lee, D. R., Zhang, Y., Rhodes, C. T., Petros, T. J. Generation of single-cell and single-nuclei suspensions from embryonic and adult mouse brains. STAR Protocols. 4 (1), 101944 (2022).
- Corces, M. R., et al. Lineage-specific and single-cell chromatin accessibility charts human hematopoiesis and leukemia evolution. Nature Genetics. 48 (10), 1193-1203 (2016).
- Ranzoni, A. M., et al. Integrative single-cell RNA-seq and ATAC-seq analysis of human developmental hematopoiesis. Cell Stem Cell. 28 (3), 472-487 (2021).
- . 10X Genomics Chromium Next GEM Single Cell Multiome ATAC + Gene Expression User Guide. Document Number CG000338 Rev F. At. , (2022).
- J, , et al. Microdissection of mouse brain into functionally and anatomically different regions. Journal of Visualized Experiments: JoVE. 168, 61941 (2021).
- . . 10X Genomics 10X Genomics Demonstrated Protocol – Nuclei Isolation for Single Cell Multiome ATAC + GEX sequencing (CG000365 – Rev C). At. , (2022).
- Haag, S., Murthy, A. Murine monocyte and macrophage culture. Bio-Protocol. 11 (6), (2021).
- Haque, A., Engel, J., Teichmann, S. A., Lönnberg, T. A practical guide to single-cell RNA-sequencing for biomedical research and clinical applications. Genome Medicine. 9 (1), (2017).
- Jiang, P. Quality control of single-cell RNA-seq. Methods in Molecular Biology. , 1-9 (1935).
- Regan, C., Preall, J. Practical considerations for single-cell genomics. Current Protocols. 2 (8), (2022).
- . . 10X Genomics 10X Genomics Demonstrated Protocol – Nuclei Isolation for Single Cell ATAC Sequencing (CG000169 – Rev E). At. , (2022).
- . 10X Genomics 10X Genomics Demonstrated Protocol – Nuclei Isolation from Complex Tissues for Single Cell Multiome. ATAC + Gene Expression Sequencing. (CG000375 – Rev C). At. , (2022).
- . . 10X Genomics 10X Genomics – Chromium Nuclei Isolation Kit (CG000505 – Rev A). AT. , (2022).
- Shomroni, O., et al. A novel single-cell RNA-sequencing approach and its applicability connecting genotype to phenotype in ageing disease. Scientific Reports. 12 (1), 4091 (2022).
- Ocañas, S. R., Pham, K. D., Blankenship, H. E., Machalinski, A. H., Chucair-Elliott, A. J., Freeman, W. M. Minimizing the ex vivo confounds of cell-isolation techniques on transcriptomic and translatomic profiles of purified microglia. 9 (2), 0348-0321 (2022).
- Gérard, A., et al. High-throughput single-cell activity-based screening and sequencing of antibodies using droplet microfluidics. Nature Biotechnology. 38 (6), 715-721 (2020).
- Vandereyken, K., Sifrim, A., Thienpont, B., Voet, T. Methods and applications for single-cell and spatial multi-omics. Nature Reviews. Genetics. 24, 494-515 (2023).

