Måling TCR-pMHC Binding<em> In Situ</em> Bruker en FRET basert Mikros analysen
Summary
This manuscript describes how to conduct (single molecule) Förster Resonance Energy Transfer (FRET)- based assays to measure the binding dynamics between T-cell antigen receptor (TCR) and antigenic peptide-loaded MHC molecules as they occur within the immunological synapse of a T-cell in contact with a functionalized planar supported lipid bilayer.
Abstract
T-cells are remarkably specific and effective when recognizing antigens in the form of peptides embedded in MHC molecules (pMHC) on the surface of Antigen Presenting Cells (APCs). This is despite T-cell antigen receptors (TCRs) exerting usually a moderate affinity (µM range) to antigen when binding is measured in vitro1. In view of the molecular and cellular parameters contributing to T-cell antigen sensitivity, a microscopy-based methodology has been developed as a means to monitor TCR-pMHC binding in situ, as it occurs within the synapse of a live T-cell and an artificial and functionalized glass-supported planar lipid bilayer (SLB), which mimics the cell membrane of an Antigen presenting Cell (APC) 2. Measurements are based on Förster Resonance Energy Transfer (FRET) between a blue- and red-shifted fluorescent dye attached to the TCR and the pMHC. Because the efficiency of FRET is inversely proportional to the sixth power of the inter-dye distance, one can employ FRET signals to visualize synaptic TCR-pMHC binding. The sensitive of the microscopy approach supports detection of single molecule FRET events. This allows to determine the affinity and off-rate of synaptic TCR-pMHC interactions and in turn to interpolate the on-rate of binding. Analogous assays could be applied to measure other receptor-ligand interactions in their native environment.
Introduction
En mer grunnleggende forståelse av hvordan T-celler gjenkjenner antigener krever ser på riktig sted, det vil si innenfor den immunologiske synapse dannet mellom T-cellen og APC. Her blir molekylære bindingskinetikken ikke bare bestemt av de iboende biokjemiske egenskaper av interaksjonspartnere som er involvert, men avhenger i stor grad av celleparametere, som inkluderer cellekrefter, membran arkitektur og laterale interaksjonene mellom membranproteiner samt synapse-spesifikke geometriske begrensninger 3. Biokjemiske fremgangsmåter er begrenset oppløsningsevne som de nødvendiggjør avbrudd av minst en av de synaptiske membraner som er involvert. Av denne grunn er et FRET-basert avbildning metode ble utviklet for å overvåke bindingen av TCR til antigeniske pMHCs 2. Her T-celler er innredet med en rekombinant og site-spesifikt merket TCRβ-reaktivt enkelt kjede antistoffragment (SCF V) og konfrontert med plan ar glass-støttet lipidbilag (SLBs), som rommer MHC klasse II molekyler lastet med en fluoresceinmerket antigen peptid, samtidig stimulerende molekyler og adhesjonsproteiner. Synaptic binding mellom dye-merket TCR og dye-merket pMHC resultater i slite, som kan overvåkes på en bulk og enkelt molekyl nivå av Total Internal Reflection Fluorescence (TIRF) mikroskopi.
I denne artikkelen er det forklart i detalj hvordan du kan utnytte SLBs for analyse av T-celle synapser, bekrefte sin integritet gjennom en funksjonell T-celle kalsium-flux analysen, oppførsel FRET målinger i bulk og med enkelt molekyl følsomhet, og analysere de innsamlede data. Anbefalingene tilbys for å produsere riktig dannet proteiner som kreves for dobbeltlag funksjon. For mer spesifikk informasjon om bilagsdannelse og oppsett av en egnet TIRF mikroskop henvises det til en ekstra offentlighet Jove publikasjon publisert rygg mot rygg fire.
telt "> Nature of SLBsFunctionalizable SLBs kan lett genereres fra unilamellære vesikler (SUV) som inneholder de to lipider 1-palmitoyl-2-oleoyl-sn-gylcero-3-fosfokolin (kort: POPC, 90-99%) og 1,2-dioleoyl- sn – glycero-3 – {[N (5-amino-1-karboksypentyl) iminodieddiksyre] succinyl} (kort: DGS NTA-Ni, 1-10%). SUVer spredt på rene glassplater for å danne en sammenhengende plan dobbeltlag fire. DGS-NTA-Ni tjener til å forankre polyhistidin-merkede proteiner via polyhistidin-mediert kompleksdannelse med det syntetiske NTA-Ni-inneholdende hodegruppe (figur 1A). For stabil assosiasjon en typisk erstatter den native transmembrandomenet og den cytoplasmiske hale av bindingsproteinet, ICAM-1 og kostimulerende molekyl B7-1 med en kode som inneholder tolv histidiner (ICAM-1-12H, B7-1 -12H) (figur 1 B) . Peptid-lastet klasse II molekyl IE k inneholder to-membran-embedded (α og β) polypeptidkjedes. De trans / cytoplasmatiske domener av begge kjedene må være erstattet med en kode som inneholder seks histidiner hver (IE k α 6H 6H β eller IE k -2x6H). Som et alternativ kan utvide α-kjede med tolv histidiner og forlater det ekstracellulære domene av den β-kjeden ukodet (som gir opphav til IE k α 12H β 0H eller IE k -12H) gir opphav til tilfredsstillende resultater (figur 1B).
Stedsspesifikk merking av pMHCs
Det er viktig å merke pMHC stoichiometrically og site-spesifikt for å kunne konvertere målt FRET avkastning til meningsfulle likevekts bindende konstanter. Dette kan oppnås ved kjemisk merking av et syntetisk peptid som er lastet inn i den peptid-bindende kløft av rekombinant histidin-merket MHC klasse II-molekyler 2,5. Peptidet omfatter alle rester av T-celle-epitop som well som en kort C-terminal linker (GGS) etterfulgt av cystein (f.eks i møll cytokrom c (MCC) peptid ANERADLIAYLKQATK- GGSC, den linker er markert med fet skrift). Dette cystein blir brukt for å merke peptidet støkiometrisk med bruk av maleimid-fargestoff-derivater. På dette punktet ekstra omsorg bør være viet til å verifisere kvantitativ dye-kobling til cystein holdige peptid. HPLC-rensing av peptid-dye Adduktet er anbefalt og har å bli etterfulgt av elektrosprayionisering massespektroskopi. Ikke registrert masser svarende til det peptidet edukt (uten fargestoff) reflekterer ufullstendig merking. Hvis dette er sant, bør HPLC-renset peptid underkastes etterfølgende runder av fargestoffmerking til merking anses kvantitativt. Legg merke til at MALDI-TOF massespektroskopi må unngås, da denne metoden innebærer laserstråling for prøve ionisering. Denne behandlingen desintegrerer vedlagte sensitive fluoroforene før peptid massen blir lest ut og dermed underrepre senterer grader av dye-konjugering.
Indirekte ennå stedsspesifikk merking av celle-bundet TCR med bruk av monovalente enkeltkjede Fv-fragmenter
Det er fortsatt utfordrende å feste fargestoffer til celleoverflaten assosierte proteiner av levende celler i en stedsspesifikk måte. For å overvinne dette hinderet for overflate utsatt TCR, har en mono enkelt kjede versjon (SCF V) fra genene av TCRβ -reactive monoklonalt antistoff H57-197 세스 blitt konstruert. Krystallstrukturen av dette antistoff i kompleks med TCR gjør det mulig å rasjonelt å utforme en versjon, hvor en serinrest i umiddelbar nærhet til den C-terminale ende av MHC tilknyttede peptid (hvor den tilsvarende FRET partner fargestoff er festet til) er substituert for et cysteinrest. Denne mutant cystein da tjener som en akseptor for fargestoff konjugasjon (figur 2).
Metoder for å registrere FRET
nt "> Bulk FRET verdier er best egnet til å bekrefte forholdet mellom valgte inter-dye avstander og FRET effektivitet målt i denne TCR-pMHC bindende system to. I tillegg bulk FRET målinger avslører kvalitative og kvantitative forskjeller i synaptiske TCR-pMHC slektskap ( se nedenfor og protokoll pkt 3.2). Ulike metoder for å kvantifisere FRET effektivitet har blitt introdusert i litteraturen 6. I denne artikkelen FRET registreres via(a) donor gjenoppretting etter akseptor bleking, og via
(b) sensitivisert FRET akseptor utslipp.
Den første metoden (a) krever bruk av et FRET-akseptor som lett kan photobleached, og en donor, som er ganske fotostabile. I tillegg er det viktig å sikre at photobleached akseptor er ikke lenger i stand til å slukke donor fluorescens. Som det samme deteksjonskanal (donor) anvendes for kvantifisering, faktorer ingen korreksjon end ingen kromatiske avvik må vurderes, noe som gjør denne metoden enkel og pålitelig. Imidlertid kan kvantitative målinger ikke gjentas på samme prøven spot og endringer i FRET kan ikke tas opp over tid. For å unngå effekter forårsaket av molekylær diffusjon eller cellulær motilitet et fast bleketrinn bør være rettet for, noe som minimaliserer den tid som går mellom den første FRET donor (før akseptor bleking) og den andre FRET donor bildeopptak (etter FRET akseptor bleking). Det er anbefalt å anvende en kraftig laserlyskilde av FRET akseptor eksitasjonsbølgelengden for å minimere belysning og bleketider.
I motsetning til dette, på tilnærmingen av sensitivisert FRET emisjonsmåling (b) FRET donor er spent og utslipp av den FRET akseptor er observert i FRET akseptor kanalen. Endringer i FRET akseptor signal kan tas opp over tid, men utslipp av FRET donor inn i den rød-skiftet akseptor kanal (termed bleedthrough) og FRET akseptor cross-eksitasjon via donor eksitasjon må være nøyaktig bestemt og trekkes fra den registrerte FRET akseptor kanal. For dette de tilsvarende FRET donor og gnage akseptor bildene må romlig justert.
Påvisning av enkelt molekyl (sm) FRET hendelser
Med bruk av lasere som eksitasjon kilde, et følsomt kamera og støydempet TIRF mikros fluorescensen av enkelt fluoroforer lett kan spores over tid. Lignende er sant for påvisning av inter smFRET hendelser. Imidlertid kan komplikasjoner være forårsaket av FRET donor bleedthrough og tverr magnetisering av FRET akseptor, og dermed stor forsiktighet ved justering fluoroforen tettheter i smFRET eksperiment for å bli tatt.
I protokollen nedenfor (protokoll seksjon 4) ble TCR valgt som FRET donor i høy overflod og pMHC som FRET akseptor i lav overflod. Å dempe FRET donor bleedthrough tilstrekkelig, dekorere 10-30% av TCR med fluorescerende SCF V og 90-70% av TCR med ikke-fluorescerende SCF V. Her gnage akseptor kanalen ble valgt som eneste molekyl kanal fordi det er konfokalt med enkelt molekyl FRET kanal. Dette bidrar til å justere smFRET hendelser med enkelt molekyl FRET-akseptorer, som er grunnlaget for smFRET validering.
Utpakking synaptiske off-priser gjennom smFRET målinger
Bleking av både FRET donor og FRET akseptor må gjøres rede for når utpakking av halveringstiden for interaksjoner fra enkelt molekyl FRET spor. Antallet observer FRET-signaler ved begynnelsen av sitt utseende som enkelt donor-akseptor paret N (0) reduseres over tid ved begge uforpliktende av reseptor-ligand-kompleks og fotobleking. Antallet overlevende komplekser på et gitt tidspunkt N (t) kan matematisk uttrykkes som følger:
<p class = "jove_content">
I bleking uttrykket exp (-t / τ blekemiddel) tiden t er beskrevet av produktet av antall observasjoner n og belysningstiden t ill på grunn av den ikke-kontinuerlige, diskret observasjon modus (dvs. bleking forekommer bare under belysningen ). Innenfor den kinetiske uttrykket exp- (t / τ av) tiden t er produktet av antallet observasjoner n og tidsforsinkelsen t for en enkelt observasjon FRET (dvs. det skjer kinetisk uforpliktende kontinuerlig). Ligning 1 kan uttrykkes som:
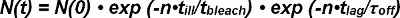
Begrepet τ bleike / τ syk describes antall observasjoner til bleking finner sted, og er definert som forventningsverdien <n bleke> av sin eksponensielle funksjon. Likning 2 kan forenkles som følger:
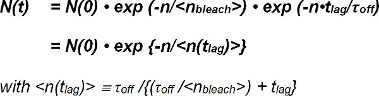
Forventningsverdien <n (t lag)> av det antall rammer N (t) med observer FRET-hendelser etter tiden t er direkte bestemt fra forsøket. Det avhenger av innstillbar tid mellom observasjoner (t hylse) valgt i eksperimentet og de ukjente verdier for τ av (den inverse av off-rate k off), og <n bleker>, forventningsverdien av antall observasjoner før bleking skjer .
Således beregning av forventningsverdien <n (t lag)> i minst to verdier av t <sub> lag gjør det eksperimentelle fastsettelse av <n bleke> og ź av.
Utpakking synaptiske 2D-K D verdier gjennom FRET baserte målinger
Måling TCR et belegg, dvs. forholdet mellom bundet TCR og total TCR, er sentralt for bestemmelse av synaptiske 2D-K-D-verdier. I henhold til ligning 4 dette begrepet er direkte proporsjonal med den målte gnage utbytte så lenge TCR tjener som FRET givere og pMHCs som FRET akseptorer.
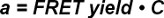
med a = TCR belegg, C = omregningsfaktor
C er en konstant, som avhenger av systemet og FRET fluoroforene brukt. Det kan bestemmes eksperimentelt, som vist nedenfor. en kan omdannes til et 2D-K D i henhold til ligning 5 nårinitial densitet på TCR ligander før tilsetning av T-celler til dobbeltlaget er kjent. Dette er på grunn av den høye mobilitet av SLB-tilknyttede proteiner og også fordi SLBs gi en nesten uuttømmelig reservoar av ligander 2.
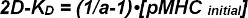
med [pMHC initial] = initial densitet på pMHC før tilsetning av T-celler
Med ligninger 4 og 5 kan man nå enkelt finne den synaptiske 2D-K D mellom TCR og pMHC. Dette er mest pålitelig gjort med FRET målinger basert på donor gjenoppretting etter akseptor bleking (se protokoll avsnitt 3.1).
Men for å måle C-forholdet mellom intensiteten I FRET FRET (korrigert for bakgrunn, FRET bleedthrough donor og akseptor FRET kryss-eksitasjon) og TCR et belegg skal bestemmes. For dette, entrenger å vite forholdet R mellom gjennomsnittlig fluorescens intensitet av enkelt TCR-forbundet FRET giver fluoroforene (f.eks Cy3 eller AF555) sm jeg FRET donor og gjennomsnittlig intensitet enkelt molekyl FRET hendelser sm jeg gnage. R er avhengig av FRET system, for emisjonsfiltre og kamera som brukes for fluorescensdeteksjon.
TCR belegget en kan deretter bli direkte bestemt i henhold til ligning 6.

med R = sm jeg FRET donor / sm jeg FRET
R ble bestemt som 1,45 for H57 scFv- Cy3 / pMHC-Cy5 system fører til:
a = bulk jeg FRET / bulk jeg TCR-Cy3 • 1,45
Forholdet mellom TCR belegg en og FRET utbytte, kan bestemmes ved FRET donor gjenopprettey etter akseptor bleking. For dette begge parametere er plottet mot hverandre for et antall TCR microclusters som vist i figur 4A sikret helningen av den lineære tilpasning angir omregningsfaktoren C (fra ligning 4).
Som vist i figur 4A, utgjør C for (a) H57 SCF V – Cy3 / pMHC-Cy5 FRET system og (b) den påførte mikroskop systemkonfigurasjon til 1,995. TCR belegget en lett kan utledes som følger:
TCR belegg a = FRET gi • 1,995
Protocol
Representative Results
Discussion
Måle protein-protein interaksjoner in situ er svært ønskelig, spesielt når du arbeider med lave affinitetsinteraksjoner som TCR-pMHC bindende 11. Dette er fordi den på-hastighet, så vel som stabiliteten av slike interaksjoner er betydelig påvirket av de spesielle omstendigheter under hvilke bindingen finner sted. Minimal-invasive FRET-baserte bilde tilnærminger er dermed i prinsippet passer perfekt for slike oppgaver, men innebærer en rekke hindringer som må først overvinnes. Støy generert av cellulær autofluorescens begrenser følsomheten av målingene og bør derfor holdes på et minimum. TIRF mikros tjener dette behovet meget godt 12, men krever at funksjonalisering av glass-slides, helst i form av et plant glass-støttet lipidbilag dekorert med proteiner av valg 13-15. En annen fordel med en delvis reconstitutive tilnærmingen er at rekombinante bilag-resident FRET partnere kan være mye mmalm lett merkes i en kvantitativ, stedsspesifikk og rasjonell måte med mindre og lysere fluoroforene enn det ville være mulig med celleoverflate uttrykte proteiner. TCR er merket med rekombinant SCF V s, som ikke påvirke T-celle-gjenkjenning, som ble testet tidligere to. Videre er proteinsammensetningen i SLB, for eksempel tettheten av pMHCs og valget av aksessoriske faktorer kan justeres til sine spesifikke behov. Vi har tidligere utført eksperimenter med varierende tettheter av stimulerende pMHCs, men har ikke påvist signifikante forskjeller i 2D-k off og 2D-K D 2.
Så langt her erkjennelsen av MHC klasse II molekyler har blitt behandlet bare, hovedsakelig på grunn av naturen av deres peptid binding kløft, som er åpen i begge ender og dermed plass til større peptider inkludert en linker for fluorophore vedlegg. I noen tilfeller slik tilnærming kan også arbeide for merking MHC CLAss Jeg molekyler 16 men stor forsiktighet bør tas for å kontrollere deres bruk i eksperimenter. Sensitiviteten av T-celler mot antigener, som kan måles via T-celle-proliferasjonsanalyser, samt pMHC-TCR-bindende kinetikk som målt in vitro ved hjelp av overflate-plasmonresonans bør ikke påvirkes av tilsetningen av linkeren og fluoroforen til peptidet. Alternativt kan MHC klasse I molekyler seg selv være merket på en sete-spesifikk måte med innføringen av en uparet cystein i sekvensen til den tunge kjeden (upubliserte observasjoner).
Med bruk av egnede molekylære prober enhver synaptiske protein-protein interaksjon kan i prinsippet bli undersøkt på en måte som er beskrevet heri. Slike sonder, f.eks, bør SCF V s eller Designet Ankyrin Gjenta Proteins (DARPins) 17, være mono og bør binde sine mål stabilt uten å påvirke samspillet av interesse. Of course, strukturelle informasjonsn er svært ønskelig for rasjonell utforming proben, men ikke absolutt nødvendig. Ved etablering av et nytt par FRET partnere, anbefales det å registrere og analysere FRET i bulk først. Nettsteder av etiketten vedlegg kan varieres mye å maksimere FRET signal og også for å verifisere at målt FRET utbytter variere basert på inter-dye avstand. Når systemet er optimalisert, enkelt molekyl FRET signaler kan bli registrert ved å begrense merking av den høye overflod FRET partner til 10-30% og bleking av lav overflod FRET partner til enkle molekyler er løses på området belysning.
Sist men ikke minst det bør bemerkes at SLBs tilnærmet noen, men ikke alle deler av en fysiologisk plasmamembranen. Egenskaper som membranen krumning og fleksibilitet, domene compartmentalization, cytoskeletal omordninger og celle motilitet, så vel som en høy variasjon av overflateuttrykt membran proteiner er ikke representert ved SLBs men kan påvirke than behandler under etterforskning. Mye arbeid må investeres å etablere avbildningsmodaliteter som tillater overvåking av protein-protein interaksjoner med enkelt molekyl oppløsning i fysiologiske synapser, som er utilgjengelige for TIRF avbildning.
Disclosures
The authors have nothing to disclose.
Acknowledgements
MA ble støttet av en Schrödinger fellesskap av den østerrikske Science Fund (FWF, J3086-B11) og takker Max-Planck-Society for økonomisk og administrativ støtte. GS og JH ble støttet av Wien Science and Technology Fund (WWTF, LS13-030).
Materials
| LB-media | Fisher Scientific | 10000713 | bacterial expression |
| Sf900 II | Life Technologies | 10227402 | insect cell media for baculo virus production |
| Insect-XPRESS with L-glutamine (Lonza) | Fisher Scientific | 10564038 | insect cell media for baculo virus expression |
| Sf9 cells | Life Technologies | 11496-015 | cells for virus production and expansion |
| High Five Cells | Life Technologies | B855-02 | cells for potein expression |
| LB-media | Fisher Scientific | 10000713 | bacterial expression |
| Centramate System | Pall | protein concentartion from large volumes | |
| Centramate cassette 10kDa cutoff | Pall | OS010T12 | protein concentartion from large volumes |
| Amicon Ultra-15 Centrifugal Filter Units | EMD Millipore | UFC900308 | protein concentartion |
| Amicon Ultra-4 Centrifugal Filter Units | EMD Millipore | UFC800308 | protein concentartion |
| Amicon Stirred Ultrafiltration Cell Model 200 mL | EMD Millipore | 5123 | protein concentartion |
| Äkta pure 25L | GE Healthcare | 29-0182-24 | protein purification |
| Superdex 200 10/300 GL | GE Healthcare | 17-5175-01 | protein purification |
| Superdex 75 10/300 GL | GE Healthcare | 17-5174-01 | protein purification |
| Mono Q 5/50GL | GE Healthcare | 17-5166-01 | protein purification |
| Ni Sepharose 6 Fast Flow | GE Healthcare | 17-5318-01 | protein purification |
| Tricorn 10/20 column | GE Healthcare | 28-4064-13 | protein purification |
| Gilson HPLC system | Gilson | purificationof fluorochrome-coupled peptides | |
| Pursuit XRs C18, 5 µm particle size, 21.2*250mm column size | Agilent | A6000250X212 | purificationof fluorochrome-coupled peptides |
| Pursuit XRs C18, 5 µm particle size, 21.2*50 mm column size | Agilent | A6000050G212 | purificationof fluorochrome-coupled peptides |
| Tricorn 10/20 column | GE Healthcare | 28-4064-13 | protein purification |
| Gilson HPLC system | Gilson | purificationof fluorochrome-coupled peptides | |
| Pursuit XRs C18, 5 µm particle size, 21.2*250mm column size | Agilent | A6000250X212 | purificationof fluorochrome-coupled peptides |
| Pursuit XRs C18, 5 µm particle size, 21.2*50 mm column size | Agilent | A6000050G212 | purificationof fluorochrome-coupled peptides |
| Cy3 maleimide | GE Healthcare | PA23031 | site-specific protein labeling via mutant unpaired cysteines |
| Cy5 maleimide | GE Healthcare | PA25031 | site-specific protein labeling via mutant unpaired cysteines |
| Alexa Fluor 555 C2 Maleimide | Life Technologies | A-20346 | site-specific protein labeling via mutant unpaired cysteines |
| Alexa Fluor 647 C2 Maleimide | Life Technologies | A-20347 | site-specific protein labeling via mutant unpaired cysteines |
| Fura-2, AM, cell permeant | Life Technologies | F-1221 | calcium-sensitive dye for cell labeling |
| dimethyl sulfoxide | Sigma Aldrich | 151874 | for dissolving fura-2 am |
| Hank's Balanced Salt Solution plus calcium/magnesium | Fisher Scientific | 10225362 | imaging buffer |
| PBS | Life Technologies | 14190-136 | |
| Bovine Serum Albumin lyophilized powder | Sigma Aldrich | A2153 | supplement for imaging buffer |
| 14-4-4S antibody | affimetrix eBioscience | 14-5980-81 | blocking antibody for H2-I-Ek (recognized by the 5c.c7, 2B4 and AND TCR) |
| 5 ml polypropylene round-bottom tube | Becton Dickinson | FALCON 352063 | |
| 0.22 μm Ultrafree-MC centrifugal filter unit | EMD Millipore | UFC30GV0S | |
| Syringe filter 0.2µm | Millipore | GVWP04700 | |
| TetraSpeck Microspheres, 0.1 µm, fluorescent blue/green/orange/dark red | Life technologies | T-7279 | |
| Microscope for fura-2-based calcium measurements | LEICA | DMI4000B | |
| Microscope for (single molecule) FRET measurements | LEICA/ZEISS/NIKON/OLYMPUS | for details please refer to parallel JoVE contribution by Axmann et al. | |
| planar supported lipid bilayers | for details please refer to parallel JoVE contribution by Axmann et al. | ||
| RPMI 1640, with L-Glutamine | Life Technologies | 11554416 | T-cell media |
| non-essential amino acid 100X | Hyclone | SH30238.01 | T-cell media supplement |
| penicillin/streptomycin/L-glutamine 100x | Life Technologies | 12000226 | T-cell media supplement |
| 2-mercaptoethanol | Sigma Aldrich | M6250 | T-cell media supplement |
| mouse interleukin-2 recombinant protein | BPS Bioscience | 90185-B | T-cell media supplement |
| Research Grade Fetal Bovine Serum | Hyclone | SV30160.03 | T-cell media supplement |
| Origin (analysis program) | OrigenLab | http://www.originlab.com/ | non-linear fitting of two parameters (tauoff, [ntlag]) |
References
- Garcia, K. C., Adams, J. J., Feng, D., Ely, L. K. The molecular basis of TCR germline bias for MHC is surprisingly simple. Nat Immunol.. 10, 143-147 (2009).
- Huppa, J. B., et al. TCR-peptide-MHC interactions in situ show accelerated kinetics and increased affinity. Nature.. 463, 963-967 (2010).
- Huppa, J. B., Davis, M. M. The interdisciplinary science of T-cell recognition. Advances in immunology.. 119, 1-50 (2013).
- Axmann, M., Schuetz, G. J., Huppa, J. B. Single Molecule Microscopy on Planar Supported Bilayers. Journal of Vizualized Experiments J. Vis. Exp.. 101, e53158 (2015).
- Xie, J., et al. Photocrosslinkable pMHC monomers stain T cells specifically and cause ligand-bound TCRs to be preferentially transported to the cSMAC. Nat Immunol. 13, 674-680 (2012).
- Jares-Erijman, E. A., Jovin, T. M. FRET imaging. Nat Biotechnol. 21, 1387-1395 (2003).
- Toebes, M., et al. Design and use of conditional MHC class I ligands. Nat Med. 12, 246-251 (2006).
- Tsumoto, K., et al. Highly efficient recovery of functional single-chain Fv fragments from inclusion bodies overexpressed in Escherichia coli by controlled introduction of oxidizing reagent–application to a human single-chain Fv fragment. J Immunol Methods. 219, 119-129 (1998).
- Ruegg, U. T., Rudinger, J. Reductive cleavage of cystine disulfides with tributylphosphine. Methods Enzymol. 47, 111-116 (1977).
- Ruprecht, V., Brameshuber, M., Schütz, G. J. Two-color single molecule tracking combined with photobleaching for the detection of rare molecular interactions in fluid biomembranes. Soft Matter. 6, 568-581 (2010).
- Dustin, M. L., Bromley, S. K., Davis, M. M., Zhu, C. Identification of self through two-dimensional chemistry and synapses. Annu Rev Cell Dev Biol. 17, 133-157 (2001).
- Axelrod, D. Cell-substrate contacts illuminated by total internal reflection fluorescence. The Journal of cell biology. 89, 141-145 (1981).
- Grakoui, A., et al. The immunological synapse: a molecular machine controlling T cell activation. Science. 285, 221-227 (1999).
- Kaizuka, Y., Douglass, A. D., Varma, R., Dustin, M. L., Vale, R. D. Mechanisms for segregating T cell receptor and adhesion molecules during immunological synapse formation in Jurkat T cells. Proc Natl Acad Sci USA. 104, 20296-20301 (2007).
- Varma, R., Campi, G., Yokosuka, T., Saito, T., Dustin, M. L. T cell receptor-proximal signals are sustained in peripheral microclusters and terminated in the central supramolecular activation cluster. Immunity. 25, 117-127 (2006).
- Purbhoo, M. A., Irvine, D. J., Huppa, J. B., Davis, M. M. T cell killing does not require the formation of a stable mature immunological synapse. Nat Immunol. 5, 524-530 (2004).
- Binz, H. K., Stumpp, M. T., Forrer, P., Amstutz, P., Pluckthun, A. Designing repeat proteins: well-expressed, soluble and stable proteins from combinatorial libraries of consensus ankyrin repeat proteins. J Mol Biol. 332, 489-503 (2003).

