Mätt TCR-pMHC Bindning<em> In Situ</em> Med en FRET-baserad Mikroskopi analys
Summary
This manuscript describes how to conduct (single molecule) Förster Resonance Energy Transfer (FRET)- based assays to measure the binding dynamics between T-cell antigen receptor (TCR) and antigenic peptide-loaded MHC molecules as they occur within the immunological synapse of a T-cell in contact with a functionalized planar supported lipid bilayer.
Abstract
T-cells are remarkably specific and effective when recognizing antigens in the form of peptides embedded in MHC molecules (pMHC) on the surface of Antigen Presenting Cells (APCs). This is despite T-cell antigen receptors (TCRs) exerting usually a moderate affinity (µM range) to antigen when binding is measured in vitro1. In view of the molecular and cellular parameters contributing to T-cell antigen sensitivity, a microscopy-based methodology has been developed as a means to monitor TCR-pMHC binding in situ, as it occurs within the synapse of a live T-cell and an artificial and functionalized glass-supported planar lipid bilayer (SLB), which mimics the cell membrane of an Antigen presenting Cell (APC) 2. Measurements are based on Förster Resonance Energy Transfer (FRET) between a blue- and red-shifted fluorescent dye attached to the TCR and the pMHC. Because the efficiency of FRET is inversely proportional to the sixth power of the inter-dye distance, one can employ FRET signals to visualize synaptic TCR-pMHC binding. The sensitive of the microscopy approach supports detection of single molecule FRET events. This allows to determine the affinity and off-rate of synaptic TCR-pMHC interactions and in turn to interpolate the on-rate of binding. Analogous assays could be applied to measure other receptor-ligand interactions in their native environment.
Introduction
En mer grundläggande förståelse för hur T-celler känner igen antigen kräver tittar på rätt ställe, det vill säga inom den immunologiska synapsen bildas mellan T-cellen och APC. Här är molekylära bindande kinetik inte bara bestäms av de inneboende biokemiska egenskaperna hos interaktions inblandade parterna utan beror i stor utsträckning på cellulära parametrar, som omfattar cellulära krafter, membran arkitektur och laterala interaktioner mellan membranproteiner samt synaps specifika geometriska begränsningar 3. Biokemiska metoder är begränsade i upplösningsförmåga som de nödvändiggör avbrott i åtminstone en av de synaptiska membranen inblandade. Av denna anledning en FRET-baserad avbildning metodik utvecklades för att övervaka bindning av TCR till antigena pMHCs 2. Här T-celler är inredda med en rekombinant och platsspecifikt märkt TCRβ-reaktivt enkelkedjigt antikroppsfragment (SCF V) och konfronteras med planen ar glas stöds lipiddubbelskikt (SLBs), som hyser MHC klass Il-molekyler laddade med en fluorescensmärkt antigen peptid, samstimulerande molekyler och vidhäftningsproteiner. Synaptic bindning mellan färgämnesmärkta TCR och färgämnesmärkta pMHC resulterar i FRET, som kan övervakas på en bulk och enda molekyl nivå genom total inre reflektion fluorescens (TIRF) mikroskopi.
I denna artikel förklaras i detalj hur man använder SLBs för analys T-cells synapser, verifiera deras integritet genom en funktionell T-cellskalciumflödesanalys, beteende FRET mätningar i bulk och med enda molekyl känslighet och analysera insamlade data. Rekommendationer erbjuds till att producera riktigt överensstämde proteiner som krävs för dubbelskiktsfunktionalisering. För mer specifik information om dubbelskiktsbildning och inställning av en lämplig TIRF mikroskop hänvisas till en extra allmänhetens tillgång JUPITER publikation publiceras rygg mot rygg 4.
tält "> Naturen av SLBsFunktionaliserbara SLBs kan lätt genereras från unilamellära vesiklar (SUV) innehållande de två lipidema 1-palmitoyl-2-oleoyl-sn-gylcero-3-fosfokolin (kort: POPC, 90-99%) och 1,2-dioleoyl- sn – glycero-3 – {[N- (5-amino-1-karboxipentyl) iminodiättiksyra] -succinyl} (kort: DGS NTA-Ni, 1-10%). SUV sprids på rena glasskivor för att bilda en sammanhängande plan tvåskiktsmembran 4. DGS-NTA-Ni tjänar till att förankra polyhistidin-märkta proteiner via polyhistidin medierad komplexbildning med den syntetiska NTA-Ni-haltiga huvudgruppen (Figur 1A). För stabil association ett ersätter typiskt den nativa transmembrandomänen och den cytoplasmiska svansen hos adhesionsproteinet ICAM-1 och den samstimulerande molekylen B7-1 med en tagg som innehåller tolv histidiner (ICAM-1-12H, B7-1 -12H) (Figur 1B) . Den peptidladdade klass II molekyl IE k innehåller två membraninbäddade (α och β) polypeptidkedjans. De trans / cytoplasmadomäner av båda kedjorna måste ersättas med en etikett som innehåller sex histidiner vardera (IE k α 6H β 6H eller IE k -2x6H). Som ett alternativ, förlängning av α-kedja med tolv histidiner och lämnar den extracellulära domänen av β-kedjan omärkta (ger upphov till IE k α 12H β 0H eller IE k -12H) ger upphov till tillfredsställande resultat (figur 1B).
Platsspecifik märkning av pMHCs
Det är viktigt att märka pMHC stökiometriskt och platsspecifikt för att kunna omvandla uppmätta FRET avkastningen till meningsfulla jämviktsbindningskonstanter. Detta kan uppnås genom kemisk märkning av en syntetisk peptid som laddas in i peptidbindningsklyftan av rekombinant histidin-taggade MHC klass Il-molekyler 2,5. Peptiden inkluderar alla rester av T-cellepitop som viktell som en kort C-terminal linker (GGS) följt av cystein (t.ex. i mal cytokrom c (MCC) peptid ANERADLIAYLKQATK- GGSC, linkern är markerad i fet stil). Denna cystein används för att märka peptiden stökiometriskt med användning av maleimid-dye-derivat. Vid det här laget extra omsorg bör ägnas åt att verifiera kvantitativ färg koppling till cystein-peptid. HPLC-rening av peptiden-dye addukten rekommenderas och måste följas av elektrosprayjonisering masspektroskopi. Alla inspelade massa som motsvarar peptiden edukt (utan färg) återspeglar ofullständig märkning. Om detta är sant, bör HPLC-renad peptid underkastas konsekutiva rundor av färgmärkning tills märkningen bedöms kvantitativt. Notera att MALDI-TOF-masspektroskopi bör undvikas eftersom denna metod innefattar laserstrålning för prov jonisering. Denna behandling sönder bifogade känsliga fluoroforer innan peptidmassa utläses och därmed underrepre senterar grader av färgämne-konjugering.
Indirekt men sätesspecifik märkning av cellbundna TCR med användning av monovalenta enkelkedjiga Fv-fragment
Det är fortfarande en utmaning att fästa färgämnen för att cellyte-associerade proteiner av levande celler i ett ställesspecifikt sätt. För att övervinna detta hinder för ytexponerade TCR har en monovalent enkelkedjigt version (scFv) från generna enligt TCRβ -reactive monoklonala antikroppen H57-197 2 konstruerats. Kristallstrukturen för denna antikropp i komplex med TCR tillåter att rationellt utforma en version, i vilken en serinrest i omedelbar närhet till C-terminalen av MHC associerad peptid (där motsvarande FRET partnern färgämne är fäst) substitueras för en cysteinrest. Denna mutant cystein fungerar sedan som en acceptor för färg konjugering (Figur 2).
Metoder för att spela FRET
nt "> Bulk FRET värden är bäst lämpade för att kontrollera förhållandet mellan valda mellan färg avstånd och FRET effektivitet mäts i denna TCR-pMHC bindande system 2. Dessutom bulkmätningar FRET avslöja kvalitativa och kvantitativa skillnader i synaptiska TCR-pMHC tillhörighet ( se nedan och protokoll avsnitt 3.2). Olika metoder för att kvantifiera FRET effektivitet har införts i litteraturen 6. I den här artikeln FRET registreras via(a) donator återhämtning efter acceptor blekning, och via
(b) strålningskänsliga FRET acceptor utsläpp.
Den första metoden (a) kräver användning av ett FRET-acceptor som lätt kan photobleached, och en givare, som är ganska fotostabila. Dessutom är det viktigt att se till att photobleached acceptorn är inte längre kan släcka donatorfluorescensen. Eftersom samma detekteringskanalen (donator) används för kvantifiering, faktorer ingen korrigering end inga kromatisk aberration måste beaktas, vilket gör denna metod enkel och tillförlitlig. Däremot kan kvantitativa mätningar inte upprepas på samma prov plats och förändringar i FRET kan inte spelas in under tiden. För att undvika effekter orsakade av molekylär diffusion eller cellulär motilitet snabb blekningssteg bör eftersträvas, vilket minimerar tiden passerar mellan första FRET donator (före acceptor blekning) och den andra FRET donator bild förvärv (efter FRET acceptor blekning). Det är rekommendera att använda en kraftfull laser ljuskälla av den FRET-acceptom excitationsvåglängden för att minimera dekoration och blekningstider.
I motsats, i tillvägagångssättet sensibiliserade mätning FRET utsläpp (b) FRET donatorn är glada och utsläpp av FRET mottagaren observeras i FRET acceptkanalen. Förändringar i FRET acceptor signal kan spelas in med tiden, men utsläpp av FRET donatorn i rödskiftade acceptor kanal (termed genomblödning) och FRET acceptor tvär excitation via givarexcite måste noggrant bestämmas och subtraheras från den inspelade FRET acceptor kanal. För detta motsvarande FRET donator och FRET-acceptor-bilder måste spatialt inriktade.
Detektion av en enda molekyl (sm) FRET händelser
Med användning av laser som exciteringskälla, en känslig kamera och buller-försvagade TIRF mikroskopi fluorescensen av enstaka fluoroforer lätt kan spåras över tiden. Liknande gäller för detektion av intermolekylära smFRET händelser. Dock kan komplikationer orsakas av FRET donator genomblödning och korsexcitering av FRET mottagaren, och därmed stor försiktighet måste iakttas vid justering av fluoroforenhetema tätheter i smFRET experimentet.
I protokollet nedan (protokoll avsnitt 4) TCR valdes FRET givare i hög förekomst och pMHC som FRET acceptor i begränsad omfattning. Att dämpa FRET donator genomblödning tillräckligt, dekorera 10-30% av TCR med fluorescerande scFv och 90-70% av TCR med icke-fluorescerande scFv. Här FRET acceptkanalen valdes som enda molekyl kanal eftersom det är konfokal med enda molekyl FRET kanal. Detta bidrar till att rikta smFRET händelser med enda molekyl FRET-acceptorer, som är grunden för smFRET validering.
Utvinna synaptiska off-hastigheter genom smFRET mätningar
Fotoblekning av både FRET givare och FRET acceptor måste redovisas vid extrahering halveringstiden interaktioner från enda molekyl FRET spår. Antalet observerbara FRET-signaler i början av sitt utseende som en enda donator-acceptor par N (0) minskas med tiden genom både ej bindande för receptor-ligandkomplex och fotoblekning. Antalet överlevande komplex vid en given tidpunkt N (t) kan matematiskt uttryckas på följande sätt:
<p class = "jove_content">
I fotoblekning termen exp (-t / τ blekmedel) tiden t beskrivs av produkten av antalet observationer n och belysningstiden t sjuk på grund av den icke-kontinuerliga, diskreta observationsmod (dvs., blekning endast sker under belysning ). Inom den kinetiska termen exp- (t / τ av) tiden t är produkten av antalet observationer n och tiden t fördröjningen för en enstaka FRET iakttagelse (dvs, händer kinetisk ej bindande kontinuerligt). Ekvation 1 kan uttryckas som:
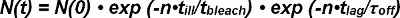
Termen τ blekmedel / τ sjuk describes antalet observationer tills blekning inträffar och definieras som väntevärdet <n bleka> sin exponentiell funktion. Ekvation 2 kan förenklas enligt följande:
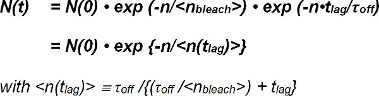
Väntevärdet <n (t eftersläpning)> av antalet bildrutor N (t) med observerbara FRET-händelser efter tiden t direkt bestäms från experimentet. Det beror på den inställbara tiden mellan observationer (t LAG) väljs i försöket och de okända värdena för τ off (inversen av off-rate k off) och <n bleka>, det förväntade värdet av antalet observationer innan blekningen sker .
Således, beräkning av väntevärdet <n (t eftersläpning)> under åtminstone två värden på t <sub> lag tillåter experimentell bestämning av <n bleka> och t bort.
Extrahera synaptiska 2D-K D-värden genom FRET baserade mätningar
Mätning TCR beläggning a, det vill säga förhållandet mellan bundna TCR och totala TCR, är centralt för att avgöra synaptiska 2D-K D-värden. Enligt ekvation 4 denna term är direkt proportionell mot den uppmätta FRET erhållande så länge TCR tjänar som FRET givare och pMHCs som FRET-acceptorer.
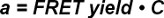
med a = TCR beläggning, C = omvandlingsfaktor
C är en konstant, som beror av FRET-systemet och fluoroforerna som används. Det kan bestämmas experimentellt, såsom visas nedan. en kan omvandlas till en 2D-Kd enligt ekvation 5, närinitial densitet av TCR-ligander före tillsats av T-celler till dubbelskiktet är känd. Detta är på grund av den höga mobiliteten hos SLB lösa proteiner och även eftersom SLBs ger en nästan outtömlig reservoar av ligander 2.
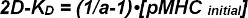
med [pMHC initial] = initial densitet av pMHC före tillsatsen av T-celler
Med ekvationerna 4 och 5 kan man nu enkelt bestämma den synaptiska 2D-K D mellan TCR och pMHC. Detta är mest tillförlitligt sker med FRET mätningar baserade på givar återhämtning efter acceptor blekning (se protokoll avsnitt 3.1).
Men för att mäta C förhållandet mellan FRET-intensiteten I FRET (korrigerat för bakgrunds, FRET-givare genomblödning och FRET acceptor tvär excitation) och TCR beläggning en måste bestämmas. För detta, enbehöver veta förhållandet R mellan den genomsnittliga fluorescensintensiteten av enstaka TCR-associerade FRET givar fluoroforer (t ex Cy3 eller AF555) sm jag FRET givare och den genomsnittliga intensitet enda molekyl FRET händelser sm jag FRET. R beror på FRET-systemet i fråga, emissionsfilter och kamera som används för fluorescensdetektering.
TCR inflyttning en kan då direkt bestämmas enligt ekvation 6.

med R = sm jag FRET donator / sm jag FRET
R bestämdes som 1,45 för H57 scFv- Cy3 / pMHC-Cy5 systemet leder till:
a = bulk jag FRET / bulk jag TCR-Cy3 • 1,45
Förhållandet mellan TCR beläggning en och FRET utbytet kan bestämmas genom FRET donator återvinnay efter acceptor blekning. För detta båda parametrarna är avsatta mot en annan för ett antal TCR microclusters såsom visas i fig 4A .Den Lutningen på den linjära passform anger omvandlingsfaktorn C (ur ekvation 4).
Såsom visas i figur 4A, uppgår för (a) H57 scFv C – Cy3 / pMHC-Cy5 FRET-systemet och (b) den applicerade mikroskopsystemet konfiguration till 1,995. TCR inflyttning en lätt kan härledas på följande sätt:
TCR beläggning a = FRET ge • 1.995
Protocol
Representative Results
Discussion
Mätt protein-protein interaktioner in situ är mycket önskvärt, särskilt när det handlar om låg affinitet interaktioner såsom TCR-pMHC-bindning 11. Detta beror på att på-hastighet samt stabiliteten hos sådana interaktioner avsevärt påverkas av de speciella omständigheter under vilka bindning sker. Minimal invasiva FRET-baserad avbildning är således i princip perfekt lämpade för sådana uppgifter, men ändå innebära ett antal hinder som först måste övervinnas. Buller som genereras av cellulär autofluorescens begränsar känsligheten av mätningarna och bör därför hållas på ett minimum. TIRF mikroskopi tjänar detta behov mycket väl 12 men kräver funktionalisering av glas diabilder, helst i form av en plan glas stöds lipiddubbelskikt dekorerad med proteiner av val 13-15. En annan fördel med en delvis reconstitutive strategi är att rekombinanta tvåskiktsmembran bosatt FRET partners kan vara mycket mmalm lätt märkt på ett kvantitativt, platsspecifika och rationellt sätt med mindre och ljusare fluoroforer än vad som skulle vara möjligt med cell ytuttryckta proteiner. TCR är märkta med rekombinant scFv V s, som inte påverkar T-celligenkänning, som testades tidigare två. Dessutom proteinkompositionen av SLB, exempelvis densiteten hos pMHCs och valet av accessoriska faktorer kan anpassas till sina specifika behov. Vi har tidigare utfört experiment med varierande densiteter stimulerande pMHCs, men har inte upptäckt signifikanta skillnader i 2D-k off och 2D-K D 2.
Hittills här erkännandet av MHC klass Il-molekyler har behandlats med enbart, främst på grund av arten av deras peptidbindande klyftan, som är öppen i båda ändar och därmed rymmer större peptider, inklusive en länk för fluorofor fastsättning. I vissa fall sådant tillvägagångssätt kan också fungera för märkning MHC class I molekyler 16 men stor försiktighet bör vidtas för att kontrollera deras användning i försök. Känsligheten hos T-celler mot antigener, som kan mätas via T-cellproliferationsanalyser, liksom pMHC-TCR-bindande kinetik mätt in vitro genom ytplasmonresonans bör inte påverkas av tillsats av linkern och fluoroforen till peptiden. Alternativt kan MHC klass I-molekyler sig märkas på ett sätesspecifikt sätt med införandet av en oparad cystein inom sekvensen av den tunga kedjan (opublicerade observationer).
Med användning av lämpliga molekylära prober kan i princip studeras någon synaptisk interaktion protein-protein i en mode som beskrivs häri. Sådana prober, t.ex. bör scFv s eller Skapat ankyrin upprepningsproteiner (DARPins) 17, vara monovalent och bör binda sitt mål stabilt utan att påverka interaktionen av intresse. Naturligtvis strukturell INFORMATIOn är mycket önskvärt för rationell sond design men inte absolut nödvändigt. Vid upprättandet av ett par nya FRET partners, är det rekommenderat att registrera och analysera FRET i bulk först. Platser av etikettfäst kan varieras avsevärt för att maximera FRET signalen och även för att verifiera att mätta FRET avkastningen skiljer sig åt beroende på inter-dye avstånd. När systemet är optimerat, enda molekyl FRET signaler kan registreras genom att begränsa märkning av den höga överflöd FRET partner till 10-30% och blekning den låga förekomsten FRET partner tills enskilda molekyler är upplösningen på området för belysning.
Sist men inte minst det bör noteras att SLBs approximera några men inte alla aspekter av en fysiologisk plasmamembranet. Egenskaper som membran krökning och flexibilitet, domän uppdelning, cytoskelettala omflyttningar och cellmotilitet samt en hög mängd ytuttryckta membranproteiner är inte företräds av SLBs men kan påverka than bearbeta under utredning. Stora ansträngningar kommer att behöva investeras för att skapa avbildningsmetoder som tillåter övervakning protein-proteininteraktioner med enda molekyl upplösning i fysiologiska synapser, som är oåtkomliga för TIRF avbildning.
Disclosures
The authors have nothing to disclose.
Acknowledgements
MA fick stöd av ett Schrödinger gemenskap i den österrikiska Science Fund (FWF, J3086-B11) och tackar Max-Planck-Society for ekonomiskt och administrativt stöd. GS och JH stöddes av Wien Science and Technology Fund (WWTF, LS13-030).
Materials
| LB-media | Fisher Scientific | 10000713 | bacterial expression |
| Sf900 II | Life Technologies | 10227402 | insect cell media for baculo virus production |
| Insect-XPRESS with L-glutamine (Lonza) | Fisher Scientific | 10564038 | insect cell media for baculo virus expression |
| Sf9 cells | Life Technologies | 11496-015 | cells for virus production and expansion |
| High Five Cells | Life Technologies | B855-02 | cells for potein expression |
| LB-media | Fisher Scientific | 10000713 | bacterial expression |
| Centramate System | Pall | protein concentartion from large volumes | |
| Centramate cassette 10kDa cutoff | Pall | OS010T12 | protein concentartion from large volumes |
| Amicon Ultra-15 Centrifugal Filter Units | EMD Millipore | UFC900308 | protein concentartion |
| Amicon Ultra-4 Centrifugal Filter Units | EMD Millipore | UFC800308 | protein concentartion |
| Amicon Stirred Ultrafiltration Cell Model 200 mL | EMD Millipore | 5123 | protein concentartion |
| Äkta pure 25L | GE Healthcare | 29-0182-24 | protein purification |
| Superdex 200 10/300 GL | GE Healthcare | 17-5175-01 | protein purification |
| Superdex 75 10/300 GL | GE Healthcare | 17-5174-01 | protein purification |
| Mono Q 5/50GL | GE Healthcare | 17-5166-01 | protein purification |
| Ni Sepharose 6 Fast Flow | GE Healthcare | 17-5318-01 | protein purification |
| Tricorn 10/20 column | GE Healthcare | 28-4064-13 | protein purification |
| Gilson HPLC system | Gilson | purificationof fluorochrome-coupled peptides | |
| Pursuit XRs C18, 5 µm particle size, 21.2*250mm column size | Agilent | A6000250X212 | purificationof fluorochrome-coupled peptides |
| Pursuit XRs C18, 5 µm particle size, 21.2*50 mm column size | Agilent | A6000050G212 | purificationof fluorochrome-coupled peptides |
| Tricorn 10/20 column | GE Healthcare | 28-4064-13 | protein purification |
| Gilson HPLC system | Gilson | purificationof fluorochrome-coupled peptides | |
| Pursuit XRs C18, 5 µm particle size, 21.2*250mm column size | Agilent | A6000250X212 | purificationof fluorochrome-coupled peptides |
| Pursuit XRs C18, 5 µm particle size, 21.2*50 mm column size | Agilent | A6000050G212 | purificationof fluorochrome-coupled peptides |
| Cy3 maleimide | GE Healthcare | PA23031 | site-specific protein labeling via mutant unpaired cysteines |
| Cy5 maleimide | GE Healthcare | PA25031 | site-specific protein labeling via mutant unpaired cysteines |
| Alexa Fluor 555 C2 Maleimide | Life Technologies | A-20346 | site-specific protein labeling via mutant unpaired cysteines |
| Alexa Fluor 647 C2 Maleimide | Life Technologies | A-20347 | site-specific protein labeling via mutant unpaired cysteines |
| Fura-2, AM, cell permeant | Life Technologies | F-1221 | calcium-sensitive dye for cell labeling |
| dimethyl sulfoxide | Sigma Aldrich | 151874 | for dissolving fura-2 am |
| Hank's Balanced Salt Solution plus calcium/magnesium | Fisher Scientific | 10225362 | imaging buffer |
| PBS | Life Technologies | 14190-136 | |
| Bovine Serum Albumin lyophilized powder | Sigma Aldrich | A2153 | supplement for imaging buffer |
| 14-4-4S antibody | affimetrix eBioscience | 14-5980-81 | blocking antibody for H2-I-Ek (recognized by the 5c.c7, 2B4 and AND TCR) |
| 5 ml polypropylene round-bottom tube | Becton Dickinson | FALCON 352063 | |
| 0.22 μm Ultrafree-MC centrifugal filter unit | EMD Millipore | UFC30GV0S | |
| Syringe filter 0.2µm | Millipore | GVWP04700 | |
| TetraSpeck Microspheres, 0.1 µm, fluorescent blue/green/orange/dark red | Life technologies | T-7279 | |
| Microscope for fura-2-based calcium measurements | LEICA | DMI4000B | |
| Microscope for (single molecule) FRET measurements | LEICA/ZEISS/NIKON/OLYMPUS | for details please refer to parallel JoVE contribution by Axmann et al. | |
| planar supported lipid bilayers | for details please refer to parallel JoVE contribution by Axmann et al. | ||
| RPMI 1640, with L-Glutamine | Life Technologies | 11554416 | T-cell media |
| non-essential amino acid 100X | Hyclone | SH30238.01 | T-cell media supplement |
| penicillin/streptomycin/L-glutamine 100x | Life Technologies | 12000226 | T-cell media supplement |
| 2-mercaptoethanol | Sigma Aldrich | M6250 | T-cell media supplement |
| mouse interleukin-2 recombinant protein | BPS Bioscience | 90185-B | T-cell media supplement |
| Research Grade Fetal Bovine Serum | Hyclone | SV30160.03 | T-cell media supplement |
| Origin (analysis program) | OrigenLab | http://www.originlab.com/ | non-linear fitting of two parameters (tauoff, [ntlag]) |
References
- Garcia, K. C., Adams, J. J., Feng, D., Ely, L. K. The molecular basis of TCR germline bias for MHC is surprisingly simple. Nat Immunol.. 10, 143-147 (2009).
- Huppa, J. B., et al. TCR-peptide-MHC interactions in situ show accelerated kinetics and increased affinity. Nature.. 463, 963-967 (2010).
- Huppa, J. B., Davis, M. M. The interdisciplinary science of T-cell recognition. Advances in immunology.. 119, 1-50 (2013).
- Axmann, M., Schuetz, G. J., Huppa, J. B. Single Molecule Microscopy on Planar Supported Bilayers. Journal of Vizualized Experiments J. Vis. Exp.. 101, e53158 (2015).
- Xie, J., et al. Photocrosslinkable pMHC monomers stain T cells specifically and cause ligand-bound TCRs to be preferentially transported to the cSMAC. Nat Immunol. 13, 674-680 (2012).
- Jares-Erijman, E. A., Jovin, T. M. FRET imaging. Nat Biotechnol. 21, 1387-1395 (2003).
- Toebes, M., et al. Design and use of conditional MHC class I ligands. Nat Med. 12, 246-251 (2006).
- Tsumoto, K., et al. Highly efficient recovery of functional single-chain Fv fragments from inclusion bodies overexpressed in Escherichia coli by controlled introduction of oxidizing reagent–application to a human single-chain Fv fragment. J Immunol Methods. 219, 119-129 (1998).
- Ruegg, U. T., Rudinger, J. Reductive cleavage of cystine disulfides with tributylphosphine. Methods Enzymol. 47, 111-116 (1977).
- Ruprecht, V., Brameshuber, M., Schütz, G. J. Two-color single molecule tracking combined with photobleaching for the detection of rare molecular interactions in fluid biomembranes. Soft Matter. 6, 568-581 (2010).
- Dustin, M. L., Bromley, S. K., Davis, M. M., Zhu, C. Identification of self through two-dimensional chemistry and synapses. Annu Rev Cell Dev Biol. 17, 133-157 (2001).
- Axelrod, D. Cell-substrate contacts illuminated by total internal reflection fluorescence. The Journal of cell biology. 89, 141-145 (1981).
- Grakoui, A., et al. The immunological synapse: a molecular machine controlling T cell activation. Science. 285, 221-227 (1999).
- Kaizuka, Y., Douglass, A. D., Varma, R., Dustin, M. L., Vale, R. D. Mechanisms for segregating T cell receptor and adhesion molecules during immunological synapse formation in Jurkat T cells. Proc Natl Acad Sci USA. 104, 20296-20301 (2007).
- Varma, R., Campi, G., Yokosuka, T., Saito, T., Dustin, M. L. T cell receptor-proximal signals are sustained in peripheral microclusters and terminated in the central supramolecular activation cluster. Immunity. 25, 117-127 (2006).
- Purbhoo, M. A., Irvine, D. J., Huppa, J. B., Davis, M. M. T cell killing does not require the formation of a stable mature immunological synapse. Nat Immunol. 5, 524-530 (2004).
- Binz, H. K., Stumpp, M. T., Forrer, P., Amstutz, P., Pluckthun, A. Designing repeat proteins: well-expressed, soluble and stable proteins from combinatorial libraries of consensus ankyrin repeat proteins. J Mol Biol. 332, 489-503 (2003).

