Inducible T7 RNA polimerasa mediada Multigene Expression System, pMGX
Summary
Este estudio describe métodos para la co-expresión mediada por T7 de múltiples genes de un único plásmido en Escherichia coli usando el sistema de plásmido pMGX.
Abstract
La co-expresión de múltiples proteínas es cada vez más esencial para la biología sintética, estudiando los complejos proteína-proteína, y caracterizando y aprovechando las vías biosintéticas. En este manuscrito, se describe el uso de un sistema altamente eficaz para la construcción de operones sintéticos multigénicos bajo el control de una ARN polimerasa T7 inducible. Este sistema permite que muchos genes se expresen simultáneamente a partir de un plásmido. En este caso, un conjunto de cuatro vectores relacionados, pMGX-A, pMGX-hisA, pMGX-K y pMGX-hisK, con el marcador seleccionable de resistencia a la ampicilina o la kanamicina (A y K) y que poseen o carecen de una hexahistidina N-terminal Etiqueta (su) se describen. Se proporcionan protocolos detallados para la construcción de operones sintéticos usando este sistema vectorial junto con los datos correspondientes, mostrando que un sistema basado en pMGX que contiene cinco genes puede ser fácilmente construido y usado para producir las cinco proteínas codificadas en Escherichia coli . Este sistemaEm y el protocolo permite a los investigadores a rutinariamente expresar complejos módulos de múltiples componentes y vías en E. coli .
Introduction
La co-expresión de múltiples proteínas es cada vez más esencial, particularmente en las aplicaciones de biología sintética, donde se deben expresar múltiples módulos funcionales 1 ; En el estudio de complejos proteína-proteína, donde la expresión y la función a menudo requieren co-expresión 2 , 3 ; Y en la caracterización y el aprovechamiento de las vías biosintéticas, en las que cada gen en la vía debe expresarse 4 , 5 , 6 , 7 , 8 . Se han desarrollado varios sistemas para la co-expresión, particularmente en el organismo huésped Escherichia coli , el caballo de trabajo para la expresión de proteínas recombinantes en laboratorio 9 . Por ejemplo, se pueden usar múltiples plásmidos con diferentes marcadores seleccionables para expresar proteínas individuales utilizando una gran cantidad de diferentes ex Vectores de presión 10 , 11 . Los sistemas individuales de plásmido para la expresión de múltiples proteínas han utilizado múltiples promotores para controlar la expresión de cada gen 10 , 12 ; Operones sintéticos, donde múltiples genes se codifican en un solo transcrito 2 , 13 ; O, en algunos casos, un solo gen que codifica un polipéptido que se procesa en última instancia proteolíticamente, produciendo las proteínas deseadas de interés 14 .
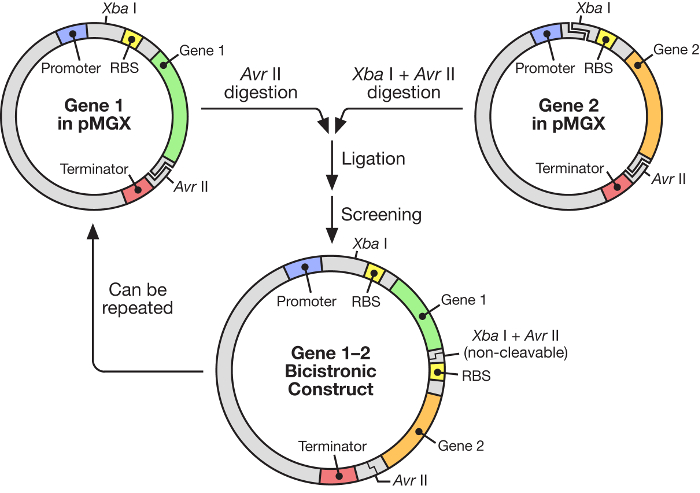
Figura 1: Flujo de trabajo pMGX mostrando la construcción de un vector policistrónico. El sistema pMGX proporciona una estrategia flexible y fácil de usar para la construcción de operones sintéticos bajo el control de un promotor T7 inducible.E.com/files/ftp_upload/55187/55187fig1large.jpg "target =" _ blank "> Haga clic aquí para ver una versión más grande de esta figura.
En este manuscrito, se describe el uso de un sistema altamente eficaz para la construcción de operones sintéticos multigénicos bajo el control de una ARN polimerasa T7 inducible ( Figura 1 ). Este sistema permite que muchos genes se expresen simultáneamente a partir de un plásmido. Se basa en un sistema de plásmidos, originalmente llamado pKH22, que se ha utilizado con éxito para un número de diferentes aplicaciones 6 , 7 , 8 . En este caso, este conjunto de plásmidos se amplía para incluir cuatro vectores relacionados: pMGX-A, un vector de expresión que carece de etiquetas C o N-terminales y con el marcador de resistencia a la ampicilina; PMGX-hisA, un vector de expresión que codifica una etiqueta de hexahistidina N-terminal y con el marcador de resistencia a la ampicilina; PMGX-K, un vector de expresión lMarcar cualquier marcador C o N-terminal y con el marcador de resistencia a la kanamicina; Y pMGX-hisK, un vector de expresión que codifica una etiqueta de hexahistidina N-terminal y con el marcador de resistencia a la kanamicina. En este estudio, se demuestra el método para generar un vector policistrónico que contiene cinco genes usando el sistema pMGX, específicamente pMGX-A, junto con la producción exitosa de cada proteína individual en Escherichia coli .
Protocol
Representative Results
Discussion
La co-expresión de múltiples genes es cada vez más esencial, en particular en la caracterización y reconstitución complejas, multigénicas vías metabólicas [ 3 , 4 , 5] . El sistema pMGX hace co-expresión multigén en la rutina de E. coli 6 , 7 , 8 y accesible a diversos investigadores. En este …
Disclosures
The authors have nothing to disclose.
Acknowledgements
Este trabajo fue apoyado por el Consejo de Investigación de Ciencias Naturales e Ingeniería de Canadá.
Materials
| Enzymes | |||
| Alkaline Phosphatase, Calf Intestinal (CIP) | New England Biolabs | M0290S | |
| AvrII | New England Biolabs | R0174S | |
| EcoRI | New England Biolabs | R0101S | |
| NdeI | New England Biolabs | R0111S | |
| XbaI | New England Biolabs | R0145S | |
| Herculase II Fusion DNA Polymerase | Agilent Technologies | 600677 | |
| T4 DNA Ligase | New England Biolabs | M0202S | |
| Name | Company | Catalog Number | Comments |
| Reagents | |||
| 1 kb DNA ladder | New England Biolabs | N3232L | |
| 4-20% Mini-PROTEAN TGX Stain-Free Protein Gels | Bio-Rad | 456-8095 | |
| 50 x TAE | Fisher Thermo Scientific | BP1332-4 | |
| Agar | Fisher Thermo Scientific | BP1423-500 | |
| Agarose | Fisher Thermo Scientific | BP160-500 | |
| Ampicilin | Sigma-Alrich | A9518-5G | |
| BL21 (DE3) chemically comeptent cells | Comeptent cell prepared in house | ||
| B-PER Bacterial Protein Extraction Reagent | Fisher Thermo Scientific | PI78243 | |
| dNTP mix | Agilent Technologies | Supplied with polymerase | |
| Gel Extraction Kit | Omega | D2500-02 | E.Z.N.A Gel Extraction, supplied by VWR Cat 3: CA101318-972 |
| Glycine | Fisher Thermo Scientific | BP381-1 | |
| His Tag Antibody [HRP], mAb, Mouse | GenScript | A00612 | |
| Immobilon Western Chemiluminescent HRP Substrate | EMD Millipore | WBKLS0100 | |
| IPTG | Sigma-Alrich | 15502-10G | |
| LB | Fisher Thermo Scientific | BP1426-500 | |
| Methanol | Fisher Thermo Scientific | A411-20 | |
| Pasteurized instant skim milk powder | Local grocery store | No-name grocery store milk is adequate | |
| Nitrocellulose membrane | Amersham Protran (GE Healthcare Life Sciences) | 10600007 | Membrane PT 0.45 µm 200 mm X 4 m, supplied by VWR Cat #: CA10061-086 |
| Plasmid DNA Isolation Kit | Omega | D6943-02 | E.Z.N.A Plasmid DNA MiniKit I, supplied by VWR Cat #: CA101318-898 |
| pMGX | Boddy Lab | Request from the Boddy Lab Contact cboddy@uottawa.ca | |
| Primers | Intergrated DNA Technologies | Design primers as needed for desired gene | |
| Synthetic Gene | Life Technologies | Design and optimize as needed | |
| Thick Blot Filter Paper | Bio-Rad | 1703932 | |
| Tris base | BioShop | TRS001.1 | |
| Tween-20 | Sigma-Alrich | P9416-50ML | |
| XL1-Blue chemically competent cells | Comeptent cell prepared in house | ||
| Name | Company | Catalog Number | Comments |
| Equipment | |||
| BioSpectrometer | Eppendorf | RK-83600-07 | |
| Gel box – PAGE | Bio-Rad | 1658005 | Mini-PROTEIN Tetra Vertical Electrophoresis Cell |
| Gel Imager | Alpha Innotech | AlphaImager EC | |
| Incubator-oven | Fisher Thermo Scientific | 11-690-650D | Isotemp |
| Incubator-shaker | Fisher Thermo Scientific | SHKE6000-7 | MaxQ 6000 |
| Personna Razors | Fisher Thermo Scientific | S04615 | |
| Power Pack | Bio-Rad | S65533Q | FB300 |
| Transilluminator | VWR International | M-10E,6W | |
| Thermocylcer | Eppendorf | Z316091 | Mastercycler Personal, supplied by Sigma |
| UV Face-Shield | 18-999-4542 | ||
| Waterbath | Fisher Thermo Scientific | 15-460-2SQ | |
| Western Transfer Apparatus | Bio-Rad | 1703935 | Mini-Trans Blot Cell |
References
- Purnick, P. E. M., Weiss, R. The second wave of synthetic biology: from modules to systems. Nat. Rev. Mol. Cell Biol. 10 (6), 410-422 (2009).
- Bieniossek, C., et al. Automated unrestricted multigene recombineering for multiprotein complex production. Nat. Methods. 6 (6), 447-450 (2009).
- Jochimsen, B., et al. Five phosphonate operon gene products as components of a multi-subunit complex of the carbon-phosphorus lyase pathway. Proc. Natl. Acad. Sci. USA. 108 (28), 11393-11398 (2011).
- Martin, V. J. J., Pitera, D. J., Withers, S. T., Newman, J. D., Keasling, J. D. Engineering a mevalonate pathway in Escherichia coli for production of terpenoids. Nat. Biotechnol. 21 (7), 796-802 (2003).
- Ajikumar, P. K., et al. Isoprenoid pathway optimization for Taxol precursor overproduction in Escherichia coli. Science. 330 (6000), 70-74 (2010).
- Boddy, C. N., Hotta, K., Tse, M. L., Watts, R. E., Khosla, C. Precursor-directed biosynthesis of epothilone in Escherichia coli. J. Am. Chem. Soc. 126 (24), 7436-7437 (2004).
- Lundgren, B. R., Boddy, C. N. Sialic acid and N-acyl sialic acid analog production by fermentation of metabolically and genetically engineered Escherichia coli. Org. Biomol. Chem. 5 (12), 1903-1909 (2007).
- Horsman, M. E., Lundgren, B. R., Boddy, C. N. N-Acetylneuraminic Acid Production in Escherichia coli Lacking N-Acetylglucosamine Catabolic Machinery. Chem. Eng. Commun. 203 (10), 1326-1335 (2016).
- Romier, C., et al. Co-expression of protein complexes in prokaryotic and eukaryotic hosts: experimental procedures, database tracking and case studies. Acta Crystallogr. D, Biol. Crystallogr. 62 (Pt 10), 1232-1242 (2006).
- Tolia, N. H., Joshua-Tor, L. Strategies for protein coexpression in Escherichia coli. Nat. Methods. 3 (1), 55-64 (2006).
- Chanda, P. K., Edris, W. A., Kennedy, J. D. A set of ligation-independent expression vectors for co-expression of proteins in Escherichia coli. Protein Expr. Purif. 47 (1), 217-224 (2006).
- Kim, K. -. J., et al. Two-promoter vector is highly efficient for overproduction of protein complexes. Protein Sci. 13 (6), 1698-1703 (2004).
- Tan, S., Kern, R. C., Selleck, W. The pST44 polycistronic expression system for producing protein complexes in Escherichia coli. Protein Expr. Purif. 40 (2), 385-395 (2005).
- Chen, X., Pham, E., Truong, K. TEV protease-facilitated stoichiometric delivery of multiple genes using a single expression vector. Protein Sci. 19 (12), 2379-2388 (2010).
- Lorenz, T. C. Polymerase chain reaction: basic protocol plus troubleshooting and optimization strategies. J. Vis. Exp. (63), e3998 (2012).
- Lee, P. Y., Costumbrado, J., Hsu, C. -. Y., Kim, Y. H. Agarose gel electrophoresis for the separation of DNA fragments. J. Vis. Exp. (62), (2012).
- Sukumaran, S. Concentration determination of nucleic acids and proteins using the micro-volume BioSpec-nano-spectrophotometer. J. Vis. Exp. (48), (2011).
- JoVE Science Education Database. Basic Methods in Cellular and Molecular Biology. Molecular Cloning. J. Vis. Exp Available from: https://www.jove.com/science-education/5074/molecular-cloning (2016)
- JoVE Science Education Database. Basic Methods in Cellular and Molecular Biology. The Western Blot. J. Vis. Exp Available from: https://www.jove.com/science-education/5065/the-western-blot (2016)
- Laible, M., Boonrod, K. Homemade site directed mutagenesis of whole plasmids. J. Vis. Exp. (27), (2009).

