En Aptamer basert sensor for uchelatert gadolinium (III)
Summary
The use of polydeoxynucleotide (44-mer aptamer) molecules for sensing unchelated gadolinium(III) ion in an aqueous solution is described. The presence of the ion is detected via an increase in the fluorescence emission of the sensor.
Abstract
A method for determining the presence of unchelated trivalent gadolinium ion (Gd3+) in aqueous solution is demonstrated. Gd3+ is often present in samples of gadolinium-based contrast agents as a result of incomplete reactions between the ligand and the ion, or as a dissociation product. Since the ion is toxic, its detection is of critical importance. Herein, the design and usage of an aptamer-based sensor (Gd-sensor) for Gd3+ are described. The sensor produces a fluorescence change in response to increasing concentrations of the ion, and has a limit of detection in the nanomolar range (~100 nM with a signal-to-noise ratio of 3). The assay may be run in an aqueous buffer at ambient pH (~7 – 7.4) in a 384-well microplate. The sensor is relatively unreactive toward other physiologically relevant metal ions such as sodium, potassium, and calcium ions, although it is not specific for Gd3+ over other trivalent lanthanides such as europium(III) and terbium(III). Nevertheless, the lanthanides are not commonly found in contrast agents or the biological systems, and the sensor may therefore be used to selectively determine unchelated Gd3+ in aqueous conditions.
Introduction
Den økende betydning av magnetisk resonansavbildning (MRI) i klinisk diagnose, som er begrenset av den iboende følsomheten av teknikken, har resultert i den raske veksten av forskning på utvikling av nye gadolinium-baserte kontrastmidler (GBCAs) 1. GBCAs er molekyler som administreres for å forbedre bildekvaliteten, og de vanligvis har den kjemiske strukturen av et treverdig ion gadolinium (Gd 3+) koordinert til en polydentat ligand. Dette kompleks er av avgjørende betydning som uchelatert Gd 3+ er giftig; det har vært innblandet i utviklingen av nefrogen systemisk fibrose hos noen pasienter med nyresykdom eller fiasko 2. Følgelig, oppdager den vandige fri ion er instrumental i å sikre sikkerheten til GBCAs. Tilstedeværelsen av uchelatert Gd 3+ i gbca løsninger ofte er resultatet av en ufullstendig reaksjon mellom liganden og den ion, dissosiasjon av komplekset, eller fortrengningt av andre biologiske metallkationer 3.
Blant de mange teknikker som for tiden anvendes for å bestemme tilstedeværelsen av Gd 3+, de som er avhengig av kromatografi og / eller spektrometri rang høyest når det gjelder fleksibilitet og anvendbarhet 4. Blant deres styrke er høy følsomhet og nøyaktighet, evnen til å analysere ulike eksempel matriser (inkludert humant serum 5, urin og hår 6, 7 avløpsvann, og kontrastmiddel formuleringer 8), og den samtidige kvantifisering av flere Gd 3 + komplekser (en liste studier før 2013 er beskrevet i en omfattende gjennomgang av Telgmann et al.) 4. Den eneste ulempen er at flere av disse metodene krever besetninger (som induktivt koplet plasma-massespektrometri) 4 at noen laboratorier kanskje ikke har tilgang til. Innenfor rammen av romanen gbca funn i forskning og proof-of-concept nivåer, arelatively mer praktisk, rask og kostnadseffektiv spektroskopisk basert metode (for eksempel UV-Vis absorpsjon eller fluorescens) kan tjene som et verdifullt alternativ. Med disse programmene i tankene, var en fluorescerende aptamer basert sensor for vann Gd 3+ utviklet ni.
Den aptamer (Gd-aptamer) er et 44-base-lang enkelt-trådet DNA-molekyl med en spesifikk sekvens av baser som ble isolert gjennom prosessen med systematiske utskilling av ligander med eksponensiell anrikning (SELEX) 9. For å tilpasse den aptamer til en fluoriserende sensor, er en fluorofor festet til 5'-terminale ende av tråden, som deretter hybridisert med en slukke tråd (QS) via 13 komplementære baser (figur 1). QS er merket med en mørk quencher molekyl ved 3'-terminus. I fravær av Gd 3+, føleren (Gd-sensor), som består av en 1: 2 molforhold av Gd-aptamer og QS henholdsvis, vil ha minimal fluorescens-emisjon på grunn av to energioverføring fra fluoroforen til drikk. Tilsetningen av vandig Gd 3+ vil fortrenge QS fra Gd-aptamer, noe som resulterer i en økning i fluorescensemisjon.
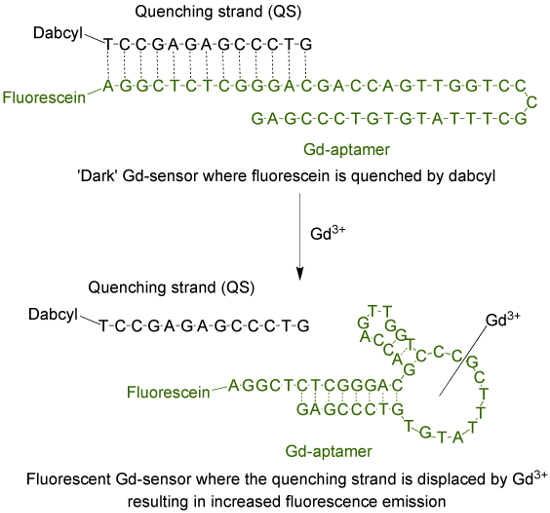
Figur 1. Sensor (Gd-sensor) som består av 44-base-lang aptamer (Gd-aptamer) merket med fluorescein (en fluorofor) og 13-base-quenching lang tråd (QS) merket med dabcyl (en mørk quencher) . I fravær av uchelatert Gd 3+, fluorescensen av sensoren er minimal. Under tilsetning av Gd 3+, forskyvning av QS inntreffer og en økning i fluorescensemisjon observeres. Klikk her for å se en større versjon av dette tallet.
Det finnes i dag, en vanlig brukt spektroskopisk basert metode for å detektereing vandig Gd 3+. Denne analysen anvender molekylet xylenolorange, som gjennomgår en forskyvning i den maksimale absorpsjon bølgelengde 433-573 nm ved chelatering å ionet 10. Forholdet mellom disse to absorbans maksima kan brukes til å kvantifisere mengden av uchelatert Gd 3+. Den aptamer sensoren er et alternativ (kan også være komplementær) til den xylenolorange assay, som de to metodene har forskjellige reaksjonsbetingelser (for eksempel pH og sammensetningen av de bufferoppløsninger som brukes), mål-selektiviteter, lineære områder av kvantifisering, og deteksjons modaliteter 9.
Protocol
Representative Results
Discussion
Ved hjelp av aptamer-baserte Gd-sensor, en økning i fluorescensemisjon som er proporsjonal med konsentrasjonen av uchelatert Gd 3+ observeres. Å minimalisere mengden av prøve som brukes, kan analysen bli kjørt i en 384-brønners mikroplate med et totalt prøvevolum på 45 ul pr brønn. I denne designen, ble valget av fluorescein (FAM) og dabcyl (DAB) i hovedsak basert på kostnaden av reagenser; for å modifisere emisjonsbølgelengden, en annen sammenkobling av fluorofor og slukkeren kan brukes 11.</…
Disclosures
The authors have nothing to disclose.
Acknowledgements
We would like to gratefully acknowledge Dr. Milan N Stojanovic from Columbia University, New York, NY for valuable scientific input. This work is supported by funding from the California State University East Bay (CSUEB) and the CSUEB Faculty Support Grant-Individual Researcher. O.E., T.C., and A.L. were supported by the CSUEB Center for Student Research (CSR) Fellowship.
Materials
| Gd-aptamer | IDTDNA | Input sequence and fluorophore modification in the order form | A fluorophore with a different emission wavelength may be used. The aptamer may also be ordered from another company. |
| Quenching strand | IDTDNA | Input sequence and quencher modification in the order form | A different quencher for optimal energy transfer from the fluorophore may be used. The aptamer may also be ordered from another company. |
| Molecular biology grade water | No specific manufacturer, both DEPC or non-DEPC treated work equally well | ||
| Gadolinium(III) chloride anhydrous | Strem | 936416 | Toxic |
| HEPES | Fisher Scientific | BP310-500 | |
| Magnesium chloride anhydrous | MP Biomedicals | 0520984480 – 100 g | |
| Sodium Chloride | Acros Organics | 327300025 | |
| Potassium chloride | Fisher Scientific | P333-500 | |
| Sodium hydroxide, pellets | Fisher Scientific | BP359 | Corrosive |
| Hydrochloric acid | Fisher Scientific | SA49 | Toxic and corrosive |
| 384-well low flange black flat bottom polystyrene NBS plates | Corning | 3575 | Plates which are suitable for fluorescence reading are required. |
| Nalgene Rapid-Flow sterile disposable bottle top filter | Thermo Scientific | 5680020 | The bottle top is fitted with 0.2 micron PES membrane |
| Disposable sterile bottles 250 mL | Corning | 430281 | A larger or smaller bottle may be used |
| 1.5 mL microcentrifuge tubes | No specific manufacturer, as long as they are DNAse and RNAse-free | ||
| 0.2 mL PCR tubes | No specific manufacturer, as long as they are DNAse and RNAse-free | ||
| Micropipets | No specific manufacturer | ||
| Pipet tips (non filter) of appropriate sizes | No specific manufacturer, as long as they are DNAse and RNAse-free | ||
| Name of Equipment | |||
| Plate reader | Biotek Synergy H1 | Plate readers from other manufacturers would work equally well |
References
- Shen, C., New, E. J. Promising strategies for Gd-based responsive magnetic resonance imaging contrast agents. Curr. Opin. Chem. Biol. 17 (2), 158-166 (2013).
- Cheong, B. Y. C., Muthupillai, R. Nephrogenic systemic fibrosis: a concise review for cardiologists. Tex. Heart Inst. J. 37 (5), 508-515 (2010).
- Hao, D., Ai, T., Goerner, F., Hu, X., Runge, V. M., Tweedle, M. MRI contrast agents: basic chemistry and safety. J Magn. Reson. Imaging. 36 (5), 1060-1071 (2012).
- Telgmann, L., Sperling, M., Karst, U. Determination of gadolinium-based MRI contrast agents in biological and environmental samples: a review. Anal. Chim. Acta. 764, 1-16 (2013).
- Frenzel, T., Lengsfeld, P., Schirmer, H., Hütter, J., Weinmann, H. -. J. Stability of gadolinium-based magnetic resonance imaging contrast agents in human serum at 37 degrees C. Invest. Radiol. 43 (12), 817-828 (2008).
- Loreti, V., Bettmer, J. Determination of the MRI contrast agent Gd-DTPA by SEC-ICP-MS. Anal. Bioanal. Chem. 379 (7), 1050-1054 (2004).
- Telgmann, L., et al. Speciation and isotope dilution analysis of gadolinium-based contrast agents in wastewater. Environ. Sci. Technol. 46 (21), 11929-11936 (2012).
- Cleveland, D., et al. Chromatographic methods for the quantification of free and chelated gadolinium species in MRI contrast agent formulations. Anal. Bioanal. Chem. 398 (7), 2987-2995 (2010).
- Edogun, O., Nguyen, N. H., Halim, M. Fluorescent single-stranded DNA-based assay for detecting unchelated gadolinium(III) ions in aqueous solution. Anal. Bioanal. Chem. 408 (15), 4121-4131 (2016).
- Barge, A., Cravotto, G., Gianolio, E., Fedeli, F. How to determine free Gd and free ligand in solution of Gd chelates. A technical note. Contrast Med. Mol. Imaging. 1 (5), 184-188 (2006).
- Johansson, M. K. Choosing reporter-quencher pairs for efficient quenching through formation of intramolecular dimers. Methods Mol. Biol. 335, 17-29 (2006).
- Sherry, A. D., Caravan, P., Lenkinski, R. E. A primer on gadolinium chemistry. J. Magn. Reson. Imaging. 30 (6), 1240-1248 (2009).
- Shakhverdov, T. A. A cross-relaxation mechanism of fluorescence quenching in complexes of lanthanide ions with organic ligands. Opt. Spectrosc. 95 (4), 571-580 (2003).
- Brittain, H. G. Submicrogram determination of lanthanides through quenching of calcein blue fluorescence. Anal. Chem. 59 (8), 1122-1125 (1987).

