En aptamer-baserad sensor för Unchelated gadolinium (III)
Summary
The use of polydeoxynucleotide (44-mer aptamer) molecules for sensing unchelated gadolinium(III) ion in an aqueous solution is described. The presence of the ion is detected via an increase in the fluorescence emission of the sensor.
Abstract
A method for determining the presence of unchelated trivalent gadolinium ion (Gd3+) in aqueous solution is demonstrated. Gd3+ is often present in samples of gadolinium-based contrast agents as a result of incomplete reactions between the ligand and the ion, or as a dissociation product. Since the ion is toxic, its detection is of critical importance. Herein, the design and usage of an aptamer-based sensor (Gd-sensor) for Gd3+ are described. The sensor produces a fluorescence change in response to increasing concentrations of the ion, and has a limit of detection in the nanomolar range (~100 nM with a signal-to-noise ratio of 3). The assay may be run in an aqueous buffer at ambient pH (~7 – 7.4) in a 384-well microplate. The sensor is relatively unreactive toward other physiologically relevant metal ions such as sodium, potassium, and calcium ions, although it is not specific for Gd3+ over other trivalent lanthanides such as europium(III) and terbium(III). Nevertheless, the lanthanides are not commonly found in contrast agents or the biological systems, and the sensor may therefore be used to selectively determine unchelated Gd3+ in aqueous conditions.
Introduction
Den ökande betydelsen av magnetisk resonanstomografi (MRT) i klinisk diagnos, som begränsas av den inneboende känsligheten av tekniken, har resulterat i den snabba tillväxten av forskning om utveckling av nya gadoliniumbaserade baserade kontrastmedel (GBCAs) 1. GBCAs är molekyler som administreras för att förbättra bildkvaliteten, och de har typiskt den kemiska strukturen hos en trevärd gadolinium jon (Gd 3+) koordinerad till en flertandad ligand. Denna komplex är av avgörande betydelse som unchelated Gd 3+ är giftig; Det har varit inblandad i utvecklingen av nefrogen systemisk fibros hos vissa patienter med njursjukdom eller fel 2. Följaktligen detektera vatten fria jonen är avgörande för att garantera säkerheten för GBCAs. Närvaron av unchelated Gd 3+ i GBCA lösningar ofta är resultatet av en ofullständig reaktion mellan liganden och den jon, dissociering av komplexet, eller displacement av andra biologiska metallkatjoner 3.
Bland de flera tekniker som för närvarande används för att bestämma närvaron av Gd 3+, som förlitar sig på kromatografi och / eller spektrometri rang störst när det gäller mångsidighet och användbarhet 4. Bland deras styrka är hög känslighet och noggrannhet, förmågan att analysera olika provmatriser (inklusive humanserum 5, urin och hår 6, avloppsvatten 7, och kontrastmedel formuleringar 8), och den samtidiga kvantifieringen av flera Gd 3+ komplex (en lista studier före 2013 beskrivs i en omfattande översyn av Telgmann et al.) 4. Den enda nackdelen är att flera av dessa metoder kräver instrumentering (såsom induktivt kopplad plasma-masspektrometri) 4 att vissa laboratorier inte kan få tillgång till. Inom ramen för nya GBCA upptäckt på forskning och proof-of-concept nivåer, arelatively mer praktiskt, snabbare och kostnadseffektiv spektroskopiska baserad metod (såsom UV-Vis absorption eller fluorescens) kan tjäna som ett värdefullt alternativ. Med dessa program i åtanke, var en fluorescerande aptamer-baserad sensor för vatten Gd 3+ utvecklats 9.
Den aptamer (Gd-aptamer) är en 44-baser lång enkelsträngad DNA-molekyl med en specifik sekvens av baser som isolerades genom processen systematisk utveckling av ligander genom exponentiell anrikning (SELEX) 9. Att anpassa aptamer till ett fluorescerande sensor, är en fluorofor fäst till 5'-terminalen av strängen, som sedan hybridiseras med en utsläckande strängen (QS) via 13 komplementära baser (figur 1). QS är märkt med en mörk släckningsmolekyl vid 3-terminalen. I frånvaro av Gd 3+, sensorn (Gd-sensor), bestående av en 1: 2 molförhållande av Gd-aptamer och QS respektive, kommer att ha minimal fluorescens-emission på grund av to energiöverföring från fluoroforen till släckare. Tillsättning av vattenhaltig Gd 3+ kommer förskjuta QS från Gd-aptamer, vilket resulterar i en ökning av fluorescensemission.
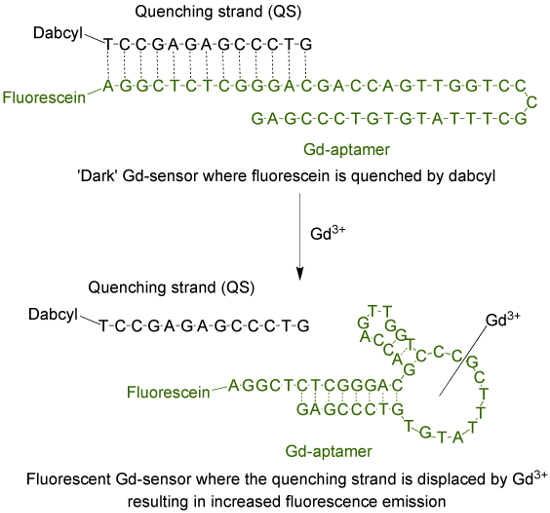
Figur 1. Sensorn (Gd-sensor) som består av 44-baser lång aptamer (Gd-aptamer) taggade med fluorescein (en fluorofor) och 13-baser lång släckning strand (QS) taggade med DABCYL (en mörk släckare) . I frånvaro av unchelated Gd 3+, är fluorescensen hos sensorn minimal. Med tillsats av Gd 3+, inträffar förskjutning av QS och en ökning i fluorescensemission observeras. Klicka här för att se en större version av denna siffra.
Det finns för närvarande ett vanligt förekommande spektroskopiska-baserad metod för att upptäckaing vattenhaltig Gd 3+. Denna analys använder molekylen xylenolorange, som undergår en förskjutning i den maximala absorptionsvåglängden 433-573 nm vid kelatering till jonen 10. Förhållandet mellan dessa två absorbansmaxima kan användas för att kvantifiera mängden unchelated Gd 3+. Den aptamer sensorn är ett alternativ (kan även vara ett komplement) till xylenolorange analysen, eftersom de två metoderna har olika reaktionsbetingelser (såsom pH och sammansättningen av buffertlösningar som används), mål selektiviteter, linjära intervall av kvantifiering, och detekterings formerna 9.
Protocol
Representative Results
Discussion
Med hjälp av aptamer-baserade Gd-sensor, en ökning av fluorescensemission som är proportionell mot koncentrationen av unchelated Gd 3+ observeras. Att minimera mängden använt prov kan analysen köras i en 384-brunnars mikroplatta med en total provvolym av 45 | il per brunn. I denna design, var valet av fluorescein (FAM) och DABCYL (Dab) huvudsakligen baserade på kostnaden för reagenser, att ändra emissionsvåglängd, en annan parning av fluorofor och quencher kan användas 11.
<p class=…Disclosures
The authors have nothing to disclose.
Acknowledgements
We would like to gratefully acknowledge Dr. Milan N Stojanovic from Columbia University, New York, NY for valuable scientific input. This work is supported by funding from the California State University East Bay (CSUEB) and the CSUEB Faculty Support Grant-Individual Researcher. O.E., T.C., and A.L. were supported by the CSUEB Center for Student Research (CSR) Fellowship.
Materials
| Gd-aptamer | IDTDNA | Input sequence and fluorophore modification in the order form | A fluorophore with a different emission wavelength may be used. The aptamer may also be ordered from another company. |
| Quenching strand | IDTDNA | Input sequence and quencher modification in the order form | A different quencher for optimal energy transfer from the fluorophore may be used. The aptamer may also be ordered from another company. |
| Molecular biology grade water | No specific manufacturer, both DEPC or non-DEPC treated work equally well | ||
| Gadolinium(III) chloride anhydrous | Strem | 936416 | Toxic |
| HEPES | Fisher Scientific | BP310-500 | |
| Magnesium chloride anhydrous | MP Biomedicals | 0520984480 – 100 g | |
| Sodium Chloride | Acros Organics | 327300025 | |
| Potassium chloride | Fisher Scientific | P333-500 | |
| Sodium hydroxide, pellets | Fisher Scientific | BP359 | Corrosive |
| Hydrochloric acid | Fisher Scientific | SA49 | Toxic and corrosive |
| 384-well low flange black flat bottom polystyrene NBS plates | Corning | 3575 | Plates which are suitable for fluorescence reading are required. |
| Nalgene Rapid-Flow sterile disposable bottle top filter | Thermo Scientific | 5680020 | The bottle top is fitted with 0.2 micron PES membrane |
| Disposable sterile bottles 250 mL | Corning | 430281 | A larger or smaller bottle may be used |
| 1.5 mL microcentrifuge tubes | No specific manufacturer, as long as they are DNAse and RNAse-free | ||
| 0.2 mL PCR tubes | No specific manufacturer, as long as they are DNAse and RNAse-free | ||
| Micropipets | No specific manufacturer | ||
| Pipet tips (non filter) of appropriate sizes | No specific manufacturer, as long as they are DNAse and RNAse-free | ||
| Name of Equipment | |||
| Plate reader | Biotek Synergy H1 | Plate readers from other manufacturers would work equally well |
References
- Shen, C., New, E. J. Promising strategies for Gd-based responsive magnetic resonance imaging contrast agents. Curr. Opin. Chem. Biol. 17 (2), 158-166 (2013).
- Cheong, B. Y. C., Muthupillai, R. Nephrogenic systemic fibrosis: a concise review for cardiologists. Tex. Heart Inst. J. 37 (5), 508-515 (2010).
- Hao, D., Ai, T., Goerner, F., Hu, X., Runge, V. M., Tweedle, M. MRI contrast agents: basic chemistry and safety. J Magn. Reson. Imaging. 36 (5), 1060-1071 (2012).
- Telgmann, L., Sperling, M., Karst, U. Determination of gadolinium-based MRI contrast agents in biological and environmental samples: a review. Anal. Chim. Acta. 764, 1-16 (2013).
- Frenzel, T., Lengsfeld, P., Schirmer, H., Hütter, J., Weinmann, H. -. J. Stability of gadolinium-based magnetic resonance imaging contrast agents in human serum at 37 degrees C. Invest. Radiol. 43 (12), 817-828 (2008).
- Loreti, V., Bettmer, J. Determination of the MRI contrast agent Gd-DTPA by SEC-ICP-MS. Anal. Bioanal. Chem. 379 (7), 1050-1054 (2004).
- Telgmann, L., et al. Speciation and isotope dilution analysis of gadolinium-based contrast agents in wastewater. Environ. Sci. Technol. 46 (21), 11929-11936 (2012).
- Cleveland, D., et al. Chromatographic methods for the quantification of free and chelated gadolinium species in MRI contrast agent formulations. Anal. Bioanal. Chem. 398 (7), 2987-2995 (2010).
- Edogun, O., Nguyen, N. H., Halim, M. Fluorescent single-stranded DNA-based assay for detecting unchelated gadolinium(III) ions in aqueous solution. Anal. Bioanal. Chem. 408 (15), 4121-4131 (2016).
- Barge, A., Cravotto, G., Gianolio, E., Fedeli, F. How to determine free Gd and free ligand in solution of Gd chelates. A technical note. Contrast Med. Mol. Imaging. 1 (5), 184-188 (2006).
- Johansson, M. K. Choosing reporter-quencher pairs for efficient quenching through formation of intramolecular dimers. Methods Mol. Biol. 335, 17-29 (2006).
- Sherry, A. D., Caravan, P., Lenkinski, R. E. A primer on gadolinium chemistry. J. Magn. Reson. Imaging. 30 (6), 1240-1248 (2009).
- Shakhverdov, T. A. A cross-relaxation mechanism of fluorescence quenching in complexes of lanthanide ions with organic ligands. Opt. Spectrosc. 95 (4), 571-580 (2003).
- Brittain, H. G. Submicrogram determination of lanthanides through quenching of calcein blue fluorescence. Anal. Chem. 59 (8), 1122-1125 (1987).

