Fase gedrag van geladen blaasjes onder voorwaarden van symmetrische en asymmetrische oplossing bewaakt met fluorescentie microscopie
Summary
Experimenten op fase gescheiden reus unilamellar blaasjes (GUVs) worden vaak verwaarloosd fysiologische oplossing voorwaarden. Dit werk presenteert benaderingen om te bestuderen van het effect van hoge-zoutgehalte buffer op vloeistof-vloeistof fasenscheiding in geladen multicomponent GUVs als een functie van trans-membraan oplossing asymmetrie en temperatuur.
Abstract
Giant unilamellar fase gescheiden blaasjes (GUVs) exposeren naast vloeistof-besteld en vloeistof-ontregelde domeinen zijn een gemeenschappelijke biofysische instrument te onderzoeken van de lipide vlot hypothese. Tal van studies, verwaarlozing echter de gevolgen van fysiologische oplossing. Op die account presenteert het huidige werk het effect van hoge-zoutgehalte buffer en trans-membraan asymmetrie van de oplossing op vloeistof-vloeistof fase-separatie zichtbaar in de geladen GUVs gegroeid uit dioleylphosphatidylglycerol, ei sphingomyelinase en cholesterol. De effecten werden bestudeerd onder isotherme en wisselende temperaturen.
We beschrijven apparatuur en experimentele strategieën die van toepassing zijn voor het toezicht op de stabiliteit van naast elkaar bestaande vloeibare domeinen in geladen blaasjes onder voorwaarden van symmetrische en asymmetrische high-zoutgehalte oplossing. Het gaat hierbij om een aanpak te bereiden geladen multicomponent GUVs in hoog-zoutgehalte buffer bij hoge temperaturen. Het protocol houdt in dat de optie voor het uitvoeren van een gedeeltelijke uitwisseling van de externe oplossing voor een eenvoudige verdunning stap terwijl het minimaliseren van het vesikel verdunning. Een alternatieve benadering wordt gepresenteerd met behulp van een microfluidic apparaat waarmee de uitwisseling van een volledige externe oplossing. De gevolgen van de oplossing voor fase-separatie zichtbaar werden ook bestudeerd onder wisselende temperaturen. Te dien einde presenteren we het basisontwerp en de nut van een in-house ingebouwde temperatuur controle kamer. Bovendien, we nadenken over de beoordeling van de GUV fase staat, valkuilen is gekoppeld en hoe het om deze te omzeilen.
Introduction
Sinds de waarneming van micron middelgrote domeinen in vloeistof-vloeistof fase gescheiden reus unilamellar blaasjes (GUVs) door fluorescentie microscopie, zijn GUVs gebruikt als een modelsysteem te onderzoeken van de lipide vlot hypothese1,2 , 3 . Het gebied van hun vrijstaande dubbelgelaagde ligt in het bereik dat uit biologische cellen, zijn ze geschikt Nabootsers van plasma membranen met de hypothetische vlotten. Talrijke studies over dergelijke GUVs zijn uitgevoerd met blaasjes gedispergeerd in zuiver water, sacharose of lage-zoutgehalte oplossingen4,5,6,7,8. Deze voorwaarden, maar komen niet overeen met fysiologisch relevante blootstelling van biomembranen aan hoge-zoutgehalte omgevingen en trans-membraan oplossing asymmetrie zoals de voorwaarden voor de cellen zijn.
In dit werk en in een eerdere publicatie van onze groep9, werden de Staten van de fase van geladen multicomponent GUVs onderzocht als een functie van de aanwezigheid van zout en oplossing asymmetrie in het membraan. GUVs waren bereid uit mengsels van verschillende verhoudingen van dioleoylphosphatidylglycerol (DOPG), ei sphingomyelinase (eSM) en cholesterol (Chol) in sacharoseoplossing (met osmolariteit van 210 mOsm/kg) of high-zoutgehalte buffer (100 mM NaCl, 10 mM Tris, pH 7.5, 210 mOsm/kg). De keuze van het lipide werd gerechtvaardigd door de gegevens reeds verkregen op het fasediagram van dit mengsel6,8.
Een aantal methoden voor de bereiding van GUVs zijn beschikbaar in de literatuur10,11,12 (merk op dat hier, zullen we niet overwegen die overdracht van lipiden van een olie-gebaseerde naar een waterige fase waarbij 13 , 14 vanwege het inherente gevaar van de resterende olie residuen in het membraan die gevolgen voor de fase-gedrag hebben kunnen). De voorbereiding van GUVs in hoog-zoutgehalte buffer wordt geassocieerd met specifieke uitdagingen. Voor oplossingen van lage Ionische sterkte presenteert de electroformation methode15,16 een snelle manier om te GUVs bereiden in hoge opbrengsten met kleine gebreken10,17. De methode is gebaseerd op een laag van lipiden storten op een geleidende oppervlak (de elektrode), drogen ze en hydraterende hen met een waterige oplossing tijdens het toepassen van een AC-veld. Deze methode vereist echter aanpassingen als zout is aanwezig in de waterige oplossing18,19. Het is ervan uitgegaan dat de drijvende kracht voor vesikel groei door electroformation electroosmosis16 , die op hoge geleidbaarheid20wordt belemmerd. Vandaar, electroswelling van GUVs in hoog-zoutgehalte oplossingen is niet een eenvoudige aanpak als het optimalisatie voor verschillende zout concentraties aanwezig in de zwelling oplossing vereist. Gel-bijgewoonde vesikel zwelling21,22 is een potentiële alternatief voor electroformation met snellere tijden van de vorming. Deze aanpak is gebaseerd op de verbeterde lipide film hydratatie wanneer een gel (agarose of polyvinylalcohol (PVA)) wordt gebruikt als substraat. Deze benaderingen, is echter voorzien van het risico van besmetting van de membraan in het geval van agarose gebaseerde zwelling23 en/of temperatuur grenzen zoals in het geval van PVA gebaseerde zwelling. Ook is een protocol bij het groeien van de GUVs op een substraat van cellulose papier gevestigde24onlangs geweest. Algemene onderwerpen van deze methode zijn het gebrek aan controle over de zuiverheid van het substraat en het gebruik van grote hoeveelheden van lipide. In dit werk, zullen wij introduceren en presenteren van de voordelen van de meest traditionele methode GUV voorbereiding, namelijk de spontane zwelling methode25,26. Het bestaat uit een lipide laag op een substraat van de lipophobic, het in waterdamp sfeer en latere zwelling in de gewenste zwelling oplossing hydraterende drogen (Zie Figuur 1 en details in de sectie Protocol). Deze methode biedt geen controle over de grootteverdeling blaasje en leidt over het algemeen kleinere blaasjes in vergelijking met de methoden waar de productie wordt bijgestaan door elektrisch veld, polymeer substraat of microfluidic betekent. Echter is de vesikel kwaliteit en grootte geschikt voor de behandeling van de membraan fase staat als onderzocht hier.
Creëren van asymmetrie tussen de oplossingen in het membraan van het vesikel wordt geassocieerd met bepaalde uitdagingen zo goed. Een veel gebruikte aanpak is de directe verdunning van het vesikel suspensie in de gewenste externe oplossing27,28. Echter, dit vermindert ook de dichtheid van het vesikel distributie. Een andere strategie is te langzaam wisselen de externe oplossing rond GUVs vestigden zich aan de onderkant van een stroom-cel waarmee voor oplossing in – en outflux. Om te voorkomen dat storend of zelfs verliezen de blaasjes met de stroom, zijn lage stroomsnelheid toegepaste8, waardoor deze aanpak tijd-inefficiënt. Bovendien garandeert geen van deze benaderingen volledige externe oplossing uitwisseling. Een voor de hand liggende oplossing is om te immobiliseren blaasjes om te voorkomen dat verliezen ze tijdens een externe oplossing uitwisseling. Biotinyleerd GUVs kan bijvoorbeeld worden aangebonden op een streptavidine-gecoate oppervlak29. Echter, deze aanpak kan leiden tot compositorische variaties op de zelfklevend en vandaar de niet-naleving membraan segmenten30,31. De toepassing van magnetische of elektrische velden wilt overlappen blaasjes resultaten in het opleggen van membraan spanning32. Optisch pincet te vangen een blaasje in dienst vereist hebbend een handvat gekoppeld (dat wil zeggen een kraal), terwijl het gebruik van optische brancards lokale verwarming33kan betrekken. Overlapping van GUVs kan ook worden bereikt door een groeiende hen op platina draden zonder definitieve detachement34. Dit levert echter blaasjes die niet geïsoleerd zijn en die zijn meestal verbonden met de draden of andere blaasjes door dunne lipide buizen (aanbinden).
Het gepresenteerde werk hoogtepunten strategieën om de bovengenoemde beperkingen te overwinnen. Eerst presenteren wij een gedetailleerde beschrijving van de spontane zwelling methode aangepast en geoptimaliseerd voor de productie van GUVs in hoog-zoutgehalte buffers. Daarna introduceren we twee benaderingen efficiënt asymmetrische oplossing om voorwaarden te scheppen door eenvoudige verdunning of het gebruik van een microfluidic apparaat. Want ons doel de analyse van de stand van de membraan-fase van GUVs in verschillende oplossing omstandigheden is, in de daaropvolgende paragrafen criteria voor succesvolle statistische analyse en huidige hints voor het vermijden van valse categorisatie.
De analyses werden uitgevoerd onder isotherme voorwaarden en onder wisselende temperaturen. Terwijl de temperatuur control is vaak werkzaam, details over experimentele temperatuur-controle kamers zijn zelden beschreven. Hier, wordt een in-house gebouwde setup GUVs bij verschillende temperaturen worden nageleefd gepresenteerd.
Protocol
Representative Results
Discussion
Succesvolle productie van GUVs voor fase staat waarnemingen voorwaarden symmetrische en asymmetrische high-zoutgehalte
De protocollen die hier gepresenteerd introduceert een strategie te beoordelen van de invloed van hoge-zoutgehalte buffer en oplossing asymmetrie op de membraan fase staat van geladen GUVs over een brede waaier van composities. Een van de belangrijkste uitdagingen bij de verwezenlijking van dit doel was de productie van geladen GUVs in hoog-zoutgehalte buffers.
Wij met succes geproduceerd GUVs in sacharoseoplossing en hoge-zoutoplossing buffer door een eenvoudige spontane zwelling benadering, waarin een stap pre hydratatie van de gedeponeerde lipide-film en een overnachting definitieve hydratatie voor vesikel groei. Het is belangrijk op te merken dat de lipide-afzetting op een geruwd PTFE plaat om ervoor te zorgen zelfs lipide verspreiden gebeuren moet zodanig dat deze unilamellar blaasjes. Bovendien is het essentieel om elke stap uitvoeren tijdens het blaasje voorbereiding bij een temperatuur waar het lipide-film bevindt zich in een homogeen en vloeibare fase staat. Anders, kan de vesikel bevolking worden polydisperse in samenstelling en bias van de bevolking van de laatste fase staat analyse. Het specifieke protocol voor de spontane zwelling van de opbrengsten van GUVs een blaasje klomp die aan de ene kant de mogelijkheid biedt om resuspendeer het in kleine hoeveelheden te verkrijgen hooggeconcentreerde vesikel dispersies, en aan de andere kant biedt asymmetrische oplossing voorwaarden over het membraan terwijl het minimaliseren van de verdunning van blaasjes8,28. Het is essentieel dat tijdens vesikel verdunning of externe oplossing wisselen, binnen en buiten osmolarities gecompenseerde blijven morfologie wijzigingen veroorzaakt door osmolariteit incongruenties kunnen veroorzaken of voorkomen van Lo + Ld fase scheiding41 of, in geval van hypotone voorwaarden, kan leiden tot het blaasje barst.
Hier, resulteerden pogingen te optimaliseren electroformation protocollen in hoge-zoutgehalte oplossing in de productie van geen GUVs terwijl PVA-bijgewoonde zwelling multilamellar blaasjes leverde. Hoewel het vereist langere bereidingstijden en resultaten in vesikel batches van lagere kwaliteit10,17, de succesvolle productie van geladen blaasjes door spontane zwelling wordt geleverd met extra voordelen. Het vereist minimale inspanning tijdens het resulterend in voldoende opbrengsten voor statistische batch analyses en in tegenstelling tot electroformation, geen geavanceerde apparatuur of optimalisatie nodig waren. Bovendien zijn geen verontreinigingen door oxidatie van lipiden waargenomen42,43. Volgens de literatuur zijn er geen verschillen tussen de lipide-composities van blaasjes en de bijbehorende bestanden waaruit ze7,17waren gegroeid. Anderzijds wordt de vesikel vorming op een substraat van PTFE niet gevraagd de opneming van alle verontreinigingen in tegenstelling tot gel-bijgewoonde zwelling methoden waar vreemde moleculen kunnen worden ingevoerd door de substraat-23. Electroformation wordt geleverd met verdere nadelen aan buitensporige vesikel verdunning gerelateerde bij het maken van asymmetrische oplossing voorwaarden. GUVs geproduceerd door electroformation zijn meestal aanwezig als een homogene dispersie (in tegenstelling tot de opschorting van de sterk geconcentreerde blaasje in de vorm van een klomp gevormd tijdens spontane zwelling). Enigerlei verdunning van de externe oplossing zou aanzienlijk het aantal blaasjes ook verdunnen. Bovendien, in de loop van dit werk die werd naar voren gebracht dat DOPG/eSM/Chol GUVs geproduceerd door electroformation in sacharose werd unstable als verdund in hoge-zoutgehalte buffer. Fluorescentie van lipide patches op het microscoopglaasje aangegeven dat blaasjes voordat hun visuele inspectie mogelijk was zou barsten. Dergelijke instabiliteit kan worden toegeschreven aan de spanning van een verhoogde membraan van blaasjes voorbereid door electroformation in vergelijking met die welke zijn verkregen door spontane zwelling10.
Hoewel de vesikel verdunning een gemakkelijke en snelle aanpak asymmetrische GUV oplossing voorwaarden te scheppen is, het slechts een deeloplossing externe uitwisseling, zij het in een hoge fractie volbrengt (hier: 95%, Figuur 2), zoals bij verdunning, sporen van de zwelling van de oplossing zal blijven. De keuze van de mate van de uitwisseling van de externe oplossing is een trade-off tussen pipetteren omhoog het blaasje klomp samen met de zwelling oplossing (sectie 2) en niet de verdunning van het te veel. Vandaar, introduceerden we een benadering van de alternatieve microfluidic elders besproken in detail37 , dat voorziet in een snelle en volledige externe oplossing uitwisseling tijdens GUV fase staat waarnemingen om te controleren of de fase staat opmerkingen voor verdund blaasjes. De opmerkingen van fase staat varianten bij de overgang van symmetrische naar asymmetrische oplossing voorwaarden werden ook opgemerkt eens te zijn. Bovendien, beide methoden voor het genereren van asymmetrische oplossing voorwaarden weergegeven hier zijn relatief snel (vergelijk Ref.8) en komen met geen bekende risico’s van lokale samenstelling (vergelijk verwijzingen30,31), wijzigingen toename van spanning van de membraan (vergelijk referentie32), of lokale verwarming (vergelijk referentie33), wat betreft de alternatieve methoden besproken in de inleiding. Tijdens het microfluidic vangen is een osmotische evenwicht tussen het blaasje interieur en exterieur niet alleen essentieel voor het vermijden van fase staat artefacten zoals hierboven vermeld, maar ook deflatie veroorzaakt door hypertonic oplossing voorwaarden kan de gevangen GUVs te glijden door de posten na een externe oplossing uitwisseling.
Hoewel spontane zwelling met succes toegepast is om te groeien ongeladen blaasjes van een DOPC/eSM/Chol systeem, in andere gevallen, het ontbreken van kosten kunnen afbreuk doen aan GUV zwelling als gevolg van het daaruit voortvloeiende gebrek aan repulsion tussen de individuele bilayers44 . Vooraf zwelling verlenging of in te voeren omvangrijk lipide headgroups kan deze kwestie45tegengaan. Bovendien is het blaasje stabiliteit na hun verdunning in oplossingen anders dan die van zwelling afwijken voor verschillende lipide composities en verdunning media, die we hier niet hebben onderzocht. We hebben ook niet onderzocht de mogelijkheid van de gemiddelde diameter van de GUV afstemmen met de voorbereiding methode hier gepresenteerd. Maar parameters zoals vesikel samenstelling en zwelling oplossing zijn waarschijnlijk om de resultaten te beïnvloeden. De toepassing van alternatieve methoden46 grotere blaasjes voor de lipiden en de oplossingen die hier gebruikt kan opleveren, maar ze kunnen komen met andere nadelen die is gekoppeld aan de methode. De hierboven beschreven aanpak voor de productie van GUVs in symmetrische en asymmetrische high-zoutgehalte voorwaarden biedt een potentieel instrument voor verdere studies van blaasjes samengesteld uit verschillende lipide composities en verspreid in verschillende media. Zoals wij die mogelijkheden niet onderzocht, zal de toekomstige studies tonen hoe in het algemeen de GUV voorbereiding en verdunning methoden kunnen worden toegepast.
Observatie van fase-separatie zichtbaar bij wisselende temperaturen
Er bestaan verschillende experimentele opstellingen geschikt om te studeren van GUVs bij wisselende temperaturen. Terwijl deze opstellingen niet vaak in detail binnen de literatuur beschreven zijn, presenteert het huidige werk een fundamentele vergadering die van toepassing zijn voor dergelijke studies.
_content “> Controlemetingen laten zien dat de temperatuur van dit intern ontworpen en gebouwd kamer juist wordt bestuurd door een thermostaat en temperatuurgradiënten binnen de kamer binnen de experimentele temperatuur resolutie. Wordt gewaarborgd dat de experimentele thermische omstandigheden met de lezing van de thermostaat stroken.
Tijdens de beoordeling van GUV fase Staten over een breed temperatuurbereik is het belangrijk dat de waargenomen blaasjes goed zijn geëquilibreerd nadat de temperatuur is veranderd. Een mogelijke manier om ervoor te zorgen dit is te controleren voor hysteresis. Als hysteresis aanwezig is, de temperatuur stappen moeten worden verlaagd en/of evenwichtsinstelling keer verhoogd. Als de temperatuur controle in dit werk komt tot stand door een thermostaat op basis van water, het bereik van temperaturen werken is idealiter beperkt tot 0 – 100 ° C. Dit bereik kan worden uitgebreid met behulp van andere temperatuur controle vloeistoffen zoals olie of door gebruik te maken van andere opstellingen, bijv een Peltier apparaat. In de praktijk wordt de werktemperatuur ook beperkt door mogelijke condensatie of verdamping. Bovendien, voor temperaturen ver weg van de kamertemperatuur wordt het vóórkomen van een steady-state temperatuur verloop in de zaal van de observatie meer kans. Ook kan de beeldvormende apparatuur bij extreme temperaturen worden geschaad. Voor typische temperatuurbereiken geschikt voor lipide vesikel studies (~ 10-50 ° C7,9) schade aan de observatie apparatuur mag worden beschouwd, maar is meestal niet te verwachten.
Vesikel domein observatie artefacten
Er zijn een aantal bronnen voor observatie artefacten met behulp van breed-gebied fluorescentie microscopie. Allereerst moet men zich ervan bewust dat de maximale resolutie r van het object toegepast voor de visuele inspectie van vesikel fase Staten wordt bepaald door de detectiegrens van lipide domeinen volgens:
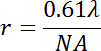
waar λ de golflengte van de emissie is, en NA is het numerieke diafragma van de doelstelling. Een typische doelstelling met een 40 x vergroting en een nb voor 0.6 die groene uitstoot detecteert licht ongeveer 560 nm zou bereiken een optische resolutie van ~0.6 µm. Vandaar, studies die blaasjes gemaakt van bepaalde lipide mengsels tussen verschillende staten fase vergelijken voorwaarden gebruik dezelfde doelstelling voor het dezelfde lipide-mengsel.
Een ander artefact is het voorkomen van lipide domeinen als gevolg van lipide-foto-oxidatie als gevolg van een langdurige blootstelling aan excitatie lichte41. Foto-schade optreedt bij voorkeur op onverzadigde koolwaterstof lipide wordt. In feite, voor sommige lipide-composities, zo’n domein vorming van aanvankelijk homogene blaasjes werd waargenomen hier na een langdurige periode van excitatie blootstelling aan licht (~ 30 s). Ter bestrijding van deze kwestie, de excitatie-licht bleef gericht op één gezichtsveld voor slechts een paar seconden voor de fase staat beoordeling. Vandaar, DiIC18 was geschikt voor onze doeleinden. Andere kleurstoffen, echter kunnen veel gevoeliger en wellicht kunnen worden gehanteerd bij lagere excitatie intensiteiten en kortere excitatie lichte blootstelling tijden.
Mechanische schuifspanning uit de overdracht van de Pipet van de blaasjes mixen mogelijk domeinen tijdelijk, waardoor de schijnbare vesikel fase gedrag verstoren. Voor sommige partijen, verschillende blaasjes toonde verschillende fase gedrag 0 min en 5 min na Pipetteer overbrengen naar de Microscoop dekglaasje aan. De schuifspanning geïnduceerd door de vloeistof stroom in het microfluidic-apparaat is ook aangetoond dat resulteren in domein47mengen. Blaasjes moeten voor een voldoende hoeveelheid tijd voor de equilibratietijd voor observatie ongemoeid gelaten worden. Binnen deze studie waren blaasjes gevangen op het microfluidic apparaat voor 1 h ongemoeid gelaten na vesikel laden en oplossing uitwisselingen voor observatie.
Om te voorkomen dat sommige van de bovengenoemde problemen, alsmede de beperkingen die zijn opgelegd door de lichte diffractie limiet, alternatieve methoden zoals nucleaire magnetische resonantie spectroscopie48 of super resolutie microscopie technieken49 kan worden ingezet.
Conclusie en vooruitzichten
Het gepresenteerde werk toont een aantal methoden waarmee voor de analyse van de invloed van de hoge zoutgehalte symmetrische en asymmetrische oplossing voorwaarden op membraan fase-separatie zichtbaar. Alle van de gepresenteerde methoden zijn geschikt voor andere toepassingen. Het microfluidic-apparaat biedt bijvoorbeeld een platform om te bestuderen van de kinetiek van domein vorming en verdwijnen bij de inductie van asymmetrie van de oplossing. Ook domein uiterlijk als functie van de zoutconcentratie kan worden bestudeerd die manier. Alle methodes kunnen ook worden gebruikt om te kijken naar de invloed op het gedrag van de fase met behulp van een andere oplossingen van belang.
Disclosures
The authors have nothing to disclose.
Acknowledgements
Dit werk is onderdeel van het MaxSynBio consortium, dat gezamenlijk wordt gefinancierd door het federale ministerie van onderwijs en onderzoek van Duitsland en de Max-Planck-Gesellschaft.
Materials
| 1,2-dioleoyl-sn-glycero-3-phospho-(1'-rac-glycerol), sodium salt | Avanti Polar Lipids | 840475C | abbreviated as DOPG in the text |
| chicken egg sphingomyelin | Avanti Polar Lipids | 860061 | abbreviated as eSM |
| cholesterol (ovine wool, > 98 %) | Avanti Polar Lipids | 700000 | abbreviated as Chol |
| 1,1'-dioctadecyl-3,3,3',3'-tetramethylindocarbocyanine perchlorate | Molecular Probes | D-282 | abbreviated as DiIC18 |
| Chloroform, HPLC grade (≥ 99.8 %) | Merck | ||
| NaCl (> 99.8 %) | Roth | ||
| HCl (37 %) | Roth | ||
| Tris (≥ 99.9 %) | Roth | ||
| Sucrose (≥ 99.5 %) | Sigma Aldrich | ||
| Parafilm | |||
| Threaded vial 45×27 mm, 15 mL | Kimble | Soda flat bottom, white screw cap | |
| pH meter | Mettler Toledo | MP220 | |
| Osmometer | Gonotec | Osmomat030 | |
| Epi-fluorescence microscope | Zeiss | Axio Observer D1 | |
| Confocal laser scanning microscope | Leica | TCS SP5 | |
| Objective 40x, 0.6 NA | Zeiss | LD Achroplan | |
| Objective 40x, 0.75 NA | Leica | 506174 | |
| Objective 63x, 0.9 NA | Leica | 506148 | |
| Microscope slide, 56×26 mm, 0.17 ± 0.01 mm | Menzel-Gläser | ||
| Cover slip, 22×22 mm, 0.17 ± 0.01 mm | Menzel-Gläaser | ||
| Parafilm "M" | Bremix Flexible Packaging | ||
| Syringes, 5 mL, 10 mL | Braun | ||
| 0.45 µm syringe filter | GVS North America | Cameo 25AS, 1213723 | Acetate, sterile |
References
- Dietrich, C., et al. Lipid rafts reconstituted in model membranes. Biophys J. 80 (3), 1417-1428 (2001).
- Bagatolli, L. A. To see or not to see: lateral organization of biological membranes and fluorescence microscopy. Biochim Biophys Acta. 1758 (10), 1541-1556 (2006).
- Carquin, M., D’Auria, L., Pollet, H., Bongarzone, E. R., Tyteca, D. Recent progress on lipid lateral heterogeneity in plasma membranes: From rafts to submicrometric domains. Prog Lipid Res. 62, 1-24 (2016).
- Baumgart, T., Hess, S. T., Webb, W. W. Imaging coexisting fluid domains in biomembrane models coupling curvature and line tension. Nature. 425 (6960), 821-824 (2003).
- Bacia, K., Schwille, P., Kurzchalia, T. Sterol structure determines the separation of phases and the curvature of the liquid-ordered phase in model membranes. Proc Natl Acad Sci U S A. 102 (9), 3272-3277 (2005).
- Vequi-Suplicy, C. C., Riske, K. A., Knorr, R. L., Dimova, R. Vesicles with charged domains. Biochim Biophys Acta. 1798 (7), 1338-1347 (2010).
- Blosser, M. C., Starr, J. B., Turtle, C. W., Ashcraft, J., Keller, S. L. Minimal effect of lipid charge on membrane miscibility phase behavior in three ternary systems. Biophys J. 104 (12), 2629-2638 (2013).
- Pataraia, S., Liu, Y., Lipowsky, R., Dimova, R. Effect of cytochrome c on the phase behavior of charged multicomponent lipid membranes. Biochim Biophys Acta. 1838 (8), 2036-2045 (2014).
- Kubsch, B., Robinson, T., Lipowsky, R., Dimova, R. Solution Asymmetry and Salt Expand Fluid-Fluid Coexistence Regions of Charged Membranes. Biophys J. 110 (12), 2581-2584 (2016).
- Dimova, R., et al. A practical guide to giant vesicles. Probing the membrane nanoregime via optical microscopy. J Phys Condens Matter. 18 (28), S1151-S1176 (2006).
- Liu, A. P., Fletcher, D. A. Biology under construction: in vitro reconstitution of cellular function. Nat Rev Mol Cell Biol. 10 (9), 644-650 (2009).
- Walde, P., Cosentino, K., Engel, H., Stano, P. Giant Vesicles: Preparations and Applications. Chembiochem. 11 (7), 848-865 (2010).
- van Swaay, D., deMello, A. Microfluidic methods for forming liposomes. Lab Chip. 13 (5), 752-767 (2013).
- Stein, H., Spindler, S., Bonakdar, N., Wang, C., Sandoghdar, V. Production of Isolated Giant Unilamellar Vesicles under High Salt Concentrations. Front Physiol. 8, 63 (2017).
- Angelova, M. I., Dimitrov, D. S. Liposome Electroformation. Faraday Discuss. 81, 303-311 (1986).
- Dimitrov, D. S., Angelova, M. I. Lipid swelling and liposome formation mediated by electric fields. Bioelectrochemistry and Bioenergetics. 19, 323-336 (1988).
- Rodriguez, N., Pincet, F., Cribier, S. Giant vesicles formed by gentle hydration and electroformation: a comparison by fluorescence microscopy. Colloids Surf B Biointerfaces. 42 (2), 125-130 (2005).
- Montes, L. R., Alonso, A., Goni, F. M., Bagatolli, L. A. Giant unilamellar vesicles electroformed from native membranes and organic lipid mixtures under physiological conditions. Biophys J. 93 (10), 3548-3554 (2007).
- Pott, T., Bouvrais, H., Meleard, P. Giant unilamellar vesicle formation under physiologically relevant conditions. Chem Phys Lipids. 154 (2), 115-119 (2008).
- Green, N. G., Ramos, A., Gonzalez, A., Morgan, H., Castellanos, A. Fluid flow induced by nonuniform ac electric fields in electrolytes on microelectrodes. I. Experimental measurements. Phys Rev E Stat Phys Plasmas Fluids Relat Interdiscip Topics. 61 (4 Pt B), 4011-4018 (2000).
- Horger, K. S., Estes, D. J., Capone, R., Mayer, M. Films of Agarose Enable Rapid Formation of Giant Liposomes in Solutions of Physiologic Ionic Strength. J Am Chem Soc. 131 (5), 1810-1819 (2009).
- Weinberger, A., et al. Gel-Assisted Formation of Giant Unilamellar Vesicles. Biophys J. 105 (1), 154-164 (2013).
- Lira, R. B., Dimova, R., Riske, K. A. Giant Unilamellar Vesicles Formed by Hybrid Films of Agarose and Lipids Display Altered Mechanical Properties. Biophys J. 107 (7), 1609-1619 (2014).
- Kresse, K. M., Xu, M., Pazzi, J., Garcia-Ojeda, M., Subramaniam, A. B. Novel Application of Cellulose Paper As a Platform for the Macromolecular Self-Assembly of Biomimetic Giant Liposomes. ACS Appl Mater Interfaces. 8 (47), 32102-32107 (2016).
- Reeves, J. P., Dowben, R. M. Formation and properties of thin-walled phospholipid vesicles. J Cell Physiol. 73 (1), 49-60 (1969).
- Needham, D., Evans, E. Structure and Mechanical-Properties of Giant Lipid (DMPC) Vesicle Bilayers from 20-Degrees-C Below to 10-Degrees-C above the Liquid-Crystal Crystalline Phase-Transition at 24-Degrees-C. 생화학. 27 (21), 8261-8269 (1988).
- Manneville, J. B., et al. COPI coat assembly occurs on liquid-disordered domains and the associated membrane deformations are limited by membrane tension. Proc Natl Acad Sci U S A. 105 (44), 16946-16951 (2008).
- Wollert, T., Wunder, C., Lippincott-Schwartz, J., Hurley, J. H. Membrane scission by the ESCRT-III complex. Nature. 458 (7235), 172 (2009).
- Kuhn, P., et al. A facile protocol for the immobilisation of vesicles, virus particles, bacteria, and yeast cells. Integr Biol (Camb). 4 (12), 1550-1555 (2012).
- Sarmento, M. J., Prieto, M., Fernandes, F. Reorganization of lipid domain distribution in giant unilamellar vesicles upon immobilization with different membrane tethers. Biochim Biophys Acta. 1818 (11), 2605-2615 (2012).
- Lipowsky, R., Rouhiparkouhi, T., Discher, D. E., Weikl, T. R. Domain formation in cholesterol-phospholipid membranes exposed to adhesive surfaces or environments. Soft Matter. 9 (35), 8438 (2013).
- Korlach, J., Reichle, C., Muller, T., Schnelle, T., Webb, W. W. Trapping, deformation, and rotation of giant unilamellar vesicles in octode dielectrophoretic field cages. Biophys J. 89 (1), 554-562 (2005).
- Delabre, U., et al. Deformation of phospholipid vesicles in an optical stretcher. Soft Matter. 11 (30), 6075-6088 (2015).
- Fidorra, M., Garcia, A., Ipsen, J. H., Hartel, S., Bagatolli, L. A. Lipid domains in giant unilamellar vesicles and their correspondence with equilibrium thermodynamic phases: a quantitative fluorescence microscopy imaging approach. Biochim Biophys Acta. 1788 (10), 2142-2149 (2009).
- Bezlyepkina, N., Gracia, R. S., Shchelokovskyy, P., Lipowsky, R., Dimova, R. Phase diagram and tie-line determination for the ternary mixture DOPC/eSM/cholesterol. Biophys J. 104 (7), 1456-1464 (2013).
- Eyer, K., Kuhn, P., Stratz, S., Dittrich, P. S. A microfluidic chip for the versatile chemical analysis of single cells. J Vis Exp. (80), e50618 (2013).
- Robinson, T., Kuhn, P., Eyer, K., Dittrich, P. S. Microfluidic trapping of giant unilamellar vesicles to study transport through a membrane pore. Biomicrofluidics. 7 (4), 44105 (2013).
- Veatch, S. L., Gawrisch, K., Keller, S. L. Closed-loop miscibility gap and quantitative tie-lines in ternary membranes containing diphytanoyl PC. Biophys J. 90 (12), 4428-4436 (2006).
- Kolesinska, B., et al. Interaction of beta(3) /beta(2) -peptides, consisting of Val-Ala-Leu segments, with POPC giant unilamellar vesicles (GUVs) and white blood cancer cells (U937)–a new type of cell-penetrating peptides, and a surprising chain-length dependence of their vesicle- and cell-lysing activity. Chem Biodivers. 12 (5), 697-732 (2015).
- Robinson, T., et al. Removal of background signals from fluorescence thermometry measurements in PDMS microchannels using fluorescence lifetime imaging. Lab Chip. 9 (23), 3437-3441 (2009).
- Morales-Penningston, N. F., et al. GUV preparation and imaging: minimizing artifacts. Biochim Biophys Acta. 1798 (7), 1324-1332 (2010).
- Zhou, Y., Berry, C. K., Storer, P. A., Raphael, R. M. Peroxidation of polyunsaturated phosphatidyl-choline lipids during electroformation. Biomaterials. 28 (6), 1298-1306 (2007).
- Breton, M., Amirkavei, M., Mir, L. M. Optimization of the Electroformation of Giant Unilamellar Vesicles (GUVs) with Unsaturated Phospholipids. J Membr Biol. 248 (5), 827-835 (2015).
- Lasic, D. D., Needham, D. The “stealth” liposome: a prototypical biomaterial. Chemical Reviews. 95, 2601-2628 (1995).
- Needham, D., McIntosh, T. J., Lasic, D. D. Repulsive interactions and mechanical stability of polymer-grafted lipid membranes. Biochim Biophys Acta. 1108 (1), 40-48 (1992).
- Akashi, K., Miyata, H., Itoh, H., Kinosita, K. Preparation of giant liposomes in physiological conditions and their characterization under an optical microscope. Biophys J. 71 (6), 3242-3250 (1996).
- Sturzenegger, F., Robinson, T., Hess, D., Dittrich, P. S. Membranes under shear stress: visualization of non-equilibrium domain patterns and domain fusion in a microfluidic device. Soft Matter. 12 (23), 5072-5076 (2016).
- Veatch, S. L., Polozov, I. V., Gawrisch, K., Keller, S. L. Liquid domains in vesicles investigated by NMR and fluorescence microscopy. Biophys J. 86 (5), 2910-2922 (2004).
- Owen, D. M., Magenau, A., Williamson, D., Gaus, K. The lipid raft hypothesis revisited–new insights on raft composition and function from super-resolution fluorescence microscopy. Bioessays. 34 (9), 739-747 (2012).

