체 외에 대사 시 토 크롬 P450s에 의해 니트로의 Nitrosamide 형성을 탐지 하기 위한 일반적인 방법
Summary
시 토 크롬 P450s에 의해 발암 성 니트로의 α-hydroxylation는 돌연변이 일으키는 원인이 되는 DNA 손상 중간체 생산 허용된 신진 대사 통로. 그러나, 새 데이터 나타냅니다 nitrosamides 산화 추가 발생할 수 있습니다. 우리는 일반 설명 nitrosamides을 탐지 하기 위한 방법 체 외에서 시 토 크롬 P450 촉매의 물질 대사 니트로에서 생산.
Abstract
N-니트로 시 토 크롬 P450 산화 전시 활동을 요구 하는 환경 발암 물질의 기초가 튼튼한 그룹. 대사 활성화의 허용된 메커니즘 저절로 DNA alkylating 에이전트를 분해 하는 α-hydroxynitrosamines의 대형을 포함 한다. DNA 손상의 결과 돌연변이 축적 궁극적으로 암으로 이어질 수 있습니다. 새로운 증거는 α-hydroxynitrosamines 수 수 추가 산화 nitrosamides에 processively 시 토 크롬 P450s에 의해 나타냅니다. Nitrosamides α-hydroxynitrosamines 보다 일반적으로 더 안정 하 고 또한 DNA를 알 수 있습니다, 때문에 nitrosamides 발암에 역할을 재생할 수 있습니다. 이 보고서에서 우리는 니트로의 생체 외에서 시 토 크롬 P450 촉매 물질 대사에서 nitrosamide 생산을 평가 하기 위한 일반 프로토콜을 설명 합니다. 이 프로토콜 관련 nitrosamides 및 생체 외에서 시 토 크롬 P450 물질 대사 분석 결과 검색에 대 한 액체 착 색 인쇄기-nanospray 이온화 높은 해상도 탠덤 질량 분석을 사용 하 여 합성 하는 일반적인 접근 방식을 활용 합니다. 이 방법은 n ′-예제 연구에서 nitrosonornicotine의 작은 대사 산물으로 n ′-nitrosonorcotinine를 감지. 메서드는 높은 감도 및 선택적으로 인해 정확한 대량 검출. 다양 한 nitrosamine-시 토 크롬 P450 시스템에이 방법의 응용이이 변환의 일반 성을 결정 하는 데 도움이 됩니다. 시 토 크롬 P450s 다형성을 활동에서 변화 하기 때문에 개별 암 위험 평가에 도움이 수 nitrosamide 대형의 더 나은 이해.
Introduction
N-니트로 사 민 다이어트, 담배 제품 및 일반 환경;에 있는 발암 물질의 큰 클래스는 1인체에서를 endogenously 형성 수 있습니다 또한. 이상의 300 N-nitroso 화합물 테스트 및 > 90%에서 발암 성 평가 했다 동물 모델2,3. 그들의 성에 전시, 먼저이 화합물 시 토 크롬 P450s1,,23에 의해 작동 한다. 연구는 시 토 크롬 P450s 쉽게 산화 α-hydroxynitrosamines (그림 1)는 ~ 5의 반감기와 반응성이 매우 높은 화합물에 니트로 자발적으로 alkyldiazohydroxides를 분해 하기 전에 s. 후자는 H2O N2의 손실 후에 DNA을 알 수 있습니다. 결과 DNA adducts unrepaired, 암 개발1이어질 중요 onco-또는 종양 억제기 유전자는 돌연변이 일으킬 수 있습니다. 이러한 이유로, 많은 노력 변화 통로의 완전 한 이해를 얻으려고 소비 되어, DNA adducts, 그리고 발암 성 니트로의 시 토 크롬 P450 산화의 다운스트림 대사 산물. 이 지식에 개별 암 위험 평가4잠재적인 응용 프로그램 합니다.
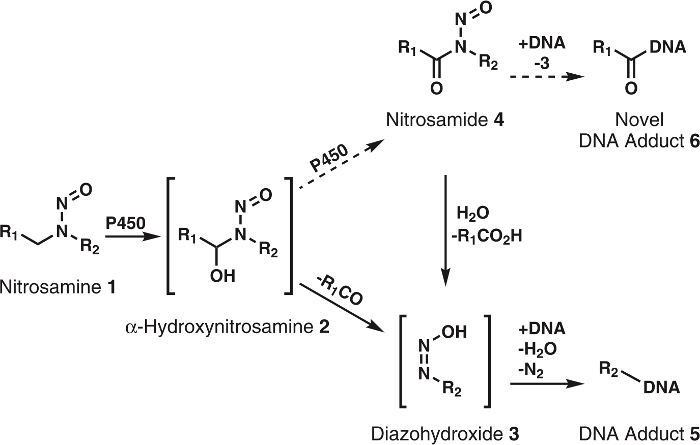
그림 1: 일반 및 니트로의 제안 된 대사.
(1) 니트로 P450s α-hydroxynitrosamines (2) 자발적으로 alkyldiazohydroxides (3)을 분해 하는에 산화 됩니다. 이러한 화합물 형태로 DNA adducts DNA에 바인딩할 수 있습니다. 그것을 가정 했다 그 2 는 nitrosamides 4P450s에 의해 더 산화 된다. 이러한 형태로 소설 DNA adducts 또는 3 알려진된 DNA adducts 형태로 분해 DNA에 직접 바인딩할 수 있습니다. R1 과 R2 알 킬 그룹을 나타냅니다. 이 그림의 더 큰 버전을 보려면 여기를 클릭 하십시오.
Α-hydroxynitrosamine 가설을 단단하게 광범위 한 데이터에 의해 지원 됩니다, 하지만 몇 가지 불일치;는 주요 것은 α-hydroxynitrosamines5,6의 짧은 반감기 이다. 이러한 화합물 바인딩과 그물 막에 생산 고 나중 핵 DNA를 알 알려져 있다. 몇 초 그들의 일생을 감안할 때, 그것은 어떻게 이러한 중간체 살아남을 필요한 여행 하지만 cytosol 수수께끼 이다. 하나의 가설은 이다 α-hydroxynitrosamines의 부분 산화 processively는 nitrosamides7,8, 비교9에서 매우 안정적입니다. 이것은 아마도 시 토 크롬 P450 활성 사이트에서 α-hydroxynitrosamines의 보존을 통해 발생 합니다. 산화의이 유형에 대 한 전례가 니코틴10, 알콜11, 그리고 간단한 alkylnitrosamines12,13보아 왔다. 또한, nitrosamides는 직접 연기 발암 물질2,3. 9그들의 반응 따라, 이러한 화합물 생산 DNA adducts 함께 새로운 α-hydroxynitrosamines에서 인 동일 하, 미개척된 DNA adducts (그림 1) 추정 된다. 따라서,이 가설 뿐만 아니라 설명 한다 cytosol, 통해 전송 하지만 또한 DNA의 형성 제품 손상.
이 문서에는 생체 외에서 시 토 크롬 P450 중재 변환 니트로의 nitrosamides 평가 하기 위한 일반 프로토콜을 설명 합니다. N ′-nitrosonorcotinine (NNC) 시 토 크롬 P450 2A6에 의해 n ′-nitrosonornicotine (NNN)의 이전에 보고 된 변환 예제14로 전시 됩니다. 다양 한 기질-효소 시스템에이 프로토콜의 응용 프로그램 전반적인 nitrosamine 대사 nitrosamides의 중요성을 결정 하는 데 도움이 됩니다.
Protocol
Representative Results
Discussion
니트로의 신진 대사를 elucidating 그들의 성에 이해 하는 중요 한 구성 요소입니다. 이기 때문에 관련 된 시 토 크롬 P450s와 다른 대사 효소 다형, 더욱이 지식을 응용 프로그램 식별할 수 있는 잠재적으로 위험이 높은 개인1,4. 새로운 데이터의 α-hydroxynitrosamines, DNA 바인딩에 관련 된 니트로의 추정된 주요 대사 산물을 더 산화, nitrosamides 하는 것은 가능 합?…
Disclosures
The authors have nothing to disclose.
Acknowledgements
이 연구 보조금에 의해 지원 되었다 아니. 캘리포니아-81301 국립 암 연구소에서. 우리 편집 지원에 대 한 칼 슨 밥, 박사 피터 Villalta 프리메이슨 암 센터의 분석 생화학 공유 리소스에서 질량 분석에 쉰 밍 박사 아담 T. Zarth 그리고 그들의 귀중 한 토론에 대 한 박사 안 나 공화국 미셸 감사 합니다. 그리고 입력. 분석 생화학 공유 리소스는 부분적으로 지원 하 여 국립 암 연구소 암 센터 지원 그랜트 CA-77598
Materials
| Norcotinine | AKoS GmbH (Steinen, Germany) | CAS 17708-87-1, AKoS AK0S006278969 | |
| Acetic acid | Sigma-Aldrich | 695092 | |
| Acetic Anhydride | Sigma-Aldrich | 242845 | |
| Ammonium Acetate | Sigma-Aldrich | 431311 | |
| Barium Hydroxide | Sigma-Aldrich | 433373 | |
| D-Chloroform | Sigma-Aldrich | 151823 | |
| HPLC Acetonitrile | Sigma-Aldrich | 34998 | |
| Magnesium Sulfate | Sigma-Aldrich | M7506 | |
| Methylene Chloride | Sigma-Aldrich | 34856 | |
| Sodium Nitrite | Sigma-Aldrich | 237213 | |
| ViVid CYP2A6 Blue Screening Kit | Life Technologies | PV6140 | |
| Zinc Sulfate | Sigma-Aldrich | 221376 | |
| 0.5 mL tubes | Fisher | AB0533 | |
| 100 mL round bottom flask | Sigma-Aldrich | Z510424 | |
| 125 mL Erlenmeyer flask | Sigma-Aldrich | CLS4980125 | |
| 125 mL Separatory Funnel | Sigma-Aldrich | Z261017 | |
| 25 mL round bottom flask | Sigma-Aldrich | Z278262 | |
| 500 MHz NMR Spectrometer | Bruker | ||
| Allegra X-22R Centrifuge | Beckman-Coulter | ||
| LC vials | ChromTech | CTC–0957–BOND | |
| LTQ Orbitrap Velos | Thermo Scientific | ||
| Magnetic Stir bar | Sigma-Aldrich | Z127035 | |
| NMR tube | Sigma-Aldrich | Z274682 | |
| P1000, P200, and P10 pipettes | Eppendorf | ||
| Rotary evaporator | Sigma-Aldrich | Z691410 | |
| RSLCnano UPLC system | Thermo Scientific | ||
| Shaking Water Bath | Fisher | FSSWB15 | |
| Stir plate | Sigma-Aldrich | CLS6795420 | |
| PicoFrit Column | New Objective | PF3607515N5 | |
| Luna C18, 5 um | Phenomenex | 535913-1 |
References
- Rom, W. N., Markowitz, S. . Environmental and Occupational Medicine. , 1226-1239 (2007).
- Preussmann, R., Stewart, B. W., Searle, C. E. . Chemical Carcinogens, ACS Monograph 182. 2, 643-828 (1984).
- Magee, P. N., Montesano, R., Preussmann, R., Searle, C. E. . Chemical Carcinogens. ACS monograph 173. , 491-625 (1976).
- Zhu, A. Z., et al. Alaska Native smokers and smokeless tobacco users with slower CYP2A6 activity have lower tobacco consumption, lower tobacco-specific nitrosamine exposure and lower tobacco-specific nitrosamine bioactivation. Carcinogenesis. 34 (1), 93-101 (2013).
- Mesić, M., Revis, C., Fishbein, J. C. Effects of structure on the reactivity of alpha-hydroxydialkynitrosamines in aqueous solutions. J. Am. Chem. Soc. 118, 7412-7413 (1996).
- Mochizuki, M., Anjo, T., Okada, M. Isolation and characterization of N-alkyl-N- (hydroxymethyl)nitrosamines from N-alkyl-N- (hydroperoxymethyl)nitrosamines by deoxygenation. Tetrahedron Lett. 21, 3693-3696 (1980).
- Guttenplan, J. B. Effects of cytosol on mutagenesis induced by N-nitrosodimethylamine, N-nitrosomethylurea and à-acetoxy-N-nitrosodimethylamine in different strains of Salmonella:evidence for different ultimate mutagens from N-nitrosodimethylmine. Carcinogenesis. 14, 1013-1019 (1993).
- Elespuru, R. K., Saavedra, J. E., Kovatch, R. M., Lijinsky, W. Examination of a-carbonyl derivatives of nitrosodimethylamine in ethylnitrosomethyamine as putative proximate carcinogens. Carcinogenesis. 14, 1189-1193 (1993).
- Chow, Y. L. . ACS Symposium Series. 101, 13-37 (1979).
- von Weymarn, L. B., Retzlaff, C., Murphy, S. E. CYP2A6- and CYP2A13-catalyzed metabolism of the nicotine delta5′(1′)iminium ion. J. Pharmacol. Exp. Ther. 343 (2), 307-315 (2012).
- Bell-Parikh, L. C., Guengerich, F. P. Kinetics of cytochrome P450 2E1-catalyzed oxidation of ethanol to acetic acid via acetaldehyde. J Biol Chem. 274 (34), 23833-23840 (1999).
- Chowdhury, G., Calcutt, M. W., Nagy, L. D., Guengerich, F. P. Oxidation of methyl and ethyl nitrosamines by cytochrome P450 2E1 and 2B1. 생화학. 51 (50), 9995-10007 (2012).
- Chowdhury, G., Calcutt, M. W., Guengerich, F. P. Oxidation of N-nitrosoalkylamines by human cytochrome P450 2A6: sequential oxidation to aldehydes and carboxylic acids and analysis of reaction steps. J Biol Chem. 285 (11), 8031-8044 (2010).
- Carlson, E. S., Upadhyaya, P., Hecht, S. S. Evaluation of nitrosamide formation in the cytochrome P450-mediated metabolism of tobacco-specific nitrosamines. Chem Res Toxicol. 29 (12), 2194-2205 (2016).
- Amin, S., Desai, D., Hecht, S. S., Hoffmann, D. Synthesis of tobacco-specific N-nitrosamines and their metabolites and results of related bioassays. Crit. Rev. Toxicol. 26, 139-147 (1996).
- Clark, A. G., Wong, S. T. A rapid chromatographic technique for the detection of dye-binding. Anal Biochem. 89 (2), 317-323 (1978).
- Pauli, G. F., et al. Importance of purity evaluation and the potential of quantitative (1)H NMR as a purity assay. J Med Chem. 57 (22), 9220-9231 (2014).
- van der Heeft, E., et al. A microcapillary column switching HPLC-electrospray ionization MS system for the direct identification of peptides presented by major histocompatibility complex class I molecules. Anal Chem. 70 (18), 3742-3751 (1998).
- White, E. H. The Chemistry of the N-Alkyl-N-nitrosoamides. I. Methods of Preparation. J. Am. Chem. Soc. 77, 6008-6010 (1955).
- Patten, C., et al. Evidence for cytochrome P450 2A6 and 3A4 as major catalysts for N’-nitrosonornicotine alpha-hydroxylation by human liver microsomes. Carcinogenesis. 18, 1623-1630 (1997).
- Wong, H. L., Murphy, S. E., Hecht, S. S. Cytochrome P450 2A-catalyzed metabolic activation of structurally similar carcinogenic nitrosamines: N’-nitrosonornicotine enantiomers, N-nitrosopiperidine, and N-nitrosopyrrolidine. Chem. Res. Toxicol. 18, 61-69 (2004).
- Hecht, S. S. Biochemistry, biology, and carcinogenicity of tobacco-specific N-nitrosamines. Chem. Res. Toxicol. 11, 559-603 (1998).
- von Weymarn, L. B., Zhang, Q. Y., Ding, X., Hollenberg, P. F. Effects of 8-methoxypsoralen on cytochrome P450 2A13. Carcinogenesis. 26 (3), 621-629 (2005).

