मानव प्रेरित Pluripotent स्टेम सेल में उप प्रकार-विशिष्ट ऑप्टिकल कार्रवाई संभावित रिकॉर्डिंग-व्युत्पंन वेंट्रिकुलर Cardiomyocytes
Summary
यहां हम ऑप्टिकली छवि कार्रवाई क्षमता के लिए एक विधि वर्तमान, वेंट्रिकुलर में विशेष रूप से प्रेरित pluripotent स्टेम सेल-व्युत्पंन cardiomyocytes की तरह । विधि प्रमोटर-एक वोल्टेज के प्रति संवेदनशील फ्लोरोसेंट प्रोटीन की अभिव्यक्ति संचालित पर आधारित है ।
Abstract
Cardiomyocytes मानव प्रेरित pluripotent स्टेम सेल से उत्पंन (iPSC-सीएमएस) हृदय अनुसंधान में एक उभरते उपकरण हैं । बजाय कोशिकाओं के एक समरूप जनसंख्या जा रहा है, iPSC-सीएमएस वर्तमान भिंनता प्रोटोकॉल द्वारा उत्पंन वेंट्रिकुलर के साथ कोशिकाओं का मिश्रण प्रतिनिधित्व करते हैं, अलिंद-, और phenotypes, जो phenotypic विश्लेषण पेचीदा की तरह नोडल । यहां, एक विधि से ऑप्टिकली रिकॉर्ड कार्रवाई संभावित वेंट्रिकुलर से विशेष रूप से iPSC-सीएमएस की तरह प्रस्तुत किया है । यह एक निर्माण जिसमें एक आनुवंशिक रूप से इनकोडिंग वोल्टेज सूचक एक वेंट्रिकुलर-विशिष्ट प्रमोटर तत्व के नियंत्रण में है के साथ lentiviral transduction द्वारा हासिल की है । जब iPSC-सीएमएस इस निर्माण के साथ transduced रहे हैं, वोल्टेज संवेदक विशेष रूप से वेंट्रिकुलर की तरह कोशिकाओं में व्यक्त की है, उपप्रकार-विशिष्ट ऑप्टिकल झिल्ली क्षमता समय चूक प्रतिदीप्ति माइक्रोस्कोपी का उपयोग कर रिकॉर्डिंग को सक्षम करने से ।
Introduction
Cardiomyocytes (सीएमएस) प्रेरित pluripotent स्टेम कोशिकाओं से व्युत्पंन (iPSCs) हृदय रोग के आणविक तंत्र काटना करने के लिए एक उभरते हुए उपकरण हैं, उपंयास उपचार की जांच करने के लिए, और प्रतिकूल कार्डियक दवा प्रभाव के लिए स्क्रीन1,2 ,3. शुरू से ही सही, channelopathies जैसे arrhythmogenic रोगों इस अनुसंधान क्षेत्र का एक महत्वपूर्ण ध्यान दिया गया है4. नतीजतन, इस तरह के ताल विकारों या कार्रवाई संभावित (एपी) morphologies में परिवर्तन के रूप में सीएमएस के विद्युत phenotypes की जांच करने के लिए तरीके, इस प्रौद्योगिकी के दिल में हैं ।
iPSC के आवेदन में एक महत्वपूर्ण विचार-सीएमएस है कि वर्तमान हृदय भेदभाव प्रोटोकॉल कोशिकाओं की एक समरूप जनसंख्या में परिणाम नहीं है । इसके बजाय, वे नहीं बल्कि परिपक्वता के विभिंन स्तरों पर साइनस नोड, अलिंद, और वेंट्रिकुलर सीएमएस जैसी कोशिकाओं का मिश्रण कर रहे है5,6,7,8। इस विविधता प्रयोगात्मक परिवर्तनशीलता के एक प्रासंगिक स्रोत है, खासकर अगर एपी अवधि (APD) के रूप में मानकों की जांच कर रहे हैं, जो आंतरिक रूप से सेमी उपप्रकार के बीच अलग हो सकता है (जैसे, APD अलिंद में वेंट्रिकुलर सेमी की तुलना में कम है) । पारंपरिक दृष्टिकोण इस समस्या का समाधान करने के लिए एक iPSC-सेमी पैच दबाना विधि का उपयोग कर की जांच करने के लिए और प्रत्येक कक्ष के रूप में वर्गीकृत करने के लिए नोडल-, अलिंद-, या वेंट्रिकुलर की तरह, अपनी एपी आकृति विज्ञान9पर आधारित है । इसके बाद किसी भी विश्लेषण के बाद ब्याज की सेमी उपप्रकार का प्रतिनिधित्व कोशिकाओं को प्रतिबंधित किया जा सकता है । इस रणनीति के प्रमुख दोष अपने सीमित प्रवाह और दरिद्रता की कमी है । इसके अलावा, पैच दबाना इलेक्ट्रोफिजियोलॉजी के इनवेसिव प्रकृति क्रमिक रूप से विस्तारित समय अवधि में एक ही कोशिकाओं के इमेजिंग की अनुमति नहीं है ।
यहां, हम एक विधि10 iPSC-सीएमएस के विशिष्ट उपप्रकार में ऑप्टिकली छवि ए पी एस के लिए विकसित पर प्रयोगात्मक विवरण प्रदान करते हैं । यह उपप्रकार विविधता की समस्या पर काबू पा और नाटकीय रूप से पारंपरिक तरीकों की तुलना में प्रवाह बढ़ जाती है, iPSC के तेजी से phenotyping-सीएमएस आनुवंशिक वेरिएंट ले जा रहा है या औषधीय एजेंटों को उजागर की अनुमति ।
उप-प्रकार-विशिष्ट ऑप्टिकल इमेजिंग approach का ओवरव्यू
एक आनुवंशिक रूप से इनकोडिंग वोल्टेज संकेतक (GEVI), जिसका प्रतिदीप्ति गुण ध्रुवीकरण और कोशिका झिल्ली के ध्रुवीकरण पर बदल, ऑप्टिकली सेमी की झिल्ली की क्षमता में परिवर्तन की छवि के लिए प्रयोग किया जाता है । यहां लागू GEVI वोल्टेज-संवेदन फ्लोरोसेंट प्रोटीन VSFP-सीआर11, जो एक वोल्टेज-संवेदन transmembrane एक जोड़ी से जुड़े डोमेन के होते है एक हरे (तिपतिया घास) और एक लाल (mRuby2) फ्लोरोसेंट प्रोटीन (आंकड़ा 1a) । दो fluorophores के करीब निकटता के कारण, उत्तेजना ऊर्जा का एक अंश में हरी फ्लोरोसेंट प्रोटीन परिणाम के उत्तेजना Förster अनुनाद ऊर्जा हस्तांतरण (झल्लाहट) के माध्यम से लाल फ्लोरोसेंट प्रोटीन को हस्तांतरित किया जा रहा है । इसलिए, हरे और लाल फ्लोरोसेंट प्रोटीन (आंकड़ा 1a, ऊपरी पैनल) दोनों से एक उत्सर्जन में हरी फ्लोरोसेंट प्रोटीन के परिणाम उत्तेजना । जब कोशिका के ध्रुवीकरण, वोल्टेज संवेदक के एक संरचनात्मक rearrangement होता है कि दो फ्लोरोसेंट प्रोटीन के एक अभिविन्यास में तब्दील हो, झल्लाहट दक्षता में वृद्धि. इस प्रकार, उत्तेजना ऊर्जा के और भी लाल फ्लोरोसेंट प्रोटीन (आंकड़ा 1a, निचले पैनल) के लिए हरी से स्थानांतरित कर रहा है । एक परिणाम के रूप में, एक विध्रुवीय कोशिका में, हरी प्रतिदीप्ति उत्सर्जन dimmer है, और लाल प्रतिदीप्ति उत्सर्जन में एक कोशिका की तुलना में उज्जवल है झिल्ली की क्षमता (आंकड़ा 1b) आराम कर रहा है ।
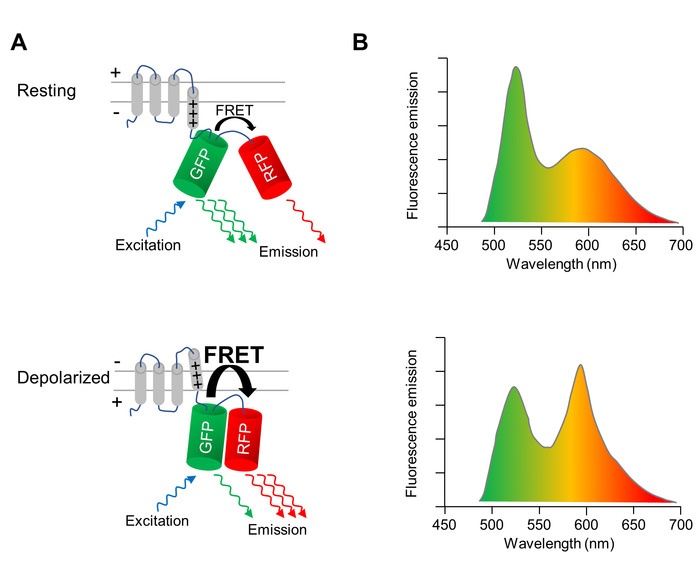
चित्रा 1: VSFP-सीआर के साथ झिल्ली क्षमता की ऑप्टिकल इमेजिंग । (क) एक योजनाबद्ध वोल्टेज की कार्रवाई के प्रति संवेदनशील फ्लोरोसेंट प्रोटीन VSFP-सीआर दर्शाया गया है । कोशिका झिल्ली के ध्रुवीकरण पर, वोल्टेज संवेदन transmembrane डोमेन में एक संरचनात्मक पुनर्स्थापन हरे (GFP) और लाल (आरएफपी) फ्लोरोसेंट प्रोटीन के एक अभिविन्यास में तब्दील हो, intramolecular Förster की क्षमता में वृद्धि अनुनाद ऊर्जा स्थानांतरण (झल्लाहट). (ख) शेष झिल्ली क्षमता (ऊपरी पैनल) में और विश्लेषित कोशिकाओं (निचले पैनल) में कोशिकाओं में GFP के उत्तेजना पर एक VSFP के उत्सर्जन स्पेक्ट्रा चित्रित कर रहे हैं । विध्रुवीकरण पर वर्णक्रमीय परिवर्तन स्पष्टता के लिए अतिरंजित है । कृपया यहां क्लिक करें इस आंकड़े का एक बड़ा संस्करण को देखने के लिए ।
झल्लाहट क्षमता में परिवर्तन झिल्ली क्षमता के उतार चढ़ाव मिरर एक प्रतिदीप्ति एक छवि अलगानेवाला है, जो लाल और हरे प्रतिदीप्ति उत्सर्जन अलग और उंहें दो आसंन क्षेत्रों पर परियोजनाओं के साथ सुसज्जित माइक्रोस्कोप का उपयोग कर imaged रहे है एक sCMOS कैमरा (चित्रा 2) की चिप । इस सेट अप के साथ, दो अलग तरंग दैर्ध्य बैंड पर प्रतिदीप्ति उत्सर्जन एक साथ दर्ज किया जा सकता है, जो एक समय चूक श्रृंखला के हर छवि में झिल्ली की क्षमता को प्रतिबिंबित करने के लिए लाल-से-हरे प्रतिदीप्ति के अनुपात की गणना की अनुमति देता है ।
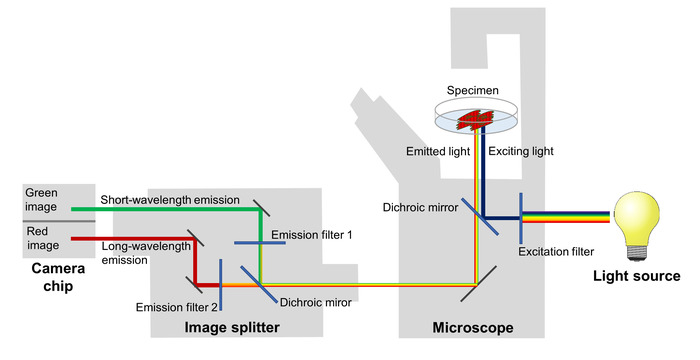
चित्र 2: इमेजिंग सिस्टम का कॉंफ़िगरेशन । इमेजिंग प्रणाली के प्रमुख घटकों को वोल्टेज के वर्णक्रमीय परिवर्तन के प्रति संवेदनशील फ्लोरोसेंट प्रोटीन एक उच्च लौकिक संकल्प पर झिल्ली संभावित परिवर्तन मिरर चित्रण किया जाता है । कृपया यहां क्लिक करें इस आंकड़े का एक बड़ा संस्करण को देखने के लिए ।
सीएमएस में VSFP-सीआर की अभिव्यक्ति lentiviral transduction ने हासिल की है. करने के लिए प्रत्यक्ष अभिव्यक्ति के लिए मुख्यमंत्री के उपप्रकार के हित, lentivirus एक प्रवर्तक तत्व ( MLC2v बढ़ाने) है कि विशेष रूप से वेंट्रिकुलर में प्रतिलेखन ड्राइव-iPSC की तरह-सीएमएस10शामिल हैं । जब iPSC-सीएमएस कि अलिंद की तरह, नोडल की तरह है, और वेंट्रिकुलर की तरह कोशिकाओं के मिश्रण का प्रतिनिधित्व इस lentivirus के साथ transduced हैं, VSFP-सीआर केवल वेंट्रिकुलर की तरह कोशिकाओं में व्यक्त की है । ऑप्टिकल कार्रवाई संभावित इमेजिंग के बाद से इस फ्लोरोसेंट संवेदक पर निर्भर करता है, दर्ज की गई कार्रवाई की क्षमता विशेष रूप से ब्याज की मुख्यमंत्री उपप्रकार का प्रतिनिधित्व (चित्रा 3) ।
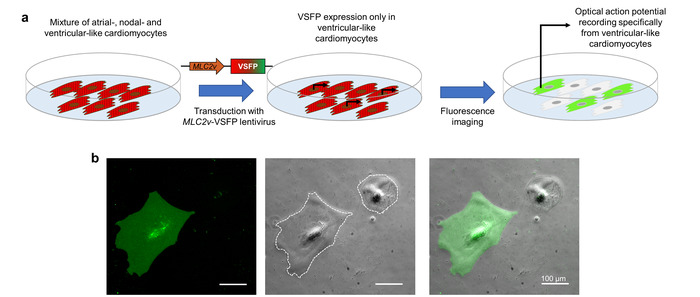
चित्र 3: उप-प्रकार-विशिष्ट झिल्ली संभावित इमेजिंग के लिए प्रवर्तक-चालित VSFP व्यंजक । (क) इस योजनाबद्ध कैसे cardiomyocyte उपप्रकार-विशिष्ट ऑप्टिकल कार्रवाई संभावित रिकॉर्डिंग प्राप्त कर रहे है दिखाता है । (ख) iPSC-सीएमएस वेंट्रिकुलर-विशिष्ट MLC2v-बढ़ाने के नियंत्रण में एक VSFP के साथ संक्रमित दिखाया गया है । वोल्टेज सेंसर की अभिव्यक्ति वेंट्रिकुलर में ही मनाया जाता है-GFP चैनल में सीएमएस की तरह (बाएँ पैनल). चरण कंट्रास्ट (मध्य पैनल) और ओवरले इमेज (दायां पैनल) भी दिए गए हैं । सफ़ेद डॉटेड रेखाएं कक्ष सीमाएं चिह्नित करतीं हैं । कृपया यहां क्लिक करें इस आंकड़े का एक बड़ा संस्करण को देखने के लिए ।
Protocol
Representative Results
Discussion
विधि यहां वर्णित एक विशिष्ट उप प्रकार से ए पी एस के एक ऑप्टिकल रिकॉर्डिंग (यानी, वेंट्रिकुलर कोशिकाओं की तरह) मानव iPSCs से उत्पंन सीएमएस के सक्षम बनाता है । मानव iPSC-सीएमएस एक उभरते उपकरण के लिए जैविक और च…
Disclosures
The authors have nothing to disclose.
Acknowledgements
यह काम जर्मन रिसर्च फाउंडेशन (एसआई 1747/1-1), और Kröner-Fresenius-Stiftung, और ड्यूश Stiftung फर Herzforschung से अनुदान द्वारा समर्थित किया गया था ।
Materials
| ß-Mercaptoethanol | Invitrogen | 21985023 | |
| DMEM-F12 Medium | Invitrogen | 21331046 | |
| FBS(Fetal Bovine Serum) | Invitrogen | 16141079 | |
| MEM Non-Essential Amino Acids | Invitrogen | 11140050 | |
| GlutaMax-I Supplement | Invitrogen | 35050061 | alternative L-Glutamine |
| Penicillin-Streptomycin | Invitrogen | 15140122 | |
| Fibronectin bovine plasma | Sigma-Aldrich | F1141 | |
| Collagenase type II | Worthington Biochem | LS004174 | |
| Hexadimethrine Bromide (Polybrene) | Sigma-Aldrich | H9268 | enhancing lentiviral infection |
| 3.5 cm glass-bottom microdishes | MatTek corporation, Ashland, MA, USA | P35G-1.5-14-C | |
| Microscope stand | Leica Microsystems, Wetzlar, Germany | DMI6000B | |
| Microscope objective | Leica Microsystems, Wetzlar, Germany | HCX PL APO 63x/1.4-0.6 Oil | |
| sCMOS camera | Andor Technology, Belfast, UK | Zyla V | |
| Microscope filter cube: excitation filter | Chroma Technology Corp, Bellows Falls, VT, USA | ET480/40X | bandpass 480/40 |
| Microscope filter cube: dichroic mirror | Chroma Technology Corp, Bellows Falls, VT, USA | T505lpxr | longpass 505 nm |
| Image splitter | Cairn Research, Faversham, UK | OptoSplit II | |
| Image splitter filter cube: dichroic mirror | AHF Analysentechnik GmbH, Tübigen, Germany | 568LPXR | longpass 568 nm |
| Image splitter filter cube: emission filter 1 (GFP emission) | AHF Analysentechnik GmbH, Tübigen, Germany | 520/28 BrightLine HC | bandpass 520/28 nm |
| Image splitter filter cube: emission filter 2 (RFP emission) | AHF Analysentechnik GmbH, Tübigen, Germany | 630/75 ET Bandpass | bandpass 630/75 nm |
| Pacing inset | Warner Instruments, Hamden, CT, USA | RC-37FS | |
References
- Sinnecker, D., Laugwitz, K. L., Moretti, A. Induced pluripotent stem cell-derived cardiomyocytes for drug development and toxicity testing. Pharmacology & Therapeutics. 143 (2), 246-252 (2014).
- Goedel, A., My, I., Sinnecker, D., Moretti, A. Perspectives and Challenges of Pluripotent Stem Cells in Cardiac Arrhythmia Research. Current Cardiology Reports. 19 (3), 23 (2017).
- Rocchetti, M., et al. Elucidating arrhythmogenic mechanisms of long-QT syndrome CALM1-F142L mutation in patient-specific induced pluripotent stem cell-derived cardiomyocytes. Cardiovascular Research. 113 (5), 531-541 (2017).
- Sinnecker, D., et al. Modeling long-QT syndromes with iPS cells. Journal of Cardiovascular Translational Research. 6 (1), 31-36 (2013).
- Talkhabi, M., Aghdami, N., Baharvand, H. Human cardiomyocyte generation from pluripotent stem cells: A state-of-art. Life Sciences. , 98-113 (2016).
- Ben-Ari, M., et al. Developmental changes in electrophysiological characteristics of human-induced pluripotent stem cell-derived cardiomyocytes. Heart Rhythm. 13 (12), 2379-2387 (2016).
- Den Hartogh, S. C., Passier, R. Concise Review: Fluorescent Reporters in Human Pluripotent Stem Cells: Contributions to Cardiac Differentiation and Their Applications in Cardiac Disease and Toxicity. Stem Cells. 34 (1), 13-26 (2016).
- Schweizer, P. A., et al. Subtype-specific differentiation of cardiac pacemaker cell clusters from human induced pluripotent stem cells. Stem Cell Research & Therapy. 8 (1), 229 (2017).
- Moretti, A., et al. Patient-specific induced pluripotent stem-cell models for long-QT syndrome. The New England Journal of Medicine. 363 (15), 1397-1409 (2010).
- Chen, Z., et al. Subtype-specific promoter-driven action potential imaging for precise disease modelling and drug testing in hiPSC-derived cardiomyocytes. European Heart Journal. 38 (4), 292-301 (2017).
- Lam, A. J., et al. Improving FRET dynamic range with bright green and red fluorescent proteins. Nature Methods. 9 (10), 1005-1012 (2012).
- Chen, G., et al. Chemically defined conditions for human iPSC derivation and culture. Nature Methods. 8 (5), 424-429 (2011).
- Burridge, P. W., et al. Chemically defined generation of human cardiomyocytes. Nature Methods. 11 (8), 855-860 (2014).
- Bhattacharya, S., et al. High efficiency differentiation of human pluripotent stem cells to cardiomyocytes and characterization by flow cytometry. Journal of Visualized Experiments. (91), e52010 (2014).
- Wang, X., McManus, M. Lentivirus production. Journal of Visualized Experiments. (32), e1499 (2009).
- Schneider, C. A., Rasband, W. S., Eliceiri, K. W. NIH Image to ImageJ: 25 years of image analysis. Nature Methods. 9 (7), 671-675 (2012).
- Schindelin, J., et al. Fiji: an open-source platform for biological-image analysis. Nature Methods. 9 (7), 676-682 (2012).
- Jung, C. B., et al. Dantrolene rescues arrhythmogenic RYR2 defect in a patient-specific stem cell model of catecholaminergic polymorphic ventricular tachycardia. EMBO Molecular Medicine. 4 (3), 180-191 (2012).
- Lemoine, M. D., et al. Human iPSC-derived cardiomyocytes cultured in 3D engineered heart tissue show physiological upstroke velocity and sodium current density. Scientific Reports. 7, 5464 (2017).
- Dorn, T., et al. Direct nkx2-5 transcriptional repression of isl1 controls cardiomyocyte subtype identity. Stem Cells. 33 (4), 1113-1129 (2015).
- Kaestner, L., et al. Genetically Encoded Voltage Indicators in Circulation Research. International Journal of Molecular Sciences. 16 (9), 21626-21642 (2015).

