Kalibratie-gratis In Vitro kwantificering van eiwit Homo-oligomerisatie met behulp van commerciële instrumentatie en Software van de analyse van de helderheid van gratis, Open Source
Summary
Dit protocol beschrijft een kalibratie-vrije aanpak voor het kwantificeren van eiwit homo-oligomerisatie in vitro op basis van fluctuatiemarges Fluorescentiespectroscopie met behulp van commerciële licht scanning microscopie. De juiste overname-instellingen en de analysemethoden worden weergegeven.
Abstract
Aantal en helderheid is een kalibratie-vrije fluorescentie schommelingen spectroscopie (FFS) techniek voor het opsporen van eiwit homo-oligomerisatie. Het kan worden gebruikt met behulp van een conventionele confocal microscoop uitgerust met digitale detectoren. Een protocol voor het gebruik van de techniek in vitro wordt weergegeven door middel van een use-case waar nummer en helderheid te nauwkeurig het kwantificeren van de oligomere Braziliaanse deelstaat mVenus-gelabelde FKBP12F36V voor en na de toevoeging van de dimerizing drug AP20187 kunnen worden gezien. Het belang van het gebruik van de juiste Microscoop verwerving parameters en de juiste gegevens voorbewerken en analysemethoden worden besproken. In het bijzonder wordt het belang van de keuze van photobleaching correctie benadrukt. Deze goedkope methode kan worden gebruikt om te studeren van eiwit-eiwitinteractie in veel biologische contexten.
Introduction
Eiwit-eiwit interacties Ik n Vitro
Traditioneel, zijn kristallografie en nucleaire magnetische resonantie experimenten in combinatie met cryo-elektronenmicroscopie (cryoEM) de technologieën gekozen om te nauwkeurig beschrijven de driedimensionale structuur van eiwitten en hun functie door afleiden onderzoekend hun structurele details in hoge resolutie. Eiwitten, echter zijn niet statisch structuren en een scala aan conformationele wijzigingen en trillingen kunnen ondergaan in tijd en ruimte. Daarom is het structurele informatie uit kristallografische of CryoEM gegevens moet worden aangevuld met andere technieken (bijvoorbeeld moleculaire dynamica simulaties en enkel molecuul technieken): de functie van een eiwit is gerelateerd aan de conformationele wijzigingen en interacties, en deze informatie is niet aanwezig in een statische-structuurdiagram. Om de sonde voor intra moleculaire dynamica, zijn technieken op basis van één molecuul Forster Resonance Energy Transfer (smFRET) zeer effectief1. Deze benaderingen zijn in staat om te beoordelen van verschillende subpopulaties van moleculen in complexe media. Dit is zeer belangrijk, aangezien deze veranderingen snelle zijn en tijdens de overname van de gegevens (dat wil zeggen, een nanoseconde naar tweede bereik optreden).
Twee van de belangrijkste benaderingen vaak werkzaam zijn voor het detecteren en kwantificeren van deze wijzigingen: eiwitten in oplossing en oppervlakte-immobilisatie. Voor de detectie van Inter moleculaire interacties en in het bijzonder, het proces van dimerisatie geïnduceerd door liganden, is smFRET niet altijd het beste instrument. Inderdaad, FRET niet alleen hangt af van de afstand (≈10 nm) maar ook op de oriëntatie van de twee dipolen (donor en acceptor, χ2) en de overlapping van de emissie van de donor met van de acceptor absorptiespectra2, maar misschien deze laatste voorwaarde is minder mits het Vejle kunt koos belangrijk de juiste FRET paar. Een bijzonder nadeel van smFRET voor het sonderen van homo-dimerisatie komt uit de etikettering van de proteïne van belang: voor hetero smFRET, dimerisatie kan alleen worden gedetecteerd tot 50% (dat wil zeggen, hetero-FRET zullen uitsluitend kundig voor speurder donor-acceptor en acceptor-donor homo-Dimeren maar niet donor-donor of acceptor-acceptor, die de overige 50% van de Dimeren). Het gebruik van fluorescentie correlatie spectroscopie (FCS) en derivaten (FCCS, etc.3) vast te stellen eiwit diffusie constanten en bindende constanten in vitro is een ander alternatief. Deze benaderingen zijn niet kundig voor homo-dimerisatie ofwel volledig te kwantificeren, zoals FCS één maatregelen concentratie en verspreiding, en de straal en diffusie coëfficiënt van een diffusing deeltje zijn zeer slecht afhankelijk van het molecuulgewicht; bijvoorbeeld zal een 10-fold verhoging van het molecuulgewicht alleen impliceren een verandering 2.15 vouwen in de diffusie coëfficiënt4. In het geval van twee kleuren FCS of FCCS, zal slechts 50% van de homo-Dimeren blijken om dezelfde reden als hierboven. De meest praktische en kwantitatieve benaderingen voor het detecteren van homo-dimerisatie in vitro en in vivo zijn homo-FRET5 en nummer en helderheid (N & B)6. Gezien het feit dat homo-FRET vereist specifieke instrumentatie herstel van de anisotropie waarde (bijvoorbeeld optische elementen/analysers om te herstellen van de parallelle en loodrechte polarisatie), N & B wordt gepresenteerd als een gunstige techniek om hier het detecteren van eiwitten homo-dimerisatie en aggregatie. Het kan worden gebruikt zowel in vitro als in vivo met een commerciële set-up.
Aantal en helderheid
N & B is onlangs herziene7. Die herziening gericht op de toepassing van de techniek in levende cellen. Het is de moeite waard om te reproduceren het wiskundig formalisme hier als deze vergelijkingen worden toegepast op de gegevens verzameld in vitro. Eerste plaats is het noodzakelijk om enkele voorwaarden en wiskundige hoeveelheden te definiëren:
- Een entiteit is een verzameling van moleculen die met elkaar zijn verbonden.
- De helderheid ε van een entiteit is het aantal fotonen die het stoot per tijdseenheid (per frame).
- n is het aantal entiteiten aanwezig.
- Voor een bepaalde pixel in de loop van een beeld-serie is dat zijn gemiddelde intensiteit en σ2 is de afwijking in de intensiteit.
Vervolgens met het foton tellen detectoren en uitgaande mobiele entiteiten en geen achtergrond,
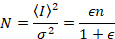
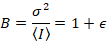
waarbij N staat voor het schijnbare aantal en B is de schijnbare helderheid. Dit resulteert in
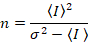
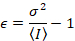
Dalal et al. 8 bleek dat met analoge apparatuur, drie correctietermen moet: de S-factor, de verschuivingvan de achtergrond en de uitlezing lawaai σ0–2. Vervolgens, wederom ervan uitgaande dat mobiele entiteiten,
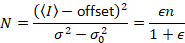
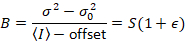
geven
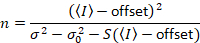
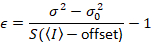
Merk op dat de bovenstaande vergelijking voor verschillende dat gegeven in Dalal et al. 8 en een latere toetsing. 7 in Dalal et al. de S in de noemer als gevolg van een typfout werd weggelaten en deze fout werd gereproduceerd in de review. De bovenstaande vergelijking is de juiste is. Instructies voor het meten van S, offset en σ02 – samen met een verklaring van hun betekenis – worden gegeven door Dalal et al. 8
De helderheid ε is evenredig aan de oligomere staat voor de diffusing entiteiten: ε zullen twee keer zo groot voor Dimeren als voor monomeren, driemaal zo groot voor trimeren als voor monomeren, tweemaal zo groot voor hexamers als voor trimeren, enzovoort. Op deze manier, meten de helderheid ε, kan een het kwantificeren van elk type multimerization.
Als er een mengsel van oligomere Staten aanwezig, nummer en helderheid is niet geschikt voor het herstellen van de individuele oligomere Staten aanwezig. Dit is een beperking van de techniek.
Detrend-algoritme en nandb software
Het belang van het corrigeren van photobleaching geweest eerder benadrukt9. Photobleaching onvermijdelijk optreedt tijdens de lichte microscopie van experimenten in time-lapse modus; zowel in levende cellen en in vitro. Vele benaderingen zijn beschreven in de literatuur om te corrigeren voor het bleken van7. De exponentiële filteringtechniek met automatische keuze van detrending parameter T is de huidige beste. Het is geïntegreerd in de gratis, open source software nandb9. Inderdaad, software die de gebruiker handmatig kiezen hun detrending parameter vereist kan leiden tot onjuiste resultaten omdat deze parameter keuze waarschijnlijk willekeurige en onjuist zullen. De automatische algoritme inspecteert de gegevens en de juiste parameter bepaalt, zonder de noodzaak voor gebruiker interventie9. Zelfs met de beste keuze van smoothing parameter, detrending heeft zijn beperkingen en werkt alleen goed met photobleaching percentages lager is dan 25%, zoals met simulaties9. Interessant is dat bij het gebruik van de automatische detrending routine, de juistheid ervan is zodanig dat men met lage helderheidswaarden werken kan (zelfs B < 1.01), en dus lage intensiteit, en nog steeds nauwkeurig genoeg om het kwantificeren van homo-dimerisatie.
Photobleaching veroorzaakt ook een ander probleem: de aanwezigheid van photobleached fluorophores in een complexe multimer. Dit maakt bijvoorbeeld een trimeer verschijnen als een dimeer wanneer één van de drie units in de trimeer is niet-belichting fluorescerende. Hur en Mueller10 toonde hoe te corrigeren voor dit en deze correctie werd ook benadrukt in een latere herziening7. De software van de nandb bevat deze correctie9.
De FKBP12 F36V systeem
FKBP12F36V is een proteïne die doet natuurlijk niet oligomerize, maar is bekend dat bij de toevoeging van de AP20187 drug (gemeenzaam bekend als de BB dimerizing ligand)11,12dimerize. Dit maakt het een ideale testcase voor nummer en helderheid: met gelabelde FKBP12F36V, een verdubbeling van de oligomere staat moet worden nageleefd bij toevoeging van BB.
Protocol
Representative Results
Discussion
N & B is een techniek voor het detecteren van multimerization met behulp van commerciële licht scannen confocal microscopen uitgerust met digitale detectoren. Deze aanpak is heel aantrekkelijk in vergelijking met aanspreekpunt FCS, FCCS en smFRET omdat het gratis kalibratie en de berekening van de helderheid is eenvoudig en concentratie onafhankelijke6. Het is van groot belang, echter om te corrigeren voor bleken en lange termijn intensiteit schommelingen voordat u helderheid berekeningen<sup cla…
Disclosures
The authors have nothing to disclose.
Acknowledgements
Dit werk werd ondersteund door de Wellcome Trust 105278/Z/14/2 toekennen R.N. De Wellcome Trust centrum voor menselijke erfelijkheid wordt gefinancierd door Wellcome Trust Core Award 203852/Z/16/2. Werk in de groep C.S. wordt ondersteund door het Cancer Research UK (C20724/A14414) en de European Research Council van de Europese Unie Horizon 2020 onderzoek en innovatie programma Grant 647278.
Materials
| RosettaTM (DE3) pLysS cells | Novagen | 70956-3 | |
| Ampicillin | Sigma Aldrich | PubChem Substance ID 329824407 | |
| Chloramphenicol | Sigma Aldrich | PubChem Substance ID: 24892250 | |
| LB starter culture | QIAGEN | ||
| LB medium | QIAGEN | https://www.sigmaaldrich.com/content/dam/sigma-aldrich/head/search/external-link-icon.gif | |
| IPTG | Sigma Aldrich | PubChem Substance ID 329815691 | |
| IMAC buffer | Medicago | 09-1010-10 | |
| EDTA-free protease inhibitors | Sigma Aldrich | 11873580001 | |
| TALON resin | Clonetech | ||
| Nickel sepharose | GE Healthcare | ||
| S200 16/60 column | GE Healthcare | ||
| Glass bottom 8 well observation dish | Ibidi | 80827 |
References
- Voith von Voithenberg, L., Lamb, D. C. Single pair forster resonance energy transfer: A versatile tool to investigate protein conformational dynamics. BioEssays. 40, (2018).
- Padilla-Parra, S., Auduge, N., Coppey-Moisan, M., Tramier, M. Quantitative FRET analysis by fast acquisition time domain FLIM at high spatial resolution in living cells. Biophysical Journal. 95, 2976-2988 (2008).
- Padilla-Parra, S., Auduge, N., Coppey-Moisan, M., Tramier, M. Dual-color fluorescence lifetime correlation spectroscopy to quantify protein-protein interactions in live cell. Microscopy Research and Technique. 74, 788-793 (2011).
- Muller, J. D., Chen, Y., Gratton, E. Fluorescence correlation spectroscopy. Methods in Enzymology. 361, 69-92 (2003).
- Tramier, M., Coppey-Moisan, M. Fluorescence anisotropy imaging microscopy for homo-FRET in living cells. Methods in Cell Biology. 85, 395-414 (2008).
- Digman, M. A., Dalal, R., Horwitz, A. F., Gratton, E. Mapping the number of molecules and brightness in the laser scanning microscope. Biophysical Journal. 94, 2320-2332 (2008).
- Nolan, R., Iliopoulou, M., Alvarez, L., Padilla-Parra, S. Detecting protein aggregation and interaction in live cells: A guide to number and brightness. Methods. , (2017).
- Dalal, R. B., Digman, M. A., Horwitz, A. F., Vetri, V., Gratton, E. Determination of particle number and brightness using a laser scanning confocal microscope operating in the analog mode. Microscopy Research and Technique. 71, 69-81 (2008).
- Nolan, R., et al. nandb-number and brightness in R with a novel automatic detrending algorithm. Bioinformatics. , (2017).
- Hur, K. H., et al. Quantitative Measurement of Brightness from Living Cells in the Presence of Photodepletion. PLoS One. 9, (2014).
- Amara, J. F., et al. A versatile synthetic dimerizer for the regulation of protein-protein interactions. Proceedings of the National Academy of Sciences of the United States of America. 94, 10618-10623 (1997).
- Clackson, T., et al. Redesigning an FKBP-ligand interface to generate chemical dimerizers with novel specificity. Proceedings of the National Academy of Sciences of the United States of America. 95, 10437-10442 (1998).
- Rollins, C. T., et al. A ligand-reversible dimerization system for controlling protein-protein interactions. Proceedings of the National Academy of Sciences of the United States of America. 97, 7096-7101 (2000).
- Schindelin, J., Rueden, C. T., Hiner, M. C., Eliceiri, K. W. The ImageJ ecosystem: An open platform for biomedical image analysis. Molecular Reproduction and Development. 82, 518-529 (2015).
- . R: A Language and Environment for Statistical Computing. R Core. , (2017).
- . RStudio: Integrated Development Environment for R. R Team. , (2016).
- . nandb R package Available from: https://CRAN.R-project.org/package=nandb (2017)
- Jung, G., Wiehler, J., Zumbusch, A. The photophysics of green fluorescent protein: influence of the key amino acids at positions 65, 203, and 222. Biophysical Journal. 88, 1932-1947 (2005).
- Shaner, N. C., Steinbach, P. A., Tsien, R. Y. A guide to choosing fluorescent proteins. Nature Methods. 2, 905-909 (2005).
- Butkevich, A. N., et al. Hydroxylated fluorescent dyes for live-cell labeling: synthesis, spectra and super-resolution STED. Chemistry: A European Journal. 23, 12114-12119 (2017).

