Protocolo clínico de producir fracción Vascular estromal derivadas de tejido adiposo para potencial regeneración del cartílago
Summary
Aquí, presentamos un protocolo para producir una fracción vascular estromal derivadas de tejido adiposo y su aplicación para mejorar las funciones de la rodilla mediante la regeneración de tejido similar al cartílago en pacientes humanos con osteoartritis.
Abstract
La osteoartritis (OA) es uno de los más comunes trastornos debilitantes. Recientemente, se hicieron numerosos intentos para mejorar las funciones de las rodillas utilizando diferentes formas de células madre mesenquimales (MSCs). En Corea, concentrados de médula y cordón de células madre procedentes de sangre han sido aprobadas por la administración de medicamentos (KFDA) Coreano para regeneración de cartílago. Además, se ha permitido una derivados del tejido adiposo stromal vascular fracción (SVF) por la KFDA para inyecciones conjuntas en pacientes humanos. SVF autóloga derivadas de tejido adiposo contiene matriz extracelular (ECM) además de las células madre mesenquimales. ECM excreta diferentes citoquinas que, junto con el ácido hialurónico (ah) y plasma rico en plaquetas (PRP) activado por el cloruro de calcio, pueden ayudar a MSCs para regenerar el cartílago y mejorar las funciones de la rodilla. En este artículo, presentamos un protocolo para mejorar las funciones de la rodilla mediante la regeneración de tejido similar al cartílago en pacientes humanos con OA. El resultado del protocolo primero fue divulgado en 2011 seguido por algunas publicaciones adicionales. El protocolo consiste en la liposucción para obtener lipoaspirates autólogo que se mezclan con colagenasa. Esta mezcla de lipoaspirates-colagenasa es luego y homogeneizada para quitar tejido fibroso grandes que puede obstruir la aguja durante la inyección. Luego, la mezcla se incuba para obtener SVF derivadas de tejido adiposo. El SVF resultante derivadas de tejido adiposo, que contienen derivados del tejido adiposo MSCs y restos de ECM, se inyecta en las rodillas de los pacientes, combinados con HA y cloruro de calcio activado PRP. Incluyen tres casos de pacientes que fueron tratados con el protocolo dando por resultado la mejora del dolor de la rodilla, hinchazón y rango de movimiento junto con evidencia de MRI de tejido similar al cartílago hialino.
Introduction
Las células madre mesenquimales (MSCs) se sabe que tienen la capacidad de regenerar cartílago1,2,3,4,5,6. Pueden ser fácilmente obtenidos de diversas fuentes: médula ósea, sangre del cordón umbilical y tejido adiposo entre muchos otros. Entre estas fuentes, el tejido adiposo es la única fuente donde se puede obtener un número suficiente de MSCs sin cualquier expansión de la cultura para la regeneración de cartílago en ajustes clínicos7,8. Fracción vascular estromal de médula ósea autóloga (SVF) puede obtenerse fácilmente así. Sin embargo, el número de células madre contenidas en la médula ampliada de cultura no es muy bajo7,8. Sangre del cordón umbilical puede contener un número suficiente de MSCs. Sin embargo, la sangre del cordón no es una fuente fácilmente disponible de SVF autólogo.
Existen numerosos métodos de procesamiento de tejido adiposo para obtener SVF para aplicaciones clínicas. Entre estos, el método de obtención de MSCs del tejido adiposo con colagenasa, desarrollado y confirmado por Zuk et al. 5 , 6, es muy bien aceptada. Este método de uso de colagenasa se ha modificado para usos clínicos en ortopedia. Para ser aplicado a contextos clínicos, el sistema debe ser un sistema cerrado para mantener la esterilidad, manteniendo la comodidad. Una modificación particular presentada en este artículo implica la homogeneización de la lipoaspirates. Lipoaspirates de tamaño pequeño son digeridos relativamente más rápido que los más grandes que están resultando en un desgaste irregular del tejido adiposo. Además, estos lipoaspirates de tamaño más grandes puede producir tejidos fibrosos que pueden obstruir las jeringas y agujas al realizar inyecciones conjuntas9,10. Para evitar estos problemas, el lipoaspirates puede ser homogeneizada mediante corte y trituración de la lipoaspirates antes de la incubación con colagenasa. El SVF resultante derivadas de tejido adiposo puede contener más uniforme matriz extracelular (ECM) en comparación con lipoaspirates que no están homogeneizadas11. El ECM averiado en el SVF puede funcionar como un andamio de12.
En 2009, SVF autóloga derivadas de tejido adiposo se ha permitido por la administración de drogas (KFDA) cuando se procesa dentro de un centro médico con un mínimo tratamiento por un médico13Coreano. Luego, SVF autóloga derivadas de tejido adiposo ha sido utilizado como un agente potencial para mejorar las funciones de la rodilla en pacientes de osteoartritis (OA) potencialmente regenerando tejido similar a cartílago10,14,15 , 16 , 17 , 18 .
En 2011, Pak demostró por primera vez que el tejido adiposo células madre derivadas (ASCs) contenidas en el SVF derivadas de tejido adiposo puede mejorar funciones de rodilla potencialmente regenerar tejido similar a cartílago en pacientes humanos de OA cuando se inyecta con rico en plaquetas plasma (PRP) 14. Además, Pak et al han informado datos de seguridad en 2013 con 91 pacientes. La tasa de eficacia media en estos datos de seguridad fue 67%15. Posteriormente, estudios adicionales por Pak et al demostraron rodilla mejora funciones potencialmente debido a la regeneración de tejido similar al cartílago en pacientes con un menisco lagrimal y condromalacia de la rótula10,16,17 ,18. Basado en artículos registrados, se sabe que el número de células madre contenidas en 100 g de tejido adiposo por el protocolo presentado en este artículo puede variar desde 40,000,000 de 1.000.000 dependiendo de las características de pacientes8, 19 , 20 , 21 , 22 , 23.
Aquí, presentamos un protocolo clínico de OA de la rodilla humana utilizando SVF autóloga derivadas de tejido adiposo con HA y PRP activado con cloruro de calcio. La primera versión de este protocolo clínico, que implica un sistema cerrado, manual para mantener la esterilidad, se reportó en 201114. El protocolo idéntico fue optimizado, mantenimiento de esterilidad y fue reportado en 2013 y 201610,15. Aquí, se presenta el protocolo optimizado. La descripción esquemática del Protocolo se presenta en la figura 1.
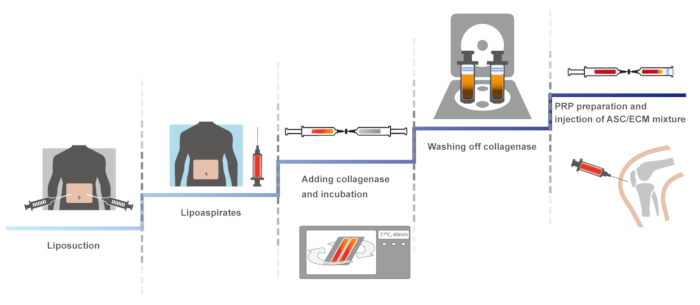
Figura 1: Descripción esquemática del protocolo. Haga clic aquí para ver una versión más grande de esta figura.
Protocol
Representative Results
Discussion
En 2001, Zuk et al. células madre aisladas del tejido adiposo por romper la matriz de colágeno colagenasa6. Luego, el grupo demostró que estas células madre aisladas del tejido adiposo podría transformar en cartílago y otros tejidos del mesodermo en origen, demostrando que estas células madre eran de origen mesenquimales.
Asimismo, el procedimiento presentado en este artículo es un modificado protocolo para aplicar el método similar a pacientes humanos…
Disclosures
The authors have nothing to disclose.
Acknowledgements
El autor reconoce el apoyo del personal de la clínica médica Mipro y el diseño de la figura de Jaepil/David Lee. Este trabajo fue apoyado por becas de investigación de la bioenergía y programa de desarrollo de tecnología médica de la NRF financiada por MSIT número NRF-2017M3A9E4078014; y el nacional investigación Fundación de Corea (NRF) financiado por el Ministerio de ciencia y TIC (números NRF-2017R1A2B4002315 y NRF-2016R1C1B2010308).
Materials
| Material | |||
| 5% Betadine (povidone-iodine) | Firson Co., Ltd. | 657400260 | |
| 2% Lidocaine | Daehan Pharmaceutical Co. | 670603480 | |
| Tumescent solution | Myungmoon Pharm. Co. Ltd. | N01BB01 | The solution was composed of 500 mL normal saline, 40 mL 2% lidocaine, 20 mL 0.5% marcaine, and 0.5 mL epinephrine 1:1000. |
| Liberase TL and TM research grade | Roche Applied Science | 5401020001 | |
| D5LR | Dahan Pharm. Co., Ltd. | 645101072 | Dextrose 5% in lactated Ringer's solution |
| Anticoagulant citrate dextrose solution | Fenwal, Inc. | NDC:0942-0641 | The solution was composed of 0.8% citric acid, 0.22% sodium citrate, and 0.223% dextrose. |
| 3% (w/v) Calcium chloride | Choongwae Pharmaceutical Co. | 644902101 | |
| 0.5% (w/v) HA (Hyaluronic acid ) | Dongkwang pharm. Co., Ltd. | 645902030 | |
| 0.25% Ropivacaine | Huons Co., Ltd. | 670600150 | |
| Equipment | |||
| 3.0 mm Cannula | WOOJU Medical Instruments Co. | ML30200 | |
| 60-mL Luer-Lock syringe | BD (Becton Dickinson) | 309653 | |
| Centrifuge Barrel Kit | CPL Co., Ltd. | 30-0827044 | |
| Tissue homogenizer that contains blades | CPL Co., Ltd. | 30-0827045 | |
| Rotating incubator mixer | Medikan Co., Ltd | MS02060092 | |
| Centrifuge | Hanil Scientific Inc. | CE1133 | |
| Magnetic Resonance Imaging | Philips Medical Systems Inc. | 18068 | |
| Ultrasound Imaging System | Samsung Medison co., Ltd | CT-LK-V10-ICM-09.05.2007 |
References
- Arnoczky, S. P. Building a meniscus. Biologic considerations. Clinical Orthopaedics and Related Research. (367 Suppl), S244-S253 (1999).
- Barry, F. P. Mesenchymal stem cell therapy in joint disease. Novartis Foundation Symposium. 249, 86-241 (2003).
- Usuelli, F. G., et al. Adipose-derived stem cells in orthopaedic pathologies. British Medical Bulletin. 124 (1), 31-54 (2017).
- Zhang, H. N., Li, L., Leng, P., Wang, Y. Z., Lv, C. Y. Uninduced adipose-derived stem cells repair the defect of full-thickness hyaline cartilage. Chinese Journal of Traumatology. 12 (2), 92-97 (2009).
- Zuk, P. A., et al. Human adipose tissue is a source of multipotent stem cells. Molecular Biology of the Cell. 13 (12), 4279-4295 (2002).
- Zuk, P. A., et al. Multilineage cells from human adipose tissue: implications for cell-based therapies. Tissue Engineering. 7 (2), 211-228 (2001).
- Baer, P. C., Geiger, H. Adipose-derived mesenchymal stromal/stem cells: tissue localization, characterization, and heterogeneity. Stem Cells International. 2012, 812693 (2012).
- Zhu, Y., et al. Adipose-derived stem cell: a better stem cell than BMSC. Cell Biochemistry and Function. 26 (6), 664-675 (2008).
- Bellei, B., Migliano, E., Tedesco, M., Caputo, S., Picardo, M. Maximizing non-enzymatic methods for harvesting adipose-derived stem from lipoaspirate: technical considerations and clinical implications for regenerative surgery. Scientific Reports. 7 (1), 10015 (2017).
- Pak, J., Lee, J. H., Park, K. S., Jeong, B. C., Lee, S. H. Regeneration of Cartilage in Human Knee Osteoarthritis with Autologous Adipose Tissue-Derived Stem Cells and Autologous Extracellular Matrix. BioResearch Open Access. 5 (1), 192-200 (2016).
- Alexander, R. W. Understanding Adipose-derived Stromal Vascular Fraction (AD-SVF) Cell Biology and Use on the Basis of Cellular, Chemical, Structural and Paracrine Components: A Concise Review. Journal of Prolotherapy. 4, e855-e869 (2012).
- Benders, K. E., et al. Extracellular matrix scaffolds for cartilage and bone regeneration. Trends in Biotechnology. 31 (3), 169-176 (2013).
- Korean Food and Drug Administration (KFDA). Cell therapy: Rules and Regulations. KFDA. , (2009).
- Pak, J. Regeneration of human bones in hip osteonecrosis and human cartilage in knee osteoarthritis with autologous adipose-tissue-derived stem cells: a case series. Journal of Medical Case Reports. 5, 296 (2011).
- Pak, J., Chang, J. J., Lee, J. H., Lee, S. H. Safety reporting on implantation of autologous adipose tissue-derived stem cells with platelet-rich plasma into human articular joints. BMC Musculoskeletal Disorders. 14, 337 (2013).
- Pak, J., Lee, J. H., Kartolo, W. A., Lee, S. H. Cartilage Regeneration in Human with Adipose Tissue-Derived Stem Cells: Current Status in Clinical Implications. BioMed Research International. 2016, 4702674 (2016).
- Pak, J., Lee, J. H., Lee, S. H. A novel biological approach to treat chondromalacia patellae. PLoS One. 8 (5), e64569 (2013).
- Pak, J., Lee, J. H., Lee, S. H. Regenerative repair of damaged meniscus with autologous adipose tissue-derived stem cells. BioMed Research International. 2014, 436029 (2014).
- Aust, L., et al. Yield of human adipose-derived adult stem cells from liposuction aspirates. Cytotherapy. 6 (1), 7-14 (2004).
- De Ugarte, D. A., et al. Comparison of multi-lineage cells from human adipose tissue and bone marrow. Cells Tissues Organs. 174 (3), 101-109 (2003).
- Guilak, F., et al. Clonal analysis of the differentiation potential of human adipose-derived adult stem cells. Journal of Cellular Physiology. 206 (1), 229-237 (2006).
- Mitchell, J. B., et al. Immunophenotype of human adipose-derived cells: temporal changes in stromal-associated and stem cell-associated markers. Stem Cells. 24 (2), 376-385 (2006).
- Oedayrajsingh-Varma, M. J., et al. Adipose tissue-derived mesenchymal stem cell yield and growth characteristics are affected by the tissue-harvesting procedure. Cytotherapy. 8 (2), 166-177 (2006).
- . Liberase TL information available from Sigma Millipore online Available from: https://www.sigmaaldrich.com/catalog/product/roche/05401020001?lang=en®ion=US (2018)
- . Liberase TM information available from Sigma Millipore online Available from: https://www.sigmaaldrich.com/catalog/product/roche/Libtmro?lang=en®ion=US (2018)
- Childs, J. D., Piva, S. R. Psychometric properties of the functional rating index in patients with low back pain. European Spine Journal. 14 (10), 1008-1012 (2005).
- Price, D. D., McGrath, P. A., Rafii, A., Buckingham, B. The validation of visual analogue scales as ratio scale measures for chronic and experimental pain. Pain. 17 (1), 45-56 (1983).
- Pilgaard, L., Lund, P., Rasmussen, J. G., Fink, T., Zachar, V. Comparative analysis of highly defined proteases for the isolation of adipose tissue-derived stem cells. Regenerative Medicine. 3 (5), 705-715 (2008).
- D’Ambrosi, R., Indino, C., Maccario, C., Manzi, L., Usuelli, F. G. Autologous Microfractured and Purified Adipose Tissue for Arthroscopic Management of Osteochondral Lesions of the Talus. Journal of Visualized Experiments. (131), e56395 (2018).
- Packer, J. D., Chang, W. T., Dragoo, J. L. The use of vibrational energy to isolate adipose-derived stem cells. Plastic Reconstructive Surgery-Global Open. 6 (1), e1620 (2018).
- Hanke, C. W., Bernstein, G., Bullock, S. Safety of tumescent liposuction in 15,336 patients. National survey results. Dermatologic Surgery. 21 (5), 459-462 (1995).
- Illouz, Y. G. Complications of liposuction. Clinics in Plastic Surgery. 33 (1), 129-163 (2006).
- Dixit, V. V., Wagh, M. S. Unfavourable outcomes of liposuction and their management. Indian Journal of Plastic Surgery. 46 (2), 377-392 (2013).
- Lehnhardt, M., et al. Major and lethal complications of liposuction: a review of 72 cases in Germany between 1998 and 2002. Plastic and Reconstructive Surgery. 121 (6), 396e-403e (2008).
- Iyer, S. S., Rojas, M. Anti-inflammatory effects of mesenchymal stem cells: novel concept for future therapies. Expert Opinion on Biological Therapy. 8 (5), 569-581 (2008).
- Zhang, J., Middleton, K. K., Fu, F. H., Im, H. J., Wang, J. H. HGF mediates the anti-inflammatory effects of PRP on injured tendons. PLoS One. 8 (6), e67303 (2013).
- Li, N. Y., Yuan, R. T., Chen, T., Chen, L. Q., Jin, X. M. Effect of platelet-rich plasma and latissimus dorsi muscle flap on osteogenesis and vascularization of tissue-engineered bone in dogs. Journal of Oral and Maxillofacial Surgery. 67 (9), 1850-1858 (2009).
- Parsons, P., et al. The biological effect of platelet rich-plasma on the fracture healing process. The Journal of bone and joint surgery. British volume. 91-B, 293 (2009).
- Wu, W., Chen, F., Liu, Y., Ma, Q., Mao, T. Autologous injectable tissue-engineered cartilage by using platelet-rich plasma: experimental study in a rabbit model. Journal of Oral and Maxillofacial Surgery. 65 (10), 1951-1957 (2007).
- Cooper, T. W., Eisen, A. Z., Stricklin, G. P., Welgus, H. G. Platelet-derived collagenase inhibitor: characterization and subcellular localization. Proceedings of the National Academy of Sciences of the United States of America. 82 (9), 2779-2783 (1985).
- Uzuki, M., Sawai, T. A. A comparison of the affinity of sodium hyaluronate of various molecular weights for degenerated cartilage: a histochemical study using hyaluronic acid binding protein. International Congress Series. 1223, 279-284 (2001).
- Pagano, C., et al. Molecular and morphometric description of adipose tissue during weight changes: a quantitative tool for assessment of tissue texture. International Journal of Molecular Medicine. 14 (5), 897-902 (2004).

