复合金属氧化物纳米粒子的熔融盐合成
Summary
在这里, 我们展示了一种独特的、相对低温的熔融盐合成方法, 用于制备均匀的复杂金属氧化物镧 hafnate 纳米粒子。
Abstract
开发可行的合成方法对于成功探索纳米材料的新特性和潜在应用至关重要。在这里, 我们介绍了熔融盐合成 (MSS) 方法制备金属氧化物纳米材料。优于其他方法的优点包括简单、绿色、可靠性、可扩展性和概化。以烧绿石镧氧化铪 (La2Hf2O7) 为代表, 我们描述了用于成功合成复杂金属氧化物纳米粒子 (NPs) 的 MSS 协议。此外, 通过改变 pH 值、温度、持续时间和退火后的各种合成参数, 该方法具有独特的生产具有不同材料特性的 NPs 的能力。通过微调这些参数, 我们能够合成高度均匀、非凝聚和高结晶性的 NPs。作为一个具体的例子, 我们改变了 La2Hf2O7 NPs 的颗粒大小, 通过更改在 MSS 过程中使用的氢氧化铵溶液的浓度, 这使我们能够进一步探索颗粒尺寸对各种性能。预计 MSS 方法将成为纳米材料的一种较为流行的合成方法, 并在今后几年中更广泛地应用于纳米科技和纳米技术领域。
Introduction
熔融盐合成 (MSS) 涉及使用熔融盐作为制备纳米材料从其组成前体的反应介质。熔融盐作用于溶剂, 通过增加反应物与其流动性之间的接触面积, 从而促进了化学反应速率的提高。熔融盐的选择对于 MSS 方法的成功至关重要。盐必须满足一些重要的质量要求, 如熔点低, 与反应物种的相容性和最佳水溶性。熔融盐以前用于提高固态反应速率;然而, 在磁通量系统中, 仅使用少量的熔融盐 (与 MSS 不同, 在这种情况下, 将大量添加到形成可溶介质中进行反应, 并控制合成纳米材料的性质, 如颗粒尺寸、形状和结晶度。等)。在这个意义上, MSS 是粉末冶金方法的修改, 不同于磁通量法1、2、3。熔融盐的运用可以 (1) 提高反应动力学速率4 , 同时降低合成温度5, (2) 提高反应物同质性6, (3) 控制结晶尺寸和形貌7, 和 (4)降低集聚水平。
纳米材料由于具有优越的电气、化学、磁性、光学、电子和热性能, 在科学研究和新型工业应用领域有着很高的需求。它们的特性高度依赖于颗粒的大小、形状和结晶度。与其他纳米材料的合成方法相比, MSS 具有一些明显的优点;虽然, 在纳米科学和纳米技术领域, 它尚未被称为其他合成方法。如下所述, 这些优点包括简单、可靠、可扩展性、概化、环境友好、成本效益、相对较低的合成温度和具有干净表面8的 NPs 自由聚集。
简单: MSS 过程可以很容易地在一个简单的实验室与基本设施进行。不需要精密的仪器。前体和熔融盐是空气稳定的, 无需手套箱处理。
可靠性: 一旦所有初始合成参数 (如浓度、pH 值、处理时间和退火温度) 得到优化, 使用 MSS 方法时, 就可以保证高质量和纯产品。如果所有的合成步骤都正确执行, 最终产品可能达到高质量 NPs 所需的所有基本标准。只要所有的合成参数都正确且仔细地遵循, MSS 方法的新手就不会改变合成结果。
可扩展性: MSS 方法能够产生大量大小和形状控制的粒子是至关重要的。这一关键因素非常重要, 因为它允许确定工业效用和效率。与其他合成技术相比, MSS 可以通过在过程中调整化学计量量来轻松生成足够数量的产品。这是该方法的一个重要特性, 因为它允许在工业层面提供便利, 因此, 由于这种可伸缩性9、10, 因此它成为一种更理想的方法。
概化: MSS 法也是一种推广技术, 可生产各种合成纳米颗粒。除了简单的金属氧化物和一些氟化物, 由 MSS 方法成功合成的复杂金属氧化物纳米材料包括 perovskites (ABO3)10、11、12、 13、14、尖晶石 (AB2O4)15、16、烧绿石 (A2B2O7)4、17、18、 19和正交结构 (A2B4O9)2,3,20。更具体地说, 这些纳米材料包括铁氧体、钛酸盐、铌酸、莫来石、硼酸铝、硅灰石和碳酸磷灰石7、9、21。MSS 方法还用于生产各种形貌的纳米材料, 如纳米球4、陶瓷粉末体22、nanoflakes23、微片7、纳米棒24和核壳纳米粒子 (NPs)25, 取决于合成条件和产品的晶体结构。
环境友好: 几种传统的纳米材料制备方法涉及使用大量有机溶剂和有毒物质产生环境问题。对其使用的部分或全部消除, 以及可持续过程产生的废弃物, 是当今绿色化学的需求8。MSS 方法是一种环保的方法, 通过采用无毒的化学和可再生材料, 最大限度地减少废弃物、副产品和能源, 合成纳米材料。
相对较低的合成温度: MSS 方法的处理温度相对于常规固态反应26或溶胶-凝胶燃烧反应27的要求较低。这种较低的温度可节省能源, 同时生产高质量的 NPs。
成本效益: MSS 方法不需要任何苛刻或昂贵的反应物或溶剂或任何专门的仪器。水是用于洗涤使用的熔融盐的主要溶剂, 这也是便宜的。此外, 所需的实验装置仅包括简单的玻璃器皿和没有专门仪器的熔炉, 而具有复杂成分和耐火材料性质的纳米材料也可以生产。
表面无结块: 在 MSS 过程中, 形成的纳米颗粒在熔融盐介质中分布很广, 由于其数量大, 与其高离子强度和粘度1、6 一起使用,8. 与胶体合成和大多数热液/溶剂热工艺不同, 不需要保护表面层来防止形成的 NPs 的连续生长和聚集。
基于 mss 方法的复杂金属氧化物 NPs 的典范合成: mss 方法作为一种普遍且经济有效的方法, 可用于合理和大规模地合成纳米材料, 以获得足够广泛的资料, 这可能受到科学家们的高度欢迎。在纳米科学和纳米技术方面工作。在这里, 选择了镧 hafnate (La2Hf2O7), 因为它在 X 射线成像、高k介电、发光、热像荧光粉、热障涂层等领域的多功能应用, 以及核废料主机。La2Hf2O7也是一个很好的主机掺杂闪烁体由于其高密度, 有效的原子数, 和其晶体结构的可能性与秩序紊乱相变的设计。它属于 a2B2O7系列化合物, 其中 “A” 是具有 +3 氧化态的稀土元素, 而 “B” 表示具有 +4 氧化态的过渡金属元素。然而, 由于耐火性和复杂的化学成分, La2Hf2O7 NPs 缺乏适当的低温和大规模合成方法。
对于基础科学调查和先进的技术应用, 它是制造单分散、高质量和均匀2B2O7 NPs 的先决条件。在这里, 我们使用高结晶 La2Hf2O7 NPs 的合成作为一个例子来证明 MSS 方法的优点。如图 1所示, La2Hf2O7 NPs 是由 MSS 方法在我们以前的报告之后的两步过程中编写的。第一, 一个单一来源的复杂前体 La (哦)3·HfO (OH)2·nH2O 是通过共沉淀路线制备的。在第二步中, 通过使用单源复合前驱体和硝酸盐混合物 (纳米3: KNO3 = 1:1、摩尔比) 在简单的 MSS 过程中合成了尺寸可控 La2Hf2O7 NPs。6小时650摄氏度。
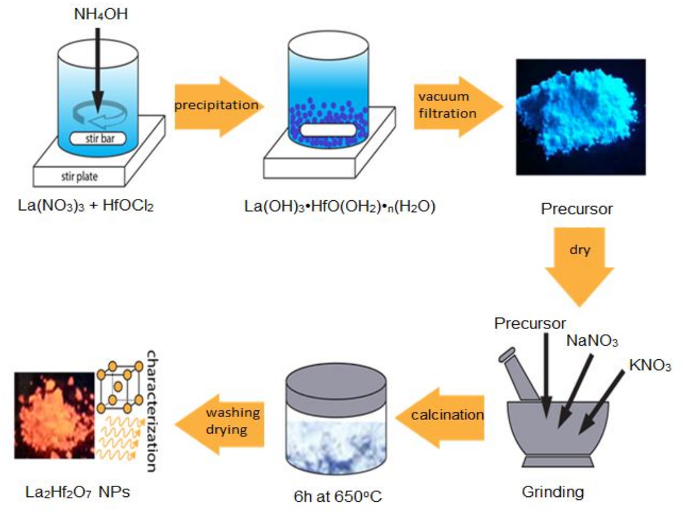
图1: La 的合成步骤示意图2Hf2O7通过 MSS 方法进行 NPs.请点击这里查看这个数字的更大版本.
Protocol
Representative Results
Discussion
图 4中的图表提供了 MSS 方法的几个可靠控制因素, 并说明了用于微调合成纳米材料特性的替代途径。此外, 它还有助于确定 MSS 流程中的关键步骤。
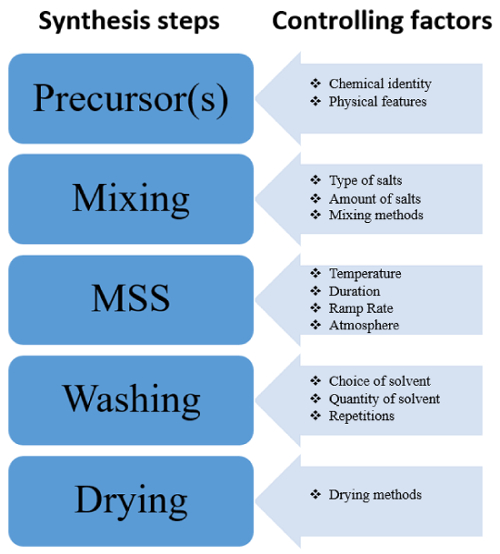
图4: MSS 关键步骤流程图, 指示 NPs 合成程序的控制因素, 并有可能的途径微调其特征.</str…
Disclosures
The authors have nothing to disclose.
Acknowledgements
作者感谢美国国家科学基金会 (#1710160 奖) 和美国农业部国家粮食及农业研究所 (奖 #2015-38422-24059) 提供的财政支持。德克萨斯大学里约格兰德河谷的化学系感谢罗伯特. 韦尔奇基金会的一项部门赠款提供的慷慨支持 (批准号:BX-0048)。S.K.G. 感谢美国-印度教育基金会 (USIEF) 和国际教育学院 (谎言) 为他的富布赖特的尼赫鲁博士后奖学金 (奖 #2268/FNPDR/2017)。
Materials
| Acetone, ACS, 99.5+% | Alfa Aesar | 67-64-1 | Dried over 4A sieves |
| Hafnium dichloride oxide octahydrate, 98+% (metals basis excluding Zr), Zr <1.5% | Alfa Aesar | 14456-34-9 | Hygroscopic |
| Lanthanum(III) nitrate hexahydrate | Aldrich | 10277-43-7 | Hygroscopic |
| Potassium nitrate, ReagentPlus R, ≥99.0% | Sigma-Aldrich | 7757-79-1 | Hygroscopic |
| Sodium nitrate, ReagentPlus R, ≥99.0% | Sigma-Aldrich | 7631-99-4 | |
| Ammonium hydroxide, 28% NH3, NH4OH | Alfa Aesar | 1336-21-6 | |
| Filter paper, P8 grade | Fisherbrand |
References
- Kimura, T. Molten salt synthesis of ceramic powders. Advances in Ceramics. , 75-100 (2011).
- Mao, Y., Park, T. J., Wong, S. S. Synthesis of classes of ternary metal oxide nanostructures. Chemical Communications. (46), 5721-5735 (2005).
- Mao, Y., Zhou, H., Wong, S. S. Perovskite-phase metal oxide nanostructures: Synthesis, properties, and applications. Material Matters. 5, 50-53 (2010).
- Mao, Y., Guo, X., Huang, J. Y., Wang, K. L., Chang, J. P. Luminescent nanocrystals with A2B2O7 composition synthesized by a kinetically modified molten salt Method. The Journal of Physical Chemistry C. 113 (4), 1204-1208 (2009).
- Yu, Y., Wang, S., Li, W., Chen, Z. Low temperature synthesis of LaB6 nanoparticles by a molten salt route. Powder Technology. 323, 203-207 (2018).
- Liu, X., Fechler, N., Antonietti, M. Salt melt synthesis of ceramics, semiconductors and carbon nanostructures. Chemical Society Reviews. 42 (21), 8237-8265 (2013).
- Chang, Y., Wu, J., Zhang, M., Kupp, E., Messing, C. L. Molten salt synthesis of morphology controlled alpha-alumina platelets. Ceramics International. 43 (15), 12684-12688 (2017).
- Mao, Y., Park, T. J., Zhang, F., Zhou, H., Wong, S. S. Environmentally friendly methodologies for nanostructure synthesis. Small. 3 (7), 1122-1139 (2007).
- Liu, J. R., Hong, R. Y., Feng, W. G., Badami, D., Wang, Y. Q. Large scale production of strontium ferrite by molten salt assited coprecipitation. Powder Technology. 262, 142-149 (2014).
- Yuanbing, M., Banerjee, S., Wong, S. S. Large-scale synthesis of single-crystalline perovskite nanostructures. Journal of the American Chemical Society. 125 (51), 15718-15719 (2003).
- Mao, Y. Facile synthesis of ferromagnetic double perovskite oxide La2BMnO6 nanoparticles. RSC Advances. 2 (33), 12675-12678 (2012).
- Hailili, R., Wang, C., Lichtfouse, E. Perovskite nanostructures assembled in molten salt based on halogen anions KX (X = F, Cl and Br): Regulated morphology and defect-mediated photocatalytic activity. Applied Catalysis B: Enviromental. 232, 531-543 (2018).
- Yuanbing Mao, J. P., McCloy, J. S. Magnetic properties of double perovskite oxide La2BMnO6 nanocrystals. Nanoscale. 5 (11), 4720-4728 (2013).
- Mao, Y., Wong, S. S. Reproducible composition and shape control of crystalline Ca1-xSrxTiO3 perovskite nanoparticles. Advanced Materials. 17 (18), 2194-2199 (2005).
- Rojas-Hernandez, R. E., et al. Original synthetic route to obtain a SrAl2O4 phosphor by the molten salt method: insights into the reaction mechanism and enhancement of the persistent luminescence. Inorganic Chemistry. 54 (20), 9896-9907 (2015).
- Reddy, M. V., Xu, Y., Rajarajan, V., Ouyang, T., Chowdari, B. V. R. Template free facile molten synthesis and energy storage studies on MCo2O4 (M = Mg, Mn) as anode for Li-ion batteries. ACS Sustainable Chemistry and Engineering. 3 (12), 3035-3042 (2015).
- Zuniga, J. P., Gupta, S. K., Pokhrel, M., Mao, Y. Exploring optical properties of La2Hf2O7:Pr3+ nanoparticles under UV and X-ray excitations for potential lighting and scintillating applications. New Journal of Chemistry. 42 (12), 9381-9392 (2018).
- Pokhrel, M., Wahid, K., Mao, Y. Systematic studies on RE2Hf2O7:5%Eu3+ (RE = Y, La, Pr, Gd, Er, and Lu) nanoparticles: Effects of the A-Site RE3+ cation and calcination on structure and photoluminescence. The Journal of Physical Chemistry C. 120 (27), 14828-14839 (2016).
- Wahid, K., Pokhrel, M., Mao, Y. Structural, photoluminescence and radioluminescence properties of Eu3+ doped La2Hf2O7 nanoparticles. Journal of Solid State Chemistry. 245, 89-97 (2017).
- Park, T. J., Papaefthymiou, G. C., Moodenbaugh, A. R., Mao, Y., Wong, S. S. Synthesis and characterization of submicron single-crystalline Bi2Fe4O9 cubes. Journal of Materials Chemistry. 15 (21), 2099-2105 (2005).
- Gilbert, M. R. Molten salt synthesis of titanate pyrochlore waste-forms. Ceramics International. 42 (4), 5263-5270 (2016).
- Huang, Z., et al. Molten salt synthesis of La2Zr2O7 ultrafine powders. Ceramics International. 42 (5), 6221-6227 (2016).
- Huang, Z., Duan, H., Liu, J., Zhang, H. Preparation of lanthanum cerate powders via a simple molten salt route. Ceramics International. 42 (8), 10482-10486 (2016).
- Wang, G., et al. Fabrication of rod-like Ti4O7 with high conductivity by molten salt synthesis. Materials Letters. 186, 361-363 (2017).
- Pokhrel, M., Burger, A., Groza, M., Mao, Y. Enhance the photoluminescence and radioluminescence of La2Zr2O7:Eu3+ core nanoparticles by coating with a thin Y2O3 shell. Optical Materials. 68, 35-41 (2017).
- Ramesh, G., Subramanian, V., Sivasubramanian, V. Dielectric properties of lead indium niobate ceramics synthesized by conventional solid state reaction method. Materials Research Bulletin. 45 (12), 1871-1874 (2010).
- Gupta, S. K., et al. Role of various defects in the photoluminescence characteristics of nanocrystalline Nd2Zr2O7: An introspection through spectroscopic and DFT calculations. Journal of Materials Chemistry C. 4 (22), 4988-5000 (2016).
- Wang, X., Zhu, Y., Zhang, W. Preparation of lanthanum zirconate nano-powders by molten salt method. Journal of Non-Crystalline Solids. 356 (20-22), 1049-1051 (2010).
- Popov, V. V., et al. Fluorite-pyrochlore phase transition in nanostructured Ln2Hf2O7 (Ln = La-Lu). Journal of Alloys and Compounds. 689, 669-679 (2016).
- Rybarczyk, M. K., Gontarek, E., Lieder, M., Titirici, M. M. Salt melt synthesis of curved nitrogen-doped carbon nanostructures: ORR kinetics boost. Applied Surface Science. 435, 543-551 (2018).
- Ozen, M., Mertens, M., Snikers, F., D’Hondt, H., Cool, P. Molten-salt synthesis of tetragonal micron-sized barium titanate from a peroxo-hydroxide precursor. Advanced Powder Technology. 28 (1), 146-154 (2017).
- Fazli, R., Fazli, M., Safaei-Naeini, Y., Golestani-Fard, F. The effects of processing parameters on formation of nano-spinel (MgAl2O4) from LiCl molten salt. Ceramics International. 39 (6), 6265-6270 (2013).
- Bortolani, F., Dorey, R. A. Molten salt synthesis of PZT powder for direct write inks. Journal of the European Ceramic Society. 30 (10), 2073-2079 (2010).
- Zhou, H., Mao, Y., Wong, S. S. Probing structure-parameter correlations in the molten synthesis of BaZrO3 perovskite submicron-sized particles. Chemistry of Materials. 19 (22), 5238-5249 (2007).
- Kimura, T., Machida, M., Yamaguchi, T., Newnham, R. E. Products of reaction between PbO and Nb2O5 in molten KCl or NaCl. Journal of the American Ceramic Society. 66 (10), 195-197 (1983).
- Liu, S., et al. A novel rechargeable zinc-air battery with molten salt electrolyte. Journal of Power Sources. 342, 435-441 (2017).
- Huang, Z., Li, B., Liu, J. Molten-salt synthesis of oxyapatite La9.33Si6O26 powders as electrolytes for intermediate temperature solid oxide fuel cells. Physica status solidi A – Applicationand Materials Science. 207 (10), 2247-2251 (2010).
- Ahmed, J., Mao, Y. Synthesis, characterization and electrocatalytic properties of delafossite CuGaO2. Journal of Solid State Chemistry. 242 (1), 77-85 (2016).
- Ahmed, J., Mao, Y. Ultrafine iridium oxide nanorods synthesized by molten salt method toward electrocatalytic oxygen and hydrogen evolution reactions. Electrochimica Acta. 212, 686-693 (2016).

