Высокопроизводительная ДНК плазменный мультиплексирование и трансфекция с использованием акустической технологии нанодозирования
Summary
Этот протокол описывает высокопроизводительную плазмидную трансфекцию клеток млекопитающих в 384-хорошую пластину с использованием акустической технологии выброса капель. Трудоемкий, подверженный ошибкам раздавливание ДНК и мультиплексирование, а также дозирование реагентов трансфекционного реагента, являются программным обеспечением и выполняются нанодайзером. Клетки затем посеяны в этих предварительно заполненных скважин.
Abstract
Трансфекция клеток, незаменимая для многих биологических исследований, требует контроля многих параметров для точного и успешного достижения. Чаще всего выполняется при низкой пропускной их, это к тому же трудоемкие и подверженные ошибкам, тем более при мультиплексации нескольких плазмидов. Мы разработали простой, быстрый и точный метод для выполнения трансфекции клеток в 384-хорошо макет пластины с использованием акустических капель катапульты (ADE) технологии. Устройство nanodispenser используемое в этом изучении основано на этой технологии и позволяет точно поставку nanovolume на высокой скорости от плиты скважины источника к назначению одному. Он может обойтись и мультиплекс ДНК и трансфекционного реагента в соответствии с заранее разработанной таблицы. Здесь мы представляем оптимальный протокол для выполнения ADE основе высокой пропускной способностью плазмидтранса, что позволяет достичь эффективности до 90% и почти 100% котрансфекции в котрансфекционных экспериментов. Мы расширяем первоначальную работу, предлагая удобный для пользователя макрос на основе электронных таблиц, способный управлять до четырех плазмидов/колодцев из библиотеки, содержащей до 1536 различных плазмидов, и приложения для планшетного нахлыстое направляющее приложение. Макрос разрабатывает необходимый шаблон (ы) исходной пластины (ы) и генерирует готовые к использованию файлы для нанодайзера и планшетного приложения. Четырехэтапный протокол трансфекции включает в себя i) разбавитель обойтись с классическим жидким обработчиком, ii) плазмидное распределение и мультиплексирование, iii) трансфекционный реагент распределяется нанодсером, и iv) клеточное покрытие на предварительно заполненных скважинах. Описанный программно-основанный контроль мультиплексирования и трансфекции Плазмидных плазмидных aDE позволяет даже неспециалистам в полевых условиях быстро и безопасно выполнять надежную трансфекцию клеток. Этот метод позволяет быстро определить оптимальные настройки для данного типа ячейки и может быть перенесен на более высокие и ручные подходы. Протокол облегчает применение, такие как человеческий белок ORFeome (набор открытых кадров чтения в геноме) или CRISPR-Cas9 на основе генной функции проверки, в непулированных стратегий скрининга.
Introduction
Представленный здесь метод подробно описывает, как выполнять мультиплексирование и трансфекцию ДНК в клетках млекопитающих при высокой пропускной состоянии с помощью жидкого нанодайзера на основе акустической системы в 384-хорошей пластине, даже для неспециалистов в этой области. Этот недавно опубликованный метод1 позволяет выполнять столько, сколько 384 независимых плазмидных мультиплексирования ДНК и трансфекции условиях в одном эксперименте, менее чем за 1 ч. Одиночные или котрансфекционные эксперименты были успешными, достигнув почти 100% котрансфекция в популяции трансинфицированных клеток. Этот протокол упрощает трансфекцию, поскольку большинство утомительных, трудоемких и подверженных ошибкам шагов теперь ориентированы на программное обеспечение (см. рисунок 1 для общего обзора). Были предприняты дальнейшие усилия по разработке специализированных инструментов для повышения простоты использования при одновременном предотвращении человеческих ошибок в ходе общего процесса и содействия успешному трансфекции даже для неспециалистов в этой области. Описанный протокол включает в себя “удобную” макротаблицу, которую мы разработали для управления 384 независимыми трансфекционными условиями с мультиплексированием возможностей до четырех плазмидов в каждой скважине. Макрос автоматически генерирует шаблоны исходной пластины (ы) для загрузки ожидаемого объема плазмидной плазмы ДНК от стартовых фондовых решений и файлов, необходимых для привода программного обеспечения нанодайзера на экспериментальной конструкции, которая была введена. Поскольку ручная раздача ДНК в 384-хорошо источник пластины утомительно и подвержены ошибкам, мы также разработали специальное приложение на основе таблетки для руководства пользователя при распределении решения ДНК в соответствии с шаблоном.
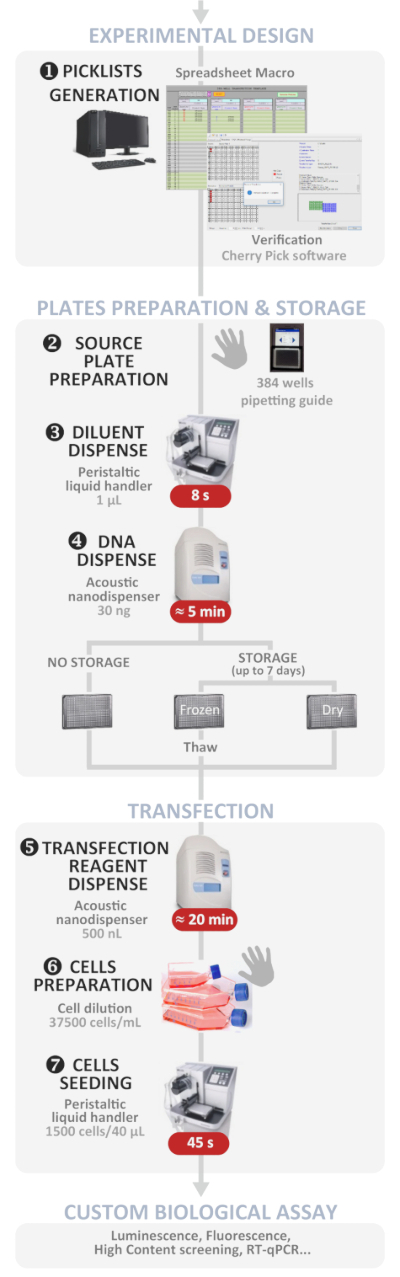
Рисунок 1: Экспериментальный рабочий процесс. Схематическое представление оптимального автоматизированного протокола обратного трансфекции высокой пропускной связи (от экспериментального проектирования до пользовательского биологического асссе). Ручные шаги указаны символом руки, а приблизительное время для каждого шага написано в красной коробке. Пожалуйста, нажмите здесь, чтобы просмотреть большую версию этой цифры.
Многие клеточные эксперименты начинаются с плазмидной трансфекции ДНК, и даже если многие выделенные реагенты были и все еще разрабатываются для повышения эффективности трансфекции и / или облегчить процедуру, многое еще предстоит сделать2,3 , 4. Трансфекция плазмидных клеток ДНК включает в себя несколько шагов для достижения высокой эффективности, таких как начальное комплексное поглощение, эндосомальный побег и цитоплазмический перенос к ядру5,6. В дополнение к выпасам кальция или физическим методам, таким как электропорация или микроинъекция с использованием специальных устройств7, современные химические методы были сосредоточены на повышении доставки клеток ДНК при снижении цитоксичности клеток8, 9. Использование липидов или катионных полимеров, образующих липосомы-подобные комплексы, а в последнее время нелипсоомальные полимерные химические системы сделали трансфекцию проще и эффективнее10. Несмотря на эти изменения, трансфекция клеток по-прежнему требует конкретных навыков, которые должны быть точно выполнены, поскольку большинство из этих физических или химических протоколов трансфекции требуют, чтобы ученые вручную подготовить каждое состояние реакции трансфекции ДНК, таким образом ухудшает пропускную выливку. Чтобы обойти эту проблему, обратные протоколы трансфекции были разработаны с использованием химических реагентов трансфекции11,12,13, что позволяет пользователю проверить или объединить несколько плазмидов в более быстрый способ. В этих протоколах перед посевом клеток на комплексах образуются нуклеиновые кислотные комплексы с трансфекционными реагентами. Однако эти обратные протоколы по-прежнему ограничены ручным управлением решениями ДНК и сочетанием каждого из независимых условий. Хотя это возможно, чтобы выполнить их в 96-ну хорошо пластины формате, подготовка ДНК и дозы будет утомительным, и там, вероятно, будут ошибки. Когда требуется различное количество нескольких плазмидов ДНК и мультиплексируется друг с другом, трансфекция клеток становится еще более трудной и более трудоемкой, и человеческие ошибки становятся совершенно неизбежными. Масштабирование до 384-колодцевого формата пластин в обратном подходе трансфекции, несмотря на несколько мультиплексированных условий трансфекции ДНК, становится невозможной задачей из-за следующих причин. i) Объемы ДНК, трансфективный реагент или объемы реакционной смеси для управления ниже, чем 1 КЛ для каждой скважины. ii) Мультиплексирование плазмидов для 384 независимых условий становится чрезвычайно сложным. Поставка в каждой из 384 скважин также iii) очень трудоемкие и iv) ошибка подвержена. Действительно, выдать правильное решение в ожидаемых скважинах трудно управлять, потому что низкие объемы уже обойтись не позволяют визуального мониторинга между пустыми и уже заполненными скважинами. v) Наконец, существует высокий риск высыхания смеси путем испарения до добавления клеток в связи со временем, необходимым для выполнения необходимых мер по дозированию. Таким образом, ограничивающим фактором для создания высокой пропускной днк плазмидных трансфекционных анализов, как представляется, миниатюризация анализа, который подразумевает малообъемный мультиплексирование и управление, которые не могут быть обработаны вручную больше, но также вряд ли достижимы в надежным способом классическими перистатическими жидкими обработчиками.
В качестве доказательства сложности автоматизировать такие assays и получить высокую пропускную стоимость, только несколько попыток автоматизировать трансфекции были опубликованы до сих пор: 96-ну хорошо пластины формат с использованием коммерческого устройства обработки жидкости и фосфата кальция осадков14 и, совсем недавно, липоплексрей, и микрофлюидный чип, позволяющий 280 независимых трансфекций15, но требующих специальных навыков в этой области. Другой метод, акоутофорез, позволяющий жидкой левитации и ведущих к жидкости манипуляции и смешивания, был использован для выполнения трансфекции ДНК в 24-96-ну хорошо пластины форматов16. Хотя этот подход является осуществимым, он страдает от крайне низкой пропускной всей перевалки, поскольку смешивание клеток с трансфекционной смесью ДНК требует инкубации 60 с для каждой точки перед посевом. Это означает продолжительность не менее 96 мин для полной 96-колодца пластины. Кроме того, этот протокол далек от того, чтобы поддаваться общей аудитории биологов, как эта работа была сделана с в доме разработан и изготовлены устройства, которые в настоящее время не доступны на рынке. Напротив, в последние несколько лет с помощью нанообъемных диспенсеров появилась простая в использовании технология акустического дозирования на основе программного обеспечения. Используя сфокусированную акустическую энергию, эти устройства позволяют жестко контролируемый выброс небольших объемов жидкости от 2,5 нл до 500 нл от исходной пластины до пункта назначения17. Эта технология, называемая акустической выкатывания капель (ADE), имеет множество преимуществ: она полностью автоматизирована, бесконтактная, без кончиков, точная, точная и высоко воспроизводимая, и имеет высокую пропускную связь18. Первый посвященный доставке диметилсульксида (DMSO) решения, настройки были расширены, чтобы обойтись aqueous буферов19. Таким образом, акустические нанодятелы, кажется, подходят для протоколов трансфекции обратных клеток и могут обойти большинство вышеупомянутых ручных ограничений. Поскольку с помощью этой технологии не было описано никаких попыток трансфекции плазмидных трансфекций, мы недавно оценили пригодность акустической системы дозирования для выполнения обратного трансфекции клеток.
Воспользовавшись пропускной стоимостью нанодчебирования и простотой использования, мы оптимизировали обратный протокол трансфекции для клеток HeLa путем перекрестного тестирования нескольких параметров, которые могут влиять на трансфекцию ДНК на 384-ну, одной пластине, а именно, общее количество ДНК и источник концентрации ДНК, разбавитель, трансфекционный реагент, и количество спреда клеток. Разработанный протокол обходит вышеописанные ручные ограничения трансфекции клеток и предоставляет ряд преимуществ по сравнению с другими автоматизированными попытками трансфекции. Во-первых, он миниатюризирован, что позволяет экономически эффективным трансфекционным реагентом, экономя препараты плазмида ДНК и трансфекционный реагент. Во-вторых, он гораздо более высокопроизводительен и воспроизводим, чем ручной протокол (даже для начинающих), так как трансфекция всей 384-й пластины может быть достигнута менее чем за 1 ч. Наконец, это программное обеспечение, что позволяет контролировать дозированных количество ДНК и мультиплексирования нескольких плазмидов. Действительно, благодаря программному обеспечению nanodispenser(Таблица материалов), пользователь может разработать план исследования для управления объемами, которые будут освобождены от определенного источника хорошо пластины назначения один.
Представленный здесь протокол предназначен в основном для тех, кто имеет доступ к нанодционизму и хотел бы создать трансфекционные эксперименты с высокой пропускной их пропускной вот и доступной, но также и для тех, кто хочет быстро оптимизировать свои параметры трансфекции для данного типа клеток применение этого протокола для перекрестного тестирования нескольких параметров при высокой пропускной состоянии. Действительно, мы показали, что оптимизированные параметры, идентифицированные с этим наномасштабным протоколом, могут быть перенесены в более масштабные и ручные трансфекционные эксперименты. Наконец, поскольку трансфекционный реагент, используемый в настоящем протоколе, позволяет трансфекцию ДНК или siRNA в соответствии с производителем, протокол также представляет интерес для тех, кто стремится к выполнению комплексных подходов к переэкспрессии генов или нокдауну. Назначения пластины предварительно заполнены ДНК могут быть сохранены до 7 дней до использования в трансфекционном анализе без потери эффективности, которая является еще одним преимуществом следующего протокола для такого рода применения.
Protocol
Representative Results
Discussion
Создание и оптимизация точного метода трансфекции высокой пропускной связи для данной клеточной линии требует от ученых следовать некоторым ключевым параметрам, описанным в этом разделе. Мы настоятельно рекомендуем начать с рекомендуемых значений во всем протоколе, так как эти парам…
Disclosures
The authors have nothing to disclose.
Acknowledgements
Авторы раскрыли получение следующей финансовой поддержки для исследования, авторства и/или публикации этой статьи: Inserm, Лилльский университет, Институт Лилля Пастера, Conseil Regional du Nord, и PRIM-HCV1 и 2 (Пале де Рехерш Междисциплинарное сюр-ле-Медикамент), Национальная эгенство Речерче (ANR-10-E-PX-04-01), Федер (12001407 (D-AL) Equipex Imaginex BioMed) и Европейское сообщество (ERC-STG INTRACETB. Авторы хотели бы поблагодарить д-ра С. Моуре, д-ра Б. Виллеман, д-ра Р. Ферру-Клемента и д-ра Х. Гроульта за их критический обзор и исправление рукописи.
Materials
| 384LDV Microplate | Labcyte | LP-0200 | |
| 384-well Microplate μClear Black | Greiner | 781906 | |
| Ampicilin | Sigma | A9393-5G | Selection antibiotic for bacteria transformed with ampicilin expressing vector |
| Android Tablet | Samsung | Galaxy Note 8 | used to guide the user while the source plate manual dispense |
| Aniospray Surf 29 | Anios | 2421073 | disinfectant to clean the MicroFlo head |
| Columbus software | Perkin Elmer | image analysis software | |
| Dulbecco's Modified Eagle Medium (DMEM), high glucose, GlutaMAX Supplement, pyruvate | Thermo Fisher Scientific | 10566032 | cell culture medium |
| Echo Cherry Pick 1.5.3 software | Labcyte | Software enabling ADE-based dispenses by the Echo550 device from a *.csv file; nanodispenser software | |
| Echo550 | Labcyte | ADE-based dispenser | |
| Fetal Bovine Serum | Thermo Fisher Scientific | 16000044 | to add in cell culture medium |
| Formalin solution, neutral buffered, 10% | Sigma-Aldrich | HT501128-4L | to fix cell |
| HeLa cells | ATCC | HeLa (ATCC® CCL-2™) | |
| Hoechst 33342, Trihydrochloride, Trihydrate | Thermo Fisher Scientific | H3570 | 10 mg/mL Solution in Water |
| INCell Analyzer 6000 | GE Healthcare | 29043323 | automated laser-based confocal imaging platform |
| LB medium | Thermoischer Scientific LB Broth Base (Lennox L Broth Base)®, powder |
12780052 | culture medium for bacteria growth |
| Lysis Buffer (A2) | Macherey-Nagel | 740912.1 | Buffer from the NucleoSpin Plasmid kit used to prepare plasmid from bacterial culture |
| MicroFlo 10µL cassette | Biotek Instruments Inc | 7170013 | to use with the Microflo Dispenser |
| MicroFlo 1μL cassette | Biotek Instruments Inc | 7170012 | to use with the Microflo Dispenser |
| MicroFlo Dispenser | Biotek Instruments Inc | 7171000 | peristaltic pump-based liquid handler device |
| Microvolume spectrophotometer | Denovix | DS-11 Spectrophotometer | Measure the DNA concentration of samples |
| mVenus plasmid | mVenus cDNA was cloned by enzymatic restriction digestion and ligation in Age1/BsrG1 sites of the tdTomato-N1 plasmid | Vector type: Mammalian Expression, Fusion Protein: mVenus | |
| Neutralization Buffer (A3) | Macherey-Nagel | 740913.1 | Buffer from the NucleoSpin Plasmid kit used to prepare plasmid from bacterial culture |
| NucleoSpin Plasmid kit | Macherey-Nagel | 740588.50 | used to prepare plasmid from bacterial culture |
| Optimal-Modified Eagle Medium (Opti-MEM) Medium | Thermo Fisher Scientific | 31985070 | |
| optional Wash bufferWash Buffer (A4) | Macherey-Nagel | 740914.1 | Buffer from the NucleoSpin Plasmid kit used to prepare plasmid from bacterial culture |
| orbital shaker | incubated large capacity shaker | 444-7084 | Used to grow bacteria under gentle agitation and 37°C |
| Penicillin-Streptomycin | Thermo Fisher Scientific | 15140122 | 10,000 U/mL |
| Phosphate-Buffered Saline | Thermo Fisher Scientific | 10010001 | |
| Plasmid mini-columns | Macherey-Nagel | 740499.250 | Silica membrane mini-column to prepare plasmid from bacterial culture |
| Resuspension Buffer (A1) | Macherey-Nagel | 740911.1 | Buffer from the NucleoSpin Plasmid kit used to prepare plasmid from bacterial culture |
| RNAse A | Macherey-Nagel | 740505 | Enzyme from the NucleoSpin Plasmid kit used to prepare plasmid from bacterial culture |
| tdTomato-N1 plasmid | Addgene | Plasmid #54642 | Vector type: Mammalian Expression, Fusion Protein: tdTomato |
| TransIT-X2 Dynamic Delivery System | Mirus Bio | MIR 6000 | |
| Wash Buffer (AW) | Macherey-Nagel | 740916.1 | Buffer from the NucleoSpin Plasmid kit used to prepare plasmid from bacterial culture |
| 3D printer | Creality | CR10S | used to print the plate adapter |
| Blender Software | https://www.blender.org/ Free software under GNU General Public License (GPL). |
version 2.79b | used to design the plate adapter |
References
- Colin, B., Deprez, B., Couturier, C. High-Throughput DNA Plasmid Transfection Using Acoustic Droplet Ejection Technology. SLAS Discovery: Advancing Life Sciences R & D. , 2472555218803064 (2018).
- Mirus Bio. . Optimising Transfection Performance. , (2019).
- Thermo Fisher Scientific. . Factors Influencing Transfection Efficiency | Thermo Fisher Scientific – FR. , (2019).
- Boussif, O., et al. A versatile vector for gene and oligonucleotide transfer into cells in culture and in vivo: polyethylenimine. Proceedings of the National Academy of Sciences of the United States of America. 92 (16), 7297-7301 (1995).
- Figueroa, E., et al. A mechanistic investigation exploring the differential transfection efficiencies between the easy-to-transfect SK-BR3 and difficult-to-transfect CT26 cell lines. Journal of Nanobiotechnology. 15 (1), 36 (2017).
- Kirchenbuechler, I., Kirchenbuechler, D., Elbaum, M. Correlation between cationic lipid-based transfection and cell division. Experimental Cell Research. 345 (1), 1-5 (2016).
- Zhang, Z., Qiu, S., Zhang, X., Chen, W. Optimized DNA electroporation for primary human T cell engineering. BMC Biotechnology. 18 (1), 4 (2018).
- Cao, D., et al. Transfection activity and the mechanism of pDNA-complexes based on the hybrid of low-generation PAMAM and branched PEI-1.8k. Molecular bioSystems. 9 (12), 3175-3186 (2013).
- Bos, A. B., et al. Development of a semi-automated high throughput transient transfection system. Journal of Biotechnology. 180, 10-16 (2014).
- Colosimo, A., et al. Transfer and expression of foreign genes in mammalian cells. BioTechniques. 29 (2), 314-318 (2000).
- Villa-Diaz, L. G., Garcia-Perez, J. L., Krebsbach, P. H. Enhanced transfection efficiency of human embryonic stem cells by the incorporation of DNA liposomes in extracellular matrix. Stem Cells and Development. 19 (12), 1949-1957 (2010).
- Sabatini, D. M. . Reverse transfection method. , WO2001020015A1 (2001).
- Raymond, C., et al. A simplified polyethylenimine-mediated transfection process for large-scale and high-throughput applications. Methods (San Diego, CA). 55 (1), 44-51 (2011).
- Junquera, E., Aicart, E. Recent progress in gene therapy to deliver nucleic acids with multivalent cationic vectors. Advances in Colloid and Interface Science. 233, 161-175 (2016).
- Woodruff, K., Maerkl, S. J. A High-Throughput Microfluidic Platform for Mammalian Cell Transfection and Culturing. Scientific Reports. 6, 23937 (2016).
- Vasileiou, T., Foresti, D., Bayram, A., Poulikakos, D., Ferrari, A. Toward Contactless Biology: Acoustophoretic DNA Transfection. Scientific Reports. 6, 20023 (2016).
- Hadimioglu, B., Stearns, R., Ellson, R. Moving Liquids with Sound: The Physics of Acoustic Droplet Ejection for Robust Laboratory Automation in Life Sciences. Journal of Laboratory Automation. 21 (1), 4-18 (2016).
- Grant, R. J., et al. Achieving accurate compound concentration in cell-based screening: validation of acoustic droplet ejection technology. Journal of Biomolecular Screening. 14 (5), 452-459 (2009).
- Sackmann, E. K., et al. Technologies That Enable Accurate and Precise Nano- to Milliliter-Scale Liquid Dispensing of Aqueous Reagents Using Acoustic Droplet Ejection. Journal of Laboratory Automation. 21 (1), 166-177 (2016).
- Day, R. N., Davidson, M. W. The fluorescent protein palette: tools for cellular imaging. Chemical Society Reviews. 38 (10), 2887-2921 (2009).
- Zielinski, D., Gordon, A., Zaks, B. L., Erlich, Y. iPipet: sample handling using a tablet. Nature Methods. 11 (8), 784-785 (2014).
- Brunner, S., et al. Cell cycle dependence of gene transfer by lipoplex, polyplex and recombinant adenovirus. Gene Therapy. 7 (5), 401-407 (2000).
- Nii, T., et al. Single-Cell-State Culture of Human Pluripotent Stem Cells Increases Transfection Efficiency. BioResearch Open Access. 5 (1), 127-136 (2016).
- Noonan, D. J., Henry, K., Twaroski, M. L. A High-Throughput Mammalian Cell-Based Transient Transfection Assay. Signal Transduction Protocols. 284, 051-066 (2004).
- . . Transfection | TransIT Transfection Reagents | Mirus Bio. , (2015).
- American Type Culture Collection. . General protocol for transfection of stem cells, primary cells, and continuous cell lines with ATCC TransfeX Transfection Reagent. , (2017).
- American Type Culture Collection. . Transfection Reagents for Nucleic Acid Transfer into ATCC Cells. , (2017).
- de Los Milagros Bassani Molinas, M., Beer, C., Hesse, F., Wirth, M., Wagner, R. Optimizing the transient transfection process of HEK-293 suspension cells for protein production by nucleotide ratio monitoring. Cytotechnology. 66 (3), 493-514 (2014).
- Promega. . FuGENE® 6 Transfection Reagent. , (2019).
- Olden, B. R., Cheng, Y., Yu, J. L., Pun, S. H. Cationic polymers for non-viral gene delivery to human T cells. Journal of Controlled Release: Official Journal of the Controlled Release Society. 282, 140-147 (2018).
- Park, E., Cho, H. B., Takimoto, K. Effective gene delivery into adipose-derived stem cells: transfection of cells in suspension with the use of a nuclear localization signal peptide-conjugated polyethylenimine. Cytotherapy. 17 (5), 536-542 (2015).
- Wood, R. W., Loomis, A. L. The physical and biological effects of high-frequency sound-waves of great intensity. The London, Edinburgh, and Dublin Philosophical Magazine and Journal of Science. 4 (22), 417-436 (1927).
- Mamat, U., et al. Eliminating Endotoxin at the Source – A Novel Competent Cell Line with Modified Lipopolysaccharide for Low-Endotoxin Plasmid Production. , (2014).
- Ivanova, N. V., Kuzmina, M. L. Protocols for dry DNA storage and shipment at room temperature. Molecular Ecology Resources. 13 (5), 890-898 (2013).
- Lesnick, J., Lejeune-Dodge, A., Ruppert, N., Jarman, C. . High-Precision Cell Dispensing with the Labcyte Echo® Liquid Handler. , (2017).
- Yang, X., et al. A public genome-scale lentiviral expression library of human ORFs. Nature Methods. 8 (8), 659-661 (2011).
- Peng, J., Zhou, Y., Zhu, S., Wei, W. High-throughput screens in mammalian cells using the CRISPR-Cas9 system. The FEBS journal. 282 (11), 2089-2096 (2015).

