בשיטת מידול סיליקו לרעלים מימיים לחישוביות חישובית של משבנים אנדוקרינים: גישה מבוססת תוכנה באמצעות ארגז הכלים QSAR
Summary
מבנה כמותי-קשרי גומלין (QSAR) מידול הוא ביואינפורמטיקה מייצגת שיטה בסיוע בהקרנה רעילות. פרוטוקול זה מדגים כיצד להעריך מבחינה חישובית את הסיכונים של המשורים האנדוקריניים (עורכים) בסביבות מימיות. באמצעות כתיבת הכלים של ה-OECD QSAR, הפרוטוקול מיישם בתוך שיטת סיליקו, לניתוח רעילות של העורכים בדגים.
Abstract
ניתוחים חישוביים של תהליכים טוקסילוגיים מאפשרים הקרנת תפוקה גבוהה של חומרים כימיים וחיזוי נקודות הקצה שלהם במערכות ביולוגיות. במיוחד, מבנה כמותי-יחסי פעילות (QSAR) מודלים הוחלו יותר ויותר כדי להעריך את ההשפעות הסביבתיות של שפע של חומרים רעילים. בשנים האחרונות, מספר סוגים מודגשים יותר של טוקסינים הם משבשים אנדוקרינים (עורכים, שהם כימיקלים העלולים להפריע לכל חילוף החומרים הקשור להורמונים). בגלל שעורכים יכולים להשפיע באופן משמעותי על פיתוח ורבייה של בעלי חיים, יש צורך לחזות במהירות את ההשפעות השליליות של עורכים המשתמשים בטכניקות סיליקו. מחקר זה מציג שיטת סיליקו כדי ליצור מידע חיזוי על ההשפעות של מייצגים העורכים בעלי חוליות מימיות, במיוחד מיני דגים. הפרוטוקול מתאר דוגמה העושה שימוש בזרימת העבודה האוטומטית של תוכנת ארגז הכלים של QSAR שפותחה על-ידי הארגון לשיתוף פעולה כלכלי ופיתוח (ה-OECD) כדי לאפשר תחזיות לפני הרעלה חריפה של עורכים. כתוצאה מכך, הבאים נקבעים: (1) חישוב של היחסים מספריים בין הריכוז עבור 50% של השפעה (LC50) ו octanol מים מקדם מחיצה (Kow), (2) הופעות פלט שבו LC50 ערכים שנקבעו בניסויים מושווים לאלה שנוצרו על ידי חישובים, ו (3) את התלות של הזיקה לקולטן אסטרוגן על הקשרבין K או ו LC50.
Introduction
התפתחויות חדשות באינפורמטיקה ובטכנולוגיה חישובית כללו את המדעים הביולוגיים עם מתודולוגיות כמותיים המציעות דיוק גבוה ואמינות1. בפרט, אלגוריתמים המשמשים בטקסונומיה מולקולרית ובסיווג הרכוש הביאו למערכת יחסים כמותית מבנה-פעילות (QSAR) מודלים2. מודלים אלה מיישמים באופן אוטומטי את המבנים הכימיים ואת הפעילות הביולוגית של מסד נתונים כימי נתון ומיישמת מהירה בהקרנה סיליקו של מגוון רחב של מצעים כימיים בהתאם לפעולות הרפואיות או הרעילות שלהם3. כלים QSAR יכול לייצר פרופילי רעילות חזוי כפונקציה של וקטורים התכונה של מתארי מולקולרית (כלומר, פרמטרים פיזיקליים) של כימיקלים של עניין ליצור מספרית נקודות הקצה4. בדרך כלל, כל נקודת קצה כמותית מוצגת כמסגרת מגרש דו-ממדי לעומת שינויים בערכי מתארים. מודל QSAR נוצר לאחר מכן באמצעות (מספר) ניתוחי רגרסיה ליניארית. לאחר שערכת נתונים נוצלה במלואה כדי לבנות מודל QSAR (המכונה קבוצת ההדרכה), אזי המודל מאומת על ידי ניבוי נקודות הקצה של קבוצת כימיקלים שאינם כלולים בערכת ההדרכה (המכונה ערכת הבדיקה). לאחר מכן ניתן להשתמש במודל כדי לנבא את הפעילות הביולוגית של תרכובות שנבדקו3.
בין כימיקלים מזיקים רבים, משבשים האנדוקרינית (עורכים) הודגש כקבוצה של רעלים שעלולים להפריע מטבוליזם רבים הקשורים להורמונים ביונקים, דו-חיים ודגים5,6. עורכים ידועים כדי לגרום למגוון של תופעות לוואי, כגון סרטן מומים, על ידי חסימת או שינוי מסלולים הורמונליים נורמלי או הפעלת סינתזה הורמון הורמונלי/אותות השפלה. כתוצאה מכך, אלה כימיקלים מחקה הורמון יכול לperturb מערכות אנדוקריניות כגון פיתוח ביולוגי רבייה של אוכלוסיות חיות הבר הם הכשלו. במיוחד, ההשפעות האקולוגיים של העורכים נחקרו בהרחבה בחוליות מימיות, אשר יש כמעט זהה הורמון קולטן מבנים לאלה של יונקים, כולל בני אדם. מכיוון שכל הפעולות ההורמונאליים מתרחשות במינונים נמוכים בvivo, חיזוי הרעלים הפוטנציאליים של מועמדים אד באמצעות הקרנה מהירה סיליקו הוא קריטי לבריאות הציבור והסביבה.
מודלים QSAR מבוסס על רעלים של עורכים נערכו ניצול שני מתארי 2D ו-3D (המכונה 2D ו-3D QSAR, בהתאמה), אשר לחשוף את ליגיום ED ומאגד מחייב של אסטרוגן, אנדרוגן, וקולטני פרוגסטרון7. למרות היתרונות הגבוהים ביותר של QSAR 3D, שבו הקונפורמציה ואינטראקציות אלקטרוסטטית נחשבים, 2D QSAR שומרת על החוסן שלה באלגוריתמים מתמטיים ישירים, חישובים מהירים, ועומסים חישובית נמוכה מאוד. בנוסף, מודלים של 2D-QSAR גמישים לשימוש במגוון רחב של יישומים תוך השגת ביצועי חיזוי מדויקים יחסית.
כיום ארגז הכלים של ה-OECD הוא אחד מכלי התוכנה הנפוצים ביותר במחשב, המספק מודלים qsar באופן חופשי ומובנה מראש,8. יוצר הפרופילים שלו משתמש במסדי נתונים של מתארי דו-ממדי. מאז שחרורו של הגרסה הראשונה ב-2008, התוכנה החלה בתחומים של תעשיות כימיות וביולוגיות, בריאות הציבור, ובטיחות סביבתית לניתוח מלא או חלקי של הסיכונים הפוטנציאליים של תרכובות טבעיות וסינתטיים, עם תחומי עניין מיוחדים בקרצינובגנזה10,11,12, מוטגניות13,14,15ו רעילות התפתחותית16. היישום לרעלים מימיים הוכח גם, עם דגש על הצטברות ביולוגית ו bioaccumulation17.
כתיבת הכלים QSAR הוכח שימושי בניבוי רעילות לטווח קצר של מגוון רחב של כימיקלים17, כמו גם קולטן אסטרוגן (ER) איגוד מחייב של עורכים18. עם זאת, לא נותחו באמצעות ארגז הכלים של QSAR את הקשרים האקוטוקטיים החריפים של העורכים בחוליות מים מימיים. במחקר זה, פרוטוקול אופייני ו נתיישב מוצג לבצע מידול qsar על תופעות לוואי חריפה של עורכים עם דגש מינים דגים. המחקר מראה כי כתיבת הכלים QSAR היא תוכנה נגישה מאוד לחישוב וחיזוי הבליות/תמותה של בעלי חוליות מימיות עבור כמה עורכים נציג. שיטות טיפול סטטיסטי לנגזרות של מערכות נתונים סיליקות מוצגות. איור 1 מציג את הערכה הכוללת עבור הפעולה הכללית של ארגז הכלים qsar. זרימת העבודה המוצגת באיור 2 מספקת הוראות ברורות לגבי אופן ההפעלה של שיטת סיליקו, כדי לחזות רעילות חריפה של חומרים ליעד כגון כימיקלים משבשי המערכת האנדוקרינית.
Protocol
Representative Results
Discussion
צדדיות של ארגז הכלים של ה-OECD QSAR כתוכנה אנליטית עבור האקוטוקסיקולוגיה מוצג כאן עם עניין ספציפי בהשפעות השליליות של כימיקלים משבשי האנדוקרינית על בעלי חוליות ימיות. בנוסף, פרוטוקול פשוט וסטנדרטי הוכח לניבוי רעילות חריפה (96-h LC50) של 74 מייצגים (שולחן 1) עבור מינים דגים. הדבר הושג על-ידי החלת בניית קטגוריה, מילוי פערי נתונים ומודולי פרופיל ER המוטבעים בארגז הכלים של qsar (איור 1, איור 2).
הקורלציה הליניארית בין יומן10LC50 ו-log10KOW עם מדרון שלילי (כפי שמוצג בדמות המשלים S1) כבר זמן רב מוכר בתור מערכת יחסים כמותית סטנדרטית בניתוח qsar25, שבו רעילות גבוהה יותר מראה את ההידרופובי יותר כימיקל נתון. כפי שניתן לראות מחישוב פשוט, הקשר המתמטי הכללי הכולל את המשוואה S1 ו- S2 המשוואה (מידע משלים) הוא ביטוי מומר מפונקציית הכוח הבאה26:
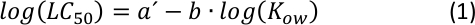

מתוך העלילה (משוואה 2), אפיון טווח ביניים של KOW26 עשוי להיות אפשרי על ידי התאמת הפרמטרים a ו-b, שבו וריאציה מסוימת ב hydrophobicity (או hydrophilicity) לא לשנות באופן משמעותי את נקודת קצה של רעילות חריפה.
ניתוחים השוואתיים בין התחזיות החישוביות והתצפיות הנסיוניות ב-LC50, כפי שמוצג באיור 3 ובאיור 4, דווחו בדרך כלל במחקרים של qsar עבור הרעילות הימית השונים, כולל טכני nonionic מסוררים27, triazole קוטלי פטריות28, ו מטבוליטים של חומרי הדברה21. סוג זה של אימות רטרוספקטיבי מספק מידע לגבי המרחק של כלי QSAR שניתן להגיע אליו במונחים של ביצועים השוואתיים לתוצאות נסיוניות. במחקר זה של רעילות חריפה דגים, את ארגז הכלים QSAR הוכח לספק תחזיות הגנה עבור מעל 90% של עורכים מנוסה בכל הדגים במין אחד, Pimephales promelas.
עוד זיהוי שלושה כימיקלים חריג חשוד טעות באיור 3 ואיור 4, אשר הראה גבוה יותר החזוי LC50 בממוצע ובמינימום, בהתאמה, נדרש. ראשית, the 3 “, 5, 7-trihydroxy-4”, 6-dimethoxyisoflavone הוא סוג של פלונואיד (יותר ספציפי, isoflavone), אשר נחשב להיות בטוח בדרך כלל בשימוש בתרופות צמחיות; עם זאת, יש עדיין הקשורות אסטרוגן חששות29 ועלול לגרום לרעילות חריפה כנראה באמצעות זירחון חמצוני לא מצמד30. בשלב הבא, ה-1, 4-benzenediol, הנקרא הידרוקווינה, הוא תרכובת פנופילית שיכולה להפעיל תגובה חיסונית לא ספציפית ו ציטוטוקסיב דגים31. בסופו של דבר, 4-הקספנול ידוע להציג פעילות אסטרוגניים חיובית מספיק כדי להיות מסווג כ-ED32. זה כבר למד היטב כי הסיבה העיקרית של רעילות חריפה של הידרוקינון היא הפחתת חמצון (מחדש) רכיבה על אופניים. ההידרוקווינה הוא תחמוצת בנזואנקי1 ומופחת בחזרה לחצי quinone או הידרוקווינה שוב ושוב, עם קופרינים מכלה ויצירת מיני חמצן תגובתי33. שני הכימיקלים האחרים עשויים לדרוש חקירות עמוקות יותר כדי לחשוף את מנגנוני הפעולה שלהם ברעילות חריפה באמצעות גישות עגינה מולקולריות, כגון השימוש ב-Panche et al.34, אשר לא ניתן לכסות על ידי ארגז הכלים qsar.
עורכים להפריע למערכת האנדוקרינית בעיקר באמצעות אינטראקציות פיסיוכימיקלים עם קולטני סטרואידים כגון אסטרוגן קולטנים אנדרוגן, אשר הם של עניין רב ב QSAR מידול לימודי35. בהתחשב בכך, ארגז הכלים QSAR הוא חסון במונחים של הסיווג המהיר של מאגד ER מחייב עבור סט של כימיקלים מבוסס רק על מתארי 2D של מבנים מולקולריים. כאשר מערכת פרופיילר ER זו הוחלה על רשימת העורכים שלנו, לא נמצאה קורלציה ברורה בין הזיקה לאיגוד המיון לבין הידרופוטביניטי (השלמה שלהאיור S2). תוצאה זו עשוי להיות מוסבר על ידי העובדה כי היווצרות של מתחם קולטן סטרואידים היא לא תוצאה ישירה של תרומה הידרופובי מליטה אבל צריך להיות מלווה על ידי שינוי קונפורמאני במבנה הפעיל באתר קולטן36. כריכת הקולטן יכול להיות גם בשל מימן מליטה ו-π-הערמה.
בנוסף, המיקום של כל קבוצה כימית על המולקולה עשויה להשפיע על כריכת הקולטן, גם אם ההידרופוטביטי ומספר המועמדים לקשר מימן-תורמים נשארים אותו דבר. שנית, היוצר של ER בייצור מגמות מנוגדות בין החזוי וניסיוני LC50 רמות ממוצע עם הגדלת זיקה מחייבת ER (איור 5). זה יכול להיות בגלל החריפות של ההורים במבחן רעילות חריפה אינם בשל מאגד ER אלא לנרקוזיס ברוב המקרים, או כדי לחדש את הרכיבה על אופניים במקרה של הhydroquinone. לדוגמה, ניתוח מקיף יותר, כולל רעילות כרונית, נדרש לקבוצה גדולה יותר של עורכים להגדיר מגבלות ניבוי של הגירסה הנוכחית של ארגז הכלים QSAR.
מחקר מקדמי זה עשוי להיות גם השלכות בריאות הציבור כי סטרואידים (אנדרוגנים, אסטרוגנים, פרוסטרינס, ו corticoids) וקולטנים שלהם להציג מבנים דומים או אפילו זהה macromolecular על פני החוליות5. סוגים אלה של מערכות איתות אנדוקריניות מקבילה עשויות לפעול באמצעות מנגנון משותף באירועי מפתח של עורכים5. עם זאת, מתודולוגיות נוספות ומשלימות נדרשות להאיר את ההיבט העצום והמורכב הזה [לדוגמה, על-ידי ביצוע מידול חישובית של קליטה, הפצה, חילוף חומרים והוצאת מטבוליזם (ADME) ו/או תוצאה שלילית מסלול (AOP)]38. יתרה מזאת, מכיוון שרוב החששות המדעיים והציבוריים שהועלו על ההשפעות השליליות של העורכים קשורות לרעלים הכרוניים שלהם, משפרים את מאגרי הנתונים והאלגוריתמים בארגז הכלים של QSAR ומייצרים לאורך זמן אמין האקוטוקסיקולוגיה. תחזיות לעורכים יש צורך.
נייר זה מדגים את היישום של כתיבת הכלים qsar כדי להשוות את ערכי LC50 של מעבר אקולוגי עבור דגים עם יומן10K הערכים של עורכים. במהלך הפרוטוקול, היא גורמת ליחסים חלשים בין שני הפרמטרים, כפי ש נחשף על ידי מחקרים קודמים (למשל, קים et al.39) כי הרישום10Kow אינו מנבא ישיר מעולה של LC מימיים50. למרות מגבלה זו, פרוטוקול זה מספק סקירה כללית או “כהות” כדי לתאר כיצד להשתמש לוח המחוונים למטרה נתונה, שכן הוא יישום חוקי להשתמש בארגז הכלים QSAR לחקירת מערכת יחסים בין LC50 (או ER הכריכה אהדה)ו –10K או ככלי עבור הקרנת רעילות האקולוגי המהירה. עם זאת, יש לציין כי (1) להאיר את הקשר בין כריכת קולטן אסטרוגן ורעילות כרונית, במקום רעילות חריפה (השפעה), רלוונטי יותר כך היחסים ברורים ניתן למצוא, ו (2) קולטן האנדרוגן, יחד עם זה של אסטרוגן, גם ממלא תפקיד קריטי ברעילות הרבייה. לכן, הוא נדרש עבור הגירסה העתידית של ארגז הכלים QSAR כדי לשפר את פונקציות חיזוי לאור שתי נקודות אלה.
Disclosures
The authors have nothing to disclose.
Acknowledgements
מחקר זה נתמך על ידי המועצה הלאומית למדעים של המדע & טכנולוגיה (NDT) מענק על ידי ממשלת דרום קוריאה (MSIP) (לא. CAP-17-01-כדור אירופה) ו-Project 11911.
Materials
| Adobe Acrobat Reader DC | Adobe Systems Software Ireland Limited | NA | Required to view prediction and category report |
| Computer | System: Microsoft Corporation | NA | Recommended system properties: (i) system type: 64 bit, Microsoft Windows 7 or newer, (ii) processor: I5 at 2.4 GHz or faster processor or equivalent AMD CPU, (iii) Installed memory (RAM): 6 GB of RAM, (iv) Hard Disk Drive (HDD): 20 GB free hard drive space |
| Microsoft Editor | Microsoft Corporation | NA | Required to upload a substance list of CAS numbers (batch mode) to the OECD QSAR Toolbox as .txt file (text file) |
| Microsoft Excel 2016 | Microsoft Corporation | NA | Required to export data from OECD QSAR Toolbox as .cvs, .xls or .xlsx files |
| OECD QSAR Toolbox version 4.0 or newer | Organisation for Economic Co-operation and Development |
NA | Required to run OECD QSAR Toolbox Automated Workflows; free download: https://qsartoolbox.org/download/ |
| OriginPro 9 | OriginLab Corporation | NA | Optional program for data analysis; similar tools possible |
References
- Najarian, K., Najarian, S., Gharibzadeh, S., Eichelberger, C. N. . Systems Biology and Bioinformatics: A Computational Approach. , (2009).
- Fujita, T., Iwasa, J., Hansch, C. A new substituent constant, π, derived from partition coefficient. Journal of the American Chemical Society. 86, 5175-5180 (1964).
- Roy, K., Kar, S., Das, R. N. . Understanding the Basics of QSAR for Applications in Pharmaceutical Sciences and Risk Assessment. , (2015).
- Raies, A. B., Bajic, V. B. In silico toxicology: computational methods for the prediction of chemical toxicity. WIREs Computational Molecular Science. 6, 147-172 (2016).
- Hayes, T. B. Welcome to the revolution: integrative biology and assessing the impact of endocrine disruptors on environmental and public health. Integrative Compuational Biology. 45, 321-329 (2005).
- Schug, T. T., et al. Minireview: endocrine disruptors: past lessons and future directions. Molecular Endocrinology. 30, 833-847 (2016).
- Devillers, J., Marchand-Geneste, N., Carpy, A., Porcher, J. M. SAR and QSAR modeling of endocrine disruptors. SAR QSAR Environmental Research. 17, 393-412 (2006).
- Dimitrov, S. D., et al. QSAR Toolbox – workflow and major functionalities. SAR QSAR Environmental Research. 27, 203-219 (2016).
- Yordanova, D., et al. Automated and standardized workflows in the OECD QSAR Toolbox. Computational Toxicology. 10, 89-104 (2019).
- Mombelli, E., Devillers, J. Evaluation of the OECD (Q)SAR Application Toolbox and Toxtree for predicting and profiling the carcinogenic potential of chemicals. SAR QSAR Environmental Research. 21, 731-752 (2010).
- Devillers, J., Mombelli, E., Samsera, R. Structural alerts for estimating the carcinogenicity of pesticides and biocides. SAR QSAR Environmental Research. 22, 89-106 (2011).
- Li, C., et al. Identifying unknown by-products in drinking water using comprehensive two-dimensional gas chromatography-quadrupole mass spectrometry and in silico toxicity assessment. Chemosphere. 163, 535-543 (2016).
- Devillers, J., Mombelli, E. Evaluation of the OECD QSAR Application Toolbox and Toxtree for estimating the mutagenicity of chemicals. Part 1. Aromatic amines. SAR QSAR Environmental Research. 21, 753-769 (2010).
- Devillers, J., Mombelli, E. Evaluation of the OECD QSAR Application Toolbox and Toxtree for estimating the mutagenicity of chemicals. Part 2. α-β unsaturated aliphatic aldehydes. SAR QSAR Environmental Research. 21, 771-783 (2010).
- Kulkarni, S. A., Barton-Maclaren, T. S. Performance of (Q)SAR models for predicting Ames mutagenicity of aryl azo and benzidine based compounds. Journal of Environmental Science and Health Part C Environmental Carcinogenesis & Ecotoxicology Reviews. 32, 46-82 (2014).
- Craig, E. A., Wang, N. C., Zhao, Q. J. Using quantitative structure-activity relationship modeling to quantitatively predict the developmental toxicity of halogenated azole compounds. Journal of Applied Toxicology. 34, 787-794 (2014).
- Tebby, C., Mombelli, E., Pandard, P., Péry, A. R. Exploring an ecotoxicity database with the OECD (Q)SAR Toolbox and DRAGON descriptors in order to prioritise testing on algae, daphnids, and fish. Science of the Total Environment. 409, 3334-3343 (2011).
- Mombelli, E. Evaluation of the OECD (Q)SAR Application Toolbox for the profiling of estrogen receptor binding affinities. SAR QSAR Environmental Research. 23, 37-57 (2012).
- Verhaar, H. J. M., van Leeuwen, C. J., Hermens, J. L. M. Classifying environmental pollutants. 1: structure-activity relationships for prediction of aquatic toxicology. Chemosphere. 25, 471-491 (1992).
- Enoch, S. J., Hewitt, M., Cronin, M. T. D., Azam, S., Madden, J. C. Classification of chemicals according to mechanism of aquatic toxicity: an evaluation of the implementation of the Verhaar scheme in Toxtree. Chemosphere. 73, 243-248 (2008).
- Burden, N., Maynard, S. K., Weltje, L., Wheeler, J. R. The utility of QSARs in predicting acute fish toxicity of pesticide metabolites: a retrospective validation approach. Regulatory Toxicology and Pharmacology. 80, 241-246 (2016).
- Nendza, M., et al. Screening for potential endocrine disruptors in fish: evidence from structural alerts and in vitro and in vivo toxicological assays. Environmental Sciences Europe. 28, 26 (2016).
- Roncaglioni, A., Piclin, N., Pintore, M., Benfenati, E. Binary classification models for endocrine disrupter effects mediated through the estrogen receptor. SAR QSAR Environmental Research. 19, 697-733 (2008).
- Sosnovcová, J., Rucki, M., Bendová, H. Estrogen receptor binding affinity of food contact material components estimated by QSAR. Central European Journal of Public Health. 24, 241-244 (2016).
- Walker, J. D., Dearden, J. C., Schultz, T. W., Jaworska, J., Comber, M. H. I., Walker, J. D. QSARs for New Practitioners. QSARs for Pollution Prevention, Toxicity Screening, Risk Assessment, and Web Applications. , (2003).
- Sánchez-Bayo, F. From simple toxicological models to prediction of toxic effects in time). Ecotoxicology. 18, 343-354 (2009).
- Sjöström, M., Lindgren, &. #. 1. 9. 7. ;., Uppgård, L. L., Chen, F., Schüürmann, G. Joint Multivariate Quantitative Structure-Property and Structure-Activity Relationships for a Series of Technical Nonionic Surfactants. Quantitative Structure-Activity Relationships in Environmental Sciences-VII. , (1997).
- Ding, F., Guo, J., Song, W., Hu, W., Li, Z. Comparative quantitative structure-activity relationship (QSAR) study on acute toxicity of triazole fungicides to zebrafish. Chemistry Ecology. 27, 359-368 (2011).
- Galati, G., O’Brien, P. J. Potential toxicity of flavonoids and other dietary phenolics: significance for their chemopreventive and anticancer properties. Free Radical Biology in Medicine. 37, 287-303 (2004).
- Russom, C. L., Bradbury, S. P., Broderius, S. J. Predicting modes of action from chemical structure: acute toxicity in the fathead minnow (Pimephales promelas). Environmental Toxicology and Chemistry. 16, 948-967 (1997).
- Taysse, L., Troutaud, D., Khan, N. A., Deschaux, P. Structure-activity relationship of phenolic compounds (phenol, pyrocatechol and hydroquinone) on natural lymphocytotoxicity of carp (Cyprinus carpio). Toxicology. 98, 207-214 (1995).
- Nishihara, T., et al. Estrogenic activities of 517 chemicals by yeast two-hybrid assay. Journal of Health Science. 46, 282-298 (2000).
- Bolton, J. L., Trush, M. A., Penning, T. M., Dryhurst, G., Monks, T. J. Role of quinones in toxicology. Chemical Research in Toxicology. 13, 135-160 (2000).
- Panche, A. N., Diwan, A. D., Chandra, S. R. Flavonoids: an overview. Journal of Nutritional Science. 5, e47 (2016).
- Li, J., Gramatica, P. QSAR classification of estrogen receptor binders and pre-screening of potential pleiotropic EDCs. SAR QSAR Environmental Research. 21, 657-669 (2010).
- Bohl, M. . Molecular Structure and Biological Activity of Steroids. , (2017).
- Kaminuma, T., Takai-Igarashi, T., Nakano, T., Nakata, K. Modeling of signaling pathways for endocrine disruptors. BioSystems. 55, 23-31 (2000).
- Lillicrap, A., et al. Alternative approaches to vertebrate ecotoxicity tests in the 21st century: a review of developments over the last 2 decades and current status. Environmental Toxicology and Chemistry. 35, 2637-2646 (2016).
- Kim, J. W., et al. Acute toxicity of pharmaceutical and personal care products on freshwater crustacean (Thamnocephalus platyurus) and fish (Oryzias latipes). Journal of Toxicological Sciences. 34, 227-232 (2009).

