タイムラプス蛍光顕微鏡を用いた細菌プレデター ブレロビトリオバクテリオボルス のライフサイクルの生細胞イメージング
Summary
ここで提示されるのは、アガロースパッドおよび細胞イメージングディッシュと組み合わせて、タイムラプス蛍光顕微鏡を使用した捕食細菌 Bdellovibrioバクテリオボルス の完全なライフサイクルのモニタリングを記述するプロトコルです。
Abstract
Bdellovibrio細菌は 、有害な病原体を含む他のグラム陰性細菌を殺す小さなグラム陰性、義務的な捕食細菌である。したがって、生きた抗生物質と考えられる。 B.バクテリオボルス を生きた抗生物質として適用するには、まず、その複雑なライフサイクルの主要な段階、特に獲物内での増殖を理解する必要があります。これまでのところ、捕食ライフサイクルの連続した段階をリアルタイムで監視することは困難でした。ここで提示されるB. バクテリオボルスの完全なライフサイクルのリアルタイムイメージングのための包括的なプロトコルは、特にホスト内での成長の間である。この目的のために、アガロースパッドからなるシステムは、捕食細胞がアガロースパッドの下を自由に移動し、固定化された獲物細胞がbdelloplastsを形成することができる細胞イメージング皿と組み合わせて使用される。DNAポリメラーゼIIIの蛍光タグ付きβサブユニットを産生する株の適用により 、B.バクテリオボルス のライフサイクルの再生段階で染色体複製を監視することがさらに可能になります。
Introduction
Bdellovibrio bacteriovorusは、クレブシエラ・ニューモニエ、緑膿菌、シゲラ・フレックスネリ11,2,32,3などの有害な病原体を含む他のグラム陰性細菌を捕食する小さな(0.3-0.5 μm by 0.5-1.4 μm)グラム陰性細菌である。B.バクテリオボルスは病原体を殺すので、細菌感染症、特に多剤耐性株によって引き起こされる細菌感染と戦うために適用できる潜在的な生きている抗生物質と考えられている。
B. バクテリオボルスは、自由に生きている非複製的攻撃期と細胞内生殖期の2つの段階からなる独特のライフサイクルを示す(図1)。自由な生活段階では、最大160μm/sの速度で移動するこの高い運動性細菌は、獲物を探します。獲物の外膜に付着した後、それは、ペリプラズム44、5に入る。B.バクテリオボルスは、子宮間生殖段階で、多量の加水分解酵素を使用して宿主の高分子を分解し、それ自身の成長のために再利用する。ペリプラズムを侵略した直後、宿主細胞は死んで膨満感を放ち、その中に捕食細胞が伸び、染色体を複製する球形の構造である。複製処理は複製元(oriC)6から始まり、染色体のコピーが完全に合成されるまで続行します 7.興味深いことに、各染色体の複製は細胞分裂に続かない。代わりに、捕食者は、長い、多核及び糸状細胞を形成するために伸びる。栄養が枯渇すると、フィラメントは同期的な敗血症を受け、子孫細胞はbdelloplast8から放出される。
B.バクテリオボルスが細菌感染症に対する生きた抗生物質として使用される前に、そのライフサイクルの主要な段階、特に獲物内の増殖に関連するものを理解することが重要である。B.バクテリオボルスの生細胞イメージングは、複雑なライフサイクルの間に捕食者とその獲物の様々な形態学的形態のために困難であった。これまで、B.バクテリオボルスとその宿主細胞との相互作用は、主に電子顕微鏡法とスナップショット分析22、9、109,10によって研究されてきたが、これらは、特に捕食期の連続した段階を監視するために使用される場合、両方に限界がある。これらの方法は、B.バクテリオボルス細胞の高解像度画像を提供し、攻撃または成長段階で小さな捕食者の観察を可能にする。しかし、それらは両方のライフサイクル段階を通して単一のB.バクテリオボルス細胞の追跡を許可しません。
ここで提示されるのは、B. バクテリオボルスの完全なライフサイクルを監視するために、タイムラプス蛍光顕微鏡(TLFM)を使用するための包括的なプロトコルです。アガロースパッドからなるシステムは、細胞イメージング皿と組み合わせて使用され、捕食細胞がアガロースパッドの下を自由に移動し、固定化された獲物細胞がbdelloplastsを形成することができる(図2)。このセットアップは、 大腸菌 と B.バクテリオボルスの両方の特定の株に基づいて調製されますが、プロトコルはユーザーの個々の株に合わせて簡単に変更することができます(例えば、異なる選択マーカーを運ぶ、異なるフルオロフォアと融合したタンパク質など)。
この場合、攻撃段階中に B.バクテリオボルス を可視化するために、細胞質タンパク質の蛍光タグ付きバージョンであるPilZ(要求に応じて入手可能)を発現する特定の株(HD100 DnaN-mNeonGreen/PilZ-mCherry)を構築した。この株は、さらにDnaN(βスライディングクランプ)、DNAポリメラーゼIIIホロエンザイムのサブユニットを、蛍光タンパク質と融合して生成する。これにより、連続的なDNA複製を、bdelloplasts内で増殖する捕食細胞内で監視することができます。
画像取得に使用されるプロトコルおよびソフトウェアは、特定の製造業者が提供する反転顕微鏡を指しますが( 材料表を参照)、この技術は、環境室または他の外部加熱ホルダを備え、タイムラプスイメージングが可能な任意の反転顕微鏡に対して調整することができます。データ分析のために、ユーザーは個々の出力形式と互換性のある利用可能なソフトウェアを選択することができます。
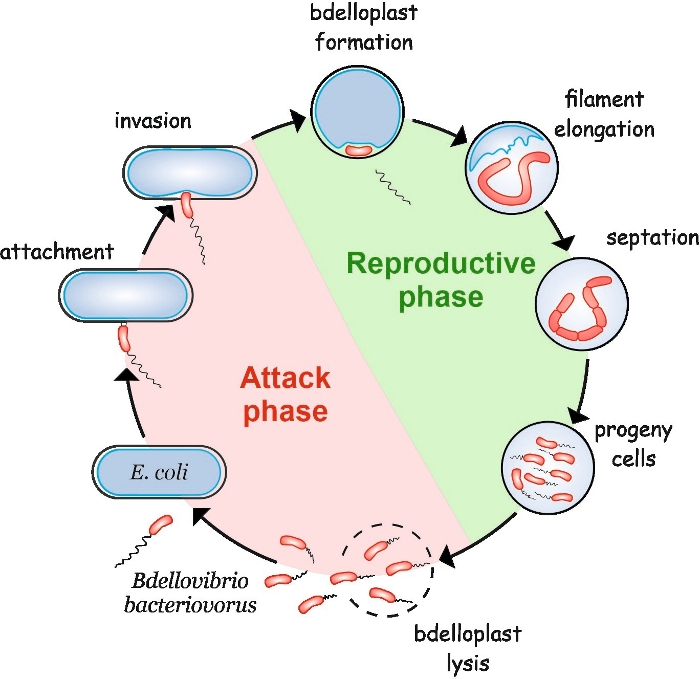
図 1:B.バクテリオボルス のライフサイクルを宿主細胞として 大腸菌 で行う。攻撃段階では、自由に泳ぐ B.バクテリオボルス 細胞が宿主 大腸菌 細胞を探し、付着する。侵入後、捕食細胞は獲物の周囲に局在し、宿主細胞の形状を変化させ、bdelloplastを形成する。生殖段階は、ブデロプラススト形成から始まる。捕食細胞は獲物細胞を消化し、単純な化合物を再利用して独自の構造を構築します。 B. バクテリオボルス は、宿主のペリプラズム内の長い単一のフィラメントとして成長する。獲物細胞の資源が枯渇すると 、B.バクテリオボルス フィラメントは同期的に敗血を起させ、前立腺細胞を形成する。子孫の細胞が彼らの旗エラを発達した後、彼らは腺芽細胞をライスする。 この図の大きなバージョンを表示するには、ここをクリックしてください。
Protocol
Representative Results
Discussion
生きた抗生物質として B.バクテリオボルス を使用することに対する関心の高まりにより、捕食性のライフサイクル、特に捕食者と病原体の相互作用を観察するための新しいツールが必要です。提示されたプロトコルは 、B.バクテリオボルス のライフサイクル全体を、特にホスト内での成長中にリアルタイムで追跡するために使用されます。さらに、DNAポリメラーゼIIIホロ酵素?…
Disclosures
The authors have nothing to disclose.
Acknowledgements
この研究は、国立科学センターの助成金Opusによってサポートされました 2018/29/B/NZ6/00539 J.Z.C.
Materials
| Centrifuge | MPW MED. INSTRUMENTS | MPW-260R | Rotor ref. 12183 |
| CertifiedMolecular Biology Agarose | BIO-RAD | 161-3100 | low fluorescence agarose for agarose pad |
| Fiji | ImageJ | https://imagej.net/Fiji | Open source image processing package |
| Glass Bottom Dish 35 mm | ibidi | 81218-200 | uncoated glass |
| Microscope | GE | DeltaVision Elite | Microtiter Stage, ultimate focus laser module, DV Elite CoolSnap HQ2 Camera, SSI assembly FP DV, kit obj. Oly 100x oil 1.4 NA, prism Nomarski 100x LWD DIC, ENV ctrl IX71 uTiter opaQ 240 V |
| Minisart Filter 0.45 µm | Sartorius | 16555———-K | Cellulose Acetate, Sterile, Luer Lock Outlet |
| Start SoftWoRx | GE | Manufacturer-supplied imaging software |
References
- Shatzkes, K., et al. Predatory Bacteria Attenuate Klebsiella pneumoniae Burden in Rat Lungs. mBio. 7 (6), (2016).
- Iebba, V., et al. Bdellovibrio bacteriovorus directly attacks Pseudomonas aeruginosa and Staphylococcus aureus Cystic fibrosis isolates. Frontiers in Microbiology. 5, (2014).
- Willis, A. R., et al. Injections of Predatory Bacteria Work Alongside Host Immune Cells to Treat Shigella Infection in Zebrafish Larvae. Current biology: CB. 26 (24), 3343-3351 (2016).
- Lambert, C., et al. Characterizing the flagellar filament and the role of motility in bacterial prey-penetration by Bdellovibrio bacteriovorus. Molecular Microbiology. 60 (2), 274-286 (2006).
- Lambert, C., et al. A Predatory Patchwork: Membrane and Surface Structures of Bdellovibrio bacteriovorus. Advances in Microbial Physiology. 54, 313-361 (2008).
- Makowski, &. #. 3. 2. 1. ;., et al. Initiation of Chromosomal Replication in Predatory Bacterium Bdellovibrio bacteriovorus. Frontiers in Microbiology. 7, 1898 (2016).
- Makowski, &. #. 3. 2. 1. ;., et al. Dynamics of Chromosome Replication and Its Relationship to Predatory Attack Lifestyles in Bdellovibrio bacteriovorus. Applied and Environmental Microbiology. 85 (14), (2019).
- Fenton, A. K., Kanna, M., Woods, R. D., Aizawa, S. I., Sockett, R. E. Shadowing the actions of a predator: backlit fluorescent microscopy reveals synchronous nonbinary septation of predatory Bdellovibrio inside prey and exit through discrete bdelloplast pores. Journal of Bacteriology. 192 (24), 6329-6335 (2010).
- Kuru, E., et al. Fluorescent D-amino-acids reveal bi-cellular cell wall modifications important for Bdellovibrio bacteriovorus predation. Nature Microbiology. 2 (12), 1648-1657 (2017).
- Dashiff, A., Junka, R. A., Libera, M., Kadouri, D. E. Predation of human pathogens by the predatory bacteria Micavibrio aeruginosavorus and Bdellovibrio bacteriovorus. Journal of Applied Microbiology. 110 (2), 431-444 (2011).

