연속 결정학 실험을 위한 Endothiapepsin 결정의 성장 최적화
Summary
이 기사의 목적은 시청자에게 대규모 단일 단백질 결정을 성장시키기 위한 소량의 증기 확산 프로토콜을 직렬 결정학을 위한 대용량 배치 미세 결정화 방법으로 변환하는 방법에 대한 확실한 이해를 제공하는 것입니다.
Abstract
여기서는 싱크로트론과 XFEL 모두에서 연속 결정학 실험에 적합한 대용량(> 100μL)의 미세 결정질 슬러리를 쉽게 생성할 수 있는 프로토콜이 제시됩니다. 이 방법은 단백질 결정상 다이어그램에 대한 이해와 그 지식을 활용할 수 있는 방법을 기반으로 합니다. 이 방법은 (1) 결정 형태 최적화, (2) 배치로의 전환 및 (3) 스케일링의 세 단계로 나뉩니다. 1단계는 큐브와 같은 형태로 나타나는 잘 회절되는 단결정을 찾는 것입니다. 2단계에서 1단계 조건은 결정 성장 시간에 의해 최적화됩니다. 이 전략은 증기 확산에 의해 성장된 결정을 배치로 변환할 수 있습니다. 약 24시간 이내에 결정 성장이 발생할 수 있게 되면 단백질과 침전제 혼합물의 형태도를 플롯하여 스케일링 전략의 기초로 사용할 수 있습니다(3단계). 결정을 일괄적으로 성장시킬 수 있는 경우 스케일링을 시도할 수 있으며 부피가 증가함에 따라 결정 크기와 농도가 최적화됩니다. 엔도티아펩신은 이 프로토콜의 시연 단백질로 사용되었습니다. 제시된 결정 중 일부는 엔도티아펩신과 관련이 있습니다. 그러나 그들이 적용된 방식이 다른 사람들이 자신의 프로젝트에 적응할 수 있도록 이 절차에 대한 사고 방식에 영감을 주기를 바랍니다.
Introduction
실온(RT) 고분자 결정학은 구조 생물학 커뮤니티에서 다시 인기를 얻고 있습니다. X선 자유 전자 레이저(XFEL) 광원의 개발은 RT 샘플 전달 접근법 1,2,3,4의 개발에 박차를 가했으며, 이러한 방법은 현재 싱크로트론(5,6,7,8)에 적용되었습니다. RT 방법은 펌프 프로브 실험 구조 9,10,11,12의 가능성을 열어줄 뿐만 아니라 단백질 13,14,15,16,17 내에서 대체 구조적 상태를 촉진한다는 증거도 있습니다.
그러나 1990년대 후반에 극저온 방식이 RT 접근 방식보다 주목을 받은 주된 이유는 영하의 결정 온도18에 의한 방사선 손상의 둔화였습니다. Cryo-methods19는 단일 단백질 결정으로부터 완전한 데이터 세트의 수집을 허용하기 시작했다. XFEL 및 싱크로트론의 최신 RT 방법은 신속한(> 100Hz) 결정 전달 전략 1,2,3,4의 개발로 단결정 방사선 손상 문제를 해결했습니다. 이러한 방법을 사용하면 개별적으로 노출된 수천 개의 결정에서 완전한 데이터 세트를 수집할 수 있습니다. 따라서 이러한 RT 전달 접근법은 균질한 미세 결정(> 100μL의 < 50μm 결정)을 포함하는 대량의 용액을 생산해야 합니다. 그러나 극저온 방법은 단결정만 필요로 하는 경향이 있기 때문에 이러한 미세 결정질 슬러리를 만드는 방법은 현재 단백질 결정학 실험실에서 보편화되지 않았습니다.
일련의 결정학 샘플에 대한 미세 결정화 최적화 절차의 일부를 수행하는 방법에 대한 문헌의 예가 있습니다. 여기서 막 단백질과 가용성 단백질을 구별해야 합니다. 지질 입방상(LCP)에 대해 모노올레인(또는 일부 다른 지질)에서 성장한 미세막 단백질 결정의 성장을 최적화하기 위한 프로토콜이 잘 설명되었습니다20,21,22. 그러나, 비-LCP 조건에서 성장한 막 단백질을 포함하는 가용성 단백질의 미세결정화를 위한 방법은 일반적으로 결여되어 있다. 이전의 연구들은 미세 결정 스크리닝(micro-crystal screening)23,24, 핵형성강화(enhancement nucleation)24, 자유 계면 확산(free-interface diffusion)25을 이용한 스케일링(scaling)과 같은 과정의 특정 부분에 초점을 맞추었지만, 완전한 방법은 아니었다.
그러나, 완전한 프로토콜을 제공하려고 시도하는 방법이 최근에 기술되었다(26 ). 단백질 결정학의 여러 측면과 마찬가지로 새로운 것은 아닙니다. 제안 된 아이디어 중 많은 부분이 이미 Rayment (2002) 27에 의해 설명되었습니다. 이 방법은 결정학자에게 증기 확산을 사용하여 성장한 단일 결정에서 수천 개의 미세 결정을 성장시키는 배치 방법론으로 변환하는 방법을 보여주는 것을 목표로 합니다. 이 방법은 모든 단백질 데이터 뱅크(PDB) 증착의 95%가 증기 확산 플레이트에서 성장한 결정에서 나오기 때문에 일반적인 출발점으로 증기 확산에 초점을 맞춥니다26. 그러나, 증기 확산은 미세-결정화(26)를 위한 이상적인 방법이 아니므로, 증기 확산을 배치 결정화로 전환시키는 방법론이 설명된다. 결정을 일괄적으로 성장시킬 수 있게 되면 경로를 더 큰 볼륨으로 확장하는 것이 더 실용적이 됩니다. 단백질 결정화의 모호함을 감안할 때 저자는 이 방법이 안전하지 않다고 강조할 것입니다. 그러나 프로토콜은 적어도 단백질의 ‘결정화 공간’에 대한 통찰력을 제공해야 합니다.
이 방법은 단백질 결정화 단계 다이어그램과 해당 다이어그램에 대한 이해가 미세 결정화 최적화 중에 가이드 역할을 할 수 있는 방법에 의존합니다. 단백질 위상 다이어그램은 일반적으로 x축과 y축에 각각 침전제 및 단백질 농도가 있는 x/y 플롯으로 표시됩니다(그림 1A). 순수한 물 지점(왼쪽 하단 모서리 – 그림 1A)에서 용해도 라인에 도달할 때까지 단백질과 침전제의 농도가 증가합니다. 용해도 선은 과포화 지점을 표시합니다(보라색 선 – 그림 1A). 단백질이 과포화되면 용액은 열역학적으로 불안정해지고 ‘단백질이 풍부한’ 용액과 안정적인 포화 용액의 두 단계로 분리되기 시작합니다. 이러한 분리는 용해도 선을 넘어 어디에서나 발생할 수 있으며 그 동역학은 단백질의 특성과 용액의 성분에 따라 달라집니다.
단백질과 침전제 농도가 너무 높으면 단백질이 용액에서 불안정하게 분해되어 비정질 침전물이 생성됩니다(분홍색 영역 – 그림 1A). 그러나, 정렬된 상 분리는 핵형성 영역에서 발생할 수 있으며[자세한 설명은 Garcia-Ruiz (2003)28 참조] 결정 핵은 형성되는 경향이 있다(녹색 영역 – 그림 1A). 핵 형성 및 성장은 용액에서 단백질을 제거하고 용해도 라인에 도달할 때까지 성장이 계속될 수 있는 준안정 영역으로 방울을 이동시킵니다[자세한 논의는 McPherson and Kuznetsov (2014)29 참조]. 이 다이어그램은, 대다수의 결정화 조건들에 대해, 총체적인 과잉 단순화(30)이다. 그러나 이것에도 불구하고, 다이어그램의 매핑을 통해 용해도 선과 핵 형성 동역학을 결정할 수 있기 때문에 다이어그램은 여전히 미세 결정학자에게 큰 유용합니다.
미세 결정을 생성하는 측면에서 결정화 중 최적화해야 하는 두 가지 요소는 결정의 수(Xn)와 평균, 가장 긴 치수(Xs)입니다. Xn 은 핵형성 사건의 수 (n)에 비례할 것이다 (식 1).
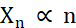 식 1
식 1
Xs는 용해도선 위의 유리 단백질 농도(Ps)를Xn으로 나눈 값에 비례한다(식 2).
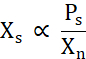 식 2
식 2
완벽한 상황에서, 모든 핵 형성 사건은 가능한 결정을 생성 할 것이고, 이들 결정들 각각은 용액에서 이용 가능한 단백질에 동등하게 접근 할 것이다. 도 2 는Xn 과Xs 사이의 관계에 대한 이상적인 시나리오로부터의 그래픽 표현이다. 실제적으로, 결정학자가Xn 및Xs 에 대해 갖는 주요 제어는 핵 형성의 양에 영향을 미치거나 종자 결정의 첨가에 의한 것입니다. 미세 결정학자는 적절한 결정 농도와 결정 크기가 모두 생성될 수 있도록Xn 을 증가시키는 방법을 판단해야 합니다.
대부분의 결정화 기술에는 ‘과도기’가 필요합니다(그림 1B). 예를 들어, 증기 확산 실험에서 단백질과 침전제 용액을 혼합할 때 방울이 웰 용액과 평형을 이루면서 각각의 농도가 변경됩니다. 이러한 변화가 결정화 성향이 증가하는 핵 형성 영역으로 점진적으로 전환되기를 희망합니다. 결정이 핵을 형성하고 성장하기 시작하면 용액에 있는 단백질의 양이 감소하기 시작하여 추가 핵 형성 가능성이 감소합니다. 핵형성의 궁극적인 양은 단백질 및 상태에 따라 다르며, 또한 핵형성 영역으로의 침투 깊이에 따라 달라집니다. 과도기적 단계를 필요로 하는 방법들의 제한된 핵형성 영역 침투를 감안할 때, 핵형성의 수준은 궁극적으로 준안정-핵형성 영역 경계에서의 핵형성 속도로 제한될 것이다.
미세 결정학자의 핵형성 수준을 향상시킬 수 있는 것이 중요하기 때문에 배치 결정화 방법론으로 이동하는 것이 중요합니다. 배치는 전체 핵형성 영역을 더 잘 활용할 수 있습니다(그림 1C). 배치 방법에서 아이디어는 단백질과 침전제를 함께 혼합하여 성분 농도의 변화 없이 과포화 용액이 생성되도록 하는 것입니다. 핵 형성은 혼합 즉시 가능해야 합니다. 따라서 배치 방법은 전체 핵 형성 영역에 이론적으로 도달 할 수 있습니다. 이어서, 준안정-핵형성 경계를 넘어서는 핵형성 동역학의 임의의 증가가 이용될 수 있다.
기저 수준의 결정 핵형성이 큰Xn을 생성하기에 충분하지 않은 경우, 마이크로시딩 방법을 사용할 수 있습니다. 미세-시딩에서, 미리 성장된 결정은 새로운 결정 성장을 위한 스캐폴드로서 작용할 수 있는 결정질 단편의 슬러리를 생성하기 위해 분해된다31,32. 마이크로 시딩은 결정 핵 형성을 증가시킬 필요 없이Xn을 증가시키는 방법으로서 일련의 결정학적 샘플 준비에 널리 사용되어 왔습니다(그림 1C).
증기 확산에서 배치로의 전환은 실험 시작점을 비과포화 또는 준안정 영역에서 핵 형성 영역으로 이동하는 것으로 위상 다이어그램에서 시각화할 수 있습니다. 이는 단백질 및/또는 침전제 농도 및/또는 방울 내 둘의 비율을 증가시키고(그림 1D) 어떤 조건에서 빠르게 나타나는 결정을 생성하는지 관찰함으로써 수행할 수 있습니다(< 24시간)26. 완전한 증기 확산 방울 평형은 며칠 또는 몇 주가 걸릴 수 있다33. 따라서 빠르게 나타나는 결정을 나타내는 조건을 찾으면 마이크로 배치34,35,36,37과 같은 대체 결정화 스크리닝 형식으로 이동하지 않고도 배치 조건을 찾을 수 있습니다.
핵 형성 영역이 발견되면 배치 조건이 발견되고 형태소도(여기서는 대략적인 위상 다이어그램)를 생성할 수 있습니다. 형태소도는 시드 배치 또는 직선 배치 프로토콜을 사용할지 여부를 고려할 때 매우 유용합니다. Xn을 단백질 및 침전제 농도의 함수로서 플롯함으로써, 핵형성 동역학의 평가가 이루어질 수 있다26. X n이 전체 핵 형성 영역에 걸쳐 낮게 유지되는 경우, 시드 배치는 Xn을 결정 성장을 제한하기에 충분히 크게 만드는 것이 필요할 수 있습니다. 이 평가는 더 큰 용량(> 100μL)으로 확장하는 프로세스의 첫 번째 단계입니다.
이 방법은 표준 증기 확산 결정화 장비를 사용하여 대부분의 결정화 실험실에서 수행 할 수 있도록 설계되었습니다. 장비를 사용할 수 있는 경우 이 프로세스의 많은 부분을 용이하게 하는 기술을 설명하는 많은 연구도 수행되었습니다. 여기에는 동적 광 산란(DLS)25,27, 비선형 이미징 20,24,25, 분말 회절 20,24,27 및 전자 현미경 26이 포함되지만 이에 국한되지는 않습니다[좋은 검토를 위해 Cheng et al. (2020)40].
이 연구의 목적은 소량( 100μL) 배치 결정화로 전환하는 방법의 시각적 시연을 제공하는 것입니다. Cryphonectria parasitica 의 엔도티아펩신은 이 번역을 시연하기 위한 예제 시스템으로 사용되었습니다. 실험의 유형 및 미세 결정이 필요한 샘플 전달 방법은 이상적인Xs 출력(26)에 영향을 미칠 것이다. 밀리초 시간 분해능(41 ) 또는 기체-역학적 가상 노즐(42)을 필요로 하는 혼합 실험의 경우, < 5 μm의 최종Xs 가 바람직할 수 있다. 이 경우 목표는 광자 활성화 펌프 프로브 실험을 위해 고정 표적 전달 접근법을 사용하여 약 1.5Å로 회절되는 단백질 결정을 생성하는 것이었습니다.
엔도티아펩신을 사용한 이러한 일련의 결정학 실험의 샘플 요구 사항을 설명하기 위해, 표 1 은 가설 실험의 실험 파라미터를 나타낸다. 샘플 정보는 아래에 설명된 프로토콜을 기반으로 합니다. 적중률 및 데이터 수집 요구 사항에 대한 일부 보수적인 추정치를 감안할 때 50mg은 전체 실험에 대한 총 샘플 소비량 추정치입니다.
그림 3 은 초기 소량 증기 확산 결정화에서 대규모 배치에 이르는 전체 최적화 프로세스의 흐름도를 보여줍니다. 대부분의 직렬 결정학 프로젝트의 경우, 이 프로토콜은 표적 단백질이 이미 결정화되었기 때문에 2단계: ‘배치로 전환’에서 시작됩니다. 그러나 1단계는 완전성과 독자들에게 그 중요성을 상기시키기 위해 포함되었습니다. 잘 회절되는 단일, 큰 결정을 발생시키는 조건을 찾는 것이 미세 결정 최적화를 위한 가장 좋은 출발점입니다. 2단계에서, 이 조건은 증기 확산에서 배치로 최적화될 수 있으며, 핵 형성 및 준안정 영역의 형태 그램이 플롯될 수 있습니다. 이 작업이 완료되면 3단계에서 배치 조건을 더 큰 볼륨으로 확장할 수 있습니다. 순서도가 끝날 때까지 결정학자는 엔도티아펩신에 대한 반복 가능한 대용량(> 100μL), 미세 결정화, 배치 프로토콜을 생성하게 됩니다. 이 방법은 관심있는 특정 단백질에 적용될 수 있습니다.
Protocol
Representative Results
Discussion
제시된 방법은 희소 매트릭스 96웰 스크린에서 성장한 큰 결정(≥ 100μm 가장 긴 치수)에서 배치를 통해 원심분리기 튜브(300μL 부피)에서 성장한 미세 결정까지 엔도티아펩신의 결정화를 최적화하는 방법을 보여줍니다. 이 프로토콜의 이면에 있는 아이디어는 엔도티아펩신을 최적화하기 위해 취한 단계가 다른 단백질에도 사용될 수 있다는 것입니다. 궁극적으로, XFEL 및 싱크로트론에서 연속 결정학 실험을 위해 대량(>100μL)의 미세 결정(10-20μm)을 생성하는 문제에 답합니다.
이 프로토콜은 대용량 미세 결정화 작업을 (1) 결정 형태 최적화, (2) 배치로의 전환 및 (3) 스케일링의 세 단계로 나눕니다. 1단계에서는 단백질이 생성할 수 있는 결정 형태의 범위를 증기 확산판에서 탐색해야 합니다. 필요한 분해능으로 회절하는 단일 상자형 결정을 생성하는 조건이 목표가 되어야 합니다. 2단계에서 선택한 조건을 증기 확산에서 배치로 변환할 수 있습니다. 여기서, 최적화 기준은 결정 성장 시간 및 24시간 이내에 단백질 결정을 발생시키는 조건을 찾는 것이다. 형태소도는 또한 실험자에게 용해도 선과 핵 형성 영역 경계의 위치에 대한 아이디어를 제공할 수 있습니다. 이 형태소도는 3단계, 스케일링에서 매우 유용합니다. 형태도는 핵 형성만으로도Xn 을 증가시키고Xs를 감소시킬 수 있는지 여부를 나타냅니다. 실험의 부피가 증가함에 따라,Xn 및Xs 는 스케일링 성공의 핵심 기준으로서 연속적으로 평가될 수 있다.
엔도티아펩신의 경우, 1단계에서는 엔도티아펩신에 대해 이전에 알려지지 않은 결정 형태가 무엇인지 발굴했습니다. 이 형태는 이전에 보고된 것과 동일한 공간군을 가졌지만 중요한 것은 직렬 결정학의 경우 더 상자와 같은 모양이었습니다. 단결정은 또한 다른 조건에서 생성된 팬과 달리 단일 핵 형성 지점에서 성장하는 것처럼 보였습니다(그림 4). 선택된 조건에 대해, 단계 2는 < 24 h에서 결정 성장이 발생함에 따라 이미 부분적으로 만족되었다. 형태소도는 3단계에서 스케일링할 때 직선 또는 시드 배치 프로토콜이 모두 성공할 수 있음을 나타냅니다. 직선 배치의 초기 스케일링은 각각 3.6 ± 1.2 x 106 결정·mL-1 및 42 ± 4.1μm의 Xn 및 Xs 범위를 갖는 결정을 생성하는 조건을 생성했습니다. 이러한 결정은 일부 연속 결정학 실험에 적합하지만 너무 큰 것으로 간주되었습니다. 따라서 추가 최적화가 수행되었습니다. 최종 프로토콜은 각각 3.1 x 106 결정·mL-1 및 15 ± 3.9μm의 농도 및 크기 범위를 가진 결정을 생성했습니다. 이것은 계획된 실험에 이상적이었습니다.
이 방법은 증기 확산 플레이트에서 성장한 ‘용해성’ 단백질 결정을 배치로 변환하는 데 중점을 둡니다. 이렇게 초점을 맞추는 이유는 대부분의 가용성 단백질 결정이 증기 확산을 통해 성장하기 때문이다26. 그러나 제시된 개념은 마이크로 배치와 같은 다른 방법을 사용하여 성장한 가용성 단백질 결정에도 적용될 수 있습니다. 이 개념은 LCP에서 성장한 막 단백질 결정에도 적용할 수 있습니다. 이것 역시 배치 결정화 과정이기 때문입니다.
프로토콜의 주요 측면은 증기 확산 플레이트에서 성장한 결정의 조건을 일괄적으로 성장할 수 있도록 변환하는 과정입니다. 이 변환을 위해 이 방법은 Beale et al. (2019)26. 증기 확산 플레이트에서도 배치 공정을 통해 성장한 결정은 빠르게 형성됩니다(< 24시간). 이 기준은 증기 확산 낙하 평형 속도를 기반으로 한 근사치이며 PEG 기반 침전제 조건에 가장 적합합니다. 그러나, 결정화 조건은 평형 시간에 영향을 미칠 매우 다양한 화합물을 함유할 것이다. 염 기반 결정화 조건(예: 고농축 염화암모늄)의 평형은 1-2일 내에 발생할 수 있습니다. 따라서 24시간 기준은 염분 기반 조건에서는 사실이 아닐 수 있습니다. 염-기반 조건들은 또한 이 프로토콜에 제시된 원형에 부합하지 않을 수 있는 더 복잡한 위상 다이어그램들(26, 30)을 가질 수 있다. 더 큰 볼륨으로 스케일링하는 것이 불가능한 것으로 판명되면 소금 기반 조건에 대한 시간 기준을 12시간 또는 6시간으로 줄여야 할 수 있습니다.
이 방법의 또 다른 한계는 명백한 복잡성입니다. 엔도티아펩신의 미세 결정화를 최적화하기 위해 따랐던 프로토콜은 실제로 희소 매트릭스 스크린에서 원래 조건을 상대적으로 거의 변경하지 않았습니다. PACT 스크린에서 관찰된 첫 번째 히트는 0.1 HEPES pH 7.0, 0.2 MMgCl2 및 20%(w/v) PEG 6,000이었다. 최종 스케일링된 결정화 완충액은 0.1 Tris-HCl pH 7.0, 0.15 MMgCl2 및 40%(w/v) PEG 6,000이었다. 또한 HEPES에서 Tris-HCl 및 MgCl2 농도로의 완충액 변화가 공정의 성공에 거의 기여하지 않았을 가능성이 매우 높습니다. PEG 6,000 농도의 증가를 유일한 최적화로 남겨두고 아주 간단하게 달성할 수 있었습니다.
그러나 이 평가는 너무 단순합니다. 스케일링 중에 발생하는 문제(즉, 종자 사용 및 담금질)를 할인할 뿐만 아니라 이 단백질이 간단하다는 것이 입증되었기 때문에 다음 단백질도 입증될 것이라는 보장이 없다는 사실도 할인합니다. 프로토콜에서 권고된 단계는 단백질 결정화 부피의 스케일링을 최적화하는 것이 매우 단백질 비용이 많이 들 수 있기 때문에 고안되었습니다. 제시된 7번의 엔도티아펩신 스케일링 시험에서 100mg의 단백질이 소비되었습니다. 틀림없이 이러한 단계 중 일부는 이 프로토콜에 비추어 그 결과를 보여주기 위해 수행되었습니다. 그럼에도 불구하고 단백질 100mg과 실험 중에 소비되는 단백질에 대해 잠재적으로 50mg을 추가로 섭취하는 경우(표 1)는 시간이나 비용에 상당한 투자가 될 수 있습니다.
다행스럽게도 이 대량의 필수 샘플이 모든 단백질에 걸쳐 어디에나 있다는 것은 분명하지 않습니다. 엔도티아펩신은 용해성이 높았기 때문에 과포화에 도달하기 위해 큰 단백질 농도가 필요했습니다. 다른 경우(현재 최적화 중) 과포화는 10 또는 5mg/mL에서 도달할 수 있습니다. 이러한 변수는 단백질에 따라 다르며 나타날 때 수용해야 합니다.
이 방법의 다른 한계로는 스크린 및 플레이트 생성을 위한 액체 처리 로봇과 필요할 때 플레이트를 자동으로 이미지화하는 이미저와 같은 복잡한 장비에 대한 의존도가 있습니다. 이러한 장비 중 일부의 필요성을 제한하기 위해 대체 루틴이 제공되었지만 프로토콜이 없으면 따르는 데 더 많은 시간이 소요됩니다. 이 프로토콜은 또한 최적화된 결정의 회절 테스트를 제안합니다. 싱크로트론에 정기적으로 접근할 수 없는 결정학자의 경우 이러한 테스트는 어려울 수 있습니다. 모든 단계에서 제어가 필요한 것은 아니지만 적중이 식별되고 사전 및 사후에 이러한 테스트를 수행하는 것이 좋습니다. 안타깝게도 XFEL에서 회절하지 않는 결정은 드문 일이 아닙니다. 이를 감안할 때 결정 회절에 대한 가정에 대해 주의를 기울이는 것이 좋습니다.
궁극적으로, 여기에 제시된 이 프로토콜과 결과는 일련의 결정학 실험을 위한 샘플 생산에 어려움을 겪고 있는 사람들에게 가이드, 아이디어 및 예를 제공할 것입니다. 바라건대, 직렬 결정학이 추가로 개발됨에 따라 기술의 샘플 요구가 줄어들어 이와 같은 프로토콜의 필요성이 줄어들 것입니다. 그러나 이 경우에도 여기에 제시된 전략은 단백질의 결정화 공간을 탐색하려는 사람들에게 여전히 유용할 것입니다.
Disclosures
The authors have nothing to disclose.
Acknowledgements
이 프로젝트는 Marie Skłodowska-Curie 보조금 계약 No 701647에 따라 유럽 연합의 Horizon 2020 연구 및 혁신 프로그램으로부터 자금을 받았습니다. Swiss Light Source beamline X10SA-PXII의 빔라인 과학자들의 도움과 지원에 깊은 감사를 드립니다.
Materials
| Swissci 96-well 2-Drop plates | Molecular Dimensions | MD11-002 | 96-well 2-drop crystallisation plate |
| Swissci 96-well 3-Drop plates | Molecular Dimensions | MD11-003 | 96-well 3-drop crystallisation plate |
| mosquito LCP liquid handling robot | sptlabtech | mosquito LCP | Crystallisation robot |
| ClearVue Sheets | Molecular Dimensions | MD6-015 | 96-well crystallization plate seals |
| Safe-Tube 1.5 mL | Eppendorf | 30120086 | 1.5 mL centrifuge tubes |
| Scaple | Swan and Morton | No. 3 scalple and No. 3 handle | Scalple for cutting open plate seals |
| MS 3 Vortex | IKA | 3319000 | Vortex for mixing solution and making seed stocks |
| 24-well XRL Plate | Molecular Dimensions | MD3-11 | 24-well hanging-drop plates |
| Tube revolver/rotator | Thermo Fischer Scientific | 88881001 | Tube revolver for mixing solution during scaling |
| Eppendorf Research plus pipettes | Eppendorf | Range of manual pipettes, 0.5-10, 1-20, 10-100, 100-1000 µL | |
| Eppendorf pipette tips | Eppendorf | Range of tip sizes for manual pipettes | |
| Suparen 600 | Prochem AG | Suparen 600 | Endothiapepsin solution |
| Sodium Acetate | Sigma-Aldrich | 241245-1KG | Sodium Acetate |
| Tris | Merck | 8382T014 | Tris |
| Magnesium Chloride | Sigma-Aldrich | M2670-1kg | Magnesium Chloride |
| PEG 6,000 | Sigma-Aldrich | 81255-1kg | PEG 6,000 |
| Ethelyene glycol | Sigma-Aldrich | 324558-1L | Ethelyene glycol for cyro-protecting the crystals |
| PACT Premier HT screen | Molecular Dimensions | MD1-36 | PACT Premier 96-well crystal screen |
| DOW CORNING high vacuum grease | Molecular Dimensions | MD6-02 | Grease for sealing 24-well plates |
| Hirschmann 22 x 22 mm glaser cover slides | Hirschmann | 8000104 | Cover slides for sealing 24-well sitting drop plates |
| Crystal pins | PSI | Manufactured inhouse | Thin-film supports for micro-crystals. |
| 1-1.3 mm SiLibeads Type S | Faust | 6239547 | Glass beads for making mico-seed stocks |
| Macbook Pro | Apple | Macbook Pro | Computer for performing data analysis |
| CCP4 software suite | CCP4 | Diffraction pattern data processing software | |
| Excel | Microsoft | Microsoft Office | Plotting tool for phase diagram |
| Hausser Scientific Bright-Line counting chamber | Thermo Fischer Scientific | 02-671-51B | Tool to calculate crystal concentration |
| PACT Premier | Molecular Dimensions | MD1-29-ECO | Sparse-matrix crystallization screen |
| Rock Imager | Formulatrix | Rock Imager | Temperature controlled crystal plate storage and imager |
| Rock MakerWeb | Formulatrix | Rock MakerWeb | Crystal plate creation and image storage stoftware |
| Formulator | Formulatrix | Formulator | 96-well crystal screen creation liquid handling robot |
| Leica MZ16 Microscope | Leica | Leica MZ16 | Light microscope |
| LAS V4.6 | Leica | LAS V4.6 | Software for Leica microscopes |
| Spectra/Por 3.5 kDa dialysis tubing | Spectrumlabs | Spectra/Por 3 Dialysis Membrane | 3.5 kDa dialysis membrane |
| Dialysis tubing closures | Spectrumlabs | Spectra/Por 3 Duniversal Closures | Clips to seal the dialysis tubing ends |
| Amicon 10 kDa centrifugal concentrator | Merck-Millipore | Amicon Ultra-15 10 kDa centrifugal concentrator | 10 kDa centrifugal filter |
| 5810 R swing bucket centrifuge | Eppendorf | 5810 R Centrifuge | Swing bucket centrifuge |
References
- DePonte, D. P., et al. Gas dynamic virtual nozzle for generation of microscopic droplet streams. Journal of Physics D: Applied Physics. 41 (19), 195505 (2008).
- Hunter, M. S., et al. Fixed-target protein serial microcrystallography with an x-ray free electron laser. Scientific Reports. 4 (1), 6026 (2014).
- Weierstall, U., et al. Lipidic cubic phase injector facilitates membrane protein serial femtosecond crystallography. Nature Communications. 5 (1), 1-6 (2014).
- Roessler, C. G. G., et al. Acoustic Injectors for Drop-On-Demand Serial Femtosecond Crystallography. Structure. 24 (4), 631-640 (2016).
- Sherrell, D. A., et al. A modular and compact portable mini-endstation for high-precision, high-speed fixed target serial crystallography at FEL and synchrotron sources. Journal of Synchrotron Radiation. 22 (6), 1372-1378 (2015).
- Roedig, P., et al. A micro-patterned silicon chip as sample holder for macromolecular crystallography experiments with minimal background scattering. Scientific Reports. 5 (1), 1-11 (2015).
- Botha, S., et al. Room-temperature serial crystallography at synchrotron X-ray sources using slowly flowing free-standing high-viscosity microstreams. Acta Crystallographica Section D Biological Crystallography. 71 (2), 387-397 (2015).
- Weinert, T., et al. Serial millisecond crystallography for routine room-temperature structure determination at synchrotrons. Nature Communications. 8 (1), 542 (2017).
- Tenboer, J., et al. Time-resolved serial crystallography captures high-resolution intermediates of photoactive yellow protein. Science. 346 (6214), 1242-1246 (2014).
- Nango, E., et al. A three-dimensionalmovie of structural changes in bacteriorhodopsin. Science. 354 (6319), 1552-1557 (2016).
- Suga, M., et al. Light-induced structural changes and the site of O=O bond formation in PSII caught by XFEL. Nature. 543 (7643), 131-135 (2017).
- Mehrabi, P., et al. Liquid application method for time-resolved analyses by serial synchrotron crystallography. Nature Methods. 16 (10), 979-982 (2019).
- Halle, B. Biomolecular cryocrystallography: structural changes during flash-cooling. Proceedings of the National Academy of Sciences of the United States of America. 101 (14), 4793-4798 (2004).
- Fraser, J. S., et al. Hidden alternative structures of proline isomerase essential for catalysis. Nature. 462 (7273), 669-673 (2009).
- Fenwick, R. B., van den Bedem, H., Fraser, J. S., Wright, P. E. Integrated description of protein dynamics from room-temperature X-ray crystallography and NMR. Proceedings of the National Academy of Sciences of the United States of America. 111 (4), 445-454 (2014).
- Keedy, D. A., et al. Mapping the conformational landscape of a dynamic enzyme by multitemperature and XFEL crystallography. Elife. 4, (2015).
- Thomaston, J. L., et al. XFEL structures of the influenza M2 proton channel: Room temperature water networks and insights into proton conduction. Proceedings of the National Academy of Sciences of the United States of America. 114 (51), 13357-13362 (2017).
- Haas, D. J., Rossmann, M. G. Crystallographic studies on lactate dehydrogenase at -75 °C. Acta Crystallographica Section B Structural Crystallography and Crystal Chemistry. 26 (7), 998-1004 (1970).
- Hope, H. Cryocrystallography of biological macromolecules: a generally applicable method. Acta Crystallographica Section B Structural Science. 44 (1), 22-26 (1988).
- Wu, W., et al. Batch crystallization of rhodopsin for structural dynamics using an X-ray free-electron laser. Acta Crystallographica Section:F Structural Biology Communications. 71 (7), 856-860 (2015).
- Ishchenko, A., Cherezov, V., Liu, W. Preparation and delivery of protein microcrystals in lipidic cubic phase for serial femtosecond crystallography. Journal of Visualized Experiments. (115), e54463 (2016).
- Andersson, R., et al. Well-based crystallization of lipidic cubic phase microcrystals for serial X-ray crystallography experiments. Acta Crystallographica Section D: Structural Biology. 75 (10), 937-946 (2019).
- Luft, J. R., et al. The detection and subsequent volume optimization of biological nanocrystals. Structural Dynamics. 2 (4), 041710 (2015).
- Lee, D. B., et al. Supersaturation-controlled microcrystallization and visualization analysis for serial femtosecond crystallography. Scientific Reports. 8 (1), 1-10 (2018).
- Kupitz, C., et al. Microcrystallization techniques for serial femtosecond crystallography using photosystem II from Thermosynechococcus elongatus as a model system. Philosophical transactions of the Royal Society of London. Series B, Biological Sciences. 369 (1647), 20130316 (2014).
- Beale, J. H., et al. Successful sample preparation for serial crystallography experiments. Journal of Applied Crystallography. 52, 1385-1396 (2019).
- Rayment, I. Small-scale batch crystallization of proteins revisited: An underutilized way to grow large protein crystals. Structure. 10 (2), 147-151 (2002).
- García-Ruiz, J. M. Nucleation of protein crystals. Journal of Structural Biology. 142 (1), 22-31 (2003).
- McPherson, A., Kuznetsov, Y. G. Mechanisms, kinetics, impurities and defects: Consequences in macromolecular crystallization. Acta Crystallographica Section F:Structural Biology Communications. 70 (4), 384-403 (2014).
- Rupp, B. Origin and use of crystallization phase diagrams. Acta crystallographica. Section F, Structural biology communications. 71, 247-260 (2015).
- Luft, J. R., DeTitta, G. T. A method to produce microseed stock for use in the crystallization of biological macromolecules. Acta Crystallographica Section D Biological Crystallography. 55 (5), 988-993 (1999).
- Ireton, G. C., Stoddard, B. L. Microseed matrix screening to improve crystals of yeast cytosine deaminase. Acta crystallographica. Section D, Biological crystallography. 60 (3), 601-605 (2004).
- Forsythe, E. L., Maxwell, D. L., Pusey, M. Vapor diffusion, nucleation rates and the reservoir to crystallization volume ratio. Acta Crystallographica Section D Biological Crystallography. 58 (10), 1601-1605 (2002).
- Chayen, N. E., Shaw Stewart, P. D., Maeder, D. L., Blow, D. M. IUCr An automated system for micro-batch protein crystallization and screening. Journal of Applied Crystallography. 23 (4), 297-302 (1990).
- Chayen, N. E., Shaw Stewart, P. D., Blow, D. M. Microbatch crystallization under oil – a new technique allowing many small-volume crystallization trials. Journal of Crystal Growth. 122 (1-4), 176-180 (1992).
- Chayen, N. E. Comparative studies of protein crystallization by vapour-diffusion and microbatch techniques. Acta Crystallographica Section D: Biological Crystallography. 54 (1), 8-15 (1998).
- D’Arcy, A., Mac Sweeney, A., Stihle, M., Haber, A. The advantages of using a modified microbatch method for rapid screening of protein crystallization conditions. Acta Crystallographica – Section D Biological Crystallography. 59 (2), 396-399 (2003).
- Darmanin, C., et al. Protein crystal screening and characterization for serial femtosecond nanocrystallography. Scientific Reports. 6, 25345 (2016).
- Gati, C., et al. Atomic structure of granulin determined from native nanocrystalline granulovirus using an X-ray free-electron laser. Proceedings of the National Academy of Sciences of the United States of America. 114 (9), 2247-2252 (2017).
- Cheng, R. K. Y. Towards an optimal sample delivery method for serial crystallography at XFEL. Crystals. 10 (3), 215 (2020).
- Schmidt, M. Mix and Inject: Reaction Initiation by Diffusion for Time-Resolved Macromolecular Crystallography. Advances in Condensed Matter Physics. 2013, 1-10 (2013).
- Oberthuer, D., et al. Double-flow focused liquid injector for efficient serial femtosecond crystallography. Scientific Reports. 7 (1), 44628 (2017).
- McPherson, A., Gavira, J. A. Introduction to protein crystallization. Acta crystallographica. Section F, Structural biology communications. 70, 2-20 (2014).
- Yaoi, M., et al. Effect of stirring method on protein crystallization. Japanese Journal of Applied Physics, Part 2: Letters. 43 (10), 1318 (2004).
- Castro, F., Ferreira, A., Teixeira, J. J., Rocha, F. Influence of Mixing Intensity on Lysozyme Crystallization in a Meso Oscillatory Flow Reactor. Crystal Growth & Design. 18 (10), 5940-5946 (2018).
- Moews, P. C., Bunn, C. W. An X-ray crystallographic study of the rennin-like enzyme of Endothia parasitica. Journal of Molecular Biology. 54 (2), 395-397 (1970).
- Newman, J., et al. Towards rationalization of crystallization screening for small- to medium-sized academic laboratories: the PACT/JCSG+ strategy. Acta crystallographica. Section D, Biological. 61, 1426-1431 (2005).
- Ebrahim, A., et al. Resolving polymorphs and radiation-driven effects in microcrystals using fixed-target serial synchrotron crystallography. Acta Crystallographica Section D Structural Biology. 75, 151-159 (2019).
- Davy, B., et al. Reducing sample consumption for serial crystallography using acoustic drop ejection. Journal of Synchrotron Radiation. 26 (5), (2019).

