心原性ショックに対する経皮心室補助装置/左心房から大腿動脈バイパスシステムへの使用
Summary
次の記事では、経皮的左心室補助装置(pLVAD)である心原性ショック(CS)および左心室から大腿動脈バイパス(LAFAB)システムにデバイス(タンデムハートなど)を配置するステップワイズ手順をCSで説明します。
Abstract
左心房から大腿動脈バイパス(LAFAB)システムは、左心房(LA)から血液を排出し、大腿動脈を介して全身動脈循環に戻すことによって左心室をバイパスする心原性ショック(CS)に使用される機械的循環支持(MCS)装置である。カニューレの大きさに応じて、2.5~5 L/分の範囲の流れを提供できます。ここでは、LAFABの作用機序、利用可能な臨床データ、心原性ショックにおけるその使用の適応症、移植のステップ、手続き後のケア、およびこの装置とその管理の使用に関連する合併症について議論する。
また、心エコーガイダンスの下での経皮穿刺によるデバイスの配置前準備、経皮穿刺による経皮的配置、デバイスパラメータの術後管理など、デバイス療法の手続きコンポーネントの簡単なビデオを提供します。
Introduction
心原性ショック(CS)は、心臓が身体の要求を満たすのに十分な血液と酸素を送達することができず、臓器不全をもたらす、付随する低血圧の有無にかかわらず組織低灌流の状態である。これは、心血管造影と介入の協会によってEにステージAに分類されます (SCAI): ステージ A – CS のリスクのある患者;ステージB – 低灌流のない低血圧または頻脈を有するCSの開始段階の患者;ステージC – 灌流を維持するためにイノトロープ/バソプレッサーまたは機械的サポートを必要とする寒さと湿式表現型と古典的なCS。ステージD – より高度なデバイスへのエスカレーションを必要とする現在の医療または機械的サポートで悪化。ステージE – 循環崩壊および継続的な心肺蘇生1で心停止を積極的に経験している難治性不整脈を有する患者が含まれる。CSの最も一般的な原因は、最近報告された分析で症例の81%を表す急性MI(AMI)および急性代償不全心不全(ADHF)である。CSは、混雑および灌流障害によって古典的に特徴付けられ、充填圧力の上昇(肺毛細管内挟み圧力[PCWP]、左心室末端拡張圧[LVEDP]、中央静脈圧[CVP]、および右心室終期拡張圧[RVEDP])、心拍出量の減少(CO)、心臓指数(CI)、心拍出量(CPO)、および臓器機能不全(CPO)、および終了臓器機能不全(CPO)、および終了機能障害.過去には、CSによって複雑化したAMIの唯一の利用可能な治療法は、イトロープおよび/またはバソプレッサー4による早期再生および医療管理であった。最近では、機械的循環サポート(MCS)デバイスの出現と血管圧突機のエスカレーションが死亡率の増加に関連しているという認識により、AMIおよびADHF関連CS5,6の治療にパラダイムシフトがありました。
経皮心室補助装置(pVAD)の現在の時代には、酸素化機能の有無にかかわらず、単心または二心室循環および心室のサポートを提供するMCSデバイスプラットフォーム/構成が数多く用意されています7。AMIとADHF CSの両方を治療するためのpVADの使用が着実に増加しているにもかかわらず、死亡率はほとんど変わっていません5。AMI8の左心室(LV)の早期アンロードおよびAMI CS9でのMCSの早期使用に対する可能な臨床的利益の新たな証拠により、MCSの使用は増加し続けています。
左心房から大腿動脈バイパス(LAFAB)MCS装置は、左心房(LA)から血液を排出し、大腿動脈を介して全身動脈循環に戻すことによってLVをバイパスする(図1)。これは、カンヌラのサイズに応じて、2.5-5.0リットル/分(L/m)の流量(新世代ポンプ、LifeSPARCとして指定され、最大8 L/mの流量が可能)を提供する外部遠心ポンプによって支えられている。血液が経皮静脈カニューレを介してLAから抽出されると、それは大腿動脈に置かれた動脈カニューレを介して患者の体に血液を再循環させる外部遠心ポンプを通過する。
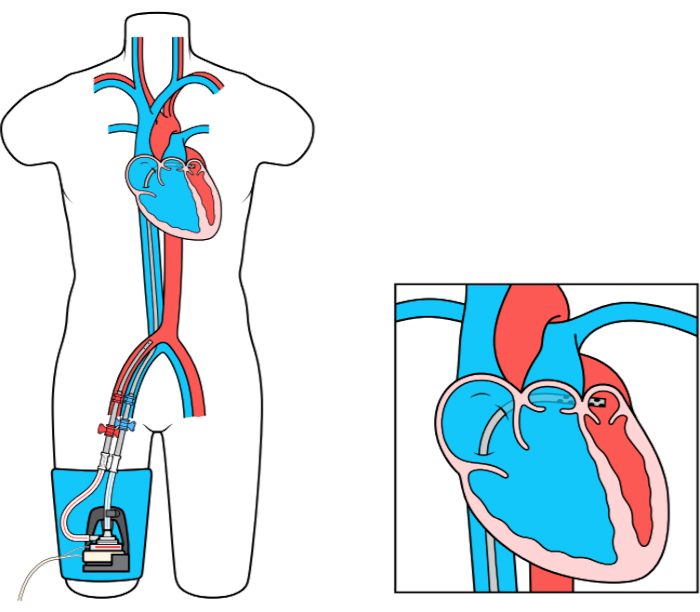
図1:LAFABのセットアップ 画像提供:LivaNova US Inc.の100%子会社であるタンデムライフは、 この図のより大きなバージョンを見るにはここをクリックしてください。
Protocol
Representative Results
Discussion
LAFABデバイスのヘモダイナミクス:
LAFABデバイスの血行性プロファイルは、他のpVADとは異なります。LAから直接血液を排出し、大腿動脈に戻すことによって、装置はLVを完全にバイパスする。その際、LV末端の拡張期容積と圧力を低減し、LV形状の改善に寄与し、LVストローク作業の低下に寄与します。しかし、腸骨動脈/下降大動脈に血液を戻すことで、後負荷が増加…
Disclosures
The authors have nothing to disclose.
Acknowledgements
ライフスパルクのタンデムハートチームへ。
Materials
| For LAFAB (TandemHeart) | |||
| Factory Supplied Equipment for circuit connections. | TandemLife | ||
| ProtekSolo 15 Fr or 17 Fr Arterial Cannula | TandemLife | ||
| ProtekSolo 62 cm or 72 cm Transseptal Cannula | TandemLife | ||
| TandemHeart Controller | TandemLife | For adjusting flows/RPM | |
| TandemHeart Pump | LifeSPARC | Centrifugal pump | |
| For RAPAB (ProtekDuo) | |||
| Factory Supplied Equipment to complete the circuit. | TandemLife | ||
| ProtekDuo 29 Fr or 31 Fr Dual Lumen Cannula | TandemLife | ||
| TandemHeart Controller | TandemLife | For adjusting flows/RPM | |
| TandemHeart Pump | LifeSPARC | Centrifugal pump |
References
- Baran, D. A., et al. SCAI clinical expert consensus statement on the classification of cardiogenic shock. Catheterization and Cardiovascular Interventions. 94 (1), 29-37 (2019).
- Harjola, V. -. P., et al. Clinical picture and risk prediction of short-term mortality in cardiogenic shock. European Journal of Heart Failure. 17 (5), 501-509 (2015).
- Furer, A., Wessler, J., Burkhoff, D. Hemodynamics of Cardiogenic Shock. Interventional Cardiology Clinics. 6 (3), 359-371 (2017).
- Hochman, J. S., et al. Cardiogenic shock complicating acute myocardial infarction–etiologies, management and outcome: a report from the SHOCK Trial Registry. SHould we emergently revascularize Occluded Coronaries for cardiogenic shocK. Journal of the American College of Cardiology. 36 (3), 1063-1070 (2000).
- Shah, M., et al. Trends in mechanical circulatory support use and hospital mortality among patients with acute myocardial infarction and non-infarction related cardiogenic shock in the United States. Clinical Research in Cardiology. 107 (4), 287-303 (2018).
- van Diepen, S., et al. Contemporary Management of Cardiogenic Shock: A Scientific Statement From the American Heart Association. Circulation. 136 (16), 232-268 (2017).
- Alkhouli, M., et al. Mechanical Circulatory Support in Patients with Cardiogenic Shock. Current Treatment Options in Cardiovascular Medicine. 22 (2), 4 (2020).
- Basir, M. B., et al. Feasibility of early mechanical circulatory support in acute myocardial infarction complicated by cardiogenic shock: The Detroit cardiogenic shock initiative. Catheterization and Cardiovascular Interventions. 91 (3), 454-461 (2018).
- Basir, M. B., et al. Improved Outcomes Associated with the use of Shock Protocols: Updates from the National Cardiogenic Shock Initiative. Catheterization and Cardiovascular Interventions. 93 (7), 1173-1183 (2019).
- Alkhouli, M., Rihal, C. S., Holmes, D. R. Transseptal Techniques for Emerging Structural Heart Interventions. JACC: Cardiovascular Interventions. 9 (24), 2465-2480 (2016).
- Dennis, C., et al. Clinical use of a cannula for left heart bypass without thoracotomy: experimental protection against fibrillation by left heart bypass. Annals of Surgery. 156 (4), 623-637 (1962).
- Dennis, C., et al. Left atrial cannulation without thoracotomy for total left heart bypass. Acta Chirurgica Scandinavica. 123, 267-279 (1962).
- Fonger, J. D., et al. Enhanced preservation of acutely ischemic myocardium with transseptal left ventricular assist. Annals of Thoracic Surgery. 57 (3), 570-575 (1994).
- Thiele, H., et al. Reversal of cardiogenic shock by percutaneous left atrial-to-femoral arterial bypass assistance. Circulation. 104 (24), 2917-2922 (2001).
- Burkhoff, D., et al. A randomized multicenter clinical study to evaluate the safety and efficacy of the TandemHeart percutaneous ventricular assist device versus conventional therapy with intraaortic balloon pumping for treatment of cardiogenic shock. American Heart Journal. 152 (3), 469 (2006).
- Thiele, H., et al. Randomized comparison of intra-aortic balloon support with a percutaneous left ventricular assist device in patients with revascularized acute myocardial infarction complicated by cardiogenic shock. European Heart Journal. 26 (13), 1276-1283 (2005).
- Gregoric, I. D., et al. TandemHeart as a rescue therapy for patients with critical aortic valve stenosis. Annals of Thoracic Surgery. 88 (6), 1822-1826 (2009).
- Kar, B., et al. The percutaneous ventricular assist device in severe refractory cardiogenic shock. Journal of the American College of Cardiology. 57 (6), 688-696 (2011).
- Patel, C. B., Alexander, K. M., Rogers, J. G. Mechanical Circulatory Support for Advanced Heart Failure. Current Treatment Options in Cardiovascular Medicine. 12 (6), 549-565 (2010).
- Tempelhof, M. W., et al. Clinical experience and patient outcomes associated with the TandemHeart percutaneous transseptal assist device among a heterogeneous patient population. Asaio Journal. 57 (4), 254-261 (2011).
- Gregoric, I. D., et al. The TandemHeart as a bridge to a long-term axial-flow left ventricular assist device (bridge to bridge). Texas Heart Institute Journal. 35 (2), 125-129 (2008).
- Bruckner, B. A., et al. Clinical experience with the TandemHeart percutaneous ventricular assist device as a bridge to cardiac transplantation. Texas Heart Institute Journal. 35 (4), 447-450 (2008).
- Agarwal, R., et al. Successful treatment of acute left ventricular assist device thrombosis and cardiogenic shock with intraventricular thrombolysis and a tandem heart. Asaio Journal. 61 (1), 98-101 (2015).
- Vetrovec, G. W. Hemodynamic Support Devices for Shock and High-Risk PCI: When and Which One. Current Cardiology Reports. 19 (10), 100 (2017).
- Al-Husami, W., et al. Single-center experience with the TandemHeart percutaneous ventricular assist device to support patients undergoing high-risk percutaneous coronary intervention. Journal of Invasive Cardiology. 20 (6), 319-322 (2008).
- Vranckx, P., et al. Clinical introduction of the Tandemheart, a percutaneous left ventricular assist device, for circulatory support during high-risk percutaneous coronary intervention. International Journal of Cardiovascular Interventions. 5 (1), 35-39 (2003).
- Vranckx, P., et al. The TandemHeart, percutaneous transseptal left ventricular assist device: a safeguard in high-risk percutaneous coronary interventions. The six-year Rotterdam experience. Euro Intervention. 4 (3), 331-337 (2008).
- Vranckx, P., et al. Assisted circulation using the TandemHeart during very high-risk PCI of the unprotected left main coronary artery in patients declined for CABG. Catheterization and Cardiovascular Interventions. 74 (2), 302-310 (2009).
- Thomas, J. L., et al. Use of a percutaneous left ventricular assist device for high-risk cardiac interventions and cardiogenic shock. Journal of Invasive Cardiology. 22 (8), 360 (2010).
- Vranckx, P., et al. Assisted circulation using the Tandemhear , percutaneous transseptal left ventricular assist device, during percutaneous aortic valve implantation: the Rotterdam experience. Euro Intervention. 5 (4), 465-469 (2009).
- Pitsis, A. A., et al. Temporary assist device for postcardiotomy cardiac failure. The Annals of Thoracic Surgery. 77 (4), 1431-1433 (2004).
- Singh, G. D., Smith, T. W., Rogers, J. H. Targeted Transseptal Access for MitraClip Percutaneous Mitral Valve Repair. Interventional Cardiology Clinics. 5 (1), 55-69 (2016).
- Subramaniam, A. V., et al. Complications of Temporary Percutaneous Mechanical Circulatory Support for Cardiogenic Shock: An Appraisal of Contemporary Literature. Cardiology and Therapy. 8 (2), 211-228 (2019).
- Morley, D., et al. Hemodynamic effects of partial ventricular support in chronic heart failure: Results of simulation validated with in vivo data. The Journal of Thoracic and Cardiovascular Surgery. 133 (1), 21-28 (2007).
- Naidu, S. S. Novel Percutaneous Cardiac Assist Devices. Circulation. 123 (5), 533-543 (2011).
- Kapur, N. K., et al. Hemodynamic Effects of Left Atrial or Left Ventricular Cannulation for Acute Circulatory Support in a Bovine Model of Left Heart Injury. ASAIO Journal. 61 (3), 301-306 (2015).
- Smith, L., et al. Outcomes of patients with cardiogenic shock treated with TandemHeart percutaneous ventricular assist device: Importance of support indication and definitive therapies as determinants of prognosis. Catheterization and Cardiovascular Interventions. 92 (6), 1173-1181 (2018).
- Ergle, K., Parto, P., Krim, S. R. Percutaneous Ventricular Assist Devices: A Novel Approach in the Management of Patients With Acute Cardiogenic Shock. The Ochsner Journal. 16 (3), 243-249 (2016).
- Sultan, I., Kilic, A., Kilic, A.Short-Term Circulatory and Right Ventricle Support in Cardiogenic Shock: Extracorporeal Membrane Oxygenation, Tandem Heart, CentriMag, and Impella. Heart Failure Clinics. 14 (4), 579-583 (2018).
- Bermudez, C., et al. . Percutaneous right ventricular support: Initial experience from the tandemheart experiences and methods (THEME) registry. , (2018).
- Aggarwal, V., Einhorn, B. N., Cohen, H. A. Current status of percutaneous right ventricular assist devices: First-in-man use of a novel dual lumen cannula. Catheterization and Cardiovascular Interventions. 88 (3), 390-396 (2016).
- Kapur, N. K., et al. Mechanical circulatory support devices for acute right ventricular failure. Circulation. 136 (3), 314-326 (2017).
- Kapur, N. K., et al. Mechanical Circulatory Support for Right Ventricular Failure. JACC: Heart Failure. 1 (2), 127-134 (2013).
- Geller, B. J., Morrow, D. A., Sobieszczyk, P. Percutaneous Right Ventricular Assist Device for Massive Pulmonary Embolism. Circulation: Cardiovascular Interventions. 5 (6), 74-75 (2013).
- Bhama, J., et al. Initial Experience with a Percutaneous Dual Lumen Single Cannula Strategy for Temporary Right Ventricular Assist Device Support Following Durable LVAD Therapy. The Journal of Heart and Lung Transplantation. 35 (4), 323 (2013).
- O’Neill, B., et al. Right ventricular hemodynamic support with the PROTEKDuo Cannula. Initial experience from the tandemheart experiences and methods (THEME) registry category. Miscellaneous. , (2018).
- O’Brien, B., et al. Fluoroscopy-free AF ablation using transesophageal echocardiography and electroanatomical mapping technology. Journal of Interventional Cardiac Electrophysiology. 50 (3), 235-244 (2017).
- O’Brien, B., et al. Transseptal puncture — Review of anatomy, techniques, complications and challenges. International Journal of Cardiology. 233, 12-22 (2017).

