Приготовление пенопластов с расширенным хитином и их использование при удалении водной меди
Summary
Это исследование описывает метод расширения хитина в пену с помощью химических методов, которые не требуют специализированного оборудования.
Abstract
Хитин является недостаточно эксплуатируемым, естественно обильным, механически прочным и химически стойким биополимером. Эти качества желательны в адсорбенте, но хитину не хватает необходимой удельной площади поверхности, а его модификация предполагает специализированные методики и оборудование. Здесь описана новая химическая процедура расширения хитиновых хлопьев, полученных из отходов скорлупы креветок, в пены с более высокой площадью поверхности. Процесс основан на эволюции газа H2 от реакцииводы с, захваченным в хитиновом геле. Способ приготовления не требует специализированного оборудования. Порошковая рентгеновская дифракция и N2-физисорбция указывают на то, что размер кристаллита уменьшается с 6,6 нм до 4,4 нм, а удельная площадь поверхности увеличивается с 12,6 ± 2,1м2/гдо 73,9 ± 0,2м2/г. Однако инфракрасная спектроскопия и термогравиметрический анализ показывают, что процесс не изменяет химическую идентичность хитина. Удельная адсорбционная способность Cu расширенного хитина увеличивается пропорционально удельной площади поверхности с 13,8 ± 2,9 мг/г до 73,1 ± 2,0 мг/г. Однако адсорбция Cu в качестве поверхностной плотности остается относительно постоянной в среднем 10,1 ± 0,8атома/нм2,что опять же говорит об отсутствии изменений в химической идентичности хитина. Этот метод предлагает средства для преобразования хитина в материал с более высокой площадью поверхности без ущерба для его желаемых свойств. Хотя хитиновая пена описывается здесь как адсорбент, ее можно представить в качестве катализаторной опоры, теплоизолятора и конструкционного материала.
Introduction
Хитин является механически прочным и химически инертным биополимером, уступая только целлюлозе в естественном изобилии1. Он является основным компонентом в экзоскелете членистоногих и в клеточных стенках грибов и дрожжей2. Хитин похож на целлюлозу, но с одной гидроксильной группой каждого мономера заменен ацетиламаминовой группой(Рисунок 1А,В). Это различие увеличивает прочность водородной связи между соседними полимерными цепями и придает хитину характерную структурную упругость и химическую инертность2,3. Благодаря своим свойствам и обилию, хитин привлек значительный промышленный и академический интерес. Он был изучен как каркас для роста тканей4,5,6,как компонент в композиционных материалах7,8,9,10,11и как опора для адсорбентов и катализаторов11,12,13,14. Его химическая стабильность, в частности, делает хитин привлекательным для адсорбционных применений, которые включают условия, негостеприимные для обычных адсорбентов14. Кроме того, обилие аминных групп делает хитин эффективным адсорбентом для ионов металлов15. Однако протонирование аминных групп в кислых условиях снижает адсорбцию металла хитином16. Успешная стратегия заключается во внедрении адсорбционных участков, более устойчивых к протонации17,18. Вместо этого в настоящем описан простой способ увеличения удельной площади поверхности и, следовательно, количества участков адсорбции в хитине.
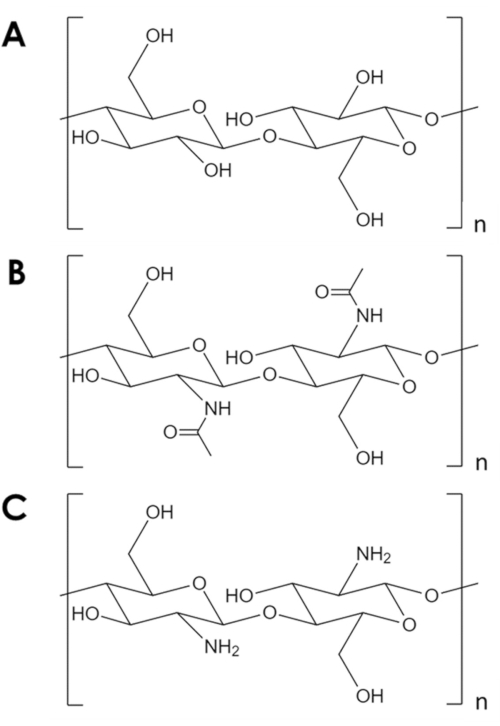
Рисунок 1. Химическая структура. (А) целлюлоза, (B) хитин, (C) хитозан. Пожалуйста, нажмите здесь, чтобы просмотреть увеличенную версию этого рисунка.
Несмотря на его многочисленные потенциальные применения, хитин недостаточно используется. Обработка хитина является сложной задачей из-за его низкой растворимости в большинстве растворителей. Ключевым ограничением его использования в катализе и адсорбции является его низкая удельная площадь поверхности. В то время как типичные углеродные и металлические оксидные опоры имеют удельные площади поверхности в порядке 102-10 3 м2/г,коммерческие хитиновые хлопья имеют площадь поверхности порядка 10м2/г19,20,21. Методы расширения хитина в пены существуют, но они неизменно опираются на высокую температуру и давление, сильные кислоты и основания или специализированное оборудование, представляющее собой значительный входной барьер5,21,22,23,24,25. Кроме того, эти способы имеют тенденцию к деацетилату хитина с образованием хитозана(фиг.1С)– более растворимого и реакционноспособного биополимера5,25,26.
В настоящем описан способ расширения хитина в твердые пены, увеличения его удельной площади поверхности и адсорбционной способности, а также поддержания его химической целостности. Метод основан на быстрой эволюции газа из хитинового геля и не требует специального оборудования. Повышенная адсорбирующая способность расширенного хитина продемонстрирована с водой Cu2+– распространенным загрязнителем в местных подземных водах26.
| Единица | Аккуратные хлопья | Обожженная пена | Лиофилизированная пена | |
| Кристалличности | % | 88 | 74 | 58 |
| Размер кристалла | Нм | 6.5 | 4.4 | 4.4 |
| Площадь поверхности | м2/г | 12.6 ± 2.1 | 43.1 ± 0.2 | 73.9 ± 0.2 |
| Поглощение Cu | мг/г | 13.8 ± 2.9 | 48.6 ± 1.9 | 73.1 ± 2.0 |
| Поглощение Cu | атом/нм2 | 10.5 ± 2.8 | 10.7 ± 0.4 | 9.4 ± 0.3 |
Таблица 1. Сводка свойств материала. Хитиновые пены имеют меньшую кристалличность и размер кристалла по сравнению с аккуратными хитиновыми хлопьями. Тем не менее, удельная площадь поверхности и поглощение Cu из хитиновых пен пропорционально выше, чем у аккуратных хитиновых хлопьев.
Protocol
Representative Results
Discussion
Предлагаемый способ изготовления хитиновой пены позволяет производить такие пены без необходимости в специализированном оборудовании или методах. Производство хитиновой пены зависит от суспензии гидрида натрия в составе хитинового золь-геля. Контакт с водой из атмосферы вызывает г?…
Disclosures
The authors have nothing to disclose.
Acknowledgements
Исследование было спонсировано Научно-исследовательской лабораторией Командования по развитию боевых возможностей армии (Соглашение о сотрудничестве No W911NF-15-2-0020). Любые мнения, выводы и заключения, или рекомендации, выраженные в этом материале, являются мнениями авторов и не обязательно отражают взгляды Армейской исследовательской лаборатории.
Мы благодарим Центр передовой обработки материалов (CAMP) при Технологическом университете Монтаны за использование некоторого специализированного оборудования, необходимого для этого исследования. Мы также благодарим Гэри Висса, Нэнси Ойер, Рика Ладусера, Джона Киртли и Кэтрин Зодроу за техническую помощь и полезные обсуждения.
Materials
| Ammonium bicarbonate | Sigma-Aldrich | 9830 | NH4HCO3, ≥99.5 % |
| Chitin | Sigma-Aldrich | C7170 | Pandalus borealis, practical grade |
| Colorimeter | Hanna Instruments | HI83399-01 | Photometer for wastewater analysis |
| Copper High Range Checker | Hanna Instruments | HI702 | Bicinchoninate colorimetric titration |
| Copper nitrate hydrate | Sigma-Aldrich | 223395 | Cu(NO3)2 · 2.5 H2O, 98 % |
| Dimethylacetamide (DMAc) | Sigma-Aldrich | 271012 | Anhydrous, 99.8 % |
| IR Spectrophotometer | Thermo Nicolet | Nexus 670 | Fitted with an ATR cell |
| Lithium chloride | Sigma-Aldrich | 310468 | LiCl, ≥99 % |
| N2 Physisorption Apparatus | Micromeritics | Tristar II | |
| Nitric acid | BDH | BDH7208-1 | HNO3, 0.1 N |
| Scanning electron microscope | Zeiss LEO | 1430 VP | 15 kV, secondary electron detector, 29-31 mm working distance |
| Sodium hydride | Sigma-Aldrich | 223441 | NaH, packed in mineral oil, 90 % |
| Thermogravimetric analyzer | TA Instruments | Q500 | 100 ml/min N2, 10 °C/min to 800 °C |
| Water Purification System | Millipore | Milli-Q | Type A water (18 MΩ) |
| X-Ray Diffractometer | Rigaku | Ultima IV | Cu K-α radiation, 8.04 keV |
References
- Rinaudo, M. Chitin and chitosan: Properties and applications. Progress in Polymer Science. 31 (7), 603-632 (2006).
- Percot, A., Viton, C., Domard, A. Optimization of chitin extraction from shrimp shells. Biomacromolecules. 4 (1), 12-18 (2003).
- Austin, P. R. Chitin solvents and solubility parameters. Chitin, Chitosan, and Related Enzymes. , 227-237 (1984).
- Deepthi, S., Venkatesan, J., Kim, S. K., Bumgardner, J. D., Jayakumar, R. An overview of chitin or chitosan/nano ceramic composite scaffolds for bone tissue engineering. International Journal of Biological Macromolecules. 93, 1338-1353 (2016).
- Tao, F., et al. Applications of chitin and chitosan nanofibers in bone regenerative engineering. Carbohydrate Polymers. 230, 115658 (2020).
- Zhao, L., et al. Regulation of the morphological and physical properties of a soft tissue scaffold by manipulating DD and DS of O-carboxymethyl chitin. ACS Applied Bio Materials. 3 (9), 6187-6195 (2020).
- Duan, Y., Freyburger, A., Kunz, W., Zollfrank, C. Cellulose and chitin composite materials from an ionic liquid and a green co-solvent. Carbohydrate Polymers. 192, 159-165 (2018).
- Kadokawa, J., Takegawa, A., Mine, S., Prasad, K. Preparation of chitin nanowhiskers using an ionic liquid and their composite materials with poly(vinyl alcohol). Carbohydrate Polymers. 84 (4), 1408-1412 (2011).
- Chen, Z., Wang, J., Qi, H. J., Wang, T., Naguib, H. E. Green and sustainable layered chitin-vitrimer composite with enhanced modulus, reprocessability, and smart actuator function. ACS Sustainable Chemistry and Engineering. 8 (40), 15168-15178 (2020).
- Zhang, Z., Lucia, L. A. Chitin-clay composite gels with enhanced thermal stability prepared in a green and facile approach. Journal of Materials Science. 56 (4), 3600-3611 (2021).
- Ahmed, M. J., Hameed, B. H., Hummadi, E. H. Review on recent progress in chitosan/chitin-carbonaceous material composites for the adsorption of water pollutants. Carbohydrate Polymers. 247, 116690 (2020).
- Matsuoka, A., et al. Hydration of nitriles to amides by a chitin-supported ruthenium catalyst. RSC Advances. 5 (16), 12152-12160 (2015).
- Wang, Y., Li, Y., Liu, S., Li, B. Fabrication of chitin microspheres and their multipurpose application as catalyst support and adsorbent. Carbohydrate Polymers. 120, 53-59 (2015).
- Anastopoulos, I., Bhatnagar, A., Bikiaris, D., Kyzas, G. Chitin Adsorbents for Toxic Metals: A Review. International Journal of Molecular Sciences. 18 (1), 114 (2017).
- Habiba, U., Afifi, A. M., Salleh, A., Ang, B. C. Chitosan/(polyvinyl alcohol)/zeolite electrospun composite nanofibrous membrane for adsorption of Cr6+, Fe3+ and Ni2+. Journal of Hazardous Materials. 322, 182-194 (2017).
- Kim, U. J., et al. Protein adsorption of dialdehyde cellulose-crosslinked chitosan with high amino group contents. Carbohydrate Polymers. 163, 34-42 (2017).
- He, Y., et al. Fabrication of PVA nanofibers grafted with octaamino-POSS and their application in heavy metal adsorption. Journal of Polymers and the Environment. , (2020).
- Tian, H., et al. Electrospinning of polyvinyl alcohol into crosslinked nanofibers: An approach to fabricate functional adsorbent for heavy metals. Journal of Hazardous Materials. 378, (2019).
- Meille, V. Review on methods to deposit catalysts on structured surfaces. Applied Catalysis A: General. 315, 1-17 (2006).
- Dotto, G. L., Cunha, J. M., Calgaro, C. O., Tanabe, E. H., Bertuol, D. A. Surface modification of chitin using ultrasound-assisted and supercritical CO2 technologies for cobalt adsorption. Journal of Hazardous Materials. 295, 29-36 (2015).
- Phongying, S., Aiba, S., Chirachanchai, S. Direct chitosan nanoscaffold formation via chitin whiskers. Polymer. 48 (1), 393-400 (2007).
- Tan, T. S., Chin, H. Y., Tsai, M. L., Liu, C. L. Structural alterations, pore generation, and deacetylation of α- and β-chitin submitted to steam explosion. Carbohydrate Polymers. 122, 321-328 (2015).
- Chang, F. S., Chin, H. Y., Tsai, M. L. Preparation of chitin with puffing pretreatment. Research on Chemical Intermediates. 44 (8), 4939-4955 (2018).
- Goodrich, J. D., Winter, W. T. α-Chitin Nanocrystals prepared from shrimp shells and their specific surface area measurement. Biomacromolecules. 8 (1), 252-257 (2007).
- Rolandi, M., Felts, J. . Naturally sourced chitin foam. , (2020).
- McDermott, S., Hailer, M. K., Lead, J. R. Meconium identifies high levels of metals in newborns from a mining community in the U.S. Science of the Total Environment. 707, 135528 (2020).
- Hach Handbook of Water Analysis. Copper, Bicinchoninate Method, Method 8506. Hach Handbook of Water Analysis. , (1979).
- Crittenden, J. C., Trusell, R. R., Hand, D. R., Howe, K. J., Tchbanoglous, G. Adsorption. MWH’s Water Treatment. , 1117 (2012).
- Focher, B., Beltrame, P. L., Naggi, A., Torri, G. Alkaline N-deacetylation of chitin enhanced by flash treatments. Reaction kinetics and structure modifications. Carbohydrate Polymers. 12 (4), 405-418 (1990).
- Scherrer, P. Determination of the size and the internal structure of colloidal particles by means of X-rays. News from the Society of Sciences in Göttingen, Mathematical- Physical Class. 2, 98-100 (1918).
- Brunauer, S., Emmett, P. H., Teller, E. Adsorption of gases in multimolecular layers. Journal of the American Chemical Society. 60 (2), 309-319 (1938).
- Sing, K. S. W. Adsorption methods for the characterization of porous materials. Advances in Colloid and Interface Science. 76-77, 3-11 (1998).
- Rouquerol, J., Llewellyn, P., Rouquerol, F. Is the bet equation applicable to microporous adsorbents. Studies in Surface Science and Catalysis. 160, 49-56 (2007).
- Vorokh, A. S. Scherrer formula: estimation of error in determining small nanoparticle size. Nanosystems: Physics, Chemistry, Mathematics. , 364-369 (2018).
- Labidi, A., Salaberria, A. M., Fernandes, S. C. M., Labidi, J., Abderrabba, M. Adsorption of copper on chitin-based materials: Kinetic and thermodynamic studies. Journal of the Taiwan Institute of Chemical Engineers. 65, 140-148 (2016).
- Tian, M., Zhao, T. Q., Chin, P. L., Liu, B. S., Cheung, A. S. -. C. Methane and propane co-conversion study over zinc, molybdenum and gallium modified HZSM-5 catalysts using time-of-flight mass-spectrometry. Chemical Physics Letters. 592, 36-40 (2014).

