Hurtig In Vivo Fiksering og isolering af translationelle komplekser fra eukaryote celler
Summary
Vi præsenterer en teknik til hurtigt at stabilisere translationelle (proteinbiosyntese) komplekser med formaldehyd crosslinking i levende gær og pattedyr celler. Tilgangen muliggør dissekering af forbigående mellemprodukter og dynamiske RNA:proteininteraktioner. De krydslinkede komplekser kan bruges i flere downstream-applikationer, såsom i dybe sekventeringsbaserede profileringsmetoder, mikroskopi og massespektrometri.
Abstract
Hurtige reaktioner, der indebærer hurtig omfordeling af messenger(m)RNA og ændringer af mRNA-oversættelse, er relevante for løbende homøostatiske justeringer af cellerne. Disse justeringer er afgørende for eukaryote celle overlevelsesevne og ‘skade kontrol’ under svingende næringsstof og saltholdighed niveauer, temperatur, og forskellige kemiske og stråling understreger. På grund af den meget dynamiske karakter af RNA-niveau svar, og ustabiliteten i mange af RNA: RNA og RNA: protein mellemprodukter, opnå et meningsfuldt øjebliksbillede af den cytoplasmatiske RNA tilstand er kun muligt med et begrænset antal metoder. Transcriptome-dækkende, RNA-seq-baserede ribosom profilering-type eksperimenter er blandt de mest informative datakilder til kontrol af oversættelse. Men, fravær af en ensartet RNA og RNA:protein mellemliggende stabilisering kan føre til forskellige fordomme, især i de hurtige cellulære respons veje. I denne artikel leverer vi en detaljeret protokol med hurtig fiksering, der gælder for eukaryote celler af forskellig permeabilitet, for at hjælpe i RNA og RNA: protein mellemliggende stabilisering. Vi giver endvidere eksempler på isolering af de stabiliserede RNA:proteinkomplekser baseret på deres co-sedimentering med ribosomale og poly (ribo)somale fraktioner. Det adskilte stabiliserede materiale kan efterfølgende bruges som en del af ribosom profileringslignende eksperimenter, f.eks. Alsidigheden af TCP-seq-stil metoder er nu blevet demonstreret af applikationerne i en række organismer og celletyper. De stabiliserede komplekser kan også desuden affinitetsrenses og afbildes ved hjælp af elektronmikroskopi, adskilt i forskellige poly (ribo)somale fraktioner og udsat for RNA-sekventering på grund af den lette krydslink-vending. Derfor kan metoder baseret på snap-chilling og formaldehydfiksering, efterfulgt af den sedimenteringsbaserede eller anden type RNA:proteinkompleks berigelse, være af særlig interesse i at undersøge finere detaljer om hurtig RNA:protein kompleks dynamik i levende celler.
Introduction
Levende organismer er underlagt dynamiske intra- og ekstracellulære ændringer i hele deres levetid, hvilket kræver hurtige reaktioner for at opretholde homøostase og sikre overlevelse. For at muliggøre miljøtilpasning justerer eukaryote celler deres stofskifte via genekspressionskontrol. Genekspressionskontrol kan udøves under transskription og/eller oversættelse; med translationelle svar generelt forekommer hurtigere1,2,3,4. For eksempel opstår der typisk translationelle ændringer inden for 1-30 min fra stressdebuten, mens ændringer på transskriptionsniveau følger timer efter stresseksponering3,4,5. Ændringer i oversættelsesoutput opnås hurtigere på grund af den vedvarende tilgængelighed af messenger (m)RNA-molekyler i cytoplasmaet. Omvendt skal nye mRNA-molekyler syntetiseres på transskriptionsniveau, og i eukaryoter skal forarbejdes og eksporteres fra kernen, hvilket giver omfattende forsinkelser i responstiden2,4,6,7,8.
Akut translationel reaktion på stress er generelt karakteriseret ved et generelt fald i oversættelsesproduktionen, med selektiv upregulation af proteiner, der er nødvendige for celleoverlevelse1,3,4,9. Reduktion af proteinproduktionsproduktionen menes at være afgørende på grund af processens høje energiomkostninger3,7. For at lette den selektive hæmning og upregulation betjenes translationelle reaktioner af en række komplekse reguleringsmekanismer. Regulering kan udøves på tværs af alle faser af oversættelsen: indledning, forlængelse, afslutning af polypeptidbiosyntese og ribosomal genanvendelse10,11,12,13, men udstilles mest i indledningsfasen5,7,9,10,13. Under indledningen binder den lille ribosomale underenhed (SSU), bistået af eukaryote indledningsfaktorer (eIF’er), sig til og scanner 5′ uoversatte regioner (UTR) i mRNA, indtil en start codon er anerkendt2,5,6,8,11,12,13. Reguleringsmekanismer er ofte rettet mod eIF’er, der påvirker vedhæftede filer, scanninger og start af codongenkendelse. F.eks. er indledningsfaktoren eIF2, en væsentlig oversættelsesfaktor, der hjælper med ansættelsen af en initiativtager Met-tRNAiMet til SSU, er ofte målrettet i eukaryoter under stress betingelser4,6,11. I gær kan fosforylering af denne faktor induceres under næringsstofmangel og osmotisk stress1,4,11,14,15og i pattedyrceller kan aminosyre sult, endoplasmisk reticulum (ER) stress, UV-stress, virusinfektion og ændrede iltniveauer udløse dette svar8,9,11. Hurtig opregulering af specifik mRNA-oversættelse er tydelig i pattedyrcellens reaktion på hypoxi, som udviser en global hurtig oversættelseshæmning og selektiv upregulering af hypoxiinukible faktorer (HIF’er) biosyntese. HIF’er er transskriptionsfaktorer, som derefter fremkalder langsigtet cellulær omprogrammering på DNA-transskriptionsniveau8,9,16. Lignende reaktioner er blevet observeret i gær under varme stress, med hurtig translationel udtryk for Heat Shock Proteins (HSP’er) efterfulgt af forsinkede transskription-niveau svar17,18. Ud over næringsstofmangel og varmechok er translationelle reaktioner i gær blevet undersøgt under varierende ilt8,19salinitet5, fosfat, svovl20,21 og kvælstof22,23 Niveauer. Denne forskning har vidtrækkende konsekvenser for den industrielle anvendelse af gær, såsom bagning og gæring24,25. Translationelle reaktioner kan også være medvirkende til at fremme forståelsen af sygdomme som neurodegenerative lidelser og hjertesygdomme, der er karakteriseret ved intracellulære belastninger som oxidativ stress. Samlet set er translationelle reaktioner en integreret del af genekspressionskontrol og letter hurtig tilpasning til en bred vifte af stressforhold i eukaryote organismer.
For at studere translationelle svar er der brug for metoder, der giver minimalt forvrængede snapshots af oversættelseslandskabet. Polysome profilering er en klassisk tilgang, der anvendes i studiet af oversættelse på tværs af mRNA, der involverer adskillelse af poly (ribo)somale fraktioner af mRNA via ultracentrifugering gennem saccharose gradienter26,27. Metoden kan anvendes til at undersøge oversættelsesniveauer for individuelle mRNA’er (med detektionsmetoder som omvendt transskription og polymerasekædereaktion, RT-PCR26) eller globalt i forbindelse med teknikker med høj kapacitet (mikroarray eller RNA-seq28,29). En mere udviklet tilgang er ribosom profilering, der gør det muligt at studere positioner af aflange ribosomer langs et mRNA-molekyle i genom-dækkende skala, samt konklusionen af effektiviteten af oversættelse på tværs af transskriptom og udnyttelse af de vigtigste og alternative startsteder30,31. Ribosom profilering indebærer isolering og sekventering af mRNA fragmenter beskyttet af ribosomal tilstedeværelse over dem. Ribosom profilering har givet betydelig indsigt i oversættelse dynamik på tværs af en række betingelser, herunder hypoxisk stress, varmechok og oxidativ stress31,32. Teknikken er blevet tilpasset flere kildematerialetyper, herunder gær- og pattedyrceller.
Mens polysome og ribosom profilering har været grundlæggende i at udvide mulighederne for forskning i oversættelse, processen med oversættelse omfatter forskellige translationelle mellemprodukter og komplekser, der er vanskelige at fange med disse metoder11,13. En yderligere begrænsning skyldes den manglende evne til at studere hurtige reaktionstyper, da translationelle komplekser enten stabiliseres in vivo ved tilsætning af specifikke oversættelseshæmmere (antibiotika), hvilket fører til visse ribosomfordelingsartefakter eller ex vivo på cellelyseis specifikt (antibiotika) eller uspecifikt (højt salt eller magnesiumioner), hvilket fører til afsavn af de korterelivede eller mindre stabile mellemprodukter33, 34,35.
Formaldehyd er meget udbredt til at krydslinke nukleinsyrer og proteiner, såsom i kromatin immunprecipitation (ChIP) og crosslinking immunoprecipitation (CLIP) undersøgelser. Dens lille størrelse og fremragende celle permeabilitet giver mulighed for en hurtig in vivo handling36. Baseret på den hurtige formaldehyd crosslinking er ribosom profileringsmetoden blevet udvidet med TCP-seq (Translation Complex Profile Sekventering)10,36,37,38,39,40. TCP-seq, der først blev udviklet i gær, gør det muligt at hente alle mellemprodukter til oversættelse, herunder scanning eller SSU-komplekser efter opsigelsen og flere ribosomale konfigurationer37,38,41,42. Metoden er blevet anvendt i flere undersøgelser10,38,39,41,42, hvoraf nogle bruger en kombinationstilgang af både oversættelseshæmmere og formaldehyd crosslinking at lette anholdelsen af oversættelse. En anden modificeret version af teknikken, selektiv TCP-seq39, er for nylig blevet anvendt til at omfatte immunpurification af de krydslinkede komplekser, der udvider omfanget af TCP-seq-applikationerne. Den formelledehydkrydsning har en hurtig, effektiv og reversibel karakter, der gør disse tilgange velegnede til at studere forbigående mRNA:oversættelseskomplekse interaktioner, især i forbindelse med meget dynamiske responsveje på oversættelsesniveau.
Her beskriver vi processerne for in vivo formaldehyd crosslinking med henblik på omfattende oversættelse kompleks stabilisering og isolation. Vi leverer separate protokoller nuanceret for gær og pattedyr celler (Figur 1). Vi skitserer endvidere eksempler på den efterfølgende anvendelse af det krydslinkstabilerede materiale (figur 1), f.eks. IP) og berigelse af translationelle komplekser, der indeholder specifikke interessefaktorer, elektronmikroskopi og RNA-sekventering.
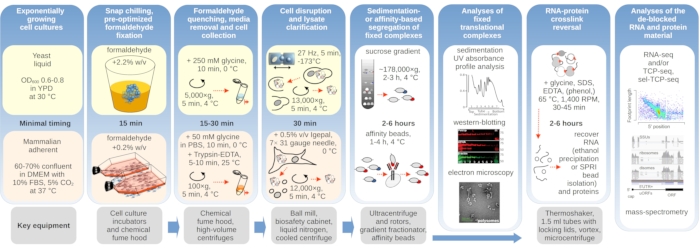
Figur 1: Skematisk, der viser en oversigt over den typiske eksperimentelle opsætning. De vigtigste trin i in vivo formaldehydstabilisering af translationelle komplekser fremstilles som et rutediagram suppleret med oplysninger om de vigtigste nødvendige instrumenter. Potentielle downstream-anvendelser af det krydslinkede materiale er skitseret, herunder eksempler, der med succes er blevet anvendt, men ikke direkte dækket i denne protokol, såsom SPRI perlerensning af RNA, RNA-sekventering og massespektrometri. Klik her for at se en større version af dette tal.
Protocol
Representative Results
Discussion
Formaldehyd fiksering er en bekvem og populær metode til at opnå hurtig in vivo crosslinking af biomolekyler10,36,45,46,47,48. Sammenlignet med de andre potentielle biomolekylemål kræver vellykket fangst af translationelle komplekser en øjeblikkelig fiksering under snapkøling af cellerne eller andet materiale. Uden den ufordedne stabilisering er der mulighed for, at forskellige oversættelsesrelaterede processer kan fortsætte, hvilket flytter den komplekse fordeling væk fra den uforstyrrede in vivo state49. Sammenlignet med de andre metoder til translationel anholdelse og ribosomal kompleks stabilisering lover formaldehydhandlingens hurtighed på tværs af cellemembraner og crosslinks vilkårlige karakter bevarelse af den maksimale mangfoldighed af oversættelseskomplekset mellemprodukter tættere på deres oprindeligt distribuerede tilstande50.
Den tilgang, der præsenteres her, er etableret og optimeret i både gær- og pattedyrceller, og metoder er nu afledt af andre grupper til brug på tværs af mere forskelligartet biologisk materiale, såsom i hele hvirveldyr (f.eks. zebrafiskembryoner)10,38,39,49,51,52 . Selv om disse værker kollektivt berolige alsidigheden og den brede anvendelighed af tilgangen, hurtig formaldehyd crosslinking af translationelle komplekser kan betragtes som noget vanskeligt at overføre til nye typer af biologisk materiale på grund af behovet for optimeringer og justeringer.
Et fremmest krav til metodens succes er reoptimering af koncentrationen af formaldehyd og celleindsamlings- og disruptionteknikken. Mindre gennemtrængelige, små og runde gærceller kræver meget højere (mindst 10 gange) formaldehydkoncentration og fysisk forstyrrelse af de faste celler. I modsætning hertil kan store og flade klæbende pattedyrceller i kultur let overfastsættes og kræve blid håndtering ved fiksering, mens ekstraktionen af de faste komplekser kan udføres kemisk med membranforstyrrelse ved hjælp af rengøringsmidler. Under-crosslinking kan tillade mindre stabile eller mere kortvarige mellemprodukter at adskille eller lække i en senere tilstand. Over-crosslinking kan have en negativ indvirkning på evnen til at isolere og studere ribosomale fraktioner og kan skabe selektive bias såsom dybere udtømning af tunge komplekser. I vores observation kan selv mindre ændringer, såsom den type klæbende menneskelige celler, der anvendes, påvirke udbyttet af de genvundne krydslinkede komplekser og kan kræve re-optimering af crosslinking regimet. Vi kan også forudse, at celler med væsentligt forskellige permeabilitetsegenskaber, såsom planteceller, vil kræve yderligere omfattende optimering af fikseringsbetingelserne52. Men det er svært at forestille sig en type biologisk materiale, der ville være helt uforeneligt med tilgangen.
En overvejelse, der er relevant for pattedyrsfikseringsprotokollen, er tætheden og mængden af cellemateriale, der anvendes som input. Det anbefales at have cellerne kontinuerligt voksende uden re-såning eller andre forstyrrelser i mindst 2 dage for at undgå ekstern indflydelse på cellulære oversættelse dynamik. Gældende for de fleste celletyper, men for de fleste klæbende celler konsekvent opnået sammenløb niveauer på ikke mere end 70% vil sikre fravær af større kontakt hæmning virkninger, der kan have en negativ og uforudsigelig indflydelse oversættelse satser.
Et andet interessant og potentielt enestående bekvemt træk ved formaldehydfiksering, der stammer fra dens vilkårlige reaktivitet, er stabiliseringseffekten på translationelle komplekser i systemer med blandet taksonomi. Bakterielle, og endnu mere translationelle komplekser af mitokondrier, kloroplaster og forskellige intracellulære parasitter, har været notorisk vanskeligt at målrette med specifikke oversættelseshæmmere. I TCP-seq-dataene kan fodspor, der er tilknytning til mitotranscriptomet, derimod let observeres i dataene38,39,50. En interessant efterfølgende udvikling kunne være anvendelsen af metoden til at undersøge oversættelse i hele mikrosamfund, f.eks. i jord-, vand- eller tarmprøver, hvor pålidelig hurtig oversættelsesarrest og kompleks stabilisering med andre midler ville være problematisk.
Det skal også nævnes, at intet forhindrer brugen af formaldehydstabilisering umiddelbart efter celleforstyrrelser og materiale homogenisering for det mest komplicerede materiale (såsom hårdt og/eller voluminøst væv). Denne fremgangsmåde anvendes allerede ofte til at fjerne celleindtastningsforsinkelsen, når du stabiliserer translationelle komplekser med specifikke små molekylehæmmere33,53,54,55. I betragtning af at formaldehydfiksering traditionelt er blevet brugt med fremragende resultater til ex vivo / in vitro-prøvestabilisering i applikationer som elektronmikroskopi45,56,57,58, kan vi forvente endnu mindre negative virkninger i dette tilfælde, især dem, der er forbundet med den dårlige ekstraktion af de translationelle komplekser fra de grundigt faste celler.
Vores resultater bekræfter anvendeligheden af hurtig formaldehydfiksering for at stabilisere meget forbigående komplekser, såsom dem, der omfatter eIF4A. Det er bemærkelsesværdigt, at gær eIF4A i modsætning til pattedyr er meget svagere forbundet med capbindingskomplekset eIF4F og som følge heraf translationelle komplekser generelt. eIF4A går normalt tabt under enhver omfattende rensning af ribosomalt materiale i gær29,59,60,61,62,63. Men i det in vivo-fastegærmateriale er det muligt at opnå pålidelig berigelse af eIF4A i alle fraktioner af translationelle komplekser, hvor dets tilstedeværelse ville blive forventet. De tidligere offentliggjorte Sel-TCP-seq-data har vist berigelsen af eIF2 og eIF3, der i højere grad forbinder med ribosomer (men også afslørede forbigående forekommende co-translationelle proteinkompleksmontering)39. Metoden er således velegnet til påvisning af både stærkere og svagere vedhæftede bestanddele af de translationelle komplekser.
Sammenfattende har vi præsenteret en tilgang, der er nyttig til at få indsigt primært i de ændringer, der sker i oversættelsesfasen, og når der kræves minimalt ribosomal fordeling over mRNA. Det er vigtigt, at tilgangen er velegnet til stabilisering af relativt labile og dynamiske komponenter i translationelle komplekser, såsom eIF4A, og kan bruges bredt udsat for nødvendige optimeringer. Vi har også fremlagt dokumentation for nytten af formaldehydfiksering i scenarierne med hurtig dynamisk ændring af oversættelsen, der åbner undersøgelsesområder såsom hurtige cellulære reaktioner på miljøændringer eller stressforhold.
Disclosures
The authors have nothing to disclose.
Acknowledgements
Dette arbejde blev støttet af Australian Research Council Discovery Project grant (DP180100111 til T.P. og N.E.S), National Health and Medical Research Council Investigator Grant (GNT1175388 til N.E.S.) og Research Fellowship (APP1135928 til T.P.). Forfatterne anerkender faciliteterne i Mikroskopi Australien på Center for Advanced Microscopy, Australian National University, en facilitet, der er finansieret af universitetet og den føderale regering.
Materials
| Yeast extract | Merck, Sigma-Aldrich | 70161 | |
| Peptone | Merck, Sigma-Aldrich | 70178 | |
| D-Glucose (Dextrose) | Merck, Sigma-Aldrich | 49139 | |
| Adenine sulphate | Amresco | 0607-50G | |
| Formaldehyde solution | Merck Sigma-Aldrich | F11635-500ML | ACS reagent, 37 wt. % in H2O, contains 10-15% Methanol as stabiliser (to prevent polymerisation) |
| RNaseOUT™ Recombinant Ribonuclease Inhibitor | Invitrogen™ byThermo Fischer Scientific | 10777019 | |
| cOmplete™, EDTA-free Protease Inhibitor Cocktail | COEDTAF-RO Roche by Merck | 11873580001 | |
| Magnesium chloride solution | (Merck/Sigma-Aldrich) | M1028 | |
| Ethylenediaminetetraacetic acid solution | (Merck/Sigma-Aldrich) | E7889 | |
| Ambion™ RNase I, cloned, 100 U/µL | Ambion | AM2294 | |
| SUPERase•In™ RNase Inhibitor (20 U/μL) | Invitrogen™ by Thermo Fisher Scientific | AM2694 | |
| Acidic phenol:chlorophorm:isoamyl alcohol 125:24:1 (pH 4.0-5.0) | (Merck/Sigma-Aldrich) | P1944-100ML | |
| Dynabeads™ Goat Anti-Mouse IgG | Invitrogen™ by Thermo Fisher Scientific) | 11033 | |
| Sodium Acetate (3 M), pH 5.5 | Invitrogen™ by Thermo Fisher Scientific) | AM9740 | |
| Glycogen (5 mg/ml) | Invitrogen™ by Thermo Fisher Scientific) | AM9510 | |
| Ethyl alcohol, Pure | Merck; Sigma Aldrich | E7023 | |
| Amersham™ Hybond® P Western blotting membranes, PVDF | Merck | GE10600023 | PVDF membrane for western blotting |
| Bolt™ 4 to 12%, Bis-Tris, 1.0 mm, Mini Protein Gel | Invitrogen™ by ThermoFischer Sientific | NW04120BOX | Protein gel |
| 4X Bolt™ LDS Sample Buffer | Invitrogen™ by ThermoFischer Sientific | B0007 | LDS sample loading buffer |
| Precision Plus Protein™ Kaleidoscope™ Prestained Protein Standards | BioRad | 1610375 | Protein ladder |
| 20X Bolt™ MES SDS Running Buffer | ThermoFischer Scientific | B0002 | PAGE runninjg buffer |
| Intercept® (PBS) Blocking Buffer | LI-COR | 927-70001 | Odyssey Blcoking buffer (PBS) |
| IRDye® 800CW Goat anti-Mouse IgG Secondary Antibody | LI-COR | 92632210 | |
| IRDye® 800CW Goat anti-Rabbit IgG Secondary Antibody | LI-COR | 92632211 | |
| TAP Tag Polyclonal Antibody | Invitrogen™ by ThermoFischer Sientific | CAB1001 | |
| Anti-beta Actin antibody | Abcam | ab8227 | |
| Sucrose | (Merck/Sigma-Aldrich) | 84097 | BioUltra, for molecular biology, ≥99.5% (HPLC) |
| DL-Dithiothreitol solution | (Merck/Sigma-Aldrich) | 43816 | BioUltra, for molecular biology, ~1 M in H2O |
| Terumo Syringe 1CC/mL | Terumo Syringe | 878499 | |
| Potassium chloride | (Merck/Sigma-Aldrich) | 60128 | |
| HEPES | (Merck/Sigma-Aldrich) | H3375 | |
| Dulbecco's Modified Eagle's Medium – high glucose | Sigma Aldrich | D5796 | |
| Fetal Bovine Serum | Sigma Aldrich | 12003C | |
| Trypsin-EDTA (0.05%), phenol red | Gibco | 25300062 | |
| Dulbecco's Phosphate Buffered Saline with Calcium and magnesium | Sigma-Aldrich | D8662 | |
| Glycine | Sigma-Aldrich | G7126 | |
| Tris hydrochloride | Merck/Sigma-Aldrich | 10812846001 | |
| Sodium dodecyl sulfate | Merck/Sigma-Aldrich | 436143 | |
| IGEPAL CA-630 | Merck/Sigma-Aldrich | I3021 | |
| Rnasin Ribonuclease Inhibitor | Promega | N2111 | |
| Stainless steel grinding jar | Retsch | 02.462.0059 | |
| MM400 mixer mill | Retsch | 20.745.0001 | |
| Gradient Fractionator | Brandel | BRN-BR-188 | |
| Thermomixer R | Eppendorf | Z605271 | |
| Nanodrop spectrophotometer | Thermo Fisher Scientific | ND-2000 | |
| 0.5-ml microcentrifuge tubes with locking devices | Eppendorf Safe-Lock | 30121023 | |
| Mini Gel Tank | (Thermo Fisher Scientific) | A25977 | PAGE running tank |
| 5 mL, Open-Top Thinwall Ultra-Clear Tube, 13 x 51mm | Beckman-Coulter | 344057 | |
| 13.2 mL, Certified Free Open-Top Thinwall Polypropylene, 14 x 89mm – 50Pk | Beckman-Coulter | 331372 | |
| Amicon Ultra-0.5 ultrafiltration devices | Merck | UFC5030 | Ultracel-30 regenerated cellulose membrane, 0.5 mL sample volume |
| Thermo Sorvall Evolution RC Floor Super Speed Centrifuge | Cambridge Scientific | 15566 | |
| Beckman Coulter Optima L-90K | GMI | 8043-30-1191 | |
| Nunc EasYFlask 175cm2 | Thermofisher Scientific | 159910 | |
| Falcon 50 mL Conical Centrifuge Tubes | Thermofisher Scientific | 14-432-22 | |
| 25 mL Serological Pipette | Sigma-Aldrich | SIAL1250 | |
| 10 mL Serological Pipette | Sigma-Aldrich | SIAL1100 | |
| DNA lobind tubes | Eppendorf | 30108051 | |
| Cold Centrifuge 5810 R | Eppendorf | EP022628188 | for 50 mL tubes |
| Orbital Shaking Incubator | Ratek | OM11 | |
| Frezco 17 Microcentrifuge | Thermofisher Scientific | 75002402 | |
| Eppendorf DNA lo-bind tubes | Merck/Sigma-Aldrich | EP0030108051 | |
| Eppendorf® Protein LoBind tubes | Merck/Sigma-Aldrich | EP0030108116 | |
| SW 41 Ti Swinging bucket rotor | Beckman-Coulter | 331362 | |
| Heracell™ 150i CO2 Incubator, 150 L | Thermofisher Scientific | 51026282 | |
| 0,3 mL ultra-fine II short insulin syringe | BD Medical | 328822 | |
| 3 mL syringe with Luer Lok tip | BD Medical | 302113 | |
| 25 G x 16 mm Hypodermic Needle | Terumo | TUAN2516R1 |
References
- Janapala, Y., Preiss, T., Shirokikh, N. E. Control of translation at the initiation phase during glucose starvation in yeast. International Journal of Molecular Sciences. 20 (16), 4043 (2019).
- Masvidal, L., Hulea, L., Furic, L., Topisirovic, I., Larsson, O. mTOR-sensitive translation: Cleared fog reveals more trees. RNA Biology. 14 (10), 1299-1305 (2017).
- Ashe, M. P., De Long, S. K., Sachs, A. B. Glucose depletion rapidly inhibits translation initiation in yeast. Molecular Biology of the Cell. 11 (3), 833-848 (2000).
- Crawford, R. A., Pavitt, G. D. Translational regulation in response to stress in Saccharomyces cerevisiae. Yeast. 36 (1), 5-21 (2019).
- Melamed, D., Pnueli, L., Arava, Y. Yeast translational response to high salinity: global analysis reveals regulation at multiple levels. RNA. 14 (7), 1337-1351 (2008).
- Hershey, J. W., Sonenberg, N., Mathews, M. B. Principles of translational control: An overview. Cold Spring Harbor Perspectives in Biology. 4 (12), 011528 (2012).
- Mata, J., Marguerat, S., Bähler, J. Post-transcriptional control of gene expression: a genome-wide perspective. Trends in Biochemical Sciences. 30 (9), 506-514 (2005).
- Spriggs, K. A., Bushell, M., Willis, A. E. Translational regulation of gene expression during conditions of cell stress. Molecular Cell. 40 (2), 228-237 (2010).
- Liu, B., Qian, S. B. Translational reprogramming in cellular stress response. Wiley Interdisciplinary Reviews RNA. 5 (3), 301-315 (2014).
- Archer, S. K., Shirokikh, N. E., Beilharz, T. H., Preiss, T. Dynamics of ribosome scanning and recycling revealed by translation complex profiling. Nature. 535 (7613), 570-574 (2016).
- Hinnebusch, A. G., Ivanov, I. P., Sonenberg, N. Translational control by 5′-untranslated regions of eukaryotic mRNAs. Science. 352 (6292), 1413-1416 (2016).
- Dever, T. E., Green, R. The elongation, termination, and recycling phases of translation in eukaryotes. Cold Spring Harbor Perspectives in Biology. 4 (7), 013706 (2012).
- Shirokikh, N. E., Preiss, T. Translation initiation by cap-dependent ribosome recruitment: Recent insights and open questions. Wiley Interdisciplinary Reviews RNA. 9 (4), 1473 (2018).
- Jiménez-Díaz, A., Remacha, M., Ballesta, J. P., Berlanga, J. J. Phosphorylation of initiation factor eIF2 in response to stress conditions is mediated by acidic ribosomal P1/P2 proteins in Saccharomyces cerevisiae. PLoS One. 8 (12), 84219 (2013).
- Sonenberg, N., Hinnebusch, A. G. Regulation of translation initiation in eukaryotes: mechanisms and biological targets. Cell. 136 (4), 731-745 (2009).
- Majmundar, A. J., Wong, W. J., Simon, M. C. Hypoxia-inducible factors and the response to hypoxic stress. Molecular Cell. 40 (2), 294-309 (2010).
- Barraza, C. E., et al. The role of PKA in the translational response to heat stress in Saccharomyces cerevisiae. PLoS One. 12 (10), 0185416 (2017).
- Richter, K., Haslbeck, M., Buchner, J. The heat shock response: Life on the verge of death. Molecular Cell. 40 (2), 253-266 (2010).
- Jamar, N. H., Kritsiligkou, P., Grant, C. M. The non-stop decay mRNA surveillance pathway is required for oxidative stress tolerance. Nucleic Acids Research. 45 (11), 6881-6893 (2017).
- Chen, Z., et al. The complete pathway for thiosulfate utilization in Saccharomyces cerevisiae. Applied and Environmental Microbiology. 84 (22), (2018).
- Marzluf, G. A. Molecular genetics of sulfur assimilation in filamentous fungi and yeast. Annual Review of Microbiology. 51, 73-96 (1997).
- Miller, D., Brandt, N., Gresham, D. Systematic identification of factors mediating accelerated mRNA degradation in response to changes in environmental nitrogen. PLoS Genetics. 14 (5), 1007406 (2018).
- Zhang, W., Du, G., Zhou, J., Chen, J. Regulation of sensing, transportation, and catabolism of nitrogen sources in Saccharomyces cerevisiae. Microbiology and Molecular Biology Reviews. 82 (1), (2018).
- Tokpohozin, S. E., Fischer, S., Becker, T. Selection of a new Saccharomyces yeast to enhance relevant sorghum beer aroma components, higher alcohols, and esters. Food Microbiology. 83, 181-186 (2019).
- Walker, G. M., Stewart, G. G. Saccharomyces cerevisiae in the production of fermented beverages. Beverages. 2 (4), 30 (2016).
- Chassé, H., Boulben, S., Costache, V., Cormier, P., Morales, J. Analysis of translation using polysome profiling. Nucleic Acids Research. 45 (3), 15 (2017).
- Jin, H. Y., Xiao, C. An integrated polysome profiling and ribosome profiling method to investigate in vivo translatome. Methods in Molecular Biology. 1712, 1-18 (2018).
- Arava, Y., et al. Genome-wide analysis of mRNA translation profiles in Saccharomyces cerevisiae. Proceedings of the National Academy of Sciences of the United States of America. 100 (7), 3889-3894 (2003).
- Lackner, D. H., et al. A network of multiple regulatory layers shapes gene expression in fission yeast. Molecular Cell. 26 (1), 145-155 (2007).
- Ingolia, N. T., Ghaemmaghami, S., Newman, J. R. S., Weissman, J. S. Genome-Wide Analysis in Vivo of Translation with Nucleotide Resolution Using Ribosome Profiling. Science. 324 (5924), 218-223 (2009).
- Ingolia, N. T., Hussmann, J. A., Weissman, J. S. Ribosome Profiling: Global Views of Translation. Cold Spring Harbor Perspectives in Biology. 11 (5), (2019).
- Gerashchenko, M. V., Lobanov, A. V., Gladyshev, V. N. Genome-wide ribosome profiling reveals complex translational regulation in response to oxidative stress. Proceedings of the National Academy of Sciences of the United States of America. 109 (43), 17394-17399 (2012).
- Hussmann, J. A., Patchett, S., Johnson, A., Sawyer, S., Press, W. H. Understanding biases in ribosome profiling experiments reveals signatures of translation dynamics in yeast. Proceedings of the National Academy of Sciences Genetics. 11 (12), 1005732 (2015).
- Santos, D. A., Shi, L., Tu, B. P., Weissman, J. S. Cycloheximide can distort measurements of mRNA levels and translation efficiency. Nucleic Acids Research. 47 (10), 4974-4985 (2019).
- Schneider-Poetsch, T., et al. Inhibition of eukaryotic translation elongation by cycloheximide and lactimidomycin. Nature Chemical Biology. 6 (3), 209-217 (2010).
- Hoffman, E. A., Frey, B. L., Smith, L. M., Auble, D. T. Formaldehyde crosslinking: A tool for the study of chromatin complexes. Journal of Biological Chemistry. 290 (44), 26404-26411 (2015).
- Kage, U., Powell, J. J., Gardiner, D. M., Kazan, K. Ribosome profiling in plants: What is not lost in translation. Journal of Experimental Botany. 71 (18), 5323-5332 (2020).
- Shirokikh, N. E., Archer, S. K., Beilharz, T. H., Powell, D., Preiss, T. Translation complex profile sequencing to study the in vivo dynamics of mRNA-ribosome interactions during translation initiation, elongation and termination. Nature Protocols. 12 (4), 697-731 (2017).
- Wagner, S., et al. Selective translation complex profiling reveals staged initiation and co-translational assembly of initiation factor complexes. Molecular Cell. 79 (4), 546-560 (2020).
- Zlotorynski, E. Profiling ribosome dynamics. Nature Reviews Molecular Cell Biology. 17 (9), 535-535 (2016).
- Sen, N. D., Gupta, N., S, K. A., Preiss, T., Lorsch, J. R., Hinnebusch, A. G. Functional interplay between DEAD-box RNA helicases Ded1 and Dbp1 in preinitiation complex attachment and scanning on structured mRNAs in vivo. Nucleic Acids Research. 47 (16), 8785-8806 (2019).
- Zhao, J., Qin, B., Nikolay, R., Spahn, C. M. T., Zhang, G. Translatomics: The global view of translation. International Journal of Molecular Sciences. 20 (1), 20010212 (2019).
- Luthe, D. S. A simple technique for the preparation and storage of sucrose gradients. Analytical Biochemistry. 135 (1), 230-232 (1983).
- Wang, Z., Gerstein, M., Snyder, M. RNA-Seq: A revolutionary tool for transcriptomics. Nature Review Genetics. 10 (1), 57-63 (2009).
- Orlando, V. Mapping chromosomal proteins in vivo by formaldehyde-crosslinked-chromatin immunoprecipitation. Trends in Biochemical Sciences. 25 (3), 99-104 (2000).
- Schmiedeberg, L., Skene, P., Deaton, A., Bird, A. A Temporal Threshold for Formaldehyde Crosslinking and Fixation. PLoS One. 4 (2), 4636 (2009).
- Solomon, M. J., Varshavsky, A. Formaldehyde-mediated DNA-protein crosslinking: A probe for in vivo chromatin structures. Proceedings of the National Academy of Sciences. 82 (19), 6470-6474 (1985).
- Solomon, M. J., Larsen, P. L., Varshavsky, A. Mapping proteinDNA interactions in vivo with formaldehyde: Evidence that histone H4 is retained on a highly transcribed gene. Cell. 53 (6), 937-947 (1988).
- Bohlen, J., Fenzl, K., Kramer, G., Bukau, B., Teleman, A. A. Selective 40S footprinting reveals cap-tethered ribosome scanning in human cells. Molecular Cell. 79 (4), 561-574 (2020).
- Shirokikh, N. E. Translation complex stabilization on messenger RNA and footprint profiling to study the RNA responses and dynamics of protein biosynthesis in the cells. Critical Reviews in Biochemistry and Molecular Biology. , (2021).
- Giess, A., et al. Profiling of small ribosomal subunits reveals modes and regulation of translation initiation. Cell Reports. 31 (3), 107534 (2020).
- Firmino, A. A. P., et al. Separation and paired proteome profiling of plant chloroplast and cytoplasmic ribosomes. Plants (Basel). 9 (7), (2020).
- Gerashchenko, M. V., Gladyshev, V. N. Translation inhibitors cause abnormalities in ribosome profiling experiments. Nucleic Acids Research. 42 (17), 134 (2014).
- Santos, D. A., Shi, L., Tu, B. P., Weissman, J. S. Cycloheximide can distort measurements of mRNA levels and translation efficiency. Nucleic Acids Research. 47 (10), 4974-4985 (2019).
- Schneider-Poetsch, T., et al. Inhibition of eukaryotic translation elongation by cycloheximide and lactimidomycin. Nature Chemical Biology. 6 (3), 209-217 (2010).
- Plénat, F., et al. Formaldehyde fixation in the third millennium. Annales De Pathologie. 21 (1), 29-47 (2001).
- Salic, A., Mitchison, T. J. A chemical method for fast and sensitive detection of DNA synthesis in vivo. Proceedings of the National Academy of Sciences. 105 (7), 2415-2420 (2008).
- Wang, N. S., Minassian, H. The formaldehyde-fixed and paraffin-embedded tissues for diagnostic transmission electron microscopy: A retrospective and prospective study. Human Pathology. 18 (7), 715-727 (1987).
- Grifo, J. A., et al. Characterization of eukaryotic initiation factor 4A, a protein involved in ATP-dependent binding of globin mRNA. Journal of Biological Chemistry. 257 (9), 5246-5252 (1982).
- Li, Y. Commonly used tag combinations for tandem affinity purification. Biotechnology and Applied Biochemistry. 55 (2), 73-83 (2010).
- Blum, S., et al. ATP hydrolysis by initiation factor 4A is required for translation initiation in Saccharomyces cerevisiae. Proceedings of the National Academy of Sciences. 89 (16), 7664-7668 (1992).
- Merrick, W. C. eIF4F: A Retrospective. Journal of Biological Chemistry. 290 (40), 24091-24099 (2015).
- Rogers, G. W., Komar, A. A., Merrick, W. C. eIF4A: The godfather of the DEAD box helicases. Progress in Nucleic Acid Research and Molecular Biology. 72, 307-331 (2002).

