Undersøgelser af Chaperone-Cochaperone interaktioner ved hjælp af homogen perle-baseret assay
Summary
Denne protokol præsenterer en teknik til sondering protein-protein interaktioner ved hjælp af glutathion-linked donor perler med GST-fusioneret TPR-motiv co-chaperones og acceptor perler kombineret med en Hsp90-afledt peptid. Vi har brugt denne teknik til at screene små molekyler til at forstyrre Hsp90-FKBP51 eller Hsp90-FKBP52 interaktioner og identificeret potente og selektive Hsp90-FKBP51 interaktionshæmmere.
Abstract
Målretning af varmechokproteinet 90 (Hsp90)-cochaperone-interaktioner giver mulighed for specifikt at regulere Hsp90-afhængige intracellulære processer. Den bevarede MEEVD pentapeptid på C-terminus af Hsp90 er ansvarlig for samspillet med tetratricopeptid repeat (TPR) motiv af co-chaperones. FK506-bindende protein (FKBP) 51 og FKBP52 er to lignende TPR-motiv co-chaperones involveret i steroid hormon-afhængige sygdomme med forskellige funktioner. Derfor giver identifikation af molekyler, der specifikt blokerer interaktioner mellem Hsp90 og FKBP51 eller FKBP52, et lovende terapeutisk potentiale for flere menneskelige sygdomme. Her beskriver vi protokollen for en forstærket selvlysende nærhed homogen analyse til sonde interaktioner mellem Hsp90 og dens partner co-chaperones FKBP51 og FKBP52. For det første har vi renset TPR-motivholdige proteiner FKBP51 og FKBP52 i glutathion S-transferase (GST)-mærket form. Ved hjælp af glutathion-forbundet donor perler med GST-fusioneret TPR-motiv proteiner og acceptor perler kombineret med en 10-mer C-terminal peptid af Hsp90, har vi undersøgt protein-protein interaktioner i et homogent miljø. Vi har brugt denne analyse til at screene små molekyler til at forstyrre Hsp90-FKBP51 eller Hsp90-FKBP52 interaktioner og identificeret potente og selektive Hsp90-FKBP51 interaktionshæmmere.
Introduction
Molekylære chaperoner bidrager til protein homøostase, herunder protein foldning, transport, og nedbrydning. De regulerer flere cellulære processer og er forbundet med mange sygdomme som kræft og neurodegenerative sygdomme1. Varmechokprotein 90 (Hsp90) er en af de vigtigste chaperoner, hvis funktion er afhængig af kropsbygningsændringer drevet af ATP hydrolyse og binding med klientproteiner medieret af sine co-chaperones2. På trods af et indlysende potentiale i Hsp90 som det terapeutiske mål udgør finjustering af dets funktion en stor udfordring. Der er flere Hsp90-hæmmere rettet mod N-terminal ATP-bindingsregionen, som er blevet evalueret i kliniske forsøg, men ingen af dem er godkendt til markedsføring3. På grund af manglen på en veldefineret ligandbindende lomme4har målretning mod C-terminal-regionen Hsp90 haft begrænset succes4. For nylig er afbrydelse af Hsp90-cochaperone interaktioner med små molekyler blevet undersøgt som en alternativ strategi5. Målretning af Hsp90-cochaperone interaktioner ville ikke fremkalde generelle celle stressrespons og giver mulighed for specifikt at regulere forskellige intracellulære processer. Den bevarede MEEVD pentapeptid ved C-terminus af Hsp90 er ansvarlig for samspillet med tetratricopeptid repeat (TPR) motiv af co-chaperones6. Af de 736 TPR-motivholdige proteiner, der er kommenteret i humanproteindatabasen, interagerer ~ 20 forskellige proteiner med Hsp90 via dette peptid7. Molekyler, der konkurrerer om MEEVD peptidbinding, ville forstyrre samspillet mellem Hsp90 og co-chaperones, der indeholder et TPR-domæne. Peptidbindingsstedet har en lignende tertiær struktur, men den overordnede homologi mellem forskellige TPR-motivdomæner er relativt lav7, hvilket giver mulighed for at identificere molekyler, der specifikt er i stand til at blokere interaktioner mellem Hsp90 og bestemte TPR-motiv co-chaperones. Blandt disse TPR-motiv co-chaperones, FK506-bindende protein (FKBP) 51 og FKBP52 er regulatorer af steroid hormon receptor (SHR) signalering og involveret i flere steroid hormon-afhængige sygdomme, herunder kræft, stress-relaterede sygdomme, metaboliske sygdomme, og Alzheimers sygdom8. Selvom FKBP51 og FKBP52 deler > 80% sekvenslighed, er deres funktioner forskellige: FKBP52 er en positiv regulator for SHR-aktivitet, mens FKBP51 er en negativ regulator i de fleste tilfælde8. Derfor giver identifikation af molekyler, der specifikt blokerer interaktioner mellem Hsp90 og FKBP51 eller FKBP52, et lovende terapeutisk potentiale for relaterede sygdomme.
Enmplified Luminescent Proximity Homogenes Assay (AlphaScreen) blev først udviklet i 1994 af Ullman EF et al.9. Nu er det meget udbredt til at opdage forskellige typer af biologiske interaktioner, såsom peptid10, protein11, DNA12,RNA13,og sukker14. I denne teknik er der to slags perler (diameter 200 nm), den ene er donorperle og den anden er acceptor perlen. Biomolekylerne er immobiliseret på disse perler; deres biologiske interaktioner bringer donor- og acceptorperler i nærheden. Ved 680 nm lyser og omdanner en fotoensibilisator i donorperlen ilt til singlet oxygen. Fordi singlet ilt har en kort levetid, kan det kun diffuse op til 200 nm. Hvis acceptor perlen er i nærheden, dens thioxen derivat reagerer med singlet ilt generere chemiluminescens ved 370 nm. Denne energi aktiverer yderligere fluorophorer i samme accept eller perle til at udsende lys ved 520-620 nm15. Hvis de biologiske interaktioner afbrydes, kan acceptorperperen og donorperlen ikke nå nærhed, hvilket resulterer i det enkelte iltfald og lavtproducerede signal.
Her beskriver vi en protokol ved hjælp af denne teknik til screening af små molekyler, der hæmmer interaktioner mellem Hsp90 og TPR co-chaperones, især FKBP51 og FKBP52. De 10 aminosyre lange peptider svarende til Hsp90 ekstreme C-endestation er knyttet til acceptor perler. Renset GST-mærkede TPR co-chaperones interagerer med glutathion-linkede donorperler. Når samspillet mellem Hsp90-afledte peptider og TPR-motiv co-chaperones bringer perlerne sammen, produceres et forstærket signal (Figur 1A). Hvis de screenede små molekyler kan hæmme samspillet mellem Hsp90 og TPR-motiv co-chaperones, vil dette forstærkede signal blive reduceret (Figur 1B). Deres IC50 kan beregnes ved kvantitativ måling. Denne protokol kan udvides til enhver chaperone – TPR-motiv co-chaperone interaktioner af interesse og er af stor betydning i udviklingen af nye molekyler, der specifikt blokerer samspillet mellem Hsp90 og FKBP51 eller FKBP52.
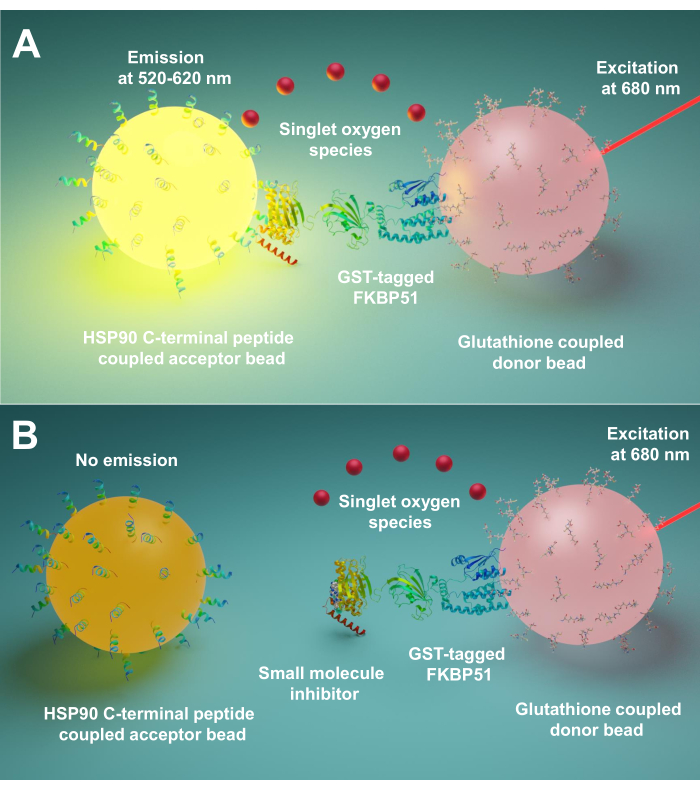
Figur 1: Det grundlæggende princip i denne analyse. (A) Renset GST-FKBP51 interagerer med glutathion-linkede donorperler. De 10 aminosyre lange peptider svarende til den ekstreme C-endestation af Hsp90 er knyttet til acceptor perler. Samspillet mellem Hsp90-afledte peptider og TPR domæne FKBP51 bringer donor og acceptor perler i nærheden. Ved 680 nm lyser og omdanner en fotoensibilisator i donorperlen ilt til singlet oxygen. Thioxen-derivatet på acceptorperlen reagerer med singlet oxygen og genererer chemiluminescens ved 370 nm. Denne energi aktiverer yderligere fluorophorer i samme accept eller perle til at udsende lys ved 520-620 nm. (B) Når små molekyler hæmmer samspillet mellem Hsp90 og FKBP51, kan donor- og acceptorperlerne ikke nå nærhed. Derefter henfalder singlet oxygen med kort levetid, og der produceres ikke noget påviseligt signal. Klik her for at se en større version af dette tal.
Protocol
Representative Results
Discussion
Her beskriver vi en protokol ved hjælp af analysen til screening af små molekyler, der hæmmer interaktioner mellem Hsp90 og TPR-motiv co-chaperones, især FKBP51 og FKBP52. Dens høje Z ‘score (>0,8) viser robusthed og pålidelighed for en høj-throughput format. Resultater kan opnås inden for en time, og små mængder af perler, protein og forbindelser er påkrævet. Desuden kan denne protokol let udvides til enhver Hsp90/Hsp70 – TPR-motiv co-chaperone interaktioner af interesse. Flere TPR-motiv co-chaperones af Hsp…
Disclosures
The authors have nothing to disclose.
Acknowledgements
Denne undersøgelse blev støttet af bevillinger fra Swedish Research Council (2018-02843), Brain Foundation (Fo 2019-0140), Foundation for Geriatric Diseases ved Karolinska Institutet, Gunvor og Josef Anérs Foundation, Magnus Bergvalls Foundation, Gun and Bertil Stohnes Foundation, Tore Nilssons Foundation for medical research, Margaretha af Ugglas foundation og Foundation for Old Servants.
Materials
| 384-well plates | Perkin Elmer | 6008350 | Assay volume 25 ml |
| Amicon 10.000 MWCO centrifugation unit | Millipore | UFC901008 | Concentrate protein |
| Ampicillin | Sigma | A0166 | Antibiotics |
| Bacteria shaker Unimax 1010 | Heidolph | Culture bacteria | |
| cDNA clones for human FKBP51 | Source BioScience | clone id: 5723416 | pCMV-SPORT6 vector |
| cDNA clones for human FKBP52 | Source BioScience | clone id: 7474554 | pCMV-SPORT6 vector |
| Chemically Competent E. coli | Invitrogen | C602003 | One Shot BL21 Star (DE3) |
| Data analysis software | GraphPad Prism | 9.0.0 | Analysis data and make figures |
| Data analysis software | Excel | Analysis data | |
| DMSO | Supelco | 1.02952.1000 | Dilute compounds |
| DPBS | Gibco | 14190-144 | Prepare solution |
| EDTA | Calbiochem | 344504 | Prevent proteolysis during sonication |
| Glutathione | Sigma | G-4251 | Elute GST-tagged proteins |
| Glutathione donor beads | Perkin Elmer | 6765300 | Donor bead |
| GST-trap column | Cytiva (GE Healthcare) | 17528201 | Purify GST-tagged proteins |
| Isopropyl-β-D-thiogalactoside | Thermo Fisher Scientific | R0392 | Induce protein expression |
| LB Broth (Miller) | Sigma | L3522 | Microbial growth medium |
| PCR instrument | BIO-RAD | S1000 Thermal Cycler | Amplification/PCR |
| PD-10 column | Cytiva (GE Healthcare) | 17085101 | Solution exchange |
| pGEX-6P-1 vector | Cytiva (GE Healthcare) | 28954648 | Plasmid |
| pGEX-6P-2 vector | Cytiva (GE Healthcare) | 28954650 | Plasmid |
| Plate reader | Perkin Elmer | EnSpire 2300 Multilabel Reader | Read alpha plate |
| Plate reader software | Perkin Elmer | EnSpire Manager | Plate reader software |
| Plate reader software protocol | Perkin Elmer | Alpha 384-well Low volume | Use this protocol to read plate |
| PMSF | Sigma | P7626 | Prevent proteolysis during sonication |
| protease inhibitor cocktail | Sigma | S8830 | Prevent proteolysis during sonication |
| Sodium azide | Sigma | S2002 | As a preservative |
| Sodium cyanoborohydride (NaBH3CN) | Sigma | 156159 | Activates matrix for coupling |
| Ten amino acid peptide NH2-EDASRMEEVD-COOH corresponding to amino acids 714-724 of human Hsp90 beta isoform | Peptide 2.0 inc | Synthesize Hsp90 C-terminal peptide | |
| Test-Tube Rotator | LABINCO | Make end-over-end agitation | |
| Tris-HCl | Sigma | 10708976001 | Block unreacted sites of acceptor beads |
| Tween-20 | Sigma | P1379 | Prevent beads aggregation |
| Ultra centrifuge Avanti J-20 XP | Beckman Coulter | Centrifuge to get bacteria cell pellets | |
| Ultrasonic cell disruptor | Microson | Sonicate cells to release protein | |
| Unconjugated acceptor beads | Perkin Elmer | 6762003 | Acceptor beads |
| XCell SureLock Mini-Cell and XCell II Blot Module | Invitrogen | EI0002 | SDS-PAGE |
References
- Muchowski, P. J., Wacker, J. L. Modulation of neurodegeneration by molecular chaperones. Nature Reviews Neuroscience. 6 (1), 11-22 (2005).
- Eckl, J. M., Richter, K. Functions of the Hsp90 chaperone system: lifting client proteins to new heights. International Journal of Biochemistry and Molecular Biology. 4 (4), 157-165 (2013).
- Yuno, A. Clinical evaluation and biomarker profiling of Hsp90 inhibitors. Methods in Molecular Biology. 1709, 426-441 (2018).
- Dutta Gupta, S., Bommaka, M. K., Banerjee, A. Inhibiting protein-protein interactions of Hsp90 as a novel approach for targeting cancer. European Journal of Medicinal Chemistry. 178, 48-63 (2019).
- Pavlov, P. F., Hutter-Paier, B., Havas, D., Windisch, M., Winblad, B. Development of GMP-1 a molecular chaperone network modulator protecting mitochondrial function and its assessment in fly and mice models of Alzheimer’s disease. Journal of Cellular and Molecular Medicine. 22 (7), 3464-3474 (2018).
- Young, J. C., Obermann, W. M., Hartl, F. U. Specific binding of tetratricopeptide repeat proteins to the C-terminal 12-kDa domain of hsp90. Journal of Biological Chemistry. 273 (29), 18007-18010 (1998).
- Scheufler, C., et al. Structure of TPR domain-peptide complexes: critical elements in the assembly of the Hsp70-Hsp90 multichaperone machine. Cell. 101 (2), 199-210 (2000).
- Storer, C. L., Dickey, C. A., Galigniana, M. D., Rein, T., Cox, M. B. FKBP51 and FKBP52 in signaling and disease. Trends in Endocrinology & Metabolism. 22 (12), 481-490 (2011).
- Ullman, E. F., et al. Luminescent oxygen channeling immunoassay: measurement of particle binding kinetics by chemiluminescence. Proceedings of the National Academy of Sciences of the United States of America. 91 (12), 5426-5430 (1994).
- Wigle, T. J., et al. Screening for inhibitors of low-affinity epigenetic peptide-protein interactions: an AlphaScreen-based assay for antagonists of methyl-lysine binding proteins. Journal of Biomolecular Screening. 15 (1), 62-71 (2010).
- Guenat, S., et al. Homogeneous and nonradioactive high-throughput screening platform for the characterization of kinase inhibitors in cell lysates. Journal of Biomolecular Screening. 11 (8), 1015-1026 (2006).
- Sabatucci, A., et al. A new methodological approach for in vitro determination of the role of DNA methylation on transcription factor binding using AlphaScreen(R) analysis: Focus on CREB1 binding at hBDNF promoter IV. Journal of Neuroscience Methods. 341, 108720 (2020).
- Mills, N. L., Shelat, A. A., Guy, R. K. Assay Optimization and Screening of RNA-Protein Interactions by AlphaScreen. Journal of Biomolecular Screening. 12 (7), 946-955 (2007).
- Huang, X., et al. A competitive alphascreen assay for detection of hyaluronan. Glycobiology. 28 (3), 137-147 (2018).
- Principles of alphascreen amplified luinescent proximmity homogenous assay. PerkinElmer Life Sciences Available from: https://www.perkinelmer.com/lab-solutions/resources/docs/APP_AlphaScreen_Principles.pdf (2021)
- Zhang, J. H., Chung, T. D., Oldenburg, K. R. A Simple statistical parameter for use in evaluation and validation of high throughput screening assays. Journal of Biomolecular Screening. 4 (2), 67-73 (1999).

