En hög genomströmnings microplate feeder analys för kvantifiering av konsumtion i Drosophila
Summary
Mikroplåtmataranalysen erbjuder en ekonomisk, hög genomströmningsmetod för kvantifiering av flytande livsmedelskonsumtion i Drosophila. En 3D-utskriven enhet ansluter en 96-brunns mikroplatta där flugor är inrymda i en 1536-brunns mikroplatta från vilken flugor konsumerar en matningslösning med ett spårämne. Lösningsvolymnedgången mäts spektralmässigt.
Abstract
Kvantifiering av födointaget i Drosophila används för att studera de genetiska och fysiologiska grunderna för konsumtionsrelaterade egenskaper, deras miljöfaktorer och de toxikologiska och farmakologiska effekterna av många ämnen. Få metoder som för närvarande implementeras är mottagliga för mätning av hög data flöde. Microplate Feeder Assay (MFA) utvecklades för att kvantifiera konsumtionen av flytande mat för enskilda flugor med hjälp av absorbans. I denna analys konsumerar flugor flytande matmedium från utvalda brunnar i en 1536-brunns mikroplatta. Genom att införliva ett utspädt spårämne i det flytande livsmedelsmediet och lasta en känd volym i varje brunn återspeglar absorbansmätningarna av den brunn som förvärvats före och efter konsumtionen den resulterande volymförändringen (dvs. förbrukad volym). För att möjliggöra analys av hög genomströmning med den här metoden utformades en 3D-printad mankpar som gör att flugor kan sorteras individuellt i 96-brunns mikroplattor. Denna enhet orienterar exakt mikroplattor med 96 och 1536 brunnar för att ge varje fluga tillgång till upp till 4 brunnar för konsumtion, vilket möjliggör kvantifiering av livsmedelspreferenser utöver regelbunden konsumtion. Dessutom har anordningen barriärremsor som växlar mellan öppna och stängda lägen för att möjliggöra kontrollerad inneslutning och utsättning av en kolonn med prover åt gången. Denna metod möjliggör höga genomströmningsmätningar av förbrukning av vattenlösningar av många flugor samtidigt. Det har också potential att anpassas till andra insekter och att screena konsumtion av näringsämnen, toxiner eller läkemedel.
Introduction
Drosophila melanogaster har sett bred användning som en genetisk modellorganism för att studera de biologiska grunderna för matintag och egenskaper i samband med konsumtion1. Det uppskattas att 65% av människans sjukdomsframkallande gener har funktionella homologer i flugor, med en betydande andel av dem som uttrycks i funktionellt likvärdiga vävnader mellan flugor och människor2. Dessutom gör D. melanogasters storlek, korta intergenerationell tid, enkelt underhåll och genetisk tractability det till en attraktiv modell för studier om konsumtion av näringsämnen3,4 ochtoxikologiska och farmakologiska effekter av en mängd olika ämnen, inklusive insekticider5, föroreningar6, läkemedel7, och läkemedel av missbruk8,9,10.
I många fall kräver studien av sådana egenskaper exakt kvantifiering av konsumtionen. Metoder för kvantifiering av förbrukningen är olika och inkluderar CApillary FEeder (CAFE) analys11, MAnual FEeding (MAFE) analys12,Proboscis Extension Response (PER) analys13,tracer färgämneextraktion 14,15,oligonukleotid spårämneextraktion 16, och radio-isotopextraktion 5,17. De senaste ansträngningarna har fokuserat på att förbättra genomströmningen av dessa analyser, som i Expresso-analysen18 eller det tallriksbaserade Hela djurfoder FLat (WAFFL) -systemet19. Trots deras nytta kan dessa analyser vara komplicerade, kostsamma eller arbetsintensiva, vilket hindrar deras användning i studier med hög genomströmning.
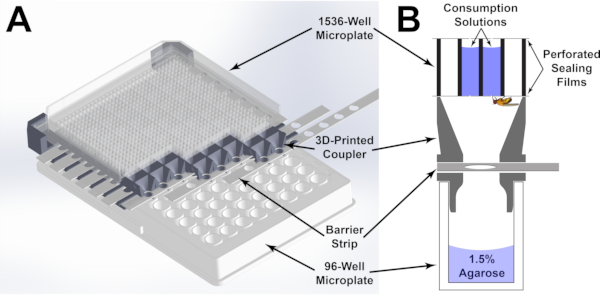
Figur 1:Komponenter i mikroplåtmataranalysen. Mikroplattan med 1536 brunnar är orienterad av det 3D-printade ihopkopplingen så att varje brunn i den nedre 96-brunnsmikroplattan har tillgång till fyra brunnar i den övre mikroplattan på 1536 brunnar. Tillträdet till brunnarna kan styras genom att justera positionen för barriärremsor som slitsas genom ihopkopplingen. B)En grafisk återgivning av varje brunn i mikroplattans mataranalys. Förbrukningslösningar behålls i varje brunn med hjälp av en tätningsfilm som har perforerats för att ge tillgång till flugan. Klicka här om du vill visa en större version av den här figuren.
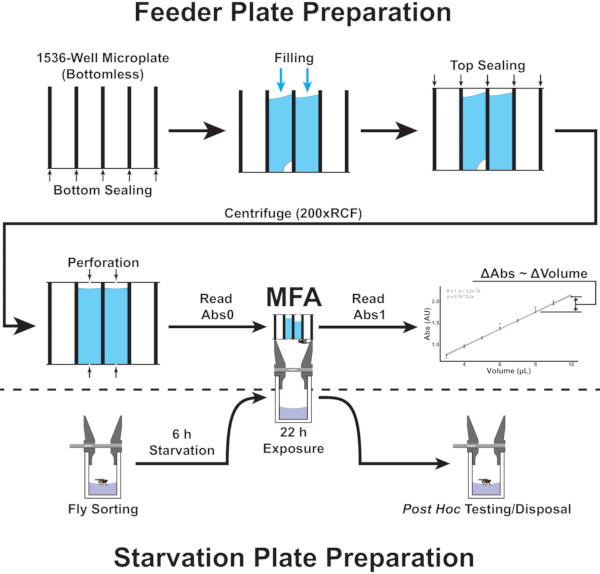
Figur 2: Översikt över procedurerna i mikroplåtmataranalysen. Figuren visar ett flödesdiagram som motsvarar steg 4.1-5.8 i protokollet. Klicka här om du vill visa en större version av den här figuren.
För att övervinna dessa hinder, Microplate Feeder Assay (MFA; Figur 1) utvecklades. I denna analys inrymts flugor individuellt i 96-brunns mikroplattor. Varje mikroplatta är kopplat till en 1536-brunns mikroplatta med en anpassad 3D-utskriven enhet. Enheten orienterar exakt de två plattorna så att var och en flyger i sin respektive brunn på 96-brunnsplattan har tillgång till 4 brunnar i 1536-brunnsmikroplattan. Genom att använda en bottenlös 1536-brunnsplatta och tätningsfilmer doseras lösningar i utvalda brunnar och perforeras med exakta nålar med diametern 0,25 mm för att ge tillgång till flugorna. Att tillåta förbrukning direkt från en mikroplatta möjliggör kritiska absorbansbaserade mätningar med hjälp av en mikroplatta. Ett utspädt spårämne ingår i konsumtionsmediet, och förändringen i absorbansen efter exponering används för att bestämma den förbrukade volymen (figur 2 och figur 3). Eftersom vätskan i varje brunn approximerar en kolonn av vätska, kommer volymetriska skillnader att manifesteras som skillnader i kolumnens höjd. (Figur 3A) Enligt Beer-Lambert lag20:
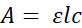
där A är absorbansen är ε molarabsorptionskoefficienten för den försvagande analyten, l är den optiska banans längd och c är koncentrationen av den dämpande analyten. Med konstant molarabsorptionskoefficient och koncentration beror således förändringar i absorbansen enbart på förändringar i den optiska ljusvägen, dvs. vätskenivån inom en viss brunn. Genom att mäta absorbansen före och efter exponeringen återspeglar den proportionella förändringen i absorbans den proportionella volymförändringen(figur 3B).
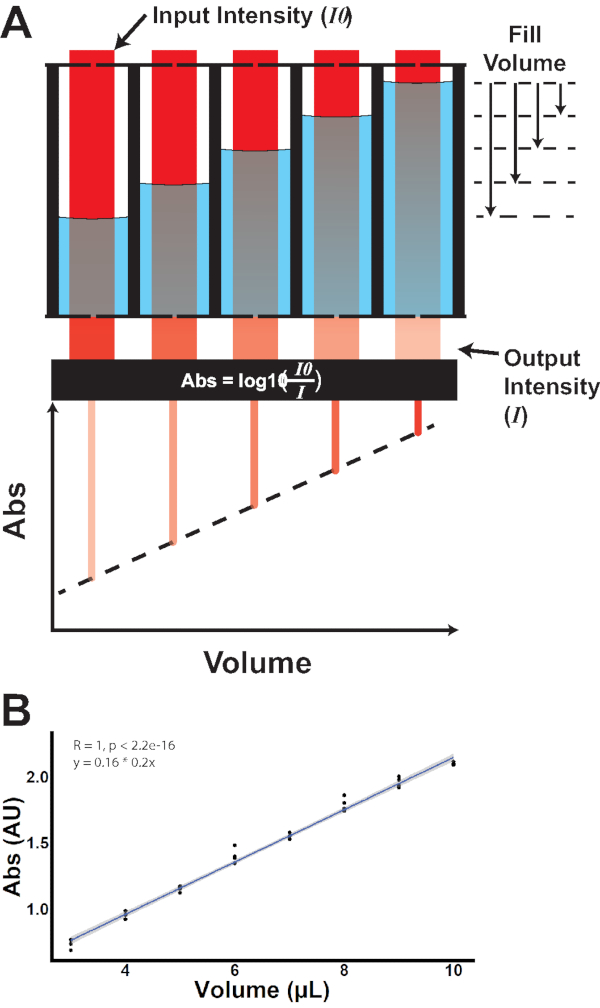
Figur 3:Absorbansbaserad kvantifiering av brunnsvolym. (A) Inincidentsljus med känd ingångsintensitet (I0) korsar varje brunn. Dämpning av ljus vid olika fyllnadsvolymer ger olika effektintensiteter (I), som uppvisar ett linjärt förhållande mellan volym och absorbans. B)Empirisk mätning av absorbans kontra volym. Klicka här om du vill visa en större version av den här figuren.
Baserat på volymförändringen kan mängden intag av föreningar beräknas utifrån dess kända koncentration i utfodringslösningen. De delar som behövs för analysen är låga i kostnad och har en hög grad av återanvändbarhet, vilket avsevärt minskar de återkommande kostnaderna för analysen. Således erbjuder detta förfarande en prisvärd, hög genomströmningsmetod för exakt kvantifiering av förbrukningen.
Protocol
Representative Results
Discussion
Studien beskriver ett nytt protokoll för kvantifiering av konsumtion i Drosophila: Microplate Feeder Assay (MFA). I denna analys förbrukar flugor från förseglade brunnar av en 1536-brunns mikroplatta genom kontrollerade perforeringar(figur 1, figur 2; Kompletterande video S.1). Eftersom flytande livsmedel färgas och tillhandahålls via mikroplatta kan mätningar av matens optiska absorbans erhållas med hjälp av en mikroplåtspektrofotometer (figur 3). På detta sätt bestäms förbrukningen genom att absorbera före och efter förbrukningen och sedan tillämpa denna andel på den kända volym som dispenserats före konsumtionen. Detta kontrollerades empiriskt genom att man mätte absorbansen av olika volymer av det färgade mediet(figur 3B).
För att utveckla denna analys behövdes en enhet som kunde utnyttja den absorbansbaserade kvantifieringen av förbrukningen. Att testa flugor i mikroplåtformat är tilltalande eftersom det kompletterar mikroplattan som används för att dela ut mat och möjliggör flexibilitet vid val av flera tallriksformat (t.ex. 6-, 12-, 48- eller 96-brunnsformat) genom att justera kopplade geometrin. Ett 96-brunns mikroplåtformat valdes för att möjliggöra individuell flugkultur.
Den 3D-utskrivna anordningen (figur 1) orienterar exakt matarplattan med 1536 brunnar med 96-brunns odlingsplattan, vilket ger varje fluga tillgång till upp till 4 brunnar på matarplattan för konsumtion. För att ge tillräckligt med tid för att distribuera flugor till höljesplattan och för att kontrollera analysinitiering, inkluderar enheten växlande barriärremsor som innehåller flugorna i sina respektive brunnar och förhindrar överträdelser. De filer som behövs för att skaffa eller modifiera dessa delar tillhandahålls (Kompletterande filer S.2–S.3), liksom de nödvändiga tillverkningsinstruktionerna för de relevanta delarna(kompletterande fil S.4).
MFA ger en enkel hög genomströmningsmetod som kompletterar mer utarbetade metoder för att övervaka Drosophilautfodringsbeteende 18,21,22. MFA erbjuder flera fördelar jämfört med andra metoder som används för att kvantifiera matintag. Dataflödet ökas genom att kvantifiera förbrukningen med hjälp av en plåtläsare. Detta eliminerar manuella mätningar och undanröjer manuell datainmatning. Data är också mottagliga för programmatisk extraktion och bearbetning. Dessutom ökar det högre genomströmningen det möjliga antalet biologiska replikat, särskilt jämfört med kommunala matardesigner, vilket avsevärt ökar kraften att upptäcka små skillnader i konsumtion. Med hjälp av MFA kan en enda experimenterare kvantifiera förbrukningen eller preferensen för över 500 flugor per nattkörning av analysen. Genom överlappande körningar av analysen kan över 2 000 flugor testas under en 5-dagarsperiod. Slutligen finns det långsiktiga kostnadsbesparingar på grund av återanvändbarheten av mikroplattor och kopplade(kompletterande fil S.5). Med hjälp av MFA kan den uppskattade kostnaden per analys vara så låg som $ 14.80, med en $ 127.60 i förskottskostnad för utrustningen. Med hjälp av den klassiska CApillary FEeder (CAFE) -analysen, som kräver kostsamma precisionsmikrokalyer, är den uppskattade kostnaden per analys för ett jämförbart antal replikat $ 46.08. Även om det finns en förskottsinvestering i förvärvet av nödvändig utrustning kan minskningen av återkommande kostnader leda till betydande besparingar, särskilt i fall där upprepade tester utförs.
Som med alla analyser har MFA vissa begränsningar. Framför allt kräver det tillgång till en mikroplatta spektrofotometer som kan avläsa 1536-brunns mikroplattor. Dessutom gör beroendet av absorbansmätningar för kvantifiering metoden mottaglig för optisk interferens. Detta visar sig som negativa förbrukningsvärden för en liten delmängd av de prover som testats. Näringsämnen, läkemedel, läkemedel eller toxiner av intresse måste också vara vattenlösliga för att vara förenliga med analysen.
Trots sina begränsningar erbjuder denna metod en hög genomströmningsmetod för att kvantifiera konsumtionsbeteenden i Drosophila. Dessutom kan kopplingsanordningen enkelt modifieras för att acceptera många plåtformat, så att den rymmer en mängd olika insektsarter.
Disclosures
The authors have nothing to disclose.
Acknowledgements
Detta arbete stöddes av ett bidrag från National Institute on Drug Abuse (U01 DA041613) till TFCM och RRHA.
Materials
| 0.25 mm Diameter Needers | Rave Scientific | RS-MN-52-001012 | |
| 0.45 µm Syringe Filters | Olympus Plastics | 25-245 | |
| 10 mL Disposable Syringe | EXELINT | 26200 | |
| Agarose | Fisher Scientific | BP1600 | |
| Barrier Strips (Laser Cut) | Ponoko | – | Material: clear PETG, 0.5mm thickness; Supplementary File: |
| Centrifuge 5810 R | Eppendorf | 22625501 | |
| Centrifuge Rotor A-4-62 with micro-titer plate buckets | Eppendorf | 22638041 | |
| FD&C Blue #1 | Spectrum Chemical Mfg Corp | FD110 | |
| Film Sealing Paddle | Fisher Scientific | 50-563-280 | |
| Flystuff Flypad | Genesee Scientific | #59-114 and #59-119 | CO2 Anesthesia: The Flypads come in two sizes, either of which is appropriate |
| Microplate Coupler (3D Printed) | Shapeways | – | Material: Multi Jet Fusion nylon (MJF PA12); Supplementary File: |
| Microplate Lids | Greiner Bio-One | 656170 | |
| Molecular Devices SpectraMax iD5 | Molecular Devices | – | Any microplate reader with 1536-well resolution will do. |
| Needle Probe Holder | Rave Scientific | RS-MN-52-001000 | |
| Polyester Sealing Film | Excel Scientific, Inc. | 100-SEAL-PLT | |
| Polystyrene 96-well microplates | Greiner Bio-One | 655101 | |
| Polystyrene, Bottomless, 15396-well microplates | Greiner Bio-One | 783000 | Made to Order; allow for adequate lead time when purchasing. |
| Rubber Bands | |||
| Sucrose | Sigma | S7903 | |
| Weather Stripping | 1/2" x 1/8" High Density Self Adhesive Neoprene Rubber | ||
| Yeast Extract | Fisher Scientific | BP1422 |
References
- Wong, R., Piper, M. D. W., Wertheim, B., Partridge, L. Quantification of food intake in Drosophila. PLoS ONE. 4 (6), (2009).
- Ugur, B., Chen, K., Bellen, H. J. Drosophila tools and assays for the study of human diseases. Disease Models & Mechanisms. 9 (3), 235-244 (2016).
- Spitaler, U., et al. Yeast species affects feeding and fitness of Drosophila suzukii adults. Journal of Pest Science. 93 (4), 1295-1309 (2020).
- Wang, Q. P., et al. PGC1α controls sucrose taste sensitization in Drosophila. Cell Reports. 31 (1), 107480 (2020).
- Valtierra-de-Luis, D., et al. Quantification of dose-mortality responses in adult Diptera: Validation using Ceratitis capitata and Drosophila suzukii responses to spinosad. PLoS ONE. 14 (2), 1-11 (2019).
- Williams, M. J., et al. Exposure to bisphenol A affects lipid metabolism in Drosophila melanogaster. Basic & Clinical Pharmacology & Toxicology. 114 (5), 414-420 (2014).
- Jajoo, A., Donlon, C., Shnayder, S., Levin, M., McVey, M. Sertraline induces DNA damage and cellular toxicity in Drosophila that can be ameliorated by antioxidants. Scientific Reports. 10 (1), 1-12 (2020).
- Fochler, S., et al. Genetics of alcohol consumption in Drosophila melanogaster. Genes, Brain and Behavior. 16 (7), 675-685 (2017).
- Highfill, C. A., Baker, B. M., Stevens, S. D., Anholt, R. R. H., Mackay, T. F. C. Genetics of cocaine and methamphetamine consumption and preference in Drosophila melanogaster. PLOS Genetics. 15 (5), 1007834 (2019).
- Keebaugh, E. S., Park, J. H., Su, C., Yamada, R., Ja, W. W. Nutrition Influences caffeine-mediated sleep loss in Drosophila. Sleep. 40 (11), (2017).
- Ja, W. W., et al. Prandiology of Drosophila and the CAFE assay. Proceedings of the National Academy of Sciences. 104 (20), 8253-8256 (2007).
- Qi, W., et al. A quantitative feeding assay in adult Drosophila reveals rapid modulation of food ingestion by its nutritional value. Molecular Brain. 8 (1), 87 (2015).
- Shiraiwa, T., Carlson, J. R. Proboscis extension response (PER) assay in Drosophila. Journal of Visualized Experiments: JoVE. (3), e193 (2007).
- Shell, B. C., et al. Measurement of solid food intake in Drosophila via consumption-excretion of a dye tracer. Scientific Reports. 8 (1), 1-13 (2018).
- Wu, Q., et al. Excreta quantification (EX-Q) for longitudinal measurements of food intake in Drosophila. iScience. 23 (1), 100776 (2020).
- Park, A., Tran, T., Atkinson, N. S. Monitoring food preference in Drosophila by oligonucleotide tagging. Proceedings of the National Academy of Sciences of the United States of America. 115 (36), 9020-9025 (2018).
- Deshpande, S. A., et al. Quantifying Drosophila food intake: Comparative analysis of current methodology. Nature Methods. 11 (5), 535-540 (2014).
- Yapici, N., Cohn, R., Schusterreiter, C., Ruta, V., Vosshall, L. B. A Taste circuit that regulates ingestion by integrating food and hunger signals. Cell. 165 (3), 715-729 (2016).
- Jaime, M. D. L. A., et al. The high-throughput WAFFL system for treating and monitoring individual Drosophila melanogaster adults. bioRxiv. , (2018).
- IUPAC. . Compendium of Chemical Terminology (The “Gold Book”). , (1997).
- Itskov, P. M., et al. Automated monitoring and quantitative analysis of feeding behaviour in Drosophila. Nature Communications. 5, 4560 (2014).
- Ro, J., Harvanek, Z. M., Pletcher, S. D. FLIC: high-throughput, continuous analysis of feeding behaviors in Drosophila. PLoS One. 9 (6), 101107 (2014).

