Dissektion og immunohistochemistry af Drosophila Voksen Ben til at opdage ændringer på Neuromuscular Junction for en identificeret Motor Neuron
Summary
Vi beskriver en dissektionsteknik, der bevarer arkitekturen i det neuromuskulære kryds og muliggør en detaljeret immuncytokemisk undersøgelse af motoriske neuroner i det voksne Drosophila-ben .
Abstract
Drosophila melanogaster repræsenterer en genetisk tractable model til at studere neuronal struktur og funktion, og efterfølgende ændringer i sygdomstilstande. Det godt karakteriserede larve neuromuskulære kryds bruges ofte til sådanne undersøgelser. Men, hurtig larve udvikling efterfulgt af muskel histolyse og nervesystem remodeling under metamorfose gør denne model problematisk for studiet af langsomme aldersafhængige degenerative ændringer som dem, der forekommer i amyotrofisk lateral sklerose. Alternativt lever voksne fluer i 90 dage, og det voksne ben kan bruges til at studere motoriske neuronændringer i løbet af voksenlevetiden ved hjælp af in vivo fluorescerende billeddannelse gennem neglebånd. Her beskriver vi en ben dissektionsteknik kombineret med immunocytokemi, som giver mulighed for undersøgelse af molekylære ændringer ved det neuromuskulære kryds af identificerede voksne benmotorneuroner. Disse teknikker kan kombineres med et utal af antistoffer, der mærker både præ- og postsynaptiske strukturer. Sammen disse procedurer giver mulighed for en mere fuldstændig karakterisering af langsomme aldersafhængige ændringer i voksne fluer og kan anvendes på tværs af flere motor neuron sygdom modeller.
Introduction
Motor neuron (MN) sygdomme omfatter en gruppe af heterogene tilstande, der omfatter progressiv degeneration fører til muskelsvind og lammelse som en primær klinisk fænotype1. Selv om det er sjældent med en global prævalens på 4,5 pr. 100.000, forventes denne prævalens at stige med en aldrende befolkning2. Amyotrofisk lateral sklerose (ALS) er den mest almindelige MN-sygdom (MND) og er typisk dødelig inden for kort tid efter diagnosen uden eksisterende sygdomsmodificerende behandlinger til rådighed3. MND’er har fælles en langvarig presymptomatisk fase med tidlige molekylære biomarkørændringer og funktionelle billeddannelsesændringer set hos patienter4. Tidlig præymptomatisk cellulær patologi observeres også i ikke-menneskelige sygdomsmodeller5,6,7,8. Studiet af tidlige ændringer på neuromuskulære junction er vigtigt for at forstå MN sygdom patogenese og kan støtte i udviklingen af tidlig diagnostik og potentielle therapeutics.
Et væld af genetiske og molekylære værktøjer findes i Drosophila at dissekere strukturen og funktionen af neuromuskulære junction (NMJ, se9 for en gennemgang af godt karakteriseret larve NMJ). Disse værktøjer kombineret med en kort levetid gør Drosophila en fremragende model til at studere neurodegenerative ændringer på NMJ. Specifikt, MNs innervating voksne muskler er til stede i hele ~ 90-dages voksen levetid og er underlagt normale aldringsprocesser10,11,12,13. De voksne MNs giver derfor mulighed for at studere langsomme degenerative ændringer i modsætning til larve NMJs, som eksisterer for kun en kort ~ 1 uge periode før metamorfose14,15.
Her beskriver vi en dissektionsprocedure, der giver os mulighed for at foretage immuncytokemisk analyse af MN’er i voksenbenet. Hvert voksent ben er innerveret af ~ 50 MNs, som synapse på det tilhørende ben muskuløs til at drive bevægelse. Benanatomien, den mekaniske fysiologi og neurobiologien er blevet godt beskrevet16,17,18. Axon arbors af ben MNs har tidligere været karakteriseret ved billeddannelse gennem neglebånd i back-fyldt eller genetisk mærket cellepopulationer ved hjælp af bipartit Gal4/ UAS system og billeddannelse metoder er blevet offentliggjort tidligere19. Dissektionsmetoderne, der præsenteres her, bevarer axonforgreningmorphology og giver os mulighed for at udnytte en bred vifte af antistoffer til at mærke forskellige molekylære komponenter i NMJ. Vores tidligere arbejde har fokuseret på fremskrivninger af en defineret MN i metathoracic (3rd) ben, som innerverer skinnebenet levator muskel (tilm) og viser konsekvent arborization mønstre og bouton numre. Oprindeligt studerede vi aldersafhængige ændringer i Drosophila superoxid dismutase 1 (dsod1) mutanter og fandt ændringer i overensstemmelse med demontering af NMJ20. Disse dissektionsmetoder giver mulighed for bedre at karakterisere langsomme degenerative ændringer på NMJ for andre ALS-modeller, grundlæggende undersøgelser af aldring og andre MN-tilknyttede sygdomme.
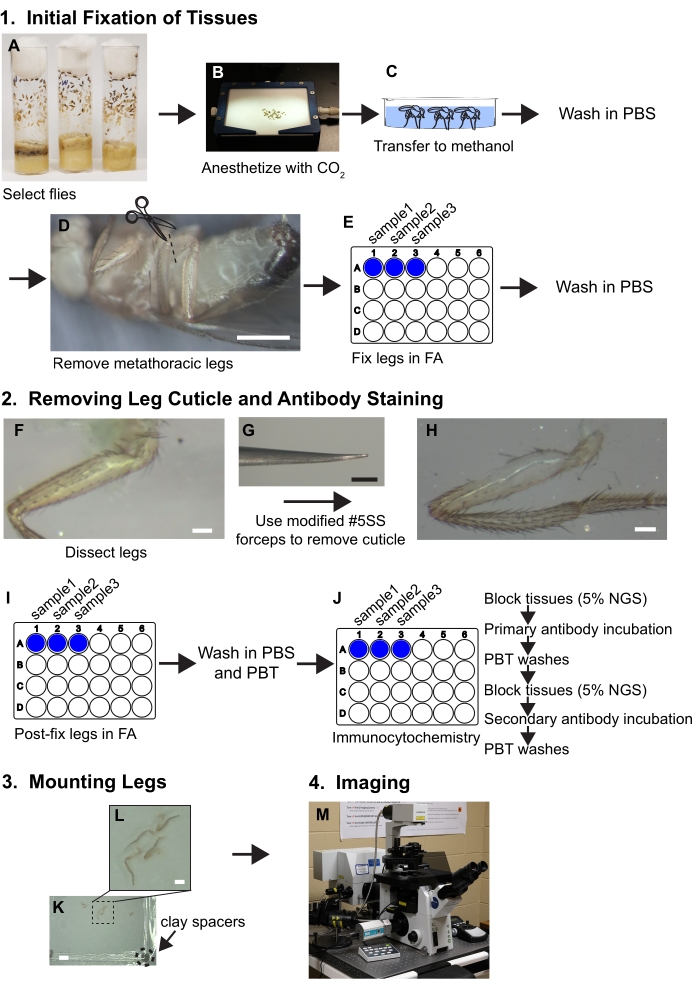
Figur 1. Arbejdsgangsoversigt for dissekering af ben. Se protokollen for at få detaljerede trin. (A,B) Fluer vælges og bedøves. (C) Fluer overføres til methanol og vaskes med PBS. (D) Metathoracic ben fjernes i bunden af coxa mens visualiseret med en dissekering mikroskop (~ 30x forstørrelse); skalalinje = 500 μm. (E) Benene fastgøres derefter i 3,7% formaldehyd/PBS (FA) opløsning i 30 minutter i brønde på 24-brøndsplader, og derefter fjernes FA ved vask med PBS. (F, G, H) Ben overføres til silikone elastomer dissekering bakker og et stykke neglebånd fjernes fra den proksimale lårben ved hjælp af facet sammenkrump, mens visualiseret under en dissekering mikroskop på 80x; skalalinje = 50 μm. (I) Benene er post-dissektion fastsat i FA og vasket i PBS og derefter PBT (PBS + 0,1% ikke-ionisk overfladeaktivt middel). (J) Benene udsættes for immuncytokemisk farvning. (K, L) Ben overføres til en glasrutschebane, ryddes i monteringsmedier og dækkes med en coverlip indeholdende lerstykker; vægtstænger = 2 mm og 500 μm. (M) Benene er afbildet af konfokal mikroskopi. Klik her for at se en større version af dette tal.
Protocol
Representative Results
Discussion
Drosophila voksenbenet er en ideel model til at studere neurodegeneration givet relativ enkelhed med velkaraktererede MNs kortlagt fra neuroblast slægter og stereotype arborization mønstre. Flere rapporter har tidligere brugt ben MNs til undersøgelse af neurodegenerativ sygdom21,22. Disse undersøgelser udnyttede GFP-udtrykke linjer kombineret med mosaik analyse med en undertrykkelig celle markør (MARCM) til billede gennem neglebånd og dokumenteret en række morfologiske ændringer. Imaging voksne NMJs af immunocytochemistry med resected kutikula muliggør yderligere karakterisering med evnen til at spore komplekse molekylære ændringer ved hjælp af en værktøjskasse af antistoffer til rådighed.
Immunocytomidelen af denne protokol er relativt standard og kan implementeres uafhængigt af genotype (se23 for en fremragende beskrivelse af generelle antistoffarvningsmetoder til brug med Drosophila). Desuden kan parametre som fluorescensintensitet, axongrenlængde og boutonnumre og størrelse bestemmes ved hjælp af en række tilgængelige ImageJ-makroer, når billederne er taget, og der er offentliggjort detaljerede metoder til kvantitativ analyse (f.eks. se 24,25,26). Således dissektion teknik er den vigtigste innovation beskrevet her. Før dissektion nedsænkes fluer i en alkohol for at fjerne cuticular kulbrinter. Både ethanol og methanol er almindeligt anvendt til dette formål; Vi har dog kun brugt methanol. Afgørende for dissektion succes er flere faktorer: For det første, ved hjælp af modificerede sammenkædninger med en facet giver mulighed for meget overfladisk kontakt med neglebånd. For det andet ved hjælp af en dissekering mikroskop i stand til 60-100x samlede forstørrelse, således at overfladen af neglebånd er tydeligt synlig. For mikroskoper med lavere maksimal forstørrelse er 2x mål tilgængelige for de fleste almindelige mærker og bør være tilstrækkelige, når de kombineres med eksisterende linser. For det tredje gør det første fikseringstrin neglebånd skørt og lettere at trække væk uden at beskadige muskler nedenunder. Overfiksering på dette trin gør hele benet for stiv til effektiv dissektion. Derfor bør den oprindelige fiksering begrænses til 30 minutter. Formaldehyd fikseringsmiddel vil ikke trænge nok til effektivt at krydse det underliggende væv i løbet af denne korte periode, og dermed en anden fiksering skridt er nødvendig. Før den anden fiksering skal væv opbevares på is for at forhindre nedbrydning og ændringer i morfologien. For det fjerde har vi fundet dissekere prøver, mens kulde er også vigtigt, sandsynligvis af lignende grunde i, at neglebånd er skør og et lille stykke kan lettere fjernes.
Med praksis finder vi ~ 50% af dissektioner vil være anvendelige inden for ingen mærkbar vævsskade. Selv om denne procentdel kan synes lav i forhold til nogle andre væv, dissektion procedure er hurtig, og mange ben kan behandles i 30- 60 minutter. Derfor, selv om succesraterne er lave i første omgang, er det muligt at opnå 4-5 gode prøver for hver eksperimentel gruppe. En begrænsning kan dog være antallet af fluer, der er tilgængelige på et givet tidspunkt, hvis genotyper og/eller alder resulterer i betydelig dødelighed.
En anden begrænsning er, at vi ikke har været i stand til at dissekere andre områder af benet ud over den proksimale region af lårbenet på grund af størrelse. Således kan vi studere identificeret MN arbors innervating TILM pålideligt, og det er muligt at dissekere kutikula over skinnebenet depressor muskel med små ændringer i den måde, benet er orienteret ved dissekering. Men adgang til andre regioner i benet har vist sig vanskeligere uden at forstyrre axonal arkitektur under dissektion.
Her præsenterer vi dissektionsmetoder til at opdage ændringer på den voksne NMJ for definerede NM’er innervering af tilm ved hjælp af immuncytokemi. Benet er nyttigt som et simpelt system, innerveret af kun ~ 50 MNs og indeholder 14 muskler med velbeskrevet anatomi. Den dissekerede ben forberedelse kan bruges på tværs af genotyper og en suite af antistoffer er tilgængelige for NMJ visualisering uden behov for at opbygge genotypically komplekse lagre af reporter genkonstruktioner i mutant baggrunde. Denne tilgang vil muliggøre en mere detaljeret karakterisering af ændringer på NMJ for MN-sygdomme og andre aldersrelaterede tilstande.
Disclosures
The authors have nothing to disclose.
Acknowledgements
Vi takker Eric Roberts for rådgivning om billeddannelse. Vi vil også gerne takke Information Technology Services på Rhode Island College og især Michael Caine og Jake Douglas for videografi. Monoklonale antistoffer mod dlg og anti-brp blev udviklet af henholdsvis UC-Berkeley og Universitaetsklinikim Wuerzburg, og blev fremstillet fra Developmental Studies Hybridoma Bank, skabt af NICHD af NIH og opretholdt på The University of Iowa, Department of Biology, Iowa City, IA 52242, USA. Den forskning, der rapporteres her, blev støttet fuldt ud af Rhode Island Institutional Development Award (IDeA) Network of Biomedical Research Excellence fra National Institute of General Medical Sciences fra National Institutes of Health under tilskudsnummer [P20GM103430].
Materials
| 10x Phosphate Buffered Saline | Fisher Scientific | BP3991 | |
| 24 well plates | Corning | 3473 | Hydrophobic, ultra-low attachment surface |
| 2x objective accessory | Olympus | 110AL2X | Screw-on attachment |
| Anti-ATP5A primary antibody | Abcam | ab14748 | Mouse monoclonal |
| Anti-bruchpilot primary antibody | Developmental Studies Hybridoma Bank | nc82 | Mouse monoclonal |
| Anti-discs large primary antibody | Developmental Studies Hybridoma Bank | 4F3 | Mouse monoclonal |
| Anti-hrp primary antibody | Jackson Immuno Research | 123-605-021 | Alexa Fluor 647 conjugated polyclonal |
| Anti-polyubiquitin (FK2) primary antibody | Millipore Sigma | 04-263 | Mouse monoclonal |
| Confocal Microscope | Olympus | FV1000 | Objectives (NA): 10x (0.4), 20x (0.85), 40x (1.20), 60x (1.42), 100x (1.40) |
| Coverslips | Corning | 285022 | 160-190 mm thickness |
| Dissecting forceps | Fine Science Tools | 11252-00 | Dumont #5SF |
| Dissecting Microscope | Olympus | SZ61 | |
| Formaldehyde | Fisher Scientific | BP531-500 | 37% stock stabilized with methanol |
| Goat anti-mouse secondary antibody | Jackson Immuno Research | 115-545-146 | Alexa Fluor 488 conjugated |
| Goat Serum | Novus Biologicals | NB036768 | 0.2 mm filtered |
| Laboratory sealing tape | Fisher Scientific | 03-448-254 | Parafilm M |
| Methanol | Fisher Scientific | A413 | |
| Microscope Slides | Fisher Scientific | 12-550-123 | 76mm x 25mm |
| Mounting media | Molecular Probes | S36972 | Slowfade Diamond mounting media |
| Nonionic surfactant | Acros Organics | 215680010 | Triton-X 100 |
| Nutator | Fisher Scientific | S06622 | |
| Phalloidin | Invitrogen | A34055 | Alexa Fluor 555- conjugated |
| Sharpening stone | Fine Science Tools | 29008-01 | |
| Silicone elastomer | Electron Microscopy Sciences | 2423610 | Sylgard 184 |
References
- McDermott, C. J., Shaw, P. J. Diagnosis and management of motor neurone disease. BMJ. 336 (7645), 658-662 (2008).
- Global Collaborators, G. B. D. M. N. D. Global, regional, and national burden of motor neuron diseases 1990-2016: a systematic analysis for the Global Burden of Disease Study 2016. Lancet Neurology. 17 (12), 1083-1097 (2018).
- Foster, L. A., Salajegheh, M. K. Motor Neuron Disease: Pathophysiology, Diagnosis, and Management. American Journal of Medicine. 132 (1), 32-37 (2019).
- Bede, P., Pradat, P. F. Editorial: Biomarkers and Clinical Indicators in Motor Neuron Disease. Frontiers in Neurology. 10, 1318 (2019).
- Clark, J. A., Southam, K. A., Blizzard, C. A., King, A. E., Dickson, T. C. Axonal degeneration, distal collateral branching and neuromuscular junction architecture alterations occur prior to symptom onset in the SOD1(G93A) mouse model of amyotrophic lateral sclerosis. Journal of Chemical Neuroanatomy. 76, 35-47 (2016).
- Martineau, E., Di Polo, A., Van de Velde, C., Robitaille, R. Dynamic neuromuscular remodeling precedes motor-unit loss in a mouse model of ALS. Elife. 7, (2018).
- Shahidullah, M., et al. Defects in synapse structure and function precede motor neuron degeneration in Drosophila models of FUS-related ALS. Journal of Neuroscience. 33 (50), 19590-19598 (2013).
- Tremblay, E., Martineau, E., Robitaille, R. Opposite Synaptic Alterations at the Neuromuscular Junction in an ALS Mouse Model: When Motor Units Matter. Journal of Neuroscience. 37 (37), 8901-8918 (2017).
- Harris, K. P., Littleton, J. T. Transmission, Development, and Plasticity of Synapses. 유전학. 201 (2), 345-375 (2015).
- Beramendi, A., Peron, S., Casanova, G., Reggiani, C., Cantera, R. Neuromuscular junction in abdominal muscles of Drosophila melanogaster during adulthood and aging. Journal of Comparative Neurology. 501 (4), 498-508 (2007).
- Banerjee, S., et al. Miniature neurotransmission is required to maintain Drosophila synaptic structures during ageing. Nature Communications. 12 (1), 4399 (2021).
- Liao, S., Broughton, S., Nassel, D. R. Behavioral Senescence and Aging-Related Changes in Motor Neurons and Brain Neuromodulator Levels Are Ameliorated by Lifespan-Extending Reproductive Dormancy in Drosophila. Frontiers in Cellular Neuroscience. 11, 111 (2017).
- Mahoney, R. E., Rawson, J. M., Eaton, B. A. An age-dependent change in the set point of synaptic homeostasis. Journal of Neuroscience. 34 (6), 2111-2119 (2014).
- Fernandes, J. J., Keshishian, H. Development of the adult neuromuscular system. International Review of Neurobiology. 43, 221-239 (1999).
- Truman, J. W. Metamorphosis of the central nervous system of Drosophila. Journal of Neurobiology. 21 (7), 1072-1084 (1990).
- Baek, M., Mann, R. S. Lineage and birth date specify motor neuron targeting and dendritic architecture in adult Drosophila. Journal of Neuroscience. 29 (21), 6904-6916 (2009).
- Enriquez, J., et al. Specification of individual adult motor neuron morphologies by combinatorial transcription factor codes. Neuron. 86 (4), 955-970 (2015).
- Soler, C., Daczewska, M., Da Ponte, J. P., Dastugue, B., Jagla, K. Coordinated development of muscles and tendons of the Drosophila leg. Development. 131 (24), 6041-6051 (2004).
- Guan, W., Venkatasubramanian, L., Baek, M., Mann, R. S., Enriquez, J. Visualize Drosophila Leg Motor Neuron Axons Through the Adult Cuticle. Journal of Visualized Experiments. (140), e58365 (2018).
- Agudelo, A., et al. Age-dependent degeneration of an identified adult leg motor neuron in a Drosophila SOD1 model of ALS. Biology Open. 9 (10), (2020).
- Fernius, J., Starkenberg, A., Thor, S. Bar-coding neurodegeneration: identifying subcellular effects of human neurodegenerative disease proteins using Drosophila leg neurons. Disease Models & Mechanisms. 10 (8), 1027-1038 (2017).
- Sreedharan, J., Neukomm, L. J., Brown, R. H., Freeman, M. R. Age-Dependent TDP-43-Mediated Motor Neuron Degeneration Requires GSK3, hat-trick, and xmas-2. Current Biology. 25 (16), 2130-2136 (2015).
- Patel, N. H. Imaging neuronal subsets and other cell types in whole-mount Drosophila embryos and larvae using antibody probes. Methods in Cell Biology. 44, 445-487 (1994).
- Guirado, R., Carceller, H., Castillo-Gomez, E., Castren, E., Nacher, J. Automated analysis of images for molecular quantification in immunohistochemistry. Heliyon. 4 (6), 00669 (2018).
- Castells-Nobau, A., et al. Two Algorithms for High-throughput and Multi-parametric Quantification of Drosophila Neuromuscular Junction Morphology. Journal of Visualized Experiments. (123), e55395 (2017).
- Brown, J. R., Phongthachit, C., Sulkowski, M. J. Immunofluorescence and image analysis pipeline for Drosophila motor neurons. Biology Methods and Protocols. 4 (1), (2019).

