Disseksjon og immunhiistokjemi av Drosophila voksenben for å oppdage endringer ved neuromuskulært kryss for en identifisert motor neuron
Summary
Vi beskriver en disseksjonsteknikk som bevarer arkitekturen til det nevromuskulære krysset og muliggjør en detaljert immunocytokjemisk studie av motoriske nevroner i det voksne Drosophila-beinet .
Abstract
Drosophila melanogaster representerer en genetisk gjennomførbar modell for å studere nevronstruktur og funksjon, og etterfølgende endringer i sykdomstilstander. Det godt karakteriserte larval neuromuskulære krysset brukes ofte til slike studier. Imidlertid gjør rask larvalutvikling etterfulgt av muskel histolyse og nervesystem ombygging under metamorfose denne modellen problematisk for studiet av langsomme aldersavhengige degenerative endringer som de som forekommer i amyotrofisk lateral sklerose. Alternativt lever voksne fluer i 90 dager, og voksenbenet kan brukes til å studere motoriske nevronforandringer i løpet av voksen levetid ved hjelp av in vivo fluorescerende avbildning gjennom kutiklet. Her beskriver vi en ben disseksjonsteknikk kombinert med immunocytokjemi, noe som gjør det mulig å studere molekylære endringer ved det nevromuskulære krysset av identifiserte voksne benmotoriske nevroner. Disse teknikkene kan kombineres med et utall antistoffer som merker både pre- og postsynaptiske strukturer. Sammen tillater disse prosedyrene en mer fullstendig karakterisering av langsomme aldersavhengige endringer i voksne fluer og kan brukes på tvers av flere motoriske nevronsykdomsmodeller.
Introduction
Motor neuron (MN) sykdommer omfatter en gruppe heterogene forhold som inkluderer progressiv degenerasjon som fører til muskelsvømt og lammelse som en primær klinisk fenotype1. Selv om denne prevalensen er sjelden med en global prevalens på 4,5 per 100 000, forventes denne prevalensen å øke med en aldrende befolkning2. Amyotrofisk lateral sklerose (ALS) er den vanligste MN-sykdommen (MND) og er vanligvis dødelig innen kort tid etter diagnosen uten eksisterende sykdomsmodifiserende behandlinger tilgjengelig3. MND-er deler til felles en langvarig presymptomatisk fase med tidlige molekylære biomarkørendringer og funksjonelle bildeendringer sett hos pasienter4. Tidlig presymptomatisk cellulær patologi observeres også i ikke-menneskelige sykdomsmodeller5,6,7,8. Studiet av tidlige endringer ved det nevromuskulære krysset er viktig for å forstå MN sykdom patogenese og kan bidra til å utvikle tidlig diagnostikk og potensielle terapeutiske stoffer.
Et vell av genetiske og molekylære verktøy finnes i Drosophila for å dissekere strukturen og funksjonen til det nevromuskulære krysset (NMJ, se9 for en gjennomgang av den godt karakteriserte larval NMJ). Disse verktøyene kombinert med kort levetid gjør Drosophila til en utmerket modell for å studere nevrodegenerative endringer ved NMJ. Spesielt MNs innervating voksne muskler er til stede gjennom ~ 90-dagers voksen levetid og er utsatt for normale aldringsprosesser10,11,12,13. De voksne MN-ene gir derfor en mulighet til å studere langsomme degenerative endringer i motsetning til larval NMJs som eksisterer i bare en kort ~ 1 ukes tidsperiode før metamorfose14,15.
Her beskriver vi en disseksjonsprosedyre som lar oss utføre immunocytokjemisk analyse av MN-er i voksenbenet. Hvert voksenben er innervated av ~ 50 MNs, som synapse på tilhørende ben muskuløs for å drive bevegelse. Benanatomi, mekanisk fysiologi og nevrobiologi er godt beskrevet16,17,18. Axon arbors av ben MNs har tidligere vært preget av avbildning gjennom kutikal i bakfylte eller genetisk merkede cellepopulasjoner ved hjelp av bipartite Gal4 / UAS-systemet og avbildningsmetoder har blitt publisert tidligere19. Disseksjonsmetodene som presenteres her bevarer axonforgreningsmorfologi og lar oss utnytte et mangfoldig spekter av antistoffer for å merke forskjellige molekylære komponenter i NMJ. Vårt tidligere arbeid har fokusert på projeksjoner av et definert MN i metathoracic (3rd) benet, som innervates tibia levator muskel (tilm) og viser konsistente arborization mønstre og bouton tall. I utgangspunktet studerte vi aldersavhengige endringer i Drosophila superoksid dismutase 1 (dsod1) mutanter og fant endringer i samsvar med demontering av NMJ20. Disse disseksjonsmetodene gir mulighet til bedre å karakterisere langsomme degenerative endringer ved NMJ for andre ALS-modeller, grunnleggende studier av aldring og andre MN-tilknyttede sykdommer.
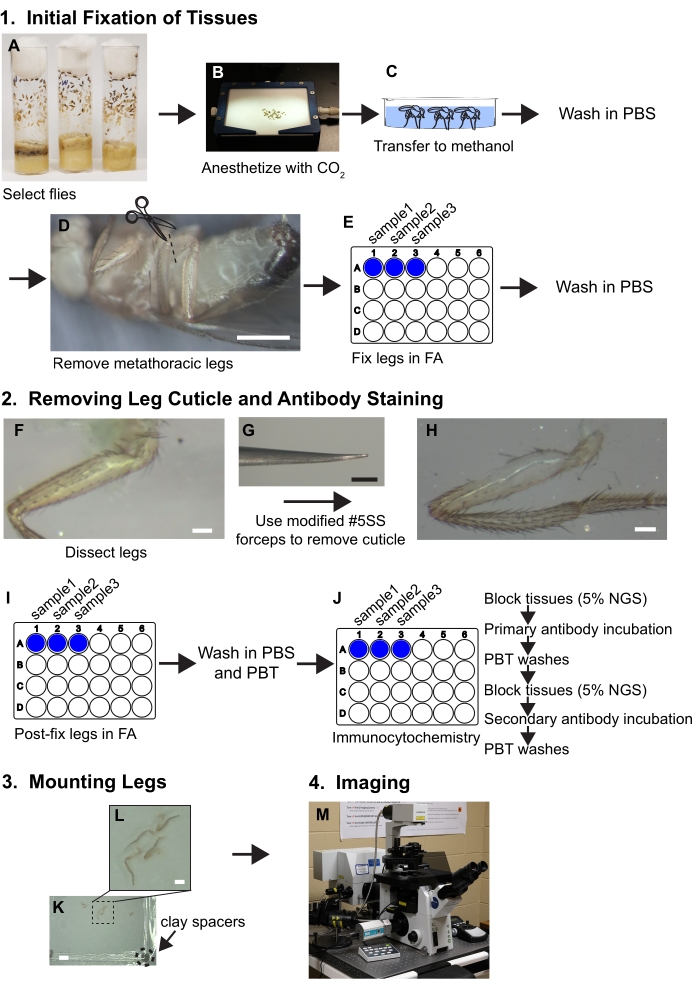
Figur 1. Arbeidsflytsammendrag for dissekering av ben. Se protokoll for detaljerte trinn. (A,B) Fluer velges og bedøves. (C) Fluer overføres til metanol og vaskes med PBS. (D) Metathoracic bena fjernes ved foten av coxa mens visualisert med et dissekering mikroskop (~ 30x forstørrelse); skala bar = 500 μm. (E) Bena festes deretter i 3,7% formaldehyd/PBS (FA)-løsning i 30 minutter i brønner på 24-brønnsplater og deretter fjernes FA ved vask med PBS. (F, G, H) Ben overføres til silikon elastomer dissekering skuffer og et stykke kutikal blir fjernet fra den proksimale lårbenet ved hjelp av skrå tang mens visualisert under et dissekering mikroskop ved 80x; skala bar = 50 μm. (I) Benene er post-disseksjon fikset i FA og vasket i PBS og deretter PBT (PBS + 0,1% ikke-ionisk overflateaktivt middel). (J) Ben utsettes for immunocytokjemisk farging. (K,L) Ben overføres til en glasssklie, ryddes i monteringsmedier og dekkes med en deksler som inneholder leire avstandsstykker; skalastenger = 2 mm og 500 μm. (M) Ben er avbildet ved konfektmikroskopi. Klikk her for å se en større versjon av denne figuren.
Protocol
Representative Results
Discussion
Drosophila voksenben er en ideell modell for å studere nevrodegenerasjon gitt relativ enkelhet med godt karakteriserte MNer kartlagt fra nevroblastomavledninger og stereotype arboriseringsmønstre. Flere rapporter har tidligere brukt ben-MN-er til studiet av nevrodegenerativ sykdom21,22. Disse studiene benyttet GFP-uttrykkende linjer kombinert med mosaikkanalyse med en trykkbar cellemarkør (MARCM) for å bilde gjennom kutiklet og dokumenterte en rekke morfologiske endringer. Avbildning av voksne NMJs ved immunocytokjemi med resected kutikol muliggjør ytterligere karakterisering med evnen til å spore komplekse molekylære endringer ved hjelp av en verktøykasse med antistoffer tilgjengelig.
Immunocytokjemidelen av denne protokollen er relativt standard og kan implementeres uavhengig av genotype (se23 for en utmerket beskrivelse av generelle antistofffargingsmetoder for bruk med Drosophila). Videre kan parametere som fluorescensintensitet, axongrenslengde og boutontall og -størrelse bestemmes ved hjelp av en rekke tilgjengelige ImageJ-makroer når bilder er tatt og detaljerte metoder for kvantitativ analyse er publisert (for eksempel se24,25,26). Dermed er disseksjonsteknikken den viktigste innovasjonen som er beskrevet her. Før disseksjonen nedsenkes fluer i en alkohol for å fjerne kuperte hydrokarboner. Både etanol og metanol brukes ofte til dette formålet; Vi har imidlertid bare brukt metanol. Kritisk for disseksjonssuksess er flere faktorer: For det første gir bruk av modifiserte tang med skråkant svært overfladisk kontakt med kutiklet. For det andre, ved hjelp av et dissekerende mikroskop som er i stand til 60-100x total forstørrelse slik at overflaten av kutiklet er tydelig synlig. For mikroskoper med lavere maksimal forstørrelse er 2x mål tilgjengelige for de fleste vanlige merker og bør være tilstrekkelig når de kombineres med eksisterende linser. For det tredje gjør det første fikseringstrinnet kutikal sprø og lettere å trekke seg bort uten å skade muskelen under. Overfiksering på dette trinnet gjør hele benet for stivt for effektiv avhandling. Derfor bør den første fikseringen begrenses til 30 minutter. Formaldehydfiksiven vil ikke trenge inn i nok til effektivt å krysskoble det underliggende vevet i løpet av denne korte perioden, og dermed er det nødvendig med et nytt fikseringstrinn. Før den andre fikseringen bør vev holdes på is for å forhindre nedbrytning og endringer i morfologi. For det fjerde har vi funnet dissekeringsprøver mens kulde også er viktig, sannsynligvis av lignende grunner ved at kutiklet er sprøtt og et lite stykke lettere kan fjernes.
Med praksis finner vi at ~ 50% av disseksjonene vil være brukbare uten merkbar vevsskade. Selv om denne prosentandelen kan virke lav i forhold til noen andre vev, er disseksjonsprosedyren rask, og mange ben kan behandles på 30-60 minutter. Derfor, selv om suksessratene er lave i utgangspunktet, er det mulig å få 4-5 gode prøver for hver eksperimentell gruppe. En begrensning kan imidlertid være antall fluer som er tilgjengelige til enhver tid hvis genotyper og/eller alder resulterer i betydelig dødelighet.
En annen begrensning er at vi ikke har vært i stand til å dissekere andre områder av beinet utover den proksimale regionen av lårbenet på grunn av størrelse. Dermed kan vi studere identifiserte MN arbors innervating TILM pålitelig, og det er mulig å dissekere kutikalle over tibia depressor muskel med små endringer i måten beinet er orientert når dissekering. Tilgang til andre regioner i beinet har imidlertid vist seg vanskeligere uten å forstyrre axonal arkitektur under disseksjon.
Her presenterer vi disseksjonsmetoder for å oppdage endringer ved den voksne NMJ for definerte MN-er som innerverer tilm ved hjelp av immunocytokjemi. Benet er nyttig som et enkelt system, innervated av bare ~ 50 MNs og inneholder 14 muskler med godt beskrevet anatomi. Dissekert benforberedelse kan brukes på tvers av genotyper, og en rekke antistoffer er tilgjengelige for NMJ-visualisering uten behov for å bygge genotypisk komplekse lagre av reportergenkonstruksjoner i mutantbakgrunn. Denne tilnærmingen vil muliggjøre en mer detaljert karakterisering av endringer ved NMJ for MN-sykdommer og andre aldersrelaterte tilstander.
Disclosures
The authors have nothing to disclose.
Acknowledgements
Vi takker Eric Roberts for råd om bildebehandling. Vi ønsker også å takke Information Technology Services på Rhode Island College og spesielt Michael Caine og Jake Douglas for videografi. Monoklonale antistoffer anti-dlg og anti-brp ble utviklet av henholdsvis UC-Berkeley og Universitaetsklinikim Wuerzburg, og ble hentet fra Developmental Studies Hybridoma Bank, opprettet av NICHD av NIH og vedlikeholdt ved University of Iowa, Department of Biology, Iowa City, IA 52242, USA. Forskningen som ble rapportert her ble støttet fullt ut av Rhode Island Institutional Development Award (IDeA) Network of Biomedical Research Excellence fra National Institute of General Medical Sciences of the National Institutes of Health under tilskuddsnummer [P20GM103430].
Materials
| 10x Phosphate Buffered Saline | Fisher Scientific | BP3991 | |
| 24 well plates | Corning | 3473 | Hydrophobic, ultra-low attachment surface |
| 2x objective accessory | Olympus | 110AL2X | Screw-on attachment |
| Anti-ATP5A primary antibody | Abcam | ab14748 | Mouse monoclonal |
| Anti-bruchpilot primary antibody | Developmental Studies Hybridoma Bank | nc82 | Mouse monoclonal |
| Anti-discs large primary antibody | Developmental Studies Hybridoma Bank | 4F3 | Mouse monoclonal |
| Anti-hrp primary antibody | Jackson Immuno Research | 123-605-021 | Alexa Fluor 647 conjugated polyclonal |
| Anti-polyubiquitin (FK2) primary antibody | Millipore Sigma | 04-263 | Mouse monoclonal |
| Confocal Microscope | Olympus | FV1000 | Objectives (NA): 10x (0.4), 20x (0.85), 40x (1.20), 60x (1.42), 100x (1.40) |
| Coverslips | Corning | 285022 | 160-190 mm thickness |
| Dissecting forceps | Fine Science Tools | 11252-00 | Dumont #5SF |
| Dissecting Microscope | Olympus | SZ61 | |
| Formaldehyde | Fisher Scientific | BP531-500 | 37% stock stabilized with methanol |
| Goat anti-mouse secondary antibody | Jackson Immuno Research | 115-545-146 | Alexa Fluor 488 conjugated |
| Goat Serum | Novus Biologicals | NB036768 | 0.2 mm filtered |
| Laboratory sealing tape | Fisher Scientific | 03-448-254 | Parafilm M |
| Methanol | Fisher Scientific | A413 | |
| Microscope Slides | Fisher Scientific | 12-550-123 | 76mm x 25mm |
| Mounting media | Molecular Probes | S36972 | Slowfade Diamond mounting media |
| Nonionic surfactant | Acros Organics | 215680010 | Triton-X 100 |
| Nutator | Fisher Scientific | S06622 | |
| Phalloidin | Invitrogen | A34055 | Alexa Fluor 555- conjugated |
| Sharpening stone | Fine Science Tools | 29008-01 | |
| Silicone elastomer | Electron Microscopy Sciences | 2423610 | Sylgard 184 |
References
- McDermott, C. J., Shaw, P. J. Diagnosis and management of motor neurone disease. BMJ. 336 (7645), 658-662 (2008).
- Global Collaborators, G. B. D. M. N. D. Global, regional, and national burden of motor neuron diseases 1990-2016: a systematic analysis for the Global Burden of Disease Study 2016. Lancet Neurology. 17 (12), 1083-1097 (2018).
- Foster, L. A., Salajegheh, M. K. Motor Neuron Disease: Pathophysiology, Diagnosis, and Management. American Journal of Medicine. 132 (1), 32-37 (2019).
- Bede, P., Pradat, P. F. Editorial: Biomarkers and Clinical Indicators in Motor Neuron Disease. Frontiers in Neurology. 10, 1318 (2019).
- Clark, J. A., Southam, K. A., Blizzard, C. A., King, A. E., Dickson, T. C. Axonal degeneration, distal collateral branching and neuromuscular junction architecture alterations occur prior to symptom onset in the SOD1(G93A) mouse model of amyotrophic lateral sclerosis. Journal of Chemical Neuroanatomy. 76, 35-47 (2016).
- Martineau, E., Di Polo, A., Van de Velde, C., Robitaille, R. Dynamic neuromuscular remodeling precedes motor-unit loss in a mouse model of ALS. Elife. 7, (2018).
- Shahidullah, M., et al. Defects in synapse structure and function precede motor neuron degeneration in Drosophila models of FUS-related ALS. Journal of Neuroscience. 33 (50), 19590-19598 (2013).
- Tremblay, E., Martineau, E., Robitaille, R. Opposite Synaptic Alterations at the Neuromuscular Junction in an ALS Mouse Model: When Motor Units Matter. Journal of Neuroscience. 37 (37), 8901-8918 (2017).
- Harris, K. P., Littleton, J. T. Transmission, Development, and Plasticity of Synapses. 유전학. 201 (2), 345-375 (2015).
- Beramendi, A., Peron, S., Casanova, G., Reggiani, C., Cantera, R. Neuromuscular junction in abdominal muscles of Drosophila melanogaster during adulthood and aging. Journal of Comparative Neurology. 501 (4), 498-508 (2007).
- Banerjee, S., et al. Miniature neurotransmission is required to maintain Drosophila synaptic structures during ageing. Nature Communications. 12 (1), 4399 (2021).
- Liao, S., Broughton, S., Nassel, D. R. Behavioral Senescence and Aging-Related Changes in Motor Neurons and Brain Neuromodulator Levels Are Ameliorated by Lifespan-Extending Reproductive Dormancy in Drosophila. Frontiers in Cellular Neuroscience. 11, 111 (2017).
- Mahoney, R. E., Rawson, J. M., Eaton, B. A. An age-dependent change in the set point of synaptic homeostasis. Journal of Neuroscience. 34 (6), 2111-2119 (2014).
- Fernandes, J. J., Keshishian, H. Development of the adult neuromuscular system. International Review of Neurobiology. 43, 221-239 (1999).
- Truman, J. W. Metamorphosis of the central nervous system of Drosophila. Journal of Neurobiology. 21 (7), 1072-1084 (1990).
- Baek, M., Mann, R. S. Lineage and birth date specify motor neuron targeting and dendritic architecture in adult Drosophila. Journal of Neuroscience. 29 (21), 6904-6916 (2009).
- Enriquez, J., et al. Specification of individual adult motor neuron morphologies by combinatorial transcription factor codes. Neuron. 86 (4), 955-970 (2015).
- Soler, C., Daczewska, M., Da Ponte, J. P., Dastugue, B., Jagla, K. Coordinated development of muscles and tendons of the Drosophila leg. Development. 131 (24), 6041-6051 (2004).
- Guan, W., Venkatasubramanian, L., Baek, M., Mann, R. S., Enriquez, J. Visualize Drosophila Leg Motor Neuron Axons Through the Adult Cuticle. Journal of Visualized Experiments. (140), e58365 (2018).
- Agudelo, A., et al. Age-dependent degeneration of an identified adult leg motor neuron in a Drosophila SOD1 model of ALS. Biology Open. 9 (10), (2020).
- Fernius, J., Starkenberg, A., Thor, S. Bar-coding neurodegeneration: identifying subcellular effects of human neurodegenerative disease proteins using Drosophila leg neurons. Disease Models & Mechanisms. 10 (8), 1027-1038 (2017).
- Sreedharan, J., Neukomm, L. J., Brown, R. H., Freeman, M. R. Age-Dependent TDP-43-Mediated Motor Neuron Degeneration Requires GSK3, hat-trick, and xmas-2. Current Biology. 25 (16), 2130-2136 (2015).
- Patel, N. H. Imaging neuronal subsets and other cell types in whole-mount Drosophila embryos and larvae using antibody probes. Methods in Cell Biology. 44, 445-487 (1994).
- Guirado, R., Carceller, H., Castillo-Gomez, E., Castren, E., Nacher, J. Automated analysis of images for molecular quantification in immunohistochemistry. Heliyon. 4 (6), 00669 (2018).
- Castells-Nobau, A., et al. Two Algorithms for High-throughput and Multi-parametric Quantification of Drosophila Neuromuscular Junction Morphology. Journal of Visualized Experiments. (123), e55395 (2017).
- Brown, J. R., Phongthachit, C., Sulkowski, M. J. Immunofluorescence and image analysis pipeline for Drosophila motor neurons. Biology Methods and Protocols. 4 (1), (2019).

