Dissekering och immunohistokemi av Drosophila Vuxen ben för att upptäcka förändringar vid neuromuskulära korsningen för en identifierad motor neuron
Summary
Vi beskriver en dissekering teknik som bevarar arkitekturen i neuromuskulära korsningen och möjliggör en detaljerad immunocytochemical studie av motor nervceller i vuxna Drosophila ben.
Abstract
Drosophila melanogaster representerar en genetiskt dragbar modell för att studera neuronal struktur och funktion, och efterföljande förändringar i sjukdomstillstånd. Den väl karakteriserade larven neuromuskulära korsningen används ofta för sådana studier. Snabb larvutveckling följt av muskel histolys och nervsystemet ombyggnad under metamorfos gör dock denna modell problematisk för studier av långsam åldersberoende degenerativa förändringar som de som förekommer i amyotrofisk lateral skleros. Alternativt lever vuxna flugor i 90 dagar och det vuxna benet kan användas för att studera motoriska neuronförändringar under vuxenlivslängden med hjälp av in vivo fluorescerande avbildning genom nagelbandet. Här beskriver vi en ben dissekering teknik i kombination med immunocytochemistry, som möjliggör studier av molekylära förändringar vid neuromuskulära korsningen av identifierade vuxna ben motor nervceller. Dessa tekniker kan kombineras med en myriad av antikroppar som märker både pre- och postsynaptiska strukturer. Tillsammans tillåter dessa förfaranden en mer fullständig karakterisering av långsamma åldersberoende förändringar hos vuxna flugor och kan tillämpas över flera motoriska neuron sjukdomsmodeller.
Introduction
Motor neuron (MN) sjukdomar omfattar en grupp heterogena villkor som inkluderar progressiv degeneration leder till muskelförtrining och förlamning som en primär klinisk fenotyp1. Även om det är sällsynt med en global prevalens på 4,5 per 100 000, förväntas denna prevalens öka med en åldrande befolkning2. Amyotrofisk lateral skleros (ALS) är den vanligaste MN-sjukdomen (MND) och är vanligtvis dödlig inom en kort tid efter diagnos utan befintliga sjukdomsmodifierande behandlingar tillgängliga3. MNDs delar gemensamt en utdragen presymtomatisk fas med tidiga molekylära biomarkörförändringar och funktionella bildframställningsförändringar som ses hos patienter4. Tidig presymtomatisk cellulär patologi observeras också i icke-mänskliga sjukdom modeller5,6,7,8. Studien av tidiga förändringar vid den neuromuskulära korsningen är viktigt för att förstå MN sjukdom patogenes och kan bidra till att utveckla tidig diagnostik och potentiella terapier.
En mängd genetiska och molekylära verktyg finns i Drosophila för att dissekera strukturen och funktionen hos den neuromuskulära korsningen (NMJ, se9 för en översyn av den väl karakteriserade larven NMJ). Dessa verktyg i kombination med en kort livslängd gör Drosophila till en utmärkt modell för att studera neurodegenerativa förändringar vid NMJ. Specifikt är MNs innervating vuxna muskler närvarande under hela ~ 90-dagars vuxen livslängd och är föremål för normala åldrandeprocesser10,11,12,13. De vuxna MN ger därför en möjlighet att studera långsamma degenerativa förändringar i motsats till larv NMJs som bara finns under en kort ~ 1 veckas tidsperiod före metamorfos14,15.
Här beskriver vi en dissekering förfarande som gör det möjligt för oss att genomföra immunocytochemical analys av MNs i vuxna benet. Varje vuxen ben är innervated av ~ 50 MNs, som synapse på det associerade benet muskulös för att driva rörelse. Benet anatomi, mekanisk fysiologi och neurobiologi har beskrivits väl16,17,18. Axon arbors av ben-MNs har tidigare kännetecknats av avbildning genom nagelband i ryggfyllda eller genetiskt märkta cellpopulationer med hjälp av bipartite Gal4/UAS-systemet och avbildningsmetoder har publicerats tidigare19. De dissekeringsmetoder som presenteras här bevarar axon förgrening morfologi och tillåter oss att utnyttja en mängd olika antikroppar för att märka olika molekylära komponenter i NMJ. Vårt tidigare arbete har fokuserat på projektioner av en definierad MN i metathoracic (3: e) benet, som innervates tibia levator muskeln (tilm) och visar konsekventa arborization mönster och bouton nummer. Inledningsvis studerade vi åldersberoende förändringar i Drosophila superoxid dismutase 1 (dsod1) mutanter och fann förändringar som överensstämmer med demontering av NMJ20. Dessa dissekeringsmetoder ger möjlighet att bättre karakterisera långsamma degenerativa förändringar vid NMJ för andra ALS-modeller, grundläggande studier av åldrande och andra MN-associerade sjukdomar.
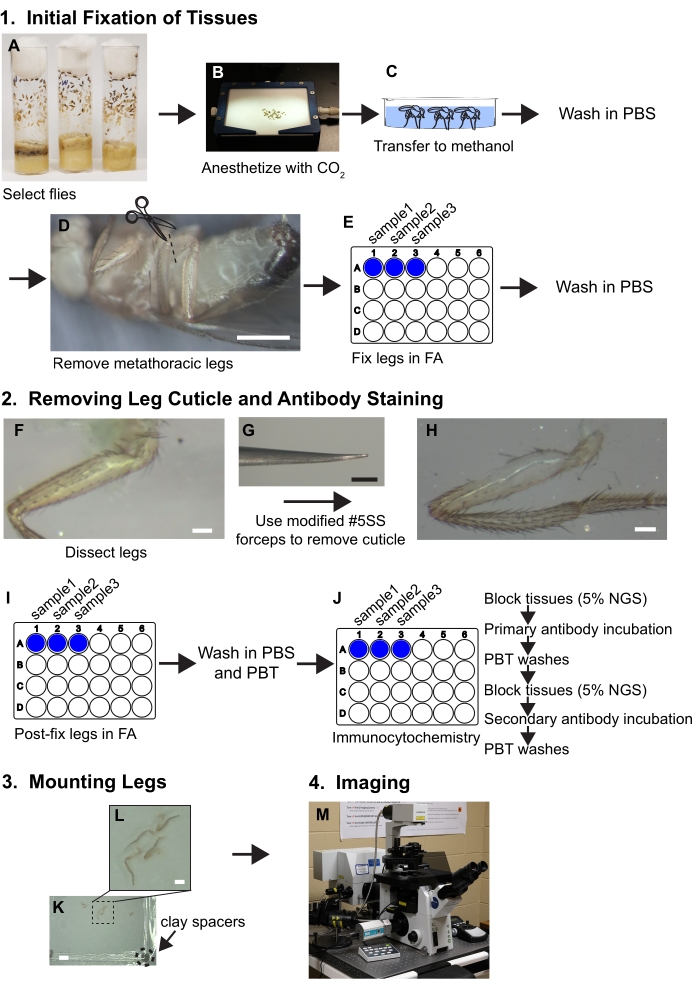
Figur 1. Arbetsflödessammanfattning för dissekering av ben. Se protokollet för detaljerade steg. (A,B) Flugor väljs och sövs. C) Flugor överförs till metanol och tvättas med PBS. (D) Metathoracicbenen avlägsnas vid basen av coxa medan de visualiseras med ett dissekerande mikroskop (~ 30x förstoring); skalstång = 500 μm. (E) Benen fixeras sedan i 3,7% formaldehyd/PBS (FA) lösning i 30 minuter i brunnar av 24-brunnsplattor och sedan tas FA bort genom tvättar med PBS. (F, G, H) Benen överförs till silikonelastomer dissekeringsbrickor och en bit nagelband avlägsnas från det proximala lårbenet med fasad tång medan de visualiseras under ett dissekerande mikroskop vid 80x; skalstång = 50 μm. (I) Benen är post-dissekering fixerade i FA och tvättas i PBS och sedan PBT (PBS + 0,1% icke-jonisk tensid). (J) Benen utsätts för immunocytokemisk färgning. (K,L) Benen överförs till en glasrutschbana, rensas i monteringsmedia och täcks med ett täckslip som innehåller lerutrymmen; skalstänger = 2 mm och 500 μm. (M) Benen avbildas av konfokal mikroskopi. Klicka här för att se en större version av den här figuren.
Protocol
Representative Results
Discussion
Drosophila vuxna ben är en idealisk modell för att studera neurodegeneration givet relativ enkelhet med väl karakteriserade MNs mappade från neuroblast härstamningar och stereotypa arborization mönster. Flera rapporter har tidigare använt ben-MNs för studier av neurodegenerativa sjukdomar21,22. Dessa studier använde GFP-uttryckande linjer i kombination med mosaik analys med en repressible cellmarkör (MARCM) att avbilda genom nagelband och dokumenterade en serie morfologiska förändringar. Imaging vuxna NMJs av immunocytochemistry med resected nagelband möjliggör ytterligare karakterisering med förmågan att spåra komplexa molekylära förändringar med hjälp av en verktygslåda av antikroppar tillgängliga.
Immunocytokemi delen av detta protokoll är relativt standard och kan genomföras oberoende av genotyp (se23 för en utmärkt beskrivning av allmänna antikropp färgningsmetoder för användning med Drosophila). Dessutom kan parametrar som fluorescensintensitet, axongrenlängd och boutonnummer och -storlek bestämmas med hjälp av en mängd tillgängliga ImageJ-makron när bilder har tagits och detaljerade metoder för kvantitativ analys har publicerats (till exempel se24,25,26). Dissekeringstekniken är således den viktigaste innovationen som beskrivs här. Före dissekering är flugor nedsänkta i en alkohol för att strippa cuticular kolväten. Både etanol och metanol används ofta för detta ändamål; emellertid, vi har bara använt metanol. Avgörande för dissekeringsframgång är flera faktorer: För det första möjliggör användning av modifierade tångar med avfasning mycket ytlig kontakt med nagelbandet. För det andra, med hjälp av ett dissekerande mikroskop som kan 60-100x total förstoring så att nagelbandets yta är tydligt synlig. För mikroskop med lägre maximal förstoring finns 2x-mål tillgängliga för de vanligaste märkena och bör vara tillräckliga i kombination med befintliga linser. För det tredje gör det första fixeringssteget nagelbandet sprött och lättare att dra bort utan att skada muskeln under. Överfixering i detta steg gör hela benet för styvt för effektiv dissekering. Därför bör den ursprungliga fixeringen begränsas till 30 minuter. Formaldehydfixativet kommer inte att tränga tillräckligt för att effektivt korsa den underliggande vävnaden under denna korta period och därför är ett andra fixeringssteg nödvändigt. Före den andra fixeringen bör vävnader hållas på is för att förhindra nedbrytning och förändringar i morfologin. För det fjärde har vi funnit dissekerande prover medan kyla också är viktigt, sannolikt av liknande skäl i att nagelband är sprött och en liten bit lättare kan avlägsnas.
Med övning finner vi ~ 50% av dissekeringarna kommer att kunna användas inom ingen märkbar vävnadsskada. Även om denna procentandel kan tyckas låg i förhållande till vissa andra vävnader, är dissekeringsproceduren snabb och många ben kan bearbetas på 30-60 minuter. Därför, även om framgångsgraden är låg inledningsvis, är det möjligt att få 4-5 bra prover för varje experimentell grupp. En begränsning kan dock vara antalet tillgängliga flugor vid en given tidpunkt om genotyper och/eller ålder leder till betydande dödlighet.
En annan begränsning är att vi inte har kunnat dissekera andra delar av benet bortom lårbenets proximala region på grund av storlek. Således kan vi studera identifierade MN arbors innervating TILM på ett tillförlitligt sätt och det är möjligt att dissekera nagelband ovanför skenbenet depressor muskeln med små förändringar i hur benet är orienterad vid dissekering. Att komma åt andra regioner i benet har dock visat sig svårare utan att störa axonal arkitektur under dissekering.
Här presenterar vi dissekeringsmetoder för att upptäcka förändringar vid vuxna NMJ för definierade MNs innervating tilm med immunocytochemistry. Benet är användbart som ett enkelt system, innervated av endast ~ 50 MN och innehåller 14 muskler med väl beskriven anatomi. Den dissekerade benberedningen kan användas över genotyper och en serie antikroppar finns tillgängliga för NMJ-visualisering utan behov av att bygga genotypiskt komplexa lager av reportergenkonstruktioner i mutanta bakgrunder. Detta tillvägagångssätt kommer att möjliggöra en mer detaljerad karakterisering av förändringar vid NMJ för MN-sjukdomar och andra åldersrelaterade tillstånd.
Disclosures
The authors have nothing to disclose.
Acknowledgements
Vi tackar Eric Roberts för råd om bildbehandling. Vi vill också tacka informationstekniktjänster vid Rhode Island College och i synnerhet Michael Caine och Jake Douglas för videografi. Monoklonala antikroppar anti-dlg och anti-brp utvecklades av UC-Berkeley respektive Universitaetsklinikim Wuerzburg, och erhölls från Developmental Studies Hybridoma Bank, skapad av NICHD av NIH och underhålls vid University of Iowa, Department of Biology, Iowa City, IA 52242, USA. Forskningen som rapporterades här stöddes fullt ut av Rhode Island Institutional Development Award (IDeA) Network of Biomedical Research Excellence från National Institute of General Medical Sciences vid National Institutes of Health under bidragsnummer [P20GM103430].
Materials
| 10x Phosphate Buffered Saline | Fisher Scientific | BP3991 | |
| 24 well plates | Corning | 3473 | Hydrophobic, ultra-low attachment surface |
| 2x objective accessory | Olympus | 110AL2X | Screw-on attachment |
| Anti-ATP5A primary antibody | Abcam | ab14748 | Mouse monoclonal |
| Anti-bruchpilot primary antibody | Developmental Studies Hybridoma Bank | nc82 | Mouse monoclonal |
| Anti-discs large primary antibody | Developmental Studies Hybridoma Bank | 4F3 | Mouse monoclonal |
| Anti-hrp primary antibody | Jackson Immuno Research | 123-605-021 | Alexa Fluor 647 conjugated polyclonal |
| Anti-polyubiquitin (FK2) primary antibody | Millipore Sigma | 04-263 | Mouse monoclonal |
| Confocal Microscope | Olympus | FV1000 | Objectives (NA): 10x (0.4), 20x (0.85), 40x (1.20), 60x (1.42), 100x (1.40) |
| Coverslips | Corning | 285022 | 160-190 mm thickness |
| Dissecting forceps | Fine Science Tools | 11252-00 | Dumont #5SF |
| Dissecting Microscope | Olympus | SZ61 | |
| Formaldehyde | Fisher Scientific | BP531-500 | 37% stock stabilized with methanol |
| Goat anti-mouse secondary antibody | Jackson Immuno Research | 115-545-146 | Alexa Fluor 488 conjugated |
| Goat Serum | Novus Biologicals | NB036768 | 0.2 mm filtered |
| Laboratory sealing tape | Fisher Scientific | 03-448-254 | Parafilm M |
| Methanol | Fisher Scientific | A413 | |
| Microscope Slides | Fisher Scientific | 12-550-123 | 76mm x 25mm |
| Mounting media | Molecular Probes | S36972 | Slowfade Diamond mounting media |
| Nonionic surfactant | Acros Organics | 215680010 | Triton-X 100 |
| Nutator | Fisher Scientific | S06622 | |
| Phalloidin | Invitrogen | A34055 | Alexa Fluor 555- conjugated |
| Sharpening stone | Fine Science Tools | 29008-01 | |
| Silicone elastomer | Electron Microscopy Sciences | 2423610 | Sylgard 184 |
References
- McDermott, C. J., Shaw, P. J. Diagnosis and management of motor neurone disease. BMJ. 336 (7645), 658-662 (2008).
- Global Collaborators, G. B. D. M. N. D. Global, regional, and national burden of motor neuron diseases 1990-2016: a systematic analysis for the Global Burden of Disease Study 2016. Lancet Neurology. 17 (12), 1083-1097 (2018).
- Foster, L. A., Salajegheh, M. K. Motor Neuron Disease: Pathophysiology, Diagnosis, and Management. American Journal of Medicine. 132 (1), 32-37 (2019).
- Bede, P., Pradat, P. F. Editorial: Biomarkers and Clinical Indicators in Motor Neuron Disease. Frontiers in Neurology. 10, 1318 (2019).
- Clark, J. A., Southam, K. A., Blizzard, C. A., King, A. E., Dickson, T. C. Axonal degeneration, distal collateral branching and neuromuscular junction architecture alterations occur prior to symptom onset in the SOD1(G93A) mouse model of amyotrophic lateral sclerosis. Journal of Chemical Neuroanatomy. 76, 35-47 (2016).
- Martineau, E., Di Polo, A., Van de Velde, C., Robitaille, R. Dynamic neuromuscular remodeling precedes motor-unit loss in a mouse model of ALS. Elife. 7, (2018).
- Shahidullah, M., et al. Defects in synapse structure and function precede motor neuron degeneration in Drosophila models of FUS-related ALS. Journal of Neuroscience. 33 (50), 19590-19598 (2013).
- Tremblay, E., Martineau, E., Robitaille, R. Opposite Synaptic Alterations at the Neuromuscular Junction in an ALS Mouse Model: When Motor Units Matter. Journal of Neuroscience. 37 (37), 8901-8918 (2017).
- Harris, K. P., Littleton, J. T. Transmission, Development, and Plasticity of Synapses. 유전학. 201 (2), 345-375 (2015).
- Beramendi, A., Peron, S., Casanova, G., Reggiani, C., Cantera, R. Neuromuscular junction in abdominal muscles of Drosophila melanogaster during adulthood and aging. Journal of Comparative Neurology. 501 (4), 498-508 (2007).
- Banerjee, S., et al. Miniature neurotransmission is required to maintain Drosophila synaptic structures during ageing. Nature Communications. 12 (1), 4399 (2021).
- Liao, S., Broughton, S., Nassel, D. R. Behavioral Senescence and Aging-Related Changes in Motor Neurons and Brain Neuromodulator Levels Are Ameliorated by Lifespan-Extending Reproductive Dormancy in Drosophila. Frontiers in Cellular Neuroscience. 11, 111 (2017).
- Mahoney, R. E., Rawson, J. M., Eaton, B. A. An age-dependent change in the set point of synaptic homeostasis. Journal of Neuroscience. 34 (6), 2111-2119 (2014).
- Fernandes, J. J., Keshishian, H. Development of the adult neuromuscular system. International Review of Neurobiology. 43, 221-239 (1999).
- Truman, J. W. Metamorphosis of the central nervous system of Drosophila. Journal of Neurobiology. 21 (7), 1072-1084 (1990).
- Baek, M., Mann, R. S. Lineage and birth date specify motor neuron targeting and dendritic architecture in adult Drosophila. Journal of Neuroscience. 29 (21), 6904-6916 (2009).
- Enriquez, J., et al. Specification of individual adult motor neuron morphologies by combinatorial transcription factor codes. Neuron. 86 (4), 955-970 (2015).
- Soler, C., Daczewska, M., Da Ponte, J. P., Dastugue, B., Jagla, K. Coordinated development of muscles and tendons of the Drosophila leg. Development. 131 (24), 6041-6051 (2004).
- Guan, W., Venkatasubramanian, L., Baek, M., Mann, R. S., Enriquez, J. Visualize Drosophila Leg Motor Neuron Axons Through the Adult Cuticle. Journal of Visualized Experiments. (140), e58365 (2018).
- Agudelo, A., et al. Age-dependent degeneration of an identified adult leg motor neuron in a Drosophila SOD1 model of ALS. Biology Open. 9 (10), (2020).
- Fernius, J., Starkenberg, A., Thor, S. Bar-coding neurodegeneration: identifying subcellular effects of human neurodegenerative disease proteins using Drosophila leg neurons. Disease Models & Mechanisms. 10 (8), 1027-1038 (2017).
- Sreedharan, J., Neukomm, L. J., Brown, R. H., Freeman, M. R. Age-Dependent TDP-43-Mediated Motor Neuron Degeneration Requires GSK3, hat-trick, and xmas-2. Current Biology. 25 (16), 2130-2136 (2015).
- Patel, N. H. Imaging neuronal subsets and other cell types in whole-mount Drosophila embryos and larvae using antibody probes. Methods in Cell Biology. 44, 445-487 (1994).
- Guirado, R., Carceller, H., Castillo-Gomez, E., Castren, E., Nacher, J. Automated analysis of images for molecular quantification in immunohistochemistry. Heliyon. 4 (6), 00669 (2018).
- Castells-Nobau, A., et al. Two Algorithms for High-throughput and Multi-parametric Quantification of Drosophila Neuromuscular Junction Morphology. Journal of Visualized Experiments. (123), e55395 (2017).
- Brown, J. R., Phongthachit, C., Sulkowski, M. J. Immunofluorescence and image analysis pipeline for Drosophila motor neurons. Biology Methods and Protocols. 4 (1), (2019).

