Microtubule Plus-End Dynamics Visualization in Huntington's Disease Model gebaseerd op humane primaire huidfibroblasten
Summary
Dit protocol is gewijd aan de microtubule plus-end visualisatie door EB3-eiwittransfectie om hun dynamische eigenschappen in primaire celkweek te bestuderen. Het protocol werd geïmplementeerd op menselijke primaire huidfibroblasten verkregen van patiënten met de Ziekte van Huntington.
Abstract
Transfectie met een fluorescerend gelabeld markereiwit van belang in combinatie met time-lapse videomicroscopie is een klassieke methode om de dynamische eigenschappen van het cytoskelet te bestuderen. Dit protocol biedt een techniek voor menselijke primaire fibroblasttransfectie, die moeilijk kan zijn vanwege de specifieke kenmerken van primaire celkweekomstandigheden. Bovendien vereist het onderhoud van de dynamische eigenschap van cytoskeletten een laag niveau van transfectie om een goede signaal-ruisverhouding te verkrijgen zonder microtubulestabilisatie te veroorzaken. Het is belangrijk om maatregelen te nemen om de cellen te beschermen tegen door licht veroorzaakte stress en fluorescerende kleurstofvervaging. In de loop van ons werk hebben we verschillende transfectiemethoden en -protocollen getest, evenals verschillende vectoren om de beste combinatie van aandoeningen te selecteren die geschikt is voor menselijke primaire fibroblaststudies. We analyseerden de resulterende time-lapse-video’s en berekenden de microtubule-dynamiek met behulp van ImageJ. De dynamiek van de plus-uiteinden van microtubuli in de verschillende celdelen is niet vergelijkbaar, dus verdeelden we de analyse in subgroepen – het centrosoomgebied, de lamellen en de staart van fibroblasten. Dit protocol kan met name worden gebruikt voor in vitro analyse van cytoskeletdynamica in patiëntmonsters, waardoor de volgende stap kan worden gezet naar het begrijpen van de dynamiek van de verschillende ziekteontwikkelingen.
Introduction
De ziekte van Huntington (ZvH) is een ongeneeslijke neurodegeneratieve pathologie veroorzaakt door een mutatie-gen dat codeert voor het kjatingtine-eiwit (HTT). HTT wordt voornamelijk geassocieerd met blaasjes en microtubuli en is waarschijnlijk betrokken bij microtubuli-afhankelijke transportprocessen1,2. Om de invloed van mutant HTT op de microtubuledynamica te bestuderen, gebruikten we in vitro visualisatie van het EB3-eiwit, dat de dynamische eigenschappen van microtubuli reguleert door de groeiende plus-uiteinden te binden en te stabiliseren. Om fluorescerend gelabelde EB3 in menselijke huidfibroblasten te laden, werd plasmidetransfectie toegepast. We gebruikten de primaire fibroblastcultuur verkregen uit de huidbiopsie van de ZvH-patiënten voor deze studie.
De mutatie in het HTT-eiwitgen leidt tot verlenging van het polyglutaminekanaal3. HTT heeft een rol in cellulaire processen zoals endocytose4,celtransport1,2,eiwitafbraak5,enz. Een substantieel deel van deze processen omvat verschillende elementen van het celcytoskelet, waaronder de microtubuli.
Menselijke primaire cellen zijn het beste model om gebeurtenissen die zich in patiëntencellen voordoen zo goed mogelijk te reproduceren. Om dergelijke modellen te maken, moet men cellen isoleren van menselijk biopsiemateriaal (bijvoorbeeld uit chirurgische monsters). De resulterende primaire cellijn is geschikt om pathogenese te bestuderen met behulp van verschillende genetische, biochemische, moleculaire en celbiologische methoden. Ook dienen menselijke primaire celculturen als een voorloper voor het creëren van verschillende transgedifferentieerde en transgene culturen6.
In tegenstelling tot vereeuwigde celculturen is het belangrijke nadeel van primaire cellen echter hun beperkte doorgangscapaciteit. Daarom raden we aan om cellen te gebruiken in de vroege passagefase (tot 15). Oudere culturen degenereren zeer snel en verliezen hun unieke eigenschappen. Daarom moeten de nieuw verkregen primaire cellen bevroren worden gehouden voor langdurige opslag.
Primaire celculturen zijn gevoelig voor kweekomstandigheden. Daarom vereisen ze vaak unieke benaderingen en optimalisatie van groeiomstandigheden. Met name de primaire fibroblasten van de menselijke huid die in onze experimenten worden gebruikt, zijn veeleisend voor het substraat. Daarom gebruikten we verschillende extra coatings (bijv. Gelatine of fibronectine), afhankelijk van het type experiment.
Het celcytoskelet bepaalt de celvorm, mobiliteit en voortbeweging. De dynamiek van het cytoskelet is cruciaal voor veel intracellulaire processen, zowel in de interfase als in mitose. In het bijzonder het cytoskelet gepolymeriseerd uit tubuline, zijn zeer dynamische en polaire structuren, waardoor motoreiwit-gemedieerd gericht intracellulair transport mogelijk is. De uiteinden van de microtubuli zijn in constante herschikking, hun assemblagefasen worden afgewisseld met de demontagefasen en dit gedrag wordt “dynamische instabiliteit” genoemd7,8,9. Verschillende geassocieerde eiwitten verschuiven het evenwicht van de polymerisatiereactie, wat leidt tot de polymeervorming of de eiwitmonomeervorming. De toevoeging van tubuline-subeenheden vindt voornamelijk plaats aan het plus-uiteinde van microtubuli10. De eindbindende (EB) eiwitfamilie bestaat uit drie leden: EB1, EB2 en EB3. Ze dienen als plus-end-tracking eiwitten (+ TIPs) en reguleren de dynamische eigenschappen van microtubuli door hun groeiende plus-ends te binden en te stabiliseren11.
Veel studies gebruiken fluorescerende molecuul-gelabelde tubuline micro-injectie of transfectie met time-lapse beeldvorming en video-analyse om microtubuli in vitrote visualiseren. Deze methoden kunnen invasief zijn en schadelijk voor cellen, vooral primaire menselijke cellen. De meest uitdagende stap is het vinden van voorwaarden voor celtransfectie. We probeerden het hoogst mogelijke niveau van transfectie te bereiken zonder de levensvatbaarheid en de morfologie van inheemse cellen te beïnvloeden. Deze studie past de klassieke methode toe om de verschillen in microtubulidynamiek in huidfibroblasten van gezonde donoren en patiënten met de Ziekte van Huntington te bestuderen.
Protocol
Representative Results
Discussion
Betere kwaliteitsresultaten voor de dynamische analyse van microtubuli kunnen worden verkregen uit microscopische beelden van hoge kwaliteit. Het is belangrijk om alle noodzakelijke voorwaarden voor time-lapse beeldvorming van levende cellen in acht te nemen en de beeldvormingsparameters correct aan te passen. Het gebruik van speciale celkweekschalen met een glazen bodem (confocale schotels) is belangrijk, omdat glas een andere brekingsindex van licht heeft dan plastic. De dikte van het glas en de uniformiteit ervan over…
Disclosures
The authors have nothing to disclose.
Acknowledgements
Dit onderzoek werd gefinancierd door het ministerie van Wetenschap en Hoger Onderwijs van de Russische Federatie, subsidie nr. 075-15-2019-1669 (transfectie van fibroblasten), door de Russian Science Foundation, subsidie nr. 19-15-00425 (alle andere werken aan de teelt van fibroblasten in vitro). Het werd gedeeltelijk ondersteund door Lomonosov Moscow State University Development program PNR5.13 (beeldvorming en analyse). De auteurs erkennen de steun van het Nikon Center of Excellence aan het A. N. Belozersky Institute of Physico-Chemical Biology. We willen onze speciale dank uitspreken aan Ekaterina Taran voor haar hulp bij stemacteren. De auteurs bedanken ook Pavel Belikov voor zijn hulp bij de videobewerking. Figuren in het manuscript zijn gemaakt met BioRender.com.
Materials
| Instrumentation | |||
| Camera iXon DU897 EMCCD | Andor Technology | ||
| Eppendorf Centrifuge 5804 R | Eppendorf Corporate | ||
| Fluorescence filter set HYQ FITC | Nikon | Alternative: Leica, Olympus, Zeiss | |
| LUNA-II Automated Cell Counte | Logos Biosystems | L40002 | |
| Microscope incubator for lifetime filming | Okolab | Temperature controller H301-T-UNIT-BL-PLUS | |
| Gas controller CO2-O2-UNIT-BL | |||
| Objective lens CFI Plan Apo Lambda 60x Oil 1.4 (WD 0.13) | Nikon | Alternative: Leica, Olympus, Zeiss | |
| Widefield fluorescence light microscope Eclipse Ti-E | Nikon | Alternative: Leica, Olympus, Zeiss | |
| Software | |||
| Fiji (Image J version 2.1.0/1.53c) | Open source image processing software | ||
| NIS Elements | Nikon | Alternative: Leica, Olympus, Zeiss | |
| Additional reagents | |||
| Mineral oil (Light white oil) | MP | 151694 | |
| Cell culture dish | |||
| Cell Culture Dish | SPL Lifesciences | 20035 | |
| Confocal Dish (glass thickness 170 µm) | SPL Lifesciences | 211350 | Alternative: MatTek |
| Conical Centrifuge tube | SPL Lifesciences | 50015 | |
| Cryogenic Vials | Corning-Costar | 430659 | |
| Microcentrifuge Tube | Nest | 615001 | |
| Cultivation | |||
| Lipofectamine 3000 Transfection Reagent | Thermo Fisher Scientific | L3000001 | |
| Dimethyl sulfoxide | PanEko | 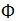 135 135 |
|
| DMEM (Dulbecco's Modified Eagle Media) | PanEko | C420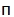 |
|
| DPBS (Dulbecco's phosphate-salt solution) | PanEko | P060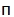 |
|
| Fetal bovine serum (FBS) | Hyclone | K053/SH30071.03 | |
| Gelatin (bovine skin) | PanEko | 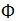 070 070 |
|
| GlutaMAX | Thermo Fisher Scientific | 35050038 | |
| Opti-MEM (1x) + Glutamax | Gibco | 519850026 | |
| Penicillin-streptomycin | PanEko | A063 |
|
| Trypsin-EDTA (0.25%) | Thermo Fisher Scientific | 25200072 | |
| Transfection | |||
| Plasmid DNA with EB3-GFP | Kind gift of Dr. I. Kaverina [Vanderbilt University, Nashville] with permission from Dr. A. Akhmanova [Erasmus University, Rotterdam] |
Stepanova et al., 2003 DOI: 10.1523/JNEUROSCI.23-07-02655.2003 |
References
- Engelender, S., et al. Huntingtin-associated Protein 1 (HAP1) Interacts with the p150 Glued Bubunit of Dynactin. Human Molecular Genetics. 6 (13), 2205-2212 (1997).
- Caviston, J. P., Ross, J. L., Antony, S. M., Tokito, M., Holzbaur, E. L. Huntingtin facilitates dynein/dynactin-mediated vesicle transport. Proceedings of the National Academy of Sciences. 104 (24), 10045-10050 (2007).
- MacMillan, J. C., et al. Molecular analysis and clinical correlations of the Huntington’s disease mutation. The Lancet. 342 (8877), 954-958 (1993).
- Proskura, A. L., Vechkapova, S. O., Zapara, T. A., Ratushniak, A. S. Protein-protein interactions of huntingtin in the hippocampus. Molecular Biology. 51 (4), 647-653 (2017).
- Steffan, J. S., et al. The Huntington’s disease protein interacts with p53 and CREB-binding protein and represses transcription. Proceedings of the National Academy of Sciences. 97 (12), 6763-6768 (2000).
- Nekrasov, E. D., et al. Manifestation of Huntington’s disease pathology in human induced pluripotent stem cell-derived neurons. Molecular Neurodegeneration. 11 (1), 1-15 (2016).
- Mitchison, T., Kirschner, M. Dynamic instability of microtubule growth. Nature. 312 (5991), 237-242 (1984).
- Walker, R. A., et al. Dynamic instability of individual microtubules analyzed by video light microscopy: rate constants and transition frequencies. The Journal of Cell Biology. 107 (4), 1437-1448 (1988).
- Desai, A., Mitchison, T. J. Microtubule polymerization dynamics. Annual Review of Cell and Developmental Biology. 13 (1), 83-117 (1997).
- Allen, C., Borisy, G. G. Structural polarity and directional growth of microtubules of Chlamydomonas flagella. Journal of Molecular Biology. 90 (2), 381-402 (1974).
- Stepanova, T., et al. Visualization of microtubule growth in cultured neurons via the use of EB3-GFP (end-binding protein 3-green fluorescent protein). Journal of Neuroscience. 23 (7), 2655-2664 (2003).
- Shelden, E., Wadsworth, P. Observation and quantification of individual microtubule behavior in vivo: microtubule dynamics are cell-type specific. Journal of Cell Biology. 120 (4), 935-945 (1993).
- O’Brien, E. T., Salmon, E. D., Walker, R. A., Erickson, H. P. Effects of magnesium on the dynamic instability of individual microtubules. 생화학. 29 (28), 6648-6656 (1990).
- Drechsel, D. N., Hyman, A. A., Cobb, M. H., Kirschner, M. W. Modulation of the dynamic instability of tubulin assembly by the microtubule-associated protein tau. Molecular Biology of the Cell. 3 (10), 1141-1154 (1992).
- Gildersleeve, R. F., Cross, A. R., Cullen, K. E., Fagen, A. P., Williams, R. C. Microtubules grow and shorten at intrinsically variable rates. Journal of Biological Chemistry. 267 (12), 7995-8006 (1992).
- Penazzi, L., Bakota, L., Brandt, R. Microtubule dynamics in neuronal development, plasticity, and neurodegeneration. International Review of Cell and Molecular Biology. 321, 89-169 (2016).
- van de Willige, D., Hoogenraad, C. C., Akhmanova, A. Microtubule plus-end tracking proteins in neuronal development. Cellular and Molecular Life Sciences. 73 (10), 2053-2077 (2016).
- Applegate, K. T., et al. plusTipTracker: Quantitative image analysis software for the measurement of microtubule dynamics. Journal of Structural Biology. 176 (2), 168-184 (2011).
- Komarova, Y. A., Vorobjev, I. A., Borisy, G. G. Life cycle of MTs: persistent growth in the cell interior, asymmetric transition frequencies and effects of the cell boundary. Journal of Cell Science. 115 (17), 3527-3539 (2002).
- Nahidiazar, L., Agronskaia, A. V., Broertjes, J., vanden Broek, B., Jalink, K. Optimizing imaging conditions for demanding multi-color super resolution localization microscopy. PLoS One. 11 (7), 0158884 (2016).
- Dixit, R., Cyr, R. Cell damage and reactive oxygen species production induced by fluorescence microscopy: effect on mitosis and guidelines for non-invasive fluorescence microscopy. The Plant Journal. 36 (2), 280-290 (2003).
- Grzelak, A., Rychlik, B., Bartosz, G. Light-dependent generation of reactive oxygen species in cell culture media. Free Radical Biology and Medicine. 30 (12), 1418-1425 (2001).

