La fabricación y operación de un sistema de microelectroporación de flujo continuo con detección de permeabilización
Summary
Este protocolo describe las técnicas de microfabricación necesarias para construir un dispositivo de electroporación microfluídica de laboratorio en un chip. La configuración experimental realiza transfecciones controladas a nivel de una sola célula en un flujo continuo y se puede extender a rendimientos más altos con control basado en la población. Se proporciona un análisis que muestra la capacidad de monitorear eléctricamente el grado de permeabilización de la membrana celular en tiempo real.
Abstract
Las innovaciones terapéuticas actuales, como la terapia de células CAR-T, dependen en gran medida de la administración de genes mediada por virus. Aunque eficiente, esta técnica se acompaña de altos costos de fabricación, lo que ha provocado un interés en el uso de métodos alternativos para la administración de genes. La electroporación es un enfoque electrofísico, no viral para la entrega intracelular de genes y otros materiales exógenos. Tras la aplicación de un campo eléctrico, la membrana celular permite temporalmente la entrega molecular en la célula. Típicamente, la electroporación se realiza en la macroescala para procesar un gran número de células. Sin embargo, este enfoque requiere un extenso desarrollo de protocolos empíricos, lo cual es costoso cuando se trabaja con tipos de células primarias y difíciles de transfetar. El largo desarrollo del protocolo, junto con el requisito de grandes voltajes para lograr suficientes intensidades de campo eléctrico para permeabilizar las células, ha llevado al desarrollo de dispositivos de electroporación a microescala. Estos dispositivos de microelectroporación se fabrican utilizando técnicas comunes de microfabricación y permiten un mayor control experimental con el potencial de mantener altas capacidades de rendimiento. Este trabajo se basa en una tecnología de electroporación microfluídica capaz de detectar el nivel de permeabilización de la membrana celular a nivel de una sola célula bajo flujo continuo. Sin embargo, esta tecnología se limitó a 4 celdas procesadas por segundo, y por lo tanto se propone y presenta aquí un nuevo enfoque para aumentar el rendimiento del sistema. Esta nueva técnica, denominada control de retroalimentación basado en la población celular, considera la respuesta de permeabilización celular a una variedad de condiciones de pulso de electroporación y determina las condiciones de pulso de electroporación más adecuadas para el tipo de célula bajo prueba. Luego se utiliza un modo de mayor rendimiento, donde este pulso “óptimo” se aplica a la suspensión celular en tránsito. Los pasos para fabricar el dispositivo, configurar y ejecutar los experimentos microfluídicos y analizar los resultados se presentan en detalle. Finalmente, esta tecnología de microelectroporación se demuestra mediante la entrega de un plásmido de ADN que codifica para la proteína fluorescente verde (GFP) en las células HEK293.
Introduction
Las innovaciones terapéuticas actuales en la investigación biomédica, como la terapia celular CAR-T (Chimeric Antigen Receptor Engineered T cell) y la edición genética utilizando CRISPR (secuencias de ADN de repetición palindrómica cortas agrupadas regularmente interespaciadas) / Cas9, dependen en gran medida de la capacidad de entregar material exógeno tanto con éxito como de manera eficiente en el espacio intracelular1. En la terapia CAR-T, el estándar de oro para realizar el paso de entrega de genes en la fabricación de terapia celular es el uso de vectores virales2. Aunque la administración de genes mediada por virus es una modalidad de entrega eficiente, también tiene varios inconvenientes. Estos incluyen costos de fabricación, citotoxicidad, inmunogenicidad, potencial de mutagénesis / tumorigénesis y limitaciones de tamaño en el gen (s) que se administrará3. Estas limitaciones han llevado a la investigación y el desarrollo de tecnologías alternativas de administración no viral.
La electroporación, una alternativa a la entrega de genes mediada por virus, se basa en la aplicación de una forma de onda de pulso eléctrico óptima para realizar transfecciones de ADN, ARN y proteínas de las células. Después de la aplicación de un campo eléctrico externo, la membrana celular se ve brevemente comprometida, lo que hace que la célula sea susceptible a la entrega intracelular de materiales exógenos impermeables4. En comparación con la administración mediada por virus, la electroporación es ventajosa ya que generalmente es segura, fácil de operar y tiene bajos costos operativos. La electroporación puede entregar carga molecular pequeña y grande y puede ser eficiente en la transfección de células independientemente del linaje5. Para lograr resultados deseables después de la electroporación, es decir, buena viabilidad y buena eficiencia de electrotransfección, es necesario cooptimizar una variedad de parámetros experimentales. Estos incluyen el tipo de célula6, la densidad celular, la concentración de la molécula7, las propiedades del tampón de electroporación (por ejemplo, composición molecular, conductividad y osmolaridad)8, el tamaño/geometría del electrodo9 y la forma de onda del pulso eléctrico (forma, polaridad, número de pulsos)10 (consulte la Figura 1 para una ilustración). Aunque cada uno de estos parámetros puede tener un efecto significativo en los resultados de los experimentos de electroporación, la forma de onda de pulso ha sido especialmente estudiada con gran detalle, ya que la energía eléctrica del pulso aplicado es la raíz de la compensación intrínseca entre la viabilidad celular resultante y la eficiencia de electrotransfección8.
Típicamente, los experimentos de electroporación se realizan en la macroescala, donde las células están suspendidas en 100s de microlitros de tampón entre un conjunto de electrodos grandes de placa paralela dentro de una cubeta de electroporación. Los electrodos se fabrican comúnmente en aluminio con una distancia de electrodo de 1-4 mm. Una vez que las celdas se cargan manualmente a través de una pipeta, la cubeta se conecta eléctricamente a un voluminoso generador de impulsos eléctricos donde el usuario puede configurar y aplicar los parámetros de forma de onda de pulso para electroporar la suspensión celular. Aunque la electroporación a macroescala o a granel puede procesar densidades celulares >106 células/ml, esta característica puede ser un desperdicio al optimizar los ajustes de la forma de onda del pulso eléctrico. Esto es particularmente preocupante cuando se electroporan tipos de células primarias donde el número de poblaciones celulares puede ser limitado. Además, debido a la gran distancia entre los electrodos, el generador de impulsos debe ser capaz de suministrar grandes voltajes para lograr intensidades de campo eléctrico >1kV / cm11. Estos altos voltajes causan una disipación de potencia resistiva a través del tampón electrolítico, lo que resulta en el calentamiento de Joule, lo que puede ser perjudicial para la viabilidad celular resultante12. Por último, la realización de la electroporación en una suspensión densa de células estará constantemente cargada con una variabilidad innata en la eficiencia de electrotransfección resultante y la viabilidad celular. Cada celda en suspensión podría experimentar una intensidad de campo eléctrico diferente debido a las células circundantes. Dependiendo de si la intensidad del campo eléctrico experimentado aumenta o disminuye, la viabilidad celular resultante o la eficiencia de la electrotransfección pueden verse afectadas negativamente11. Estas desventajas de la electroporación a macroescala han llevado a la búsqueda y desarrollo de tecnologías alternativas que operan a microescala y permiten un mejor control a nivel de una sola célula.
El campo de BioMEMS, o sistemas biomédicos microelectromecánicos, se deriva de los avances tecnológicos realizados en la industria de la microelectrónica. Específicamente, utilizando procesos de microfabricación para desarrollar microdispositivos para el avance de la investigación biomédica. Estos avances incluyen el desarrollo de matrices de microelectrodos para monitoreo eléctrico in vivo13, microelectrodos capacitivos para electroporación in situ 14, dispositivos miniaturizados de órgano en un chip 15, diagnósticos microfluídicos en el punto de atención16, biosensores 17 y sistemas de administración de fármacos 18, incluidos dispositivos de nano y microelectroporación 19,20,21 . Debido a la capacidad de diseñar y fabricar dispositivos a la misma escala de tamaño que las células biológicas, las tecnologías de nano y microelectroporación son ventajosas en comparación con su contraparte a macroescala22,23. Estos dispositivos de electroporación eliminan el requisito de aplicaciones de pulsos de alto voltaje, ya que los conjuntos de electrodos con espaciamientos de 10s a 100s de micrómetros suelen estar integrados. Esta característica reduce drásticamente la corriente a través del electrolito, lo que a su vez reduce la acumulación de productos tóxicos de electrólisis y los efectos del calentamiento Joule en estos sistemas. Los canales a microescala también aseguran que un campo eléctrico mucho más uniforme se aplique de manera confiable a las células durante la aplicación del pulso, lo que resulta en resultados más consistentes24. Además, también es común que los dispositivos de microelectroporación se integren en una plataforma microfluídica que se presta para la futura integración en una tecnología totalmente automatizada, una capacidad altamente deseable en la fabricación de terapia celular25. Por último, la electroporación a microescala permite la interrogación eléctrica de eventos de electroporación. Por ejemplo, el grado de permeabilización de la membrana celular puede ser monitoreado en tiempo real a un nivel de una sola célula26,27. El propósito de este método es describir la microfabricación, el funcionamiento del sistema y el análisis de un dispositivo microfluídico de microelectroporación unicelular capaz de medir el grado de permeabilización de la membrana celular para optimizar los protocolos de electroporación, pero aumentando el rendimiento sobre el estado de la técnica anterior.
La realización de electroporación a nivel unicelular ya no es una técnica novedosa, como fue demostrado por primera vez por Rubinsky et al. en 2001 con el desarrollo de una tecnología de electroporación de células estáticas28. Su microdispositivo fue innovador, ya que fueron los primeros en demostrar la capacidad de monitorear eléctricamente el evento de electroporación. Esto ha llevado al desarrollo de tecnologías estáticas de electroporación unicelular capaces de detectar eléctricamente el grado de permeabilización de la membrana celular de manera paralelizada para aumentar el rendimiento de los dispositivos. Sin embargo, incluso con paralelización y procesamiento por lotes, estos dispositivos carecen gravemente del número total de celdas que pueden procesar por unidad de tiempo29,30. Esta limitación ha llevado al desarrollo de dispositivos de flujo continuo capaces de realizar microelectroporación a nivel de una sola célula a rendimientos mucho mayores31. Esta transición del dispositivo, de entorno estático a entorno de flujo continuo, limita la capacidad de monitorear eléctricamente el grado de permeabilización de la membrana celular después de la aplicación del pulso de electroporación. El método descrito en este trabajo cierra la brecha entre estas dos tecnologías, una tecnología de microelectroporación capaz de detectar eléctricamente, pulsar y monitorear el grado de permeabilización de la membrana celular de células individuales, de manera continua y en serie.
Esta tecnología fue descrita recientemente en Zheng et al. En ese trabajo, las capacidades de esta tecnología fueron introducidas con la realización de un estudio paramétrico, donde se varió tanto la amplitud como la duración del pulso de electroporación, y se exploró la consiguiente señal eléctrica, indicativa de permeabilización de la membrana celular32. Los resultados mostraron que un aumento en la intensidad del pulso de electroporación (es decir, aumento en el campo eléctrico aplicado o aumento en la duración del pulso) causó un aumento en la permeabilización de la membrana celular medida. Para validar aún más el sistema, se agregó un indicador fluorescente común de electroporación exitosa, yoduro de propidio33, a la suspensión celular, y se capturó una imagen de fluorescencia inmediatamente después de la aplicación del pulso eléctrico. La señal óptica, es decir, la intensidad de fluorescencia del yoduro de propidio dentro de la célula, se correlacionó fuertemente con la medición eléctrica del grado de permeabilización de la membrana celular, verificando la fiabilidad de esta medición eléctrica. Sin embargo, este trabajo solo consideró la entrega de la molécula pequeña yoduro de propidio, que tiene poca o ninguna importancia traducible.
En este trabajo, se introduce una nueva aplicación de esta tecnología para mejorar el rendimiento del sistema mientras se entrega un vector de ADN plásmido (ADNp) biológicamente activo y se evalúa la eficiencia de electrotransfección de las células rechapadas y cultivadas después de la electroporación. Aunque el trabajo anterior supera las tecnologías de microelectroporación existentes que son capaces de medir eléctricamente el evento de electroporación, el estado actual del dispositivo aún requiere largos tiempos de tránsito celular entre el conjunto de electrodos (~ 250 ms) para realizar la detección celular, la aplicación de pulsos y la medición de permeabilización de la membrana celular. Con un solo canal, esto limita el rendimiento a 4 celdas/s. Para combatir esta limitación, se introduce un nuevo concepto de electroporación controlada por retroalimentación basada en la población celular para realizar la electrotransfección de ADN. Mediante el uso de un tampón de electroporación de conductividad hipofisiológica, este sistema permite la interrogación eléctrica de células individuales a través de una multitud de aplicaciones de pulso de electroporación. Sobre la base de la respuesta eléctrica, se determina un pulso de electroporación “óptimo”. Luego se implementa un modo de “alto rendimiento” donde se anula la determinación de permeabilización de la membrana celular, se aumenta el caudal y el ciclo de trabajo del pulso de electroporación se adapta al tiempo de tránsito de la celda para garantizar un pulso por celda en tránsito entre los electrodos. Este trabajo proporcionará amplios detalles sobre los pasos de microfabricación para la fabricación del microdispositivo, el material / equipo y su configuración necesarios para realizar la experimentación, y la operación / análisis del dispositivo y su eficiencia de electrotransfección (eTE).
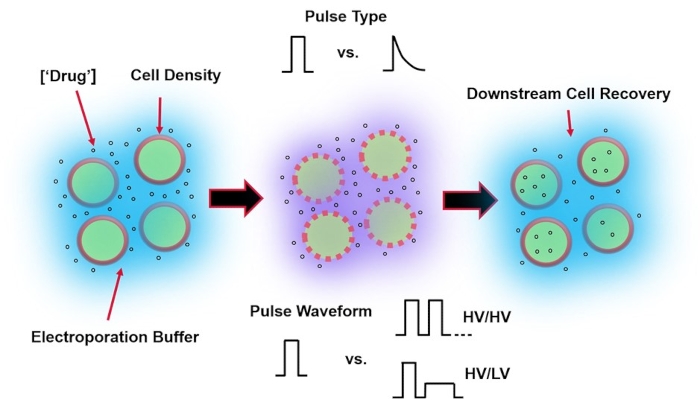
Figura 1: Factores experimentales que afectan los resultados de electroporación. (Izquierda) Suspensión celular: los factores importantes a considerar antes del inicio de la electroporación incluyen: carga útil (en este caso, ADNp), concentración, densidad celular y propiedades tampón de electroporación. Las propiedades del tampón de electroporación a considerar son la conductividad, la osmolaridad y la composición molecular exacta que contribuye a estos valores. (Medio) Aplicación de pulso: el tipo de pulso exacto (onda cuadrada vs. decaimiento exponencial) y la forma de onda de pulso (pulso único vs. tren de pulso) deben optimizarse para maximizar tanto la viabilidad celular resultante como la eficiencia de electrotransfección. Los trenes de pulsos comunes implementados en los procesos de electroporación generalmente se componen de una serie de pulsos de alto voltaje (HV) o una serie de pulsos que giran entre HV y magnitudes de pulso de bajo voltaje (LV). (Derecha) Recuperación celular: los pasos de procesamiento aguas abajo, en particular, los medios de cultivo celular de recuperación a los que se transfieren las células, deben optimizarse. No destacado (extremo izquierdo), se pueden implementar pasos adicionales de procesamiento de celdas aguas arriba para la optimización general del proceso de electroporación. Haga clic aquí para ver una versión más grande de esta figura.
Protocol
Representative Results
Discussion
La metodología presentada dentro de este protocolo se centra principalmente en la microfabricación de un dispositivo microfluídico que luego se integra en una configuración experimental especializada de electroporación. El término “receta”, que a menudo se usa cuando se describen los detalles del proceso de microfabricación, sugiere la importancia de seguir / optimizar cada paso para fabricar con éxito un dispositivo que funcione. Sin embargo, ciertos pasos críticos dentro del proceso, cuando no están optimizad…
Disclosures
The authors have nothing to disclose.
Acknowledgements
Los autores desean agradecer el apoyo financiero de la National Science Foundation (NSF CBET 0967598, DBI IDBR 1353918) y la Capacitación de Posgrado en Áreas Emergentes de Precisión y Medicina Personalizada del Departamento de Educación de los Estados Unidos (P200A150131) para financiar al estudiante graduado J.J.S. en beca.
Materials
| 150-mm diameter petri dishes | VWR | 25384-326 | step 6.1.1 to secure wafer |
| 24-well tissue culture plates | VWR | 10062-896 | step 10.3.6 to plate electroporated cells |
| 33220A Waveform/Function generator | Agilent | step 9.2.3 electroporation pulse generator | |
| 4'' Si-wafers | University Wafer | subsection 2.1 for microfluidic channel fabrication | |
| 6-well tissue culture plates | VWR | 10062-892 | step 8.1.8 to plate cells |
| Acetone | Fisher Scientific | A18-4 | step 2.1.2 for cleaning and step 5.1 photoresist lift-off |
| Allegra X-22R Centrifuge | Beckman Coulter | steps 8.1.4 , 8.3.2. and 8.3.3. to spin down cells | |
| AutoCAD 2018 | Autodesk | subsection 1.1. to design transparency masks | |
| Buffered oxide etchant 10:1 | VWR | 901621-1L | subsection 3.1 for HF etching |
| CCD Monochrome microscope camera | Hamamatsu | Orca 285 C4742-96-12G04 | step 11.2.3. for imaging |
| CMOS camera- Sensicam QE 1.4MP | PCO | subsection 9.3 part of the experimental setup | |
| Conductive Epoxy | CircuitWorks | CW2400 | subsection 7.6. for wire attachement |
| Conical Centrifuge Tubes, 15 mL | Fisher Scientific | 14-959-70C | step 8.1.4. for cell centrifuging |
| Dektak 3ST Surface Profilometer | Veeco (Sloan/Dektak) | step 2.1.15 and 5.4 for surface profilometry | |
| Disposable biopsy punch, 0.75 mm | Robbins Instruments | RBP075 | step 6.2.3 for inlet access |
| Disposable biopsy punch, 3 mm | Robbins Instruments | RBP30P | step 6.2.3 for outlet access |
| DRAQ5 | abcam | ab108410 | step 11.2.2. for live cell staining |
| Dulbecco’s Modified Eagle’s Medium | ThermoFisher Scientific | 11885084 | step 8.1.2. part of media composition |
| E3631A Bipolar Triple DC power supply | Agilent | step 9.2.1.-9.2.2.part of the experimental setup | |
| Eclipse TE2000-U Inverted Microscope | Nikon | subsection 9.3. part of the experimental setup | |
| EVG620 UV Lithography System | EVG | step 2.1.9. and 2.2.7. for UV Exposure | |
| Fetal Bovine Serum | Neuromics | FBS001 | step 8.1.2. part of media composition |
| FS20 Ultrasonic Cleaner | Fisher Scientific | subsection 5.1. for photoresist lift-off | |
| Glass Media Bottle with Cap, 100mL | Fisher Scientific | FB800100 | step 8.2.1. for buffer storage |
| Glass Media Bottle with Cap, 500mL | Fisher Scientific | FB800500 | step 8.1.2.for media storage |
| HEK-293 cell line | ATCC | CRL-1573 | subsection 8.1 for cell culturing |
| HEPES buffer solution | Sigma Aldrich | 83264-100ML-F | step 8.2.1 part of electroporation buffer composition |
| Hexamethyldisilazane | Sigma Aldrich | 379212-25ML | step 2.2.3 adhesion promoter |
| HF2LI Lock-in Amplifier | Zurich Instruments | subsection 9.2 part of the experimental setup | |
| HF2TA Current amplifier | Zurich Instruments | subsection 9.2 part of the experimental setup | |
| Isopropyl Alcohol | Fisher Scientific | A459-1 | step 2.1.2 for cleaning, step 2.1.14 for rinsing wafer following SU-8 development, and step 6.3.1 for cleaning PDMS |
| IX81 fluorescence microscope | Olympus | step 11.2.3 for imaging | |
| L-Glutamine Solution | Sigma Aldrich | G7513-20ML | step 8.1.2. part of media composition |
| M16878/1BFA 22 gauge wire | AWC | B22-1 | subsection 7.5 for device fabrication |
| Magnesium chloride | Sigma Aldrich | 208337-100G | step 8.1.2 part of electroporation buffer composition |
| MF 319 Developer | Kayaku Advanced Materials | 10018042 | step 2.2.9. photoresist developer |
| Microposit S1818 photoresist | Kayaku Advanced Materials | 1136925 | step 2.2.4 positive photoresist for electrode patterning |
| Microscope slides, 75 x 25 mm | VWR | 16004-422 | step 2.2.1 electrode soda lime glass substrate |
| Model 2350 High voltage amplifier | TEGAM | 2350 | step 9.2.5. part of the experimental setup |
| National Instruments LabVIEW | National Instruments | data acquisition | |
| Needle, 30G x 1 in | BD Scientific | 305128 | step 10.1.1. part of the system priming |
| PA90 IC OPAMP Power circuit | Digi-key | 598-1330-ND | Part of the custom circuit |
| Penicillin-Streptomycin | Sigma Aldrich | P4458-20ML | step 8.1.2. part of media composition |
| Plasmid pMAX-GFP | Lonza | VCA-1003 | step 8.3.4. for intracellular delivery |
| Plastic tubing, 0.010'' x 0.030" | VWR | 89404-300 | step 10.1.2. for system priming |
| Platinum targets | Kurt J. Lesker | subsection 4.2. for physical vapor deposition | |
| Potassium chloride | Sigma Aldrich | P9333-500G | step 8.2.1. part of electroporation buffer composition |
| Pump 11 PicoPlus microfluidic syringe pump | Harvard Apparatus | MA1 70-2213 | step 10.1.4. for system priming |
| PVD75 Physical vapor deposition system | Kurt J. Lesker | subsection 4.1. for physical vapor deposition | |
| PWM32 Spinner System | Headway Research | steps 2.1.6 and 2.2.2. for substrate coating with photoresist | |
| PX-250 Plasma treatment system | March Instruments | subsection 7.2 for PDMS and glass substrate bonding | |
| SDG1025 Function/Waveform generator | Siglent | step 9.2.2. part of the experimental setup | |
| Sodium hydroxide | Sigma Aldrich | S8045-500G | step 8.2.1. part of electroporation buffer composition |
| SU-8 2010 negative photoresist | Kayaku Advanced Materials | Y111053 | step 2.1.7. for microfluidic channel patterning |
| SU-8 developer | Microchem | Y010200 | step 2.1.12. for photoresist developing |
| Sucrose | Sigma Aldrich | S7903-1KG | step 8.2.1. part of electroporation buffer composition |
| Sylgard 184 elastomer kit | Dow Corning | 3097358-1004 | step 6.2.1 10 : 1 mixture of PDMS polymer and hardening agent |
| Syringe, 1 ml | BD Scientific | 309628 | step 8.3.4. part of system priming |
| SZ61 Stereomicroscope System | Olympus | subsection 7.3. for channel and electrode alignment | |
| Tissue Culture Treated T25 Flasks | Falcon | 353108 | step 8.1.2 for cell culturing |
| Titanium targets | Kurt J. Lesker | subsection 4.2. for physical vapor deposition | |
| Transparency masks | CAD/ART Services | steps 2.1.9. and 2.2.7. for photolithography | |
| Trichloro(1H,1H,2H,2H-perfluorooctyl)silane | Sigma Aldrich | 448931-10G | step 6.1.2. for wafer silanization |
| Trypsin-EDTA solution | Sigma Aldrich | T4049-100ML | steps 8.1.3. and 8.3.1. for cell harvesting |
References
- Gao, Q. Q., et al. Therapeutic potential of CRISPR/Cas9 gene editing in engineered T-cell therapy. Cancer Medicine. 8 (9), 4254-4264 (2019).
- Aijaz, A., et al. Biomanufacturing for clinically advanced cell therapies. Nature Biomedical Engineering. 2 (6), 362-376 (2018).
- Milone, M. C., O’Doherty, U. Clinical use of lentiviral vectors. Leukemia. 32 (7), 1529-1541 (2018).
- Weaver, J. C., Chizmadzhev, Y. A. Theory of electroporation: A review. Bioelectrochemistry and Bioenergetics. 41 (2), 135-160 (1996).
- Kotnik, T., Rems, L., Tarek, M., Miklavcic, D. Membrane electroporation and electropermeabilization: mechanisms and models. Annual Review of Biophysics. 48, 63-91 (2019).
- Rosazza, C., Meglic, S. H., Zumbusch, A., Rols, M. P., Miklavcic, D. Gene electrotransfer: A mechanistic perspective. Current Gene Therapy. 16 (2), 98-129 (2016).
- Clauss, J., et al. Efficient non-viral T-cell engineering by sleeping beauty minicircles diminishing DNA toxicity and miRNAs silencing the endogenous T-cell receptors. Human Gene Therapy. 29 (5), 569-584 (2018).
- Sherba, J. J., et al. The effects of electroporation buffer composition on cell viability and electro-transfection efficiency. Scientific Reports. 10 (1), 3053 (2020).
- Lu, H., Schmidt, M. A., Jensen, K. F. A microfluidic electroporation device for cell lysis. Lab on a Chip. 5 (1), 23-29 (2005).
- Kar, S., et al. Single-cell electroporation: current trends, applications and future prospects. Journal of Micromechanics and Microengineering. 28 (12), (2018).
- Shi, J. F., et al. A review on electroporation-based intracellular delivery. Molecules. 23 (11), (2018).
- Wang, S. N., Zhang, X. L., Wang, W. X., Lee, L. J. Semicontinuous flow electroporation chip for high-throughput transfection on mammalian cells. Analytical Chemistry. 81 (11), 4414-4421 (2009).
- Wei, W. J., et al. An implantable microelectrode array for simultaneous L-glutamate and electrophysiological recordings in vivo. Microsystems & Nanoengineering. 1, (2015).
- Maschietto, M., Dal Maschio, M., Girardi, S., Vassanelli, S. In situ electroporation of mammalian cells through SiO2 thin film capacitive microelectrodes. Scientific Reports. 11 (1), (2021).
- Wu, Q. R., et al. Organ-on-a-chip: recent breakthroughs and future prospects. Biomedical Engineering Online. 19 (1), (2020).
- Pandey, C. M., et al. Microfluidics Based Point-of-Care Diagnostics. Biotechnology Journal. 13 (1), (2018).
- Vigneshvar, S., Sudhakumari, C. C., Senthilkumaran, B., Prakash, H. Recent advances in biosensor technology for potential applications – An overview. Frontiers in Bioengineering and Biotechnology. 4, (2016).
- Nuxoll, E. BioMEMS in drug delivery. Advanced Drug Delivery Reviews. 65 (11-12), 1611-1625 (2013).
- Kang, S., Kim, K. H., Kim, Y. C. A novel electroporation system for efficient molecular delivery into Chlamydomonas reinhardtii with a 3-dimensional microelectrode. Scientific Reports. 5, (2015).
- Zheng, M. D., Shan, J. W., Lin, H., Shreiber, D. I., Zahn, J. D. Hydrodynamically controlled cell rotation in an electroporation microchip to circumferentially deliver molecules into single cells. Microfluidics and Nanofluidics. 20 (1), (2016).
- Santra, T. S., Kar, S., Chang, H. Y., Tseng, F. G. Nano-localized single-cell nano-electroporation. Lab on a Chip. 20 (22), 4194-4204 (2020).
- Lee, W. G., Demirci, U., Khademhosseini, A. Microscale electroporation: challenges and perspectives for clinical applications. Integrative Biology. 1 (3), 242-251 (2009).
- Santra, T. S., Chang, H. Y., Wang, P. C., Tseng, F. G. Impact of pulse duration on localized single-cell nano-electroporation. Analyst. 139 (23), 6249-6258 (2014).
- Geng, T., Lu, C. Microfluidic electroporation for cellular analysis and delivery. Lab on a Chip. 13 (19), 3803-3821 (2013).
- Hsi, P., et al. Acoustophoretic rapid media exchange and continuous-flow electrotransfection of primary human T cells for applications in automated cellular therapy manufacturing. Lab on a Chip. 19 (18), 2978-2992 (2019).
- Khine, M., Ionescu-Zanetti, C., Blatz, A., Wang, L. P., Lee, L. P. Single-cell electroporation arrays with real-time monitoring and feedback control. Lab on a Chip. 7 (4), 457-462 (2007).
- Ye, Y. F., et al. Single-cell electroporation and real-time electrical monitoring on a microfluidic chip. 2020 33rd Ieee International Conference on Micro Electro Mechanical Systems (Mems 2020). , 1040-1043 (2020).
- Huang, Y., Rubinsky, B. Microfabricated electroporation chip for single cell membrane permeabilization. Sensors and Actuators a-Physical. 89 (3), 242-249 (2001).
- Guo, X. L., Zhu, R. Controllable in-situ cell electroporation with cell positioning and impedance monitoring using micro electrode array. Scientific Reports. 6, (2016).
- Punjiya, M., Nejad, H. R., Mathews, J., Levin, M., Sonkusale, S. A flow through device for simultaneous dielectrophoretic cell trapping and AC electroporation. Scientific Reports. 9, (2019).
- Wang, H. Y., Lu, C. Microfluidic electroporation for delivery of small molecules and genes into cells using a common DC power supply. Biotechnology and Bioengineering. 100 (3), 579-586 (2008).
- Zheng, M. D., et al. Continuous-flow, electrically-triggered, single cell-level electroporation. Technology. 5 (1), 31-41 (2017).
- Batista Napotnik, T., Miklavcic, D. In vitro electroporation detection methods – An overview. Bioelectrochemistry. 120, 166-182 (2018).
- MICROPOSIT™ S1800® G2 Series Photoresists. KAYAKU Available from: https://kayakuam.com/wp-content/uploads/2019/09/S1800-G2.pdf (2021)
- SU-8 2000 Permanent Negative Epoxy Photoresist. KAYAKU Available from: https://kayakuam.com/wp-content/uploads/2020/08/KAM-SU-8-2000-2000.5-2015-Datasheet-8.13.20-final.pdf (2001)
- Substrate Preparation. MicroChemicals Available from: https://www.microchemicals.com/technical_information/subtrate_cleaning_adhesion_photoresist.pdf (2021)
- Lisinenkova, M., Hahn, L., Schulz, J. . 4M 2006 – Second International Conference on Multi-Material Micro Manufacture. , 91-94 (2006).
- Beh, C. W., Zhou, W. Z., Wang, T. H. PDMS-glass bonding using grafted polymeric adhesive – alternative process flow for compatibility with patterned biological molecules. Lab on a Chip. 12 (20), 4120-4127 (2012).
- PA90 High Voltage Power Operational Amplifiers. APEX Available from: https://www.apexanalog.com/resources/products/pa90u.pdf (2021)
- Lissandrello, C. A., et al. High-throughput continuous-flow microfluidic electroporation of mRNA into primary human T cells for applications in cellular therapy manufacturing. Scientific Reports. 10 (1), 18045 (2020).

